傳承中華優(yōu)秀成果 彰顯學科核心素養(yǎng)
顏建河
新高考“以核心素養(yǎng)為測試宗旨,以真實情景為測試載體,以實際問題為測試任務”為命題原則。核心素養(yǎng)培育“是學科育人價值的集中體現(xiàn),是學生通過學科學習而逐步形成的正確價值觀念,必備品質和關鍵能力”。基于此,在高三復習教學中要引導學生進行深度學習,既能有效夯實基礎,提升思維水平,又能促進學生的認知發(fā)展,培育學生的化學學科核心素養(yǎng)。同時,必須關注和落實化學學科核心素養(yǎng),關注學生綜合能力的提升,關注化學知識的實際應用。這樣,才能在復習中有的放失,提高化學學科復習效率。
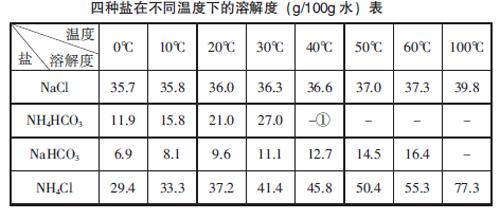
【案例】根據(jù)侯德榜制堿法原理并參考下表的數(shù)據(jù),實驗室制備純堿Na2CO3的主要步驟是:將配制好的飽和NaCl溶液倒入燒杯中加熱,控制溫度在30~35 ℃,攪拌下分批加入研細的NH4HCO3固體,加料完畢后,繼續(xù)保溫30分鐘,靜置、過濾得NaHCO3晶體。用少量蒸餾水洗滌除去雜質,抽干后,轉入蒸發(fā)皿中,灼燒2小時,制得Na2CO3固體。
請回答:
(1)反應溫度控制在30~35℃,是因為若高于35℃,則_______________,若低于30℃,則_________________;為控制此溫度范圍,采取的加熱方法為____________________。
(2)加料完畢后,繼續(xù)保溫30分鐘,目的是__________ _____________。靜置后只析出NaHCO3晶體的原因是__________________。用蒸餾水洗滌NaHCO3晶體的目的是除去_______________雜質(以化學式表示)。
(3)過濾所得母液中含有_____________(以化學式表示),需加入_______________,并作進一步處理,使NaCl溶液循環(huán)使用,同時可回收NH4Cl。
(4)測試純堿產(chǎn)品中NaHCO3含量的方法是:準確稱取純堿樣品W,放入錐形瓶中加蒸餾水溶解,加1~2滴酚酞指示劑,用物質的量濃度為c(mol/L)的HCl溶液滴定至溶液由紅色到無色(指示CO32-+H+=HCO3-反應的終點),所用HCl溶液體積為V1mL,再加1~2滴甲基橙指示劑,繼續(xù)用HCl溶液滴定至溶液由黃變橙,所用HCl溶液體積為V2mL。寫出純堿樣品中NaHCO3質量分數(shù)的計算式:NaHCO3(%)=___________。
分析:本題是一道以侯德榜為依托的實驗設計題,著力考查學生利用圖表信息及中和滴定中雙指示劑法的應用;第(1)、(2)、(3)問要求利用圖表信息,結合制堿原理及生活中的化學知識,弄清水浴加熱的優(yōu)點,找出溶液轉化法的守恒關系,第(4)問以中和滴定中雙指示劑原理進行設計,進而測定產(chǎn)品的純度,整個試題設計精巧,逐層深入,將生產(chǎn)、生活中的化學知識考查得淋漓盡致。
(1)碳酸氫銨10~20℃時,不易分解,30℃時開始大量分解. 若溫度過低,則反應速率較慢,故反應溫度控制在30~35℃之間為宜。水浴加熱是把要加熱的物質放在水中,通過給水加熱達到給物質加熱的效果,一般都是把要反應的物質放在試管中,再把試管放在裝有水的燒杯中,再在燒杯中插一根溫度計,可以控制反應溫度. 水浴加熱的優(yōu)點是避免了直接加熱造成的過度劇烈與溫度的不可控性,可以平穩(wěn)地加熱,許多反應需要嚴格的溫度控制,就需要水浴加熱. 水浴加熱的缺點是加熱溫度最高只能達到100度。故答案為:NH4HCO3分解;反應速率降低;水浴加熱
(2)加料完畢后,繼續(xù)保溫30分鐘,可以使反應充分進行,使反應完全. 碳酸氫銨0℃時溶解度為11.3%;20℃時為21%;40℃時為35%.碳酸氫鈉0℃溶解度為6.9g,5℃為7.45g,10℃為8.15g,15℃為8.85g,20℃為9.6g,25℃為10.35g,30℃為11.1g,35℃為11.9g,40℃為12.7g,45℃為13.55g,50℃為14.45g,55℃為15.4g,60℃為16.4g.30℃時碳酸氫鈉的溶解度更小,故碳酸氫鈉先析出. 用蒸餾水洗滌NaHCO3晶體的目的是為了除去雜質,此反應中雜質為 NaCl、NH4Cl、NH4HCO3。故答案為:使反應充分進行;NaHCO3的溶解度最小;NaCl、NH4Cl、NH4HCO3
(3)過濾除去析出的碳酸氫鈉,溶液中還有部分碳酸氫鈉未析出,還有溶解在溶液中的NaCl、NH4Cl、NH4HCO3,所得的母液主要成分為NaHCO3、NaCl、NH4Cl、NH4HCO3 . 加入鹽酸后,碳酸氫鈉轉化為氯化鈉,碳酸氫銨轉化為氯化銨,這時溶液中的NaCl溶液循環(huán)使用,同時可回收NH4Cl。故答案為:NaHCO3、NaCl、NH4Cl、NH4HCO3;HCl
(4)加酚酞指示劑,用物質的量濃度為c(mol/L)的HCl溶液滴定至溶液由紅色到無色,指示CO32-+H+=HCO3- 反應的終點,所用HCl溶液體積為V1mL;再加甲基橙指示劑,繼續(xù)用HCl溶液滴定至溶液由黃變橙,指示HCO3-+H+=CO2+H2O反應的終點,所用HCl溶液體積為V2mL. 上述的兩個離子方程式為①CO32-+H+=HCO3- ②HCO3-+H+=CO2+H2O,故樣品中含有的碳酸氫鈉反應消耗鹽酸體積為(V2-V1)mL,消耗鹽酸的物質的量為c(V2-V1)÷1000 mol,故碳酸氫鈉的物質的量為c(V2-V1)÷1000 mol,碳酸氫鈉的質量為c(V2-V1)M÷1000 g,碳酸氫鈉的質量分數(shù)為[ c(V2-V1)M/1000W] ×100%,故答案為:[c(V2-V1)M/1000W]×100%
【對策】侯氏制堿法是核心素養(yǎng)的一個好素材,更是高中化學的一個重要知識點和高考的高頻考點。為此,全面而詳實把侯氏制堿法的原理、原料、設備、優(yōu)缺點進行復習,明確侯氏制堿法(又稱聯(lián)合制堿法)它是我國化學工程專家侯德榜(1890~1974)于1943年創(chuàng)立的。將氨堿法和合成氨法(合成氨廠用水煤氣制取氫氣時的廢氣:C+H2O(g) →O2+H2、CO+H2O(g)→CO2+H2)聯(lián)合起來生產(chǎn)的。聯(lián)合制堿法包括兩個過程:第一個過程是將氨通入飽和食鹽水而成氨鹽水,再通入二氧化碳生成碳酸氫鈉沉淀,經(jīng)過濾、洗滌得NaHCO3微小晶體,再煅燒制得純堿產(chǎn)品,其濾液是含有氯化銨和氯化鈉的溶液;第二個過程是從含有氯化銨和氯化鈉的濾液中結晶沉淀出氯化銨晶體。由于氯化銨在常溫下的溶解度比氯化鈉要大,低溫時的溶解度則比氯化鈉小,而且氯化銨在氯化鈉的濃溶液里的溶解度要比在水里的溶解度小。
【總結】工業(yè)制純堿的方法: 一是氨堿法; 二是聯(lián)合制堿法(侯氏制堿法)。
1. 氨堿法(索爾維制堿法)
基本原理: 向飽和食鹽水中通入足量氨氣至飽和,然后,在加壓下通入CO2(經(jīng)由CaCO3煅燒而得),且NaHCO3溶解度較小,故有下列反應發(fā)生:NH3+CO2+H2O=NH4HCO3、NaCl+NH4HCO3=NaHCO3↓+NH4Cl,將析出的NaHCO3晶體煅燒即得Na2CO3:2NaHCO3=Na2CO3+CO2↑+H2O。同時,母液中的NH4Cl加消石灰可回收氨,以便循環(huán)使用:2NH4Cl+Ca(OH)2 =CaCl2+2NH3↑+2H2O。
(1)優(yōu)點:原料經(jīng)濟,能連續(xù)生產(chǎn),CO2和NH3能回收使用。
(2)缺點:大量CaCl2用途不大,NaCl利用率只有70%,約有30%的NaCl留在母液中。
2. 聯(lián)合制堿法(侯氏制堿法)
基本原理:依據(jù)離子反應發(fā)生會向著離子濃度減小的方向進行(勒夏特原理),且NH4Cl在常溫時的溶解度比NaCl大,而在低溫下卻比NaCl溶解度小的,在278K~283K(5℃~10℃)時,向母液中加入食鹽細粉,而使NH4Cl結晶析出,成為氮肥產(chǎn)品。
優(yōu)點:保留了氨堿法的優(yōu)點,消除了它的缺點,使食鹽的利用率提高到96%;NH4Cl可做氮肥;可與合成氨廠聯(lián)合,使合成氨的原料氣CO轉化成CO2,革除了CaCO3制CO2這一工序。
總之,在2020復習備考進程中,一定要避免將高考評價體系中的考查內容與具體試題機械綁定。要從新時代的高考重點考查學科核心素養(yǎng)出發(fā),通過試卷的整體設計來實現(xiàn),而不是機械地落實到某一道試題或某一類試題上。從而實現(xiàn)多種知識與能力的有效建構并對外輸出,提升有效解決各種問題的綜合能力,促進學生化學學科核心素養(yǎng)的發(fā)展。
責任編輯? ?李平安

