多角度深層次復習銅及其化合物
◇ 陳 飛(特級教師)
銅及其化合物的知識在教材中沒有系統講述,零星分散在不同章節里,但是銅及其化合物在生產和生活中有著廣泛的用途,能夠很好地體現化學學科的核心素養,因此銅的相關知識是高考命題的重點,在高考中頻頻出現.復習時如果運用“發散思維”,從多角度和多層面進行復習,會有一種“橫看成嶺側成峰,遠近高低各不同”的感覺,能起到“事半功倍”的效果.本文從不同角度進行歸納整理,供同學們復習時參考.
1 從顏色的角度來復習
【教材尋源】人教版《必修1》第46頁圖3-2有關金屬化學性質的一些實驗;第57頁圖3-14金屬的焰色反應;第62頁圖3-21的銅綠,資料卡片中的銅鹽.人教版《必修2》第93頁習題3中的藍銅礦.
【高考鏈接】(2019年全國卷Ⅱ)下列化學方程式中,不能正確表達反應顏色變化的是( ).
A.向CuSO4溶液中加入足量Zn粉,溶液藍色消失:Zn+CuSO4=Cu+ZnSO4
B.澄清的石灰水久置后出現白色固體:Ca(OH)2+CO2=CaCO3↓+H2O
C.Na2O2在空氣中放置后由淡黃色變為白色:2Na2O2=2Na2O+O2↑
D.向Mg(OH)2懸濁液中滴加足量FeCl3溶液出現紅褐色沉淀:3Mg(OH)2+2FeCl3=2Fe(OH)3+3MgCl2

向硫酸銅溶液中加入足量鋅粉,會發生發下反應:Zn+CuSO4=ZnSO4+Cu,硫酸銅不斷減少,溶液的藍色就會消失,選項A正確;澄清石灰水吸收空氣中的CO2生成碳酸鈣白色沉淀,選項B正確;過氧化鈉與空氣中的H2O和CO2發生反應,最終生成白色的Na2CO3,選項C錯誤;Mg(OH)2和FeCl3可以反應生成溶解度更小的Fe(OH)3,選項D正確.答案為C.
【要點歸納】銅的焰色:綠色.銅及其化合物的顏色:Cu(紫紅或暗紅),Cu2O(紅色),CuO(黑色),CuSO4(白色),CuSO4·5H2O(藍色),Cu(OH)2(藍色),CuCO3(藍色),CuCl(白色),CuCl2(淡綠色),Cu2(OH)2CO3(綠色),[Cu(NH3)4]2+(深藍色).
2 從物質分類的角度來復習
【教材尋源】人教版《必修1》第26頁“科學探究2”:硫酸銅溶液用激光筆照射.
【高考鏈接】(2017年浙江卷)下列分散系能產生“丁達爾效應”的是( ).
A.稀硫酸 B.硫酸銅溶液
C.氫氧化鐵膠體 D.酒精溶液

從物質分類的角度考慮,膠體為分散質粒子直徑介于1~100 nm之間的分散系,能夠產生丁達爾效應.稀硫酸、硫酸銅溶液和酒精溶液均是溶液,故不能產生丁達爾效應.答案為C.
【要點歸納】分散系可以分為溶液、膠體和濁液,丁達爾效應是膠體的特有性質.
3 從離子反應的角度來復習
【教材尋源】人教版《必修1》第34頁第6題和第10題,涉及和銅有關的離子反應方程式.
【高考鏈接】(2019年江蘇卷)下列指定反應的離子方程式正確的是( ).
A.室溫下用稀NaOH溶液吸收Cl2:Cl2+2OH-=Cl O-+Cl-+H2O
B.用鋁粉和NaOH溶液反應制取少量H2:Al+2OH-=+H2↑
C.室溫下用稀HNO3溶解銅:Cu++2 H+=Cu2++2NO2↑+H2O
D.向Na2SiO3溶液中滴加稀鹽酸:
Na2SiO3+2H+=H2SiO3↓+2Na+

室溫下用稀NaOH溶液吸收Cl2,離子方程式為Cl2+2OH-=ClO-+Cl-+H2O,選項A正確;鋁粉和NaOH溶液反應的離子方程式為2Al+2H2O+2OH-=2Al O-2+3 H2↑,選項B錯誤;室溫下用稀HNO3溶解銅的離子方程式為3Cu++8 H+=3Cu2++2NO↑+4 H2O,選項C錯誤;向Na2SiO3溶液中滴加稀鹽酸離子方程式為+2 H+=H2SiO3↓,選項D錯誤.答案為A.
【要點歸納】銅可以和濃硝酸、稀硝酸等物質發生離子反應.與稀硝酸反應的離子方程式為:3Cu++8H+=3Cu2++2NO↑+4H2O;與濃硝酸反應的離子方程式為Cu++4 H+=Cu2++2NO2↑+2 H2O.Cu O、Cu(OH)2、CuCO3均可溶于強酸,離子反應方程式學生可自己寫出.
4 從氧化還原的角度來復習
【教材尋源】人教版《必修1》第35頁木炭還原氧化銅,鐵和硫酸銅溶液反應.人教版《必修2》第89頁表4-1銅的冶煉.
【高考鏈接】(2017年浙江卷)為探究黑色固體X(僅含2種元素)的組成和性質,設計并完成如圖1所示實驗.

圖1
請回答:
(1)X的化學式是________.
(2)固體甲與稀硫酸反應的離子方程式是_________.
(3)加熱條件下氨氣被固體X氧化成一種氣體單質,寫出該反應的化學方程式:_______.

根據題中信息,32 g X隔絕空氣加熱生成了能使帶火星木條復燃的氣體,則該氣體應為氧氣,因此可確定X中一定含有氧元素.生成氧氣的質量為m=32.0 g-28.8 g=3.2 g,氧氣中含有氧原子的物質的量為0.2 mol.甲和稀硫酸反應生成的溶液為藍色,可知溶液中應該含有Cu2+,說明甲中含有銅元素,故X中也含有銅元素.因此可判斷黑色固體X為Cu O,其物質的量為
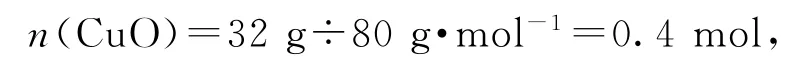
根據氧原子守恒可知,甲中
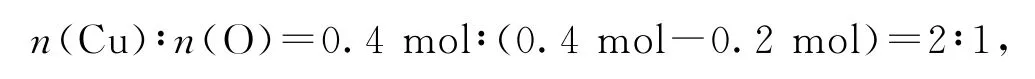
所以甲的化學式為Cu2O,固體單質乙為Cu,藍色溶液為CuSO4,加入NaOH生成的沉淀為Cu(OH)2,加熱分解得到16.0 g CuO.(1)X為Cu O;(2)Cu2O和稀硫酸反應的離子方程式為Cu2O+2 H+=Cu2++Cu+H2O;(3)加熱條件下NH3被CuO氧化成的氣體單質應為N2,化學方程式為3Cu+N2+3H2O.
【要點歸納】“銅三角”的氧化還原反應轉化關系如圖2所示.

圖2

5 從電化學角度來復習
【教材尋源】人教版《必修2》第40頁實驗2-4銅—鋅原電池實驗.人教版《選修4》第71頁圖4-1鋅—銅原電池裝置;第79頁實驗4-2電解氯化銅溶液;第81頁電鍍.
【高考鏈接】(2019年北京卷)下列示意圖與化學用語表述內容不相符的是( )(水合離子用相應離子符號表示).
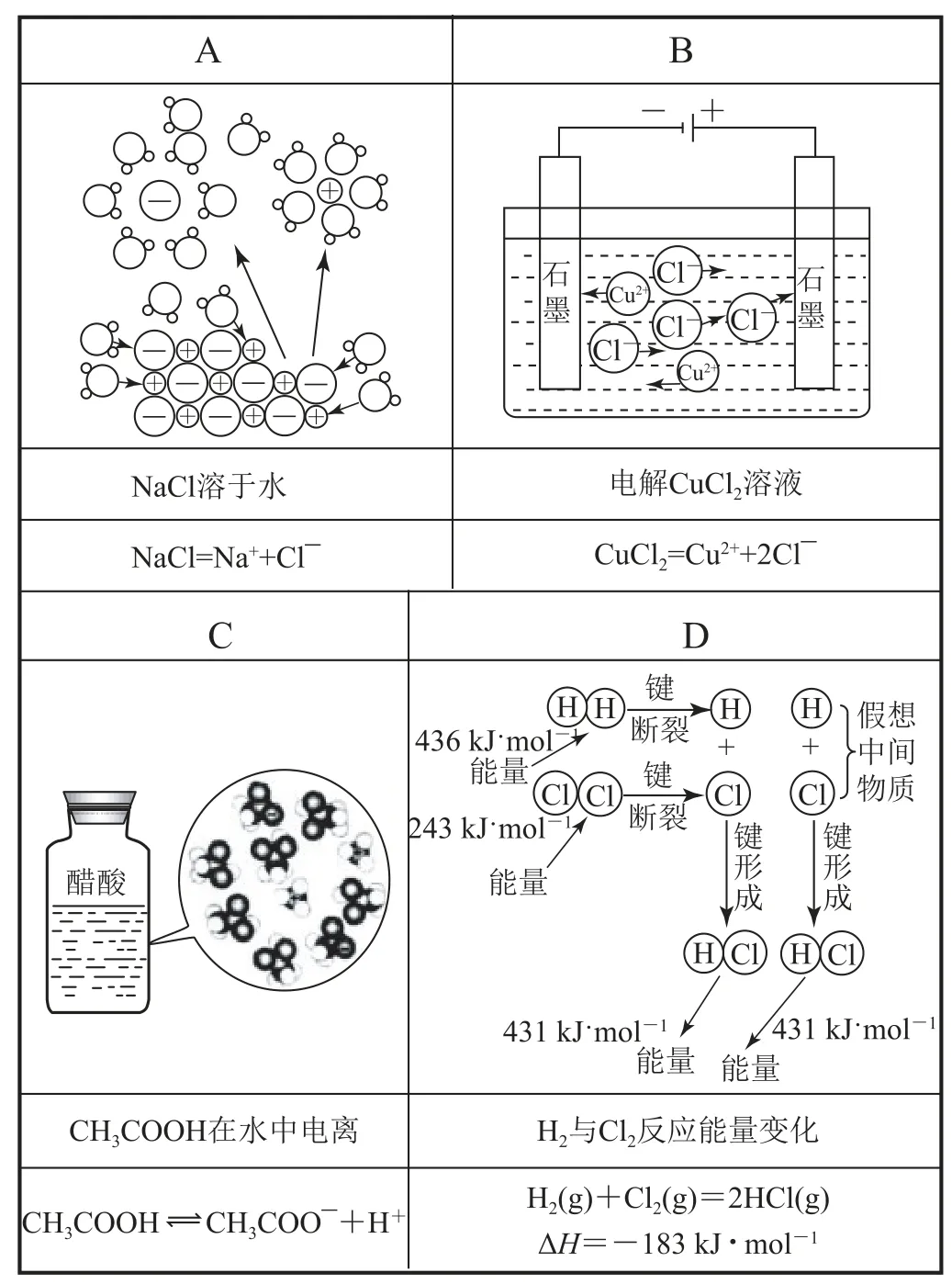

電解CuCl2溶液,是化學變化,反應方程式為,選項B不符合化學用語表述內容;選項A、C、D示意圖與化學用語表達內容相符.答案為B.
【要點歸納】1)銅—鋅—稀硫酸構成的原電池,負極為鋅,正極為銅.
2)電解:①以惰性電極電解硫酸銅溶液和氯化銅溶液:

②電解精煉銅:以粗銅為陽極、純銅為陰極、CuSO4溶液為電解液進行電解,可將粗銅提純.
③電鍍銅:以銅為陽極、鍍件為陰極、CuSO4溶液為電鍍液,可以在鍍件表面鍍一層銅.
6 從鹽的水解角度來復習
【教材尋源】人教版《選修4》第54頁“科學探究1”中可以增加硫酸銅溶液.
【高考鏈接】(2019年北京卷)實驗測得0.5 mol·L-1CH3COONa溶 液、0.5 mol·L-1CuSO4溶液以及H2O的pH隨溫度變化的曲線如圖3所示.下列說法正確的是( ).
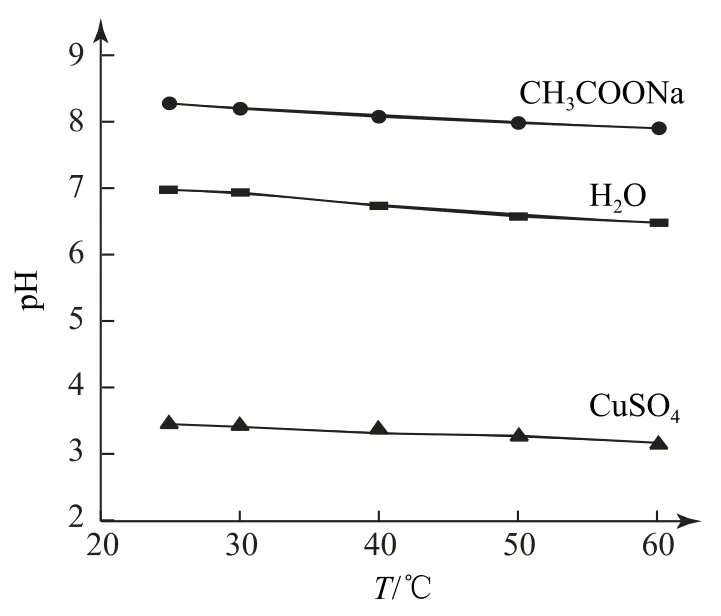
圖3
A.隨溫度升高,純水中c(H+)>c(OH-)
B.隨溫度升高,CH3COONa溶液的c(OH-)減小
C.隨溫度升高,CuSO4溶液的pH變化是Kw改變與水解平衡移動共同作用的結果
D.隨溫度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因為CH3COO-、Cu2+水解平衡移動方向不同

無論是否升溫,純水均為中性,c(H+)=c(OH-),選項A錯誤;CH3COONa水解顯堿性,升高溫度,促進水解,堿性增強,c(OH-)增大,選項B錯誤;硫酸銅水解顯酸性,升溫促進水解,酸性增強,c(H+)增加,升溫也促進水的電離,水電離生成的c(H+)增加,二者疊加,酸性變化趨勢一致,pH=-lgc(H+),c(H+)越大,pH越低,選項C正確;水解吸熱,故升高溫度CH3COO-、Cu2+的水解平衡都正向移動,硫酸銅溶液的pH降低.升溫促進CH3COO-水解,c(OH-)增大,但pH不一定也增大,因為升溫也同時促進了水的電離,Kw增大,當Kw增大幅度大于c(OH-)的增大幅度時也增大,pH=,故pH減小,選項D錯誤.答案為C.
【要點歸納】在銅鹽溶液中存在Cu2++2H2O?Cu(OH)2+2H+,升高溫度,水解平衡向右移動,水解程度增大;隨著溫度升高,水的電離程度也增大.
7 從催化劑角度來復習
【教材尋源】人教版《選修4》第23頁“科學探究1”中硫酸銅作過氧化氫分解的催化劑.
【高考鏈接】(2019年全國卷Ⅲ,節選)近年來,隨著聚酯工業的快速發展,氯氣的需求量和氯化氫的產出量也隨之迅速增長.因此,將氯化氫轉化為氯氣的技術成為科學研究的熱點.
Deacon直接氧化法可按下列催化過程進行:
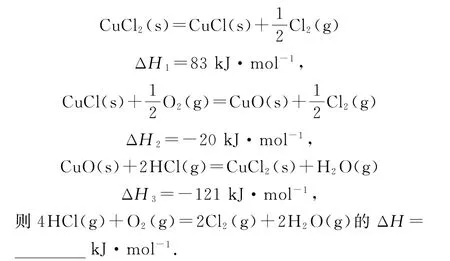

把上述反應分別標為反應①、②、③,根據蓋斯定律,反應4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g)由(反應①+反應②+反應③)×2所得,所以ΔH=(ΔH1+ΔH2+ΔH3)×2=-116 kJ·mol-1.
【要點歸納】本題設計的目的是考查化學反應與能量變化,借助CuCl2作催化劑來加快反應速率.
8 從化學實驗角度來復習
【教材尋源】人教版《必修1》第101頁,實驗4-9中濃硫酸與銅的反應.
【高考鏈接】(2019年北京卷,節選)化學小組實驗探究SO2與Ag NO3溶液的反應.
實驗一:用圖4所示裝置(夾持、加熱儀器略)制備SO2,將足量SO2通入Ag NO3溶液中,迅速反應,得到無色溶液A和白色沉淀B.

圖4
①濃H2SO4與Cu反應的化學方程式是_________.
②試劑a是_________.

Cu和濃硫酸反應,生成的二氧化硫氣體中混有酸霧,會對后面的實驗造成干擾,故需要用飽和Na HSO3溶液進行洗氣.答案為①Cu+;②飽和Na HSO3溶液.
【要點歸納】有關銅及其化合物的實驗較多,往往與銅的氧化還原反應及離子反應同時出現.如銅和硝酸反應、氫氣還原氧化銅、氨氣還原氧化銅、制取硝酸銅、制取硫酸銅、銅綠受熱分解、五水硫酸銅受熱分解曲線等.通過對實驗的分析可以進一步理解銅及其化合物的性質.
9 從難溶電解質的角度來復習
【教材尋源】人教版《選修4》第65頁,表3-5硫化銅和氫氧化銅的溶度積.
【高考鏈接】(2017年全國卷Ⅲ)在濕法煉鋅的電解循環溶液中,較高濃度的Cl-會腐蝕陽極板而增大電解能耗.可向溶液中同時加入Cu和CuSO4,生成CuCl沉淀從而除去Cl-.根據溶液中平衡時相關離子濃度的關系圖(如圖5),下列說法錯誤的是( ).
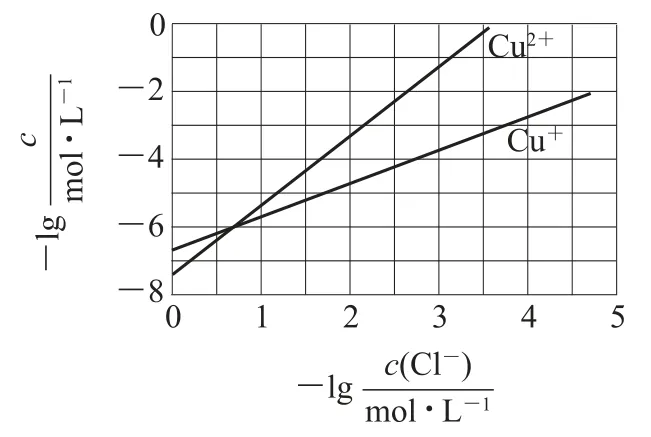
圖5
A.Ksp(CuCl)的數量級為10-7
B.除去Cl-的反應為Cu+Cu2++2Cl-=2CuCl
C.加入Cu越多,Cu+濃度越高,除去Cl-的效果越好
D.2Cu+=Cu2++Cu平衡常數很大,反應趨于完全

觀察圖象可知,當橫坐標為0時,c(Cl-)=1 mol·L-1,再看Cu+曲線對應的縱坐標為-6.7,lgc(Cu+)=-6.7,c(Cu+)=10-6.7mol·L-1,Ksp(CuCl)=c(Cl-)c(Cu+)=1×10-6.7=10-6.7=100.3×10-7,100.3為大于1小于10的一個數(100<100.3<101),所以Ksp(CuCl)的數量級為10-7,選項A說法正確;銅、硫酸銅以及氯離子發生反應,生成CuCl沉淀,反應的離子方程式應為Cu+Cu2++2Cl-=2CuCl,選項B說法正確;反應Cu+Cu2++2Cl-=2CuCl的效果也取決于Cu2+的量,如果Cu2+不足,即使加入再多Cu也不會改變除去Cl-的效果,選項C說法錯誤;平衡常數K的數值越大,反應程度越大,2Cu+=Cu2++Cu的平衡常數很大,說明反應趨于完全,選項D說法正確.答案為C.
【要點歸納】根據難溶電解質的溶解平衡及沉淀的轉化,利用CuCl的難溶性可以除去溶液中的Cl-.也可以利用水解平衡原理通過加入氧化銅或碳酸銅的方法除去溶液中的Fe3+.
10 從環保的角度來復習
【教材尋源】人教版《必修1》第20頁復習題第8題,從工業廢水中回收硫酸亞鐵和銅.人教版《選修4》第62頁最后一句:“以Na2S、H2S等作沉淀劑,使某些金屬離子如Cu2+、Hg2+等,生成極難溶的硫化物CuS、HgS等沉淀,也是分離、除去雜質常用的方法”.
【高考鏈接】(2017年天津卷)下列有關水處理方法不正確的是( ).
A.用石灰、碳酸鈉等堿性物質處理廢水中的酸
B.用可溶性的鋁鹽和鐵鹽處理水中的懸浮物
C.用氯氣處理水中的Cu2+、Hg2+等重金屬離子

氯氣不能和Cu2+、Hg2+反應生成沉淀,用氯氣不能除去水中的Cu2+、Hg2+等重金屬離子,選項C說法錯誤;其余選項說法均正確.答案為C.
【要點歸納】水中含有較多的Cu2+時,會造成水體污染,需要加入Na2S等物質把銅離子變成沉淀除去后達到標準才能排放.
11 從物質結構的角度來復習
【教材尋源】人教版《選修3》第14頁注釋,銅的電子排布;第42頁實驗2-2硫酸銅和氨水反應;第76頁資料卡片,金屬晶體的堆積模型對比.
【高考鏈接】(2019年江蘇卷,節選)Cu2O廣泛應用于太陽能電池領域.以CuSO4、NaOH和抗壞血酸為原料,可制備Cu2O.
(1)Cu2+基態核外電子排布式為_________.
(2)Cu2+與OH-反應能生成[Cu(OH)4]2-,[Cu(OH)4]2-中的配位原子為________(填元素符號).
(3)1個Cu2O晶胞(如圖6)中,Cu原子的數目為_____.

(1)Cu原子的價電子排布為3d104s1,Cu原子失去2個電子變為Cu2+,所以基態Cu2+的核外電子排布式為1s22s22p63s23p63d9;(2)在[Cu(OH)4]2-中,Cu2+提供空軌道,OH-中的O原子提供孤對電子,所以[Cu(OH)4]2-的配位原子為O原子;(3)1個Cu2O晶胞中,頂點和體心的白色原子的數目為1+8×1/8=2,位于內部的黑色原子的數目為4,根據化學式Cu2O可知,Cu原子的數目為4.
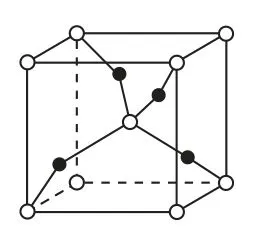
圖6
【要點歸納】在結構化學中,銅原子的電子排布式、電子排布圖、銅離子形成的配位化合物以及和銅有關的晶胞都是高考的重點.
12 從有機化學角度來復習
【教材尋源】人教版《必修2》第74頁實驗3-3,銅作催化劑乙醇被氧氣氧化;人教版《必修2》第79頁實驗3-5,葡萄糖被新制氫氧化銅氧化;人教版《選修5》第57頁實驗3-6,乙醛被新制氫氧化銅氧化.


【要點歸納】1)銅作催化劑的條件下乙醇可以被氧氣氧化為乙醛:
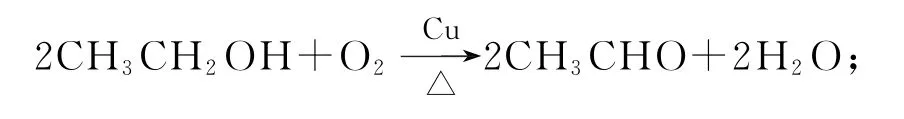
2)新制的堿性氫氧化銅懸濁液,可以與含有醛基的醛類、甲酸、甲酸某酯類、甲酸鹽以及葡萄糖等發生反應,例如,CH3CHO+2Cu(OH)2+Cu2O↓+3H2O+CH3COONa.利用這個性質可以檢驗醛基.
總之,關于銅及其化合物的知識在高考中屢屢出現,只要我們復習時從不同角度分析總結,抓住重點,抓住主干,構建銅的知識網絡,可以達到事半功倍的復習效果.
鏈接練習
1.(2020年全國卷Ⅱ)北宋沈括《夢溪筆談》中記載:“信州鉛山有苦泉,流以為澗.挹其水熬之則成膽礬,烹膽礬則成銅.熬膽礬鐵釜,久之亦化為銅.”下列有關敘述錯誤的是( ).
A.膽礬的化學式為CuSO4
B.膽礬可作為濕法冶銅的原料
C.“熬之則成膽礬”是濃縮結晶過程
D.“熬膽礬鐵釜,久之亦化為銅”是發生了置換反應
2.(2020年全國卷Ⅲ)宋代《千里江山圖》描繪了山清水秀的美麗景色,歷經千年色彩依然,其中綠色來自孔雀石顏料(主要成分為Cu(OH)2·CuCO3),青色來自藍銅礦顏料(主要成分為Cu(OH)2·2CuCO3).下列說法錯誤的是( ).
A.保存《千里江山圖》需控制溫度和濕度
B.孔雀石、藍銅礦顏料不易被空氣氧化
C.孔雀石、藍銅礦顏料耐酸耐堿
D.Cu(OH)2·CuCO3中銅的質量分數高于Cu(OH)2·2CuCO3
鏈接練習參考答案
1.A 2.C

