頸動脈CT 斑塊特征與頸動脈支架成形術后新發腦缺血灶的相關性
季愛華 林 江 唐 驍 郭大喬 呂 鵬△
(1復旦大學附屬中山醫院放射科,3血管外科 上海 200032;2上海市影像醫學研究所 上海 200032)
近年來頸動脈支架成形術(carotid artery stenting,CAS)已經逐步應用于臨床,可部分替代頸動脈內膜切除術(carotid endarterectomy,CEA)用于治療頸動脈粥樣硬化狹窄。Sardar 等[1]的研究顯示,多項隨機前瞻性研究結果表明CAS 在防治頸動脈粥樣硬化引起的腦卒中方面與CEA 能力相當。
CAS 術后顱內DWI-MRI 顯示的新發腦缺血灶(new brain ischemic lesion,NBIL)是常見并發癥。CAS 術后出現新發腦缺血梗死灶提高了患者遠期腦血管缺血事件的再發率[2],也與CAS 術后認知功能下降[3]和癡呆[4]的發生密切相關。
顱內缺血梗塞灶的發生主要是支架置入頸動脈的過程中頸動脈斑塊脫落所致,而這又與頸動脈斑塊特征關系密切。Yoshimura 等[5]利用TOFMRI 序列識別斑塊內出血(intraplaque hemorrhage,IPH),并得出IPH 斑塊CAS 術后發生NBIL 的風險更大,據此建議含IPH 斑塊患者盡量選擇CEA 手術。Chung 等[6]對IPH 較敏感的重T1 序列分析后,認為IPH 與CAS 術后發生NBIL 無關。但是,Yoshimura 等[5]TOF 序列識別IPH 的準確率不高,以上研究均只涉及MRI 圖像上IPH 單個因素的定性研究。Stojanov 等[7]的研究顯示,CTA 圖像上的纖維脂質斑塊較纖維鈣化斑塊CAS 在術后出現的NBIL 數量更多。但以上研究只按有無鈣化粗略分組,沒有細致對斑塊的成分及相關特征進行分析。
既往缺乏系統和定量化地研究斑塊內各種成分及位置,且CT 相關研究甚少。而頸動脈CT 血管成像(computed tomography angiography,CTA)簡便易行,在臨床中應用廣泛。CT 不僅能夠準確評價頸動脈狹窄程度,還能清晰顯示頸動脈斑塊的表面形態、區分鈣化斑塊與非鈣化斑塊[8-9],檢測鈣化斑塊的敏感度為100%[10]。因此,本研究旨在通過頸動脈CTA 成像定量及綜合分析多種斑塊特征,探索CTA 斑塊特征與CAS 術后NBIL 之間的相關性。
資料和方法
研究對象回顧性分析2015 年1 月至2019 年10 月于復旦大學附屬中山醫院行頸動脈支架手術治療的頸動脈狹窄患者。納入標準:(1)擬行CAS手術;(2)癥狀性頸動脈狹窄≥50%或非癥狀性頸動脈狹窄≥70%。排除標準:(1)血管炎、夾層等非粥樣硬化疾病導致的頸動脈狹窄;(2)血管閉塞;(3)頸動脈狹窄術后再狹窄;(4)CT 檢查禁忌證。
所有患者均于術前2 周內接受頸動脈CTA 檢查,術前1 周內接受頭顱DWI-MRI 檢查,期間患者無一過性腦缺血發作或腦卒中等新發缺血事件發生。術后72 h 內接受頭顱DWI-MRI 復查。研究由本院醫學倫理委員會批準(倫理號:B2014-004),所有患者均于檢查前簽署知情同意書。
頸動脈CTA 檢查所有檢查均在佳能320CT(Aquilion ONE)上完成。掃描范圍為自主動脈根部到顱頂,掃描參數為:管電壓140 kV,管電流80 mAs,螺距為0.6 mm,球管旋轉時間為0.5 s/圈,層厚為1 mm。使用非離子型對比劑(碘必樂,I 370 mg/mL),根據患者體重計算對比劑總量,男性為75~80 mL,女性為65~75 mL。雙筒高壓注射器,經肘靜脈注入造影劑,注射流率為4~5 mL/s,隨后注射生理鹽水約25~30 mL。采用團注追蹤程序自動觸發技術,觸發掃描點位置定在主動脈弓,閾值設為100 Hu。
頭顱DWI-MRI 檢查頭顱3T DWI 具體參數為:TR/TE 6400/86.0 ms,層厚5 mm,層間距1.5 mm,b 值為0 和1 000 s/mm2,FOV 220 mm×220 mm。掃描時間為46 s。
CAS 手術過程所有CAS 手術均由同一組的血管外科團隊操作。所有患者術前1 周內開始口服腸溶阿司匹林(100 mg/d)和氯吡格雷75 mg/d,所有患者均行全身麻醉、經股動脈入路。通過頭頸部血管造影評估顱內大腦半球血流狀態、頸動脈狹窄程度及斑塊表面形態。腦保護傘釋放到位后進行頸動脈狹窄的預擴,所有患者在路徑圖模式下釋放腦保護傘及頸動脈支架,殘余狹窄≤30%。本研究應用了3 種腦保護裝置:Emboshield NAV6(美國Abbott 公司),Filterwire EZ(美國Boston Scientific公司),Spider FX(美國Medtronic 公司);4 種支架:RX Acculink(美國Abbott 公司),Wallstent(美國Boston Scientific 公司),Precise(美國強生Cordis 公司),Protege(美國ev3 公司)。支架置入后即行血管造影,確認頸動脈遠端有無新發栓塞,確保支架術后殘余狹窄≤30%。
圖像分析
頸動脈狹窄程度 參照NASCET 標準[11]:Ⅰ級(1%~29%),輕度狹窄;Ⅱ級(30%~49%)和Ⅲ級(50%~69%),中度狹窄;Ⅳ級(70%~99%),重度狹窄;Ⅴ級,閉塞。頸動脈斑塊病變長度:將斑塊長度定義為沿頸動脈長軸的病變范圍。
不同類型斑塊的分類標準 軟斑塊CT 值<60 HU,混合斑塊CT 值為60~130 HU,鈣化斑塊CT值>130 HU[12]。
斑塊表面形態學分類 根據文獻[8]將頸動脈斑塊的表面形態分為光滑、不規則以及潰瘍3 種類型。潰瘍定義為斑塊表面局限性內膜缺損,寬度≥1 mm,CTA 上表現為突向斑塊內的小龕影,深度至少為1 mm[13]。
鈣化分類標準 根據管腔最窄處鈣化斑塊的位置將鈣化斑塊分為3 組:(1)內膜鈣化組,鈣化緊貼血管管腔面;(2)中間鈣化組,鈣化介于管腔面、血管外膜之間的斑塊;(3)外膜鈣化組,鈣化位于血管腔外膜處。鈣化范圍分為5 級:0 級,無鈣化;1級,鈣化范圍<1/4 血管圓周;2 級,鈣化范圍界于血管圓周的1/4~1/2;3 級,鈣化范圍界于血管圓周的1/2~3/4;4 級,鈣化范圍>3/4 血管圓周。
頸動脈斑塊圖像后處理所有CTA 原始圖像上傳至佳能工作站,利用Viteafx 6 軟件進行后處理,軟件自動勾畫出斑塊層面血管管腔和管壁,自動識別各類型斑塊。橫斷面勾畫出管壁區域及斑塊成分后手動修改,軟件自動計算出斑塊總體積、長度、最大面積及最大厚度。記錄并測量鈣化斑塊的范圍、大小及位置,觀察并記錄斑塊表面形態。
統計學分析采用SPSS 21.0 軟件進行統計學分析。連續型變量用描述,應用獨立樣本t檢驗。分類變量用百分比表達,應用χ2檢驗。所有潛在危險因素進行單因素分析后,將P<0.05 的因素納入多因素回歸分析模型計算出預測CAS 術后出現NBIL 的獨立危險因素。P<0.05 為差異有統計學意義。
結果
臨床基本資料共有127 例擬行CAS 治療的頸動脈狹窄患者滿足入組標準,其中4 例患者因圖像質量欠佳而被排除,最終共納入患者123 例,其中男性107 例,女性16 例;年齡48~86 歲,平均(67.97±6.96)歲。所有患者均成功實施CAS 手術,1 例患者術后出現視網膜動脈栓塞,無患者圍手術期出現心肌梗死或死亡等嚴重并發癥。
患者術后3 天內復查頭顱DWI-MRI 顯示61 例NBIL(61/123,49.6%)。顱內NBIL 共142 灶,9 例患者出現雙側顱內NBIL。根據CAS 術后有無NBIL 將患者分為NBIL(+)組及NBIL(-)組,兩組患者臨床基本資料見表1。
單因素和多因素回歸分析NBIL(+)組內有癥狀患者36 例(59.0%),NBIL(-)組內有癥狀患者35 例(56.5%),兩組間差異無統計學意義。同時兩組患者基本臨床資料,包括缺血性心腦血管疾病、高血壓、糖尿病的發病率、是否吸煙、主動脈弓類型、腦保護裝置類型、支架類型的分布差異均無統計學意義。CTA 共檢測出19 例斑塊潰瘍。CTA 所示斑塊特性中斑塊體積、斑塊長度、斑塊表面形態的差異均無統計學意義(表1)。
NBIL(+)組鈣化總體積與NBIL(-)組比較差異無統計學意義[(225.40±179.35)mm3vs.(192.69±162.94)mm3],而NBIL(+)組最窄處鈣化厚度大于NBIL(-)組[(1.79±1.38)mmvs.(1.38±0.83)mm,P=0.020]。NBIL(+)組內膜鈣化的概率明顯高于NBIL(-)組(34.4%vs.8.1%,P=0.002)。1 例術后出現右側額葉NBIL(圖1)。將以上兩者納入多因素回歸分析模型中,并校正年齡、性別及斑塊患側因素,分析得出與無鈣化斑塊相比內膜鈣化斑塊(OR=15.65,95%CI:1.34~98.75,P=0.028)及斑塊最狹窄處鈣化厚度(OR=1.35,95%CI:1.01~2.10,P=0.045)是預測CAS 術后NBIL 的獨立危險因素(表2)。而外膜鈣化斑塊及中間鈣化斑塊與CAS 術后NBIL 的發生無明確相關性。
表1 NBIL(+)組和NBIL(-)組患者臨床基本資料和CT 斑塊特征比較Tab 1 Patient clinical information and CT features between NBIL(+)group and NBIL(-)group[n(%)or]
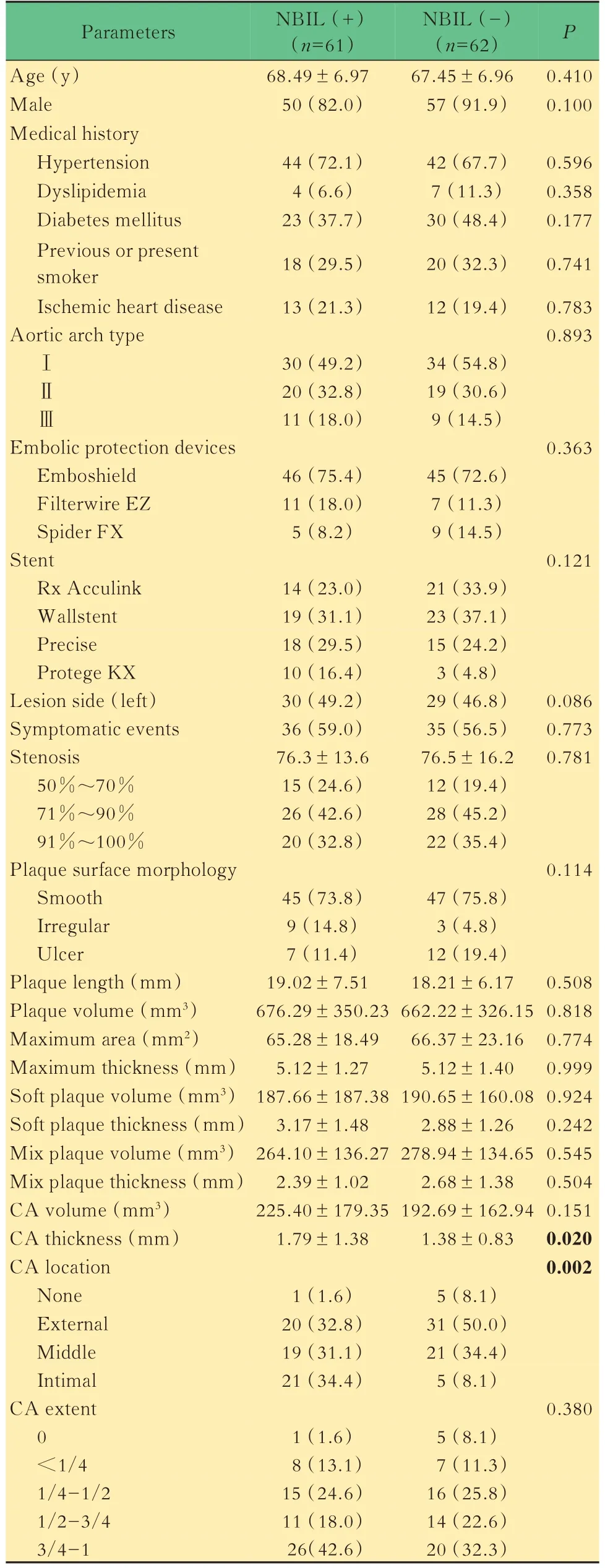
表1 NBIL(+)組和NBIL(-)組患者臨床基本資料和CT 斑塊特征比較Tab 1 Patient clinical information and CT features between NBIL(+)group and NBIL(-)group[n(%)or]
狹窄處鈣化厚度預測NBIL 的ROC 曲線分析斑塊最窄處鈣化厚度預測NBIL 的ROC 曲線下面積是0.726(圖2),臨界值為1.75 mm,特異性為88.7%,敏感性為57.4%。陽性預測值為83.3%,陰性預測值為67.9%。
討論
CAS 手術因創傷小、術后恢復快、無顱神經麻痹的風險以及術后心血管并發癥發生率較低在臨床的應用越來越廣泛。但Cho 等[14]通過Meta 分析得出CAS 組術后出現NBIL 的概率明顯高于CEA組(37.4%vs.13.0%),同時CAS 組術后發生腦卒中及一過性腦缺血事件的概率也高于CEA 組(4.1%vs.1.8%)。因此,術前評估CAS 手術的安全性并調整治療方案降低術后NBIL 的發生是必要的。
本研究中,我們利用CTA 分析得出CAS 術后NBIL 的發生與狹窄處鈣化的位置及厚度相關。當鈣化斑塊位于管腔內膜時,CAS 術后發生NBIL 的比例為34.4%,發生NBIL 的風險是無鈣化病灶的約15 倍。當狹窄處鈣化厚度以1.75 mm 作為預測CAS 術后NBIL 發生的界值時,其具有較高的特異性(83.3%)和陽性預測值(88.7%)。斑塊的其他易損因素,如脂質壞死核心、薄的或破損纖維帽等,也有可能參與形成CAS 術后NBIL,導致狹窄處鈣化厚度單因素的預測敏感度較低(57.3%)。

圖1 1 例頸動脈內膜鈣化患者CAS 術后出現NBILFig 1 NBIL of a patient with intimal calcified carotid plaque after CAS

表2 單因素及多因素Logistic 回歸分析CAS 術后NBIL 相關因素Tab 2 Factors related to NBIL after CAS predicted by univariate and multivariate Logistic regression analysis

圖2 狹窄處鈣化厚度預測CAS術后NBIL 的ROC 曲線分析Fig 2 The ROC of the CA thickness for the predicton of NBIL after CAS
既往臨床研究結果顯示,鈣化斑塊是頸動脈斑塊的穩定成分、不易自發破裂,頸動脈斑塊鈣化患者較無鈣化患者較少表現出腦卒中等腦缺血癥狀[15]。但對于CAS 手術,鈣化斑塊會使支架擴展不充分、產生遠端栓塞,且術后易產生持續性低血壓、術后再狹窄、支架斷裂等嚴重并發癥[16]。而鈣化斑塊是否會引起CAS 術后顱內NBIL 的研究較少且結論存在爭議[7,17-19]。Stojanov 等[7]的研究顯示,CTA 圖像上的纖維脂質斑塊較纖維鈣化斑塊CAS術后出現的NBIL 數量更多。AbuRahma 等[18]的研究結果則顯示,重度鈣化組(鈣化范圍超過周長的1/2)在術后30 天內發生腦卒中的概率為6.3%,而無鈣化或輕中度鈣化組的概率為1.2%。Setacci等[20]的研究得出類似結論,即病灶處鈣化組圍手術期發生腦卒中的概率大于無鈣化組(6.5%vs.2.3%)。以上研究在考慮鈣化因素時,或沒有對鈣化進行明確的定量,或沒有考慮鈣化位置的因素。本研究對鈣化斑塊成分進行了定性定量分析,明確了鈣化位置的重要性,提示位于內膜的鈣化及鈣化厚度是CAS 的危險因素。
重度鈣化斑塊增加了CAS 術中預擴、釋放腦保護裝置(embolic protection device,EPD)、支架定位、支架擴張等操作技術上的難度[19]。在重度狹窄斑塊病例中,通常需對病變處進行漸進性預擴,先使用較小直徑(2 mm)球囊進行預擴,以降低斑塊破裂、遠端栓塞的概率。而重度鈣化斑塊病例則需要使用更大直徑的球囊(5 mm)進行預擴,確保隨后支架能夠順利到位。預擴時重度鈣化斑塊需要更大的球囊壓力來克服鈣化斑塊的擠壓,鈣化斑塊受到的壓力增大,增加了鈣化斑塊碎屑脫落的風險。重度鈣化也增加了EPD 通過斑塊的技術難度,使EPD無法順利通過病變位置。在支架擴張時,由于病變處鈣化、局部血管壁僵硬,導致血管壁與支架貼覆不完全,斑塊局部壓力增大[18],可造成支架內栓子形成,或支架內再狹窄及局部支架斷裂。Barrett等[21]通過體外模型試驗得出頸動脈斑塊處增大的鈣化體積將降低斑塊拉伸力,會增加支架在置入頸動脈時斑塊破裂的風險。而在支架置入過程中形成的較堅硬的鈣化碎片更容易通過過濾器的孔隙導致遠端顱內微栓塞的形成[22]。本研究中鈣化體積在兩組間的差異無統計學意義,提示單純的鈣化成分定量分析仍不能預測NBIL 發生,位于中層或外膜的鈣化亦可形成較大體積的鈣化。而位于狹窄處內膜粗大鈣化直接承受球囊擴張、支架擴張時施加于斑塊的壓力,更易造成斑塊碎片脫落,導致遠端顱內微栓子形成。
我們的研究存在一些局限性。首先,鑒于CT無法準確地區分斑塊內纖維組織、脂質核心、疏松基質、斑塊內出血、纖維帽的成分,未對上述因素進行更細致的統計分析,在今后的研究中可聯合MRI斑塊序列共同分析斑塊各項特征;其次,本項研究為單中心研究,仍需要更大的樣本量及多中心研究來進一步驗證鈣化斑塊預測CAS 術后發生NBIL的能力;再次,研究對象為CAS 手術患者,存在一定的入院偏倚;最后,研究對象為CAS 手術患者,無法獲得斑塊病理標本進行病理對照研究。
頸動脈鈣化位置及鈣化厚度與CAS 術后發生NBIL 相關。因此,在頸動脈支架術前CTA 檢查中如檢測出內膜鈣化、狹窄處鈣化厚度大于1.75 mm時,應評估患者全身狀態,謹慎選擇手術方式以降低術后心腦血管缺血事件的發生。

