氨基苯磺酸鋁催化苯乙酮、芳香醛和芳香胺的反應
畢曉雪
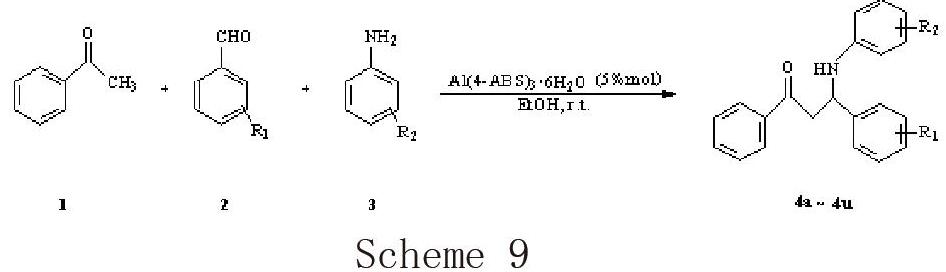
一、引言
(一)β-氨基酮Mannich反應簡介
一直以來,Mannich反應都是合成含氮化合物的最為常用的反應之一。人們對Mannich反應的興趣在于,Mannich反應產物(又叫Mannich堿)不僅在藥物、農藥、染料、調料、涂料、炸藥等方面有著廣泛的用途,而且還是有機化學中合成天然生物活性分子的重要中間體[1]。酮、醛、胺三組分合成β-氨基酮的反應是最為典型的一類Mannich反應
(二)合成β-氨基酮Mannich的方法
1. 濃HCl/EtOH作催化劑
采用HCl作催化劑所形成的鹽酸鹽極不穩定,易分解而變紅,受熱或暴露在空氣中更會加速其分解[7]。同時,濃HCl等質子酸往往是有毒、有腐蝕性的,并且反應完成以后很難實現回收利用,這就必然導致酸性廢物的排放和對環境的污染。
2. 新型催化劑
(1) Yb(OTf)3催化
王利民等取苯乙酮(2 mmol)、芳香醛(2 mmol)和芳香胺(2 mmol)加入到單口燒瓶中, 稱取Yb(OTf)3 (0.062 g, 5 mol%)加入反應燒瓶中, 加入3 mL乙醇, 室溫下攪拌8~14 h,有大量固體析出, 過濾得粗產物. 將濾液中乙醇真空旋出, 加入3 mL去離子水和3 mL乙酸乙酯溶解,分液,將水蒸干以回收催化劑。乙酸乙酯蒸干的粗產物,合并得到固體用乙醇重結晶, 得到相應的產物,其產率高達91%。
(2) 雜多酸催化
Najmodin Azizi等人用醛3(mmol),胺3.1(mmol),丁酮5(mmol),苯乙酮3(mmol)以及磷鎢酸(0.02 g)進行反應.
(三)論文選題及方向
本論文討論在50 mL反應瓶中加入11 mmol苯乙酮,10 mmol芳香醛,10 mmol芳胺,0.3 mmol Al(4-ABS)3·6H2O,5 mL乙醇,考察苯乙酮、芳香醛和芳香胺在在上述反應條件下的一鍋法”Mannich”反應。
二、實驗部分
(一)反應方程式
(二)實驗儀器
熔點用RY-1型顯微熔點儀測定;
紅外光譜用美國VARIAN公司Scimitar 2000型光譜儀測定(KBr壓片);
核磁共振譜用Bruker ARX-600型核磁共振儀測定,DMSO-d6作溶劑,TMS作內標;
Agilent 1100系列LC/MSD VL ESI型質譜儀。
(三)合成反應
在50 mL反應瓶中加入11 mmol苯乙酮,10 mmol芳香醛,10 mmol芳香胺,0.3 mmol Al(4-ABS)3·6H2O,5 mL乙醇,在室溫下攪拌反應(TLC跟蹤反應進程),有大量固體析出。反應結束后,室溫干燥(充分揮發乙醇和水),分兩次加入60 mL熱CH2Cl2溶解產物,趁熱過濾,濾出的催化劑用CH2Cl2洗滌干燥后,直接用于下一次催化反應;有機相依次用10 mL飽和NaHCO3洗滌2次,再用無水Na2SO4干燥,蒸發溶劑得到粗產物。粗產物進一步用乙醇或乙醇-丙酮重結晶,得到的產品用IR, 1H NMR及質譜進行表征。
三、結果與討論
(一)Al(4-ABS)3·6H2O催化的Mannich反應條件的優化
以苯乙酮、苯甲醛(10 mmol)、苯胺(10 mmol)三組分Mannich反應為例,考察苯乙酮、催化劑和乙醇用量對產率的影響,反應時間5 h,其結果見表1。隨著苯乙酮用量的增加,產率逐漸升高,當苯乙酮用量高于11 mmol時,產率提高不明顯,因此,苯乙酮用量為11 mmol適宜(反應序號1-3)。催化劑用量對產率的影響較大,當其用量低于3 mol%時(基于苯甲醛用量,下同),隨著催化劑用量的增加,產率提高較大,當催化劑的用量高于3 mol%時,隨著催化劑用量的繼續增加,產率提高不明顯,因此選擇催化劑的用量為3 mol%(反應序號2, 4, 5)。此外,溶劑用量對反應有顯著影響,乙醇用量為5 mL時,產率最高,減少或增加乙醇用量,產率反而降低(反應序號2, 6, 7)。因此,較佳反應條件為苯乙酮、苯甲醛、苯胺摩爾比為1.1:1:1,Al(4-ABS)3·6H2O 3 mol%,乙醇5 mL。實驗中也考察了Al(4-ABS)3·6H2O的回收使用情況,將Al(4-ABS)3·6H2O重復使用4次,催化活性無明顯下降(反應序號2)。
(二)Al(4-ABS)3·6H2O對不同底物Mannich反應的催化效果
在較佳反應條件下,考察Al(4-ABS)3·6H2O對苯乙酮、芳香醛和芳香胺三組分“一鍋法”Mannich反應的催化效果,實驗結果見表2。可以看出,苯乙酮、苯甲醛與間、對位連有弱供電子基的芳香胺反應時,時間短,產率較高(4c, 4d);而與間、對位上連有強吸電子基或強供電子基的芳香胺反應時,反應時間相對較長(4e-4i)。同時,芳香胺上取代基位置對產率有影響。苯乙酮、苯甲醛與鄰氯苯胺的反應,由于鄰位取代時,空間位阻較強,經過較長時間,只獲得中等產率(4b);間、對位取代,對產率影響不大。
此外,苯乙酮、苯胺與取代芳香醛的反應,無論芳香醛的芳環上連有供電子基還是吸電子基,反應都可以順利進行(4j-4m)。當底物醛為4-OHC6H4CHO時,經過30小時,產率僅為15%(4n)。這可能是由于對羥基苯甲醛存在著醌式結構和醛式結構的平衡,羥基的強供電子作用導致醛基鈍化。
(三)催化反應機理
關于Mannich反應機理,一般認為,首先是芳香醛與芳香胺生成亞胺鹽中間體I,該中間體作為親電試劑去進攻酮的烯醇式II[23]。對本實驗Al(4-ABS)3·6H2O中的S=O有較強的雙鍵性質,在苯環的電子誘導和電子離域作用下,Al(4-ABS)3·6H2O具有強Lewis酸性,可使第一步生成的亞胺中間體更穩定,有利于I進攻酮的烯醇式II,使反應順利進行。另外,Al(4-ABS)3·6H2O分子中具有芳環結構,使催化劑與底物接觸更充分,有利于反應的進行。
四、結論
與已報道的文獻合成方法相比,Al(4-ABS)3·6H2O催化的苯乙酮、芳香醛、芳香胺三組分“一鍋法”Mannich反應,具有反應條件溫和、產率高、催化劑催化活性好、操作簡單等優點,避免了傳統合成方法使用強酸作催化劑的不足。為β-氨基酮衍生物的合成提供了新途徑,符合綠色化學要求,有潛在的應用前景。

