超聲引導下胸神經Ⅱ阻滯對乳腺癌根治術患者鎮痛效果及并發癥的影響
周一鳴,惠康祥,曹文珺,涂立剛
信陽市中心醫院麻醉科,河南 信陽 464000
乳腺癌是起源于乳腺上皮組織的惡性腫瘤,其中99%發生于女性,僅1%發生于男性,相關調查報道,如今中國乳腺癌發病率居女性惡性腫瘤首位[1]。乳腺癌根治術是乳腺癌臨床常用的術式,手術主要清掃腋窩淋巴結,并保留外側胸神經、胸大肌及胸小肌,但手術對患者機體創傷較大,應激反應強烈,患者術后常發生肩部活動受限及急性劇烈疼痛,所以有效、合理的鎮痛措施有助于穩定患者各項生命體征,減輕患者疼痛感,避免術后并發癥[2]。胸椎旁神經(thoracic paravertebral nerve,TPVN)阻滯廣泛應用于乳腺癌根治術后鎮痛,但患者多表現腋窩和上臂疼痛不適,原因可能是TPVN阻滯無法有效阻滯胸內側、外側神經及胸長神經、胸背神經,導致鎮痛不完全,同時,TPVN阻滯伴有較高的氣胸、脊神經損傷、低血壓等并發癥發生率[3-4]。胸神經(pectoral nerves,Pecs)阻滯則是在胸大肌與胸小肌之間、胸肩峰動脈胸肌支旁注入局部麻醉藥,能夠有效阻滯胸內側、外側神經。近年來國外相關學者提出,PecsⅡ阻滯適用于乳腺癌全切術及腋窩淋巴結清掃,不僅能夠阻滯支配T2~6乳腺皮區的肋間神經外側皮支,還可阻滯胸長神經、胸背神經及肋間臂神經[5-6]。目前臨床關于兩種阻滯方式對乳腺癌根治術患者的效果比較尚存在爭議,基于此,本研究回顧性分析80例乳腺癌根治術患者的病歷資料,探討比較超聲引導下TPVN阻滯與PecsⅡ阻滯對乳腺癌根治術患者鎮痛效果、麻醉用量及術后并發癥的影響,以期為臨床選取合適的阻滯方式提供參考,現報道如下。
1 資料與方法
1.1 一般資料
收集信陽市中心醫院2018年1月至2019年1月收治的行乳腺癌根治術患者的病歷資料。納入標準:符合《中國晚期乳腺癌臨床診療專家共識2016》[7]中乳腺癌相關診斷標準;術前經病理組織學或細胞學檢查確診;美國麻醉醫師協會(American Society of Anesthesiologists,ASA)[8]分級為Ⅰ~Ⅱ級;未進行放療或化療;卡式功能狀態評分>70分;TNM分期為Ⅰ~Ⅱ期;病歷資料完整。排除標準:身體狀況較差;阻滯部位感染;合并其他惡性腫瘤;腫瘤多處轉移;造血系統、神經系統、消化系統及免疫系統疾病;凝血功能障礙;胃腸道、食管存在穿孔;過敏體質;精神疾病;心、肝、腎等重要器官嚴重功能不全或障礙;哺乳或妊娠期婦女;局部麻醉藥物過敏。根據納入、排除標準,共納入80例行乳腺癌根治術的患者,按乳腺癌根治術阻滯方式不同分為P組和T組。P組43例,均為女性,年齡30~65歲,平均(43.15±7.42)歲;ASA分級:Ⅰ級28例,Ⅱ級15例;腫塊位置:右側23例,左側20例;腫塊直徑1.5~3.5 cm,平均(2.12±0.69)cm;手術時間60~80 min,平均(71.22±6.49)min。T組37例,均為女性,年齡32~66歲,平均(42.97±8.02)歲;ASA分級:Ⅰ級26例,Ⅱ級11例;腫塊位置:右側20例,左側17例;腫塊直徑1.5~3.5 cm,平均(2.09±0.75)cm;手術時間60~80 min,平均(70.81±7.11)min。兩組患者年齡、ASA分級、腫塊位置、腫瘤直徑及手術時間比較,差異均無統計學意義(P>0.05),具有可比性。
1.2 治療方法
兩組患者進入手術室后均開放靜脈通道,常規監測生命體征。T組采用超聲引導下TPVN阻滯,患者取坐位,通過觸診尋找第3胸椎椎間隙,常規消毒后利用超聲探頭按照肋間走行在T3矢狀面上掃描,從而獲取胸膜、橫突及肋橫突韌帶的圖像;沿著探頭的外側緣緩慢進針,通過進針點注入2%利多卡因進行局部麻醉,利用短軸平面內技術推進針尖至肋橫突韌帶,注射2 ml生理鹽水后推進針尖至肋橫突韌帶,注入25 ml 0.5%羅哌卡因,回抽無血及腦脊液。P組采用超聲引導下PecsⅡ阻滯,患者取平臥位,手術側上臂呈外展位,于鎖骨中線部位的下方放置探頭以尋找腋靜脈及腋動脈,探頭沿著腋前線向外側移動至T3水平,獲取胸小肌與深部前鋸肌圖像;采用利多卡因進行局部浸潤麻醉,進針方法同T組,針尖由內向外,通過超聲圖像確保針尖位于前鋸肌與胸小肌之間,注入15 ml 0.5%羅哌卡因后將針尖推至胸大肌與胸小肌間隙,再次注入10 ml 0.5%羅哌卡因。
確認阻滯成功后,兩組患者均實施喉罩麻醉,以 1.5~2.0 μg/ml丙泊酚、0.1 μg/kg 舒芬太尼、0.15 mg/kg苯磺順阿曲庫銨作為麻醉誘導藥物,術中依據患者自身情況調節丙泊酚輸注效應室濃度,間斷性推注舒芬太尼維持麻醉效果,保持腦電雙頻指數為40~60。手術結束前,靜脈推注10 mg阿扎司瓊預防患者嘔吐。兩組患者術后均采用經靜脈自控鎮痛,靜脈注射曲馬多1~2 mg/kg作為術后自控鎮痛負荷劑量,術畢即刻接靜脈自控鎮痛泵(曲馬多400 mg+芬太尼0.2 mg+生理鹽水,總量為120 ml;設定劑量2 ml/h,患者自控鎮痛劑量每次2.0 ml,鎖定間隔時間15 min)。
1.3 觀察指標
①比較兩組患者術后鎮痛時間及術后24 h內麻醉藥物(舒芬太尼)使用量。②采用視覺模擬評分(visual analogue scale,VAS)[9]評估兩組患者術后1、5、8、12 h的疼痛程度,該評分通過患者主觀感受進行評價,分值0~10分,分值越高表明疼痛程度越強烈。③阻滯30 min后,由麻醉醫師采用針刺法檢測兩組患者第 2~6 胸椎(T2~T6)皮區節段痛覺減退情況。④比較兩組患者術后并發癥發生情況。
1.4 統計學方法
采用SPSS 21.0統計軟件進行數據分析,計數資料以例數及率(%)表示,兩組比較采用χ2檢驗和Fisher精確概率法;計量資料以均數±標準差(±s)表示,兩組比較采用兩獨立樣本t檢驗,多組比較采用重復測量方差分析,多組間兩兩比較采用SNK-q法;以P<0.05為差異有統計學意義。
2 結果
2.1 術后鎮痛時間及麻醉藥物用量的比較
P組患者術后鎮痛時間明顯長于T組,麻醉藥物用量明顯少于T組,差異均有統計學意義(P<0.01)。(表1)
表1 兩組患者術后鎮痛時間及麻醉藥物用量的比較(±s)
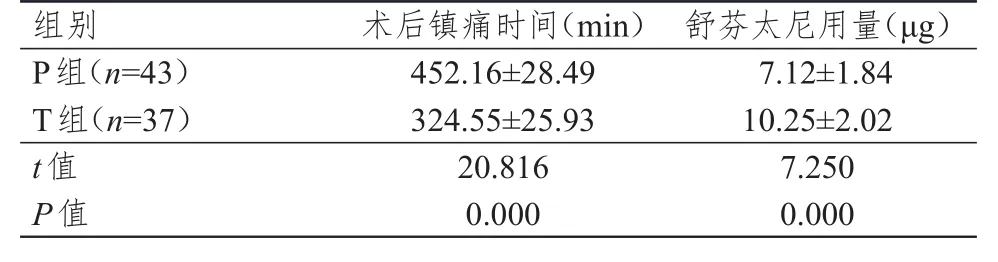
表1 兩組患者術后鎮痛時間及麻醉藥物用量的比較(±s)
組別P組(n=43)T組(n=37)t值P值452.16±28.49 324.55±25.93 20.816 0.000 7.12±1.84 10.25±2.02 7.250 0.000術后鎮痛時間(min) 舒芬太尼用量(μg)
2.2 術后疼痛情況的比較
術后1、5、8 h,P組患者VAS評分均明顯低于T組,差異均有統計學意義(P<0.01);術后12 h,兩組患者VAS評分比較,差異無統計學意義(P>0.05)。(表2)
表2 兩組患者術后VAS評分的比較(±s)
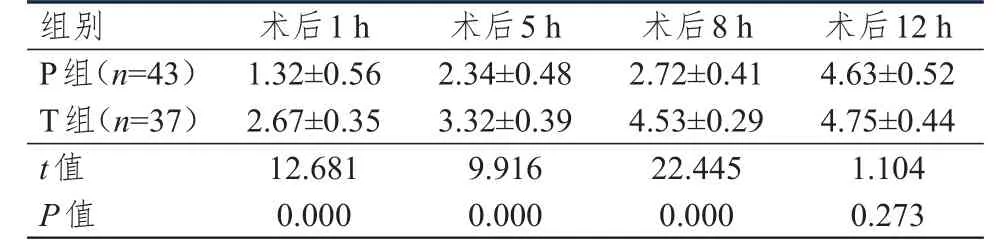
表2 兩組患者術后VAS評分的比較(±s)
組別P組(n=43)T組(n=37)t值P值1.32±0.56 2.67±0.35 12.681 0.000 2.34±0.48 3.32±0.39 9.916 0.000 2.72±0.41 4.53±0.29 22.445 0.000 4.63±0.52 4.75±0.44 1.104 0.273術后1 h 術后5 h 術后8 h 術后12 h
2.3 各胸段皮區痛覺減退情況的比較
兩組患者T3~T5節段皮區痛覺減退情況比較,差異均無統計學意義(P>0.05);P組患者T2節段皮區痛覺減退率高于T組,T6節段皮區痛覺減退率低于T組,差異均有統計學意義(P<0.05)。(表3)
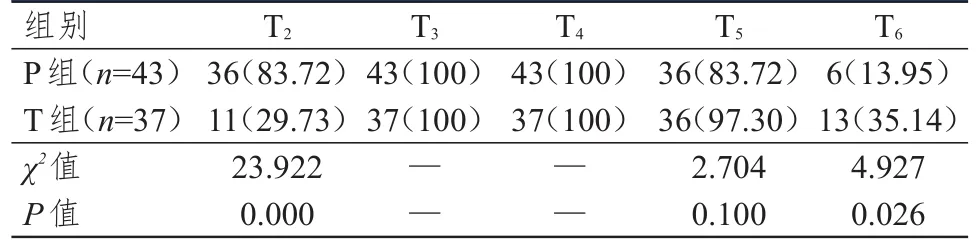
表3 兩組患者各胸段皮區痛覺減退情況的比較[n(%)]
2.4 并發癥發生率的比較
P組患者并發癥總發生率為2.33%(1/43),低于T組的21.62%(8/37),差異有統計學意義(P=0.010)。(表4)
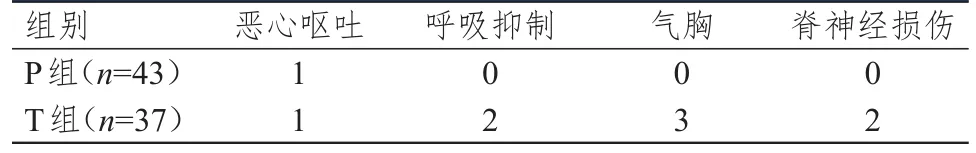
表4 兩組患者的并發癥發生情況
3 討論
乳腺癌根治術對患者機體創傷較大,相關研究證實,乳腺癌患者術后普遍存在中度以上急性疼痛,嚴重影響其術后恢復及生活質量[10]。TPVN阻滯是乳腺癌根治術后常用鎮痛方法,但研究表明,經TPVN阻滯的乳腺癌根治術后患者仍存在腋窩和上臂疼痛不適[11]。自首次提出將TPVN阻滯應用于乳腺癌根治術以來,便取得顯著臨床療效。但關于TPVN阻滯與PecsⅡ阻滯兩種方式在乳腺癌根治術中麻醉效果、鎮痛效果的比較尚無明確依據及定論,因此本研究探討比較兩種阻滯方式的療效及對麻醉用量、并發癥的影響。
本研究中兩種阻滯方式均在超聲定位下進行,超聲的運用能夠確保兩種阻滯方式的安全性,通過探頭準確定位神經,從而避免血管損傷,同時探頭的輔助能夠直觀觀測進針途徑,相較于傳統盲法穿刺,在超聲引導下更加準確。超聲引導下TPVN阻滯過程中,患者術后大多出現上臂、腋窩疼痛不適,認為與胸內側、外側神經及胸長神經、胸背神經無法得到有效阻滯有關,因此鎮痛效果雖然顯著,但術后仍會產生疼痛不適。超聲引導下PecsⅡ阻滯是近年來提出的一種新型的胸部神經阻滯技術,是由PecsⅠ阻滯改良而來,通過將局部麻醉藥物注入前鋸肌與胸小肌、胸小肌與胸大肌之間的肌間隙內,有效發揮對胸內側、外側神經及胸長神經、胸背神經的阻滯作用,且可有效阻滯肋間臂神經、第2~6肋間神經,因此對乳腺癌術后鎮痛具有良好效果[12-14]。本研究選取25 ml 0.5%羅哌卡因進行阻滯,此劑量的局部阻滯作用已出現封頂效應,若劑量過大,則部分患者會出現鎮靜過度、循環功能抑制等現象,此劑量羅哌卡因阻滯具有較好的神經阻滯效果,且不良反應較少。
本研究比較兩組患者疼痛情況,結果顯示,隨著時間延長,兩組患者VAS評分呈現逐步上升趨勢,且術后1、5、8 h,P組患者VAS評分均明顯低于T組,術后12 h兩組患者VAS評分比較無差異,說明術后兩組患者鎮痛效果均隨時間延長而減弱,但TPVN阻滯鎮痛效果消散更快,超聲引導下PecsⅡ阻滯能夠有效保證麻醉藥物的擴散,充分發揮阻滯效果,有助于鎮痛[15]。兩組患者術后12 h VAS評分比較無差異,認為可能是因為隨著時間延長,麻醉藥物鎮痛效果已減弱并對機體疼痛影響不大[16]。
本研究還表明,P組患者術后鎮痛時間明顯長于T組,說明超聲引導下PecsⅡ阻滯對神經阻滯效果更佳,提供更長時間的鎮痛。既往有相關研究證實,PecsⅡ阻滯可為乳腺癌根治術患者提供約8 h的鎮痛時間[17],亦說明PecsⅡ阻滯具有較優異的鎮痛效果。同時,P組患者麻醉藥物用量明顯少于T組,在PecsⅡ阻滯過程中,其能夠有效阻滯胸內側、外側神經及胸長神經、胸背神經,擴散麻醉藥物效果,減輕術后各階段疼痛程度,延長鎮痛時間,疼痛程度亦在患者承受范圍內,因此減少了麻醉藥物的用量。
PecsⅡ阻滯時局部麻醉藥物會向兩端擴散,至少產生T2~T5節段感覺阻滯,國外相關研究亦證實,PecsⅡ阻滯能夠阻滯T2~T4節段皮區,甚至可達到T6節段感覺阻滯[18];但亦有相關研究表明,TPVN阻滯產生的感覺阻滯多在T3~T6皮區部位[19]。本研究通過比較兩組患者各胸段皮區痛覺減退情況發現,兩組患者T3~T5節段皮區痛覺減退情況比較無差異,P組患者T2胸段皮區痛覺減退率高于T組,T6胸段皮區痛覺減退率低于T組,說明TPVN阻滯產生多在T3~T6節段,部分可超出穿刺針注射藥物在T2節段,而PecsⅡ阻滯在T2~T5節段的阻滯效果更好,少部分可產生T6阻滯。認為原因是兩種阻滯方式患者采取不同體位,且PecsⅡ阻滯藥物向兩端擴散,而TPVN阻滯則采用的是單點技術,因此藥物難以向T2節段擴散,另外,藥物的擴散與針尖位置、注射速度等因素均具有一定關系[20]。比較兩組患者并發癥發生情況可知,P組患者并發癥發生率低于T組,說明PecsⅡ阻滯具有更高的安全性,超聲引導下PecsⅡ阻滯能夠減少針尖誤入胸肩峰動脈及頭靜脈,從而降低氣胸等并發癥發生率。TPVN阻滯雖存在血管損傷、低血壓、胸膜刺破、神經損傷等潛在并發癥,但本研究在超聲引導下實施TPVN阻滯,能夠直觀觀測進針路徑及周圍組織結構,觀察局部麻醉藥物擴散情況,有效減少上述并發癥。
綜上所述,超聲引導下PecsⅡ阻滯應用于乳腺癌根治術相較于TPVN阻滯更加安全、可靠、有效,能夠減少麻醉藥物用量,延長鎮痛時間,發揮更顯著的鎮痛效果,且減少術后并發癥。但本研究樣本量有限且為回顧性分析,結果可能存在偏倚,針對研究結果還需擴大樣本量進行多中心、前瞻性研究證實。

