miR-365通過調控ATG3對HCC細胞自噬的作用機制
王麗紅 吳慧麗 張利 李賓 劉迎
鄭州大學附屬鄭州中心醫(yī)院1消化內科,2門診綜合診療中心(鄭州450000)
肝細胞性肝癌(hepatocellular carcinoma,HCC)是臨床上最為常見的惡性腫瘤之一,具有較高發(fā)病率和致死率,嚴重威脅人類生命健康。臨床上治療肝癌常見的方式有手術切除、放射治療、免疫治療等,但HCC患者預后仍不理想[1]。自噬是細胞自我消化過程,可將細胞質內衰老或受損細胞器及一些大分子物質包裹在囊泡,形成自噬泡,與溶酶體融合,降解為小分子物質,對維持細胞內環(huán)境穩(wěn)態(tài)至關重要[2]。自噬過程在細胞內受嚴格調控,不僅是細胞正常生理狀態(tài)下的生存機制,同時與腫瘤發(fā)生發(fā)展密切相關[3]。在HCC發(fā)展過程中,自噬具有雙重作用,HCC發(fā)展初期,自噬可抑制腫瘤細胞生長,在發(fā)展階段,自噬可為腫瘤細胞提供營養(yǎng)促進腫瘤細胞增殖[4]。微小RNA(microRNA,miRNA)參與基因表達與調控,與自噬過程密切相關,其通過對自噬水平的調控,影響腫瘤結局。miR-365是miRNA家族一員,在肝癌細胞中表達下調,但關于miR-365與HCC細胞自噬關系報道較少[5]。本研究通過探討miR-365在HCC中對自噬的作用及可能機制,旨在為治療HCC提供新的靶點和方向。
1 材料與方法
1.1 材料
1.1.1 臨床資料選取本院收治確診為HCC患者13例,其中男性8例,女性5例,年齡26 ~61歲,平均年齡(41.37 ± 5.16)歲,收集患者術后HCC組織與癌旁組織,保存于液氮中。納入標準:年齡18歲;符合臨床HCC診斷標準,患者均接受根治術,術后經病理驗證為HCC。排除標準:無影像學資料及合并其他惡性腫瘤患者。
1.1.2 細胞系和試劑人肝癌SMMC-7721細胞、肝癌HepG2細胞,人正常肝細胞L02購于中國科學院上海細胞庫。DMEM培養(yǎng)基、胎牛血清(fetal bovine serum,FBS)(美國Gibco公司),含有miR-365激動劑(miR-365-mimics)、無義隨機序列(miR-365-NC)的pcDNA3.1重組質粒(上海吉瑪制藥技術有限公司),兔抗人自噬相關基因3(autophagy related gene 3,ATG3)多抗、自噬微管相關蛋白輕鏈3-II(microtubule-associated protein1 light chain3-II,LC3-II)多抗、p62單抗、Beclin1單抗(美國Abcam公司),HRP標記的山羊抗兔二抗(北京中杉金橋生物技術有限公司),雙熒光素酶報告基因檢測試劑盒(美國Promega公司)。
1.2 方法
1.2.1 細胞培養(yǎng)、轉染及分組取人肝癌SMMC-7721細胞、肝癌HepG2細胞,人正常肝細胞L02,放入含有10%FBS+100 U/mL青霉素+100 μg/mL鏈霉素的DMEM培養(yǎng)基中,于體積分數5%CO2、37 ℃條件下恒溫培養(yǎng)。2 ~3 d傳代一次,取對數生長期SMMC-7721細胞,按1×105個/mL接種于6孔板,隨機分為對照組、NC組(轉染miR-365無序對照序列miR-365-NC)過表達組(轉染miR-365-mimics)。繼續(xù)培養(yǎng)48 h,熒光顯微鏡下觀察轉染效率均>85%,可用于后續(xù)實驗。
1.2.2 RT-qPCR 檢測組織與細胞中miR-365、ATG3 mRNA 表達水平取患者HCC組織與癌旁組織,轉染與未轉染SMMC-7721細胞,HepG2肝癌細胞,人正常肝細胞L02,Trizol法提取總RNA,測定總RNA濃度和純度,逆轉錄cDNA,進行RT-qPCR。反應體系:上下游引物各1 μL,cDNA 2 μL,SYBR Green PCR Master Mix 10 μL,加ddH2O至總體積25 μL。反應條件:95 ℃預變性10 min,95 ℃變性10 s,55 ℃退火10 s,70 ℃延伸30 s,45個循環(huán)。miR-365以U6為內參,ATG3以β-actin為內參,采用2-CT法計算目的基因的相對表達水平。引物由上海生工合成,引物序列見表1。

表1 引物序列Tab.1 Primer sequence
1.2.3 MTT 法檢測細胞增殖情況各組細胞,按2 × 105個/mL接種于96孔板,培養(yǎng)48 h后,20 μL/孔加入MTT溶液(5 mg/mL),繼續(xù)孵育4 h,150 μL/孔加入DMSO,震蕩10 min,用酶標儀在450 nm處檢測吸光度(A)值。
1.2.4 流式細胞術檢測細胞凋亡情況各組細胞按1 × 106個/mL接種于6孔板,培養(yǎng)48 h,胰酶消化,1 500 r/min離心5 min,棄上清,加入200 μL Binding Buffer重懸細胞,加入5 μL Annexin V-FITC和5 μL PI染色液,混勻,室溫避光孵育20 min,上流式細胞儀檢測凋亡情況。
1.2.5 電鏡觀察細胞自噬情況取各組細胞按1×106個/mL接種于6孔板,培養(yǎng)48 h后胰酶消化收集細胞,1 200 r/min離心10 min,棄上清,加入4%戊二醛,4 ℃固定24 h,1%四氧化鋨4 ℃固定1 h,梯度乙醇和丙醇脫水,環(huán)氧樹脂包埋,切片(片厚約100 μm),醋酸鈾和枸櫞酸鉛定位染色后封片,電鏡觀察。
1.2.6 Western blot 法檢測細胞中ATG3、LC3-II、Beclin1、p62蛋白相對表達水平取各組細胞,加入細胞裂解液,提取總蛋白,BCA法定量,蛋白變性,上樣進行SDS-PAGE電泳,轉至PVDF膜,5%脫脂奶粉室溫封閉2 h,TBST洗膜,加入1∶2 000稀釋的ATG3、LC3-II、Beclin1、p62一抗4 ℃孵育過夜,TBST洗膜,加入二抗37 ℃孵育2 h,加入ECL曝光顯影,以β-actin為內參,采用Image J軟件進行灰度分析,計算目的蛋白相對表達水平。
1.2.7 雙熒光素酶報告基因系統(tǒng)檢測miR-365 與ATG3靶向性根據生物信息學軟件分析預測miR-365與ATG3之間的結合位點,將ATG3-3′UTR插入熒光素酶報告載體pMIR-REPORT,分別構建野生型重組質粒pMIR-ATG3-MT和突變型重組質粒pMIR-ATG3-MUT,利用LipofectamineTM 2000轉染試劑將miR-365-mimcs-NC/miR-365-mimcs與野生組和突變組質粒共轉染SMMC-7721細胞,48 h后,檢測熒光素酶活性。
1.3 統(tǒng)計學方法采用SPSS 25.0統(tǒng)計軟件分析數據,計量資料以均數±標準差表示,多樣本計量資料比較采用單因素方差分析,兩兩樣本比較采用LSD-t檢驗。P <0.05為差異有統(tǒng)計學意義。
2 結果
2.1 HCC 患者組織與不同肝細胞系中miR-365 和ATG3 mRNA 表達情況HCC患者癌組織中miR-365、ATG3表達明顯低于癌旁組織(P <0.05),見圖1。肝癌SMMC-7721細胞、HepG2細胞中miR-365和ATG3表達均低于正常L02細胞(P <0.05),且SMMC-7721細胞較HepG2細胞更低(P <0.05),見圖2。后續(xù)實驗選擇SMMC-7721細胞。
2.2 SMMC-7721 細胞轉染后miR-365 和ATG3 mRNA 表達情況過表達組miR-365、ATG3相對表達量明顯高于對照組、NC組(P <0.05),見圖3。
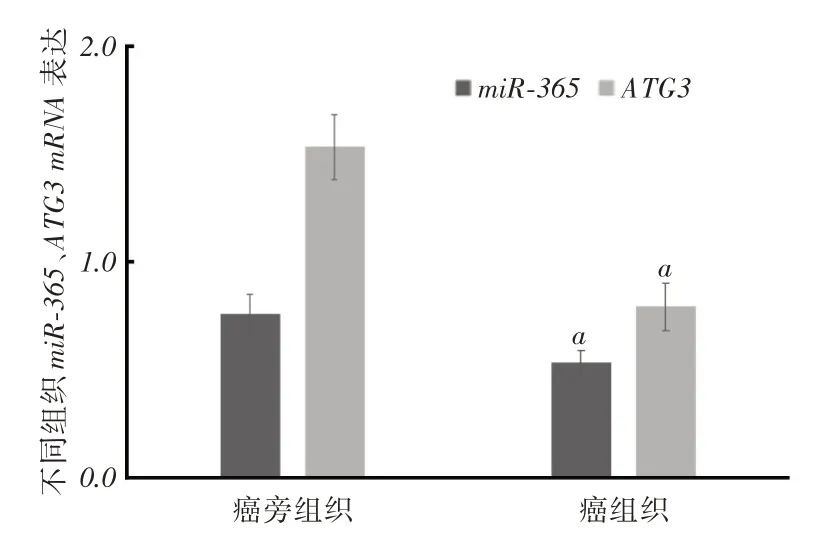
圖1 HCC 患者不同組織miR-365、ATG3 表達情況Fig.1 The expression of miR-365 and ATG3 in different tissues of HCC patients
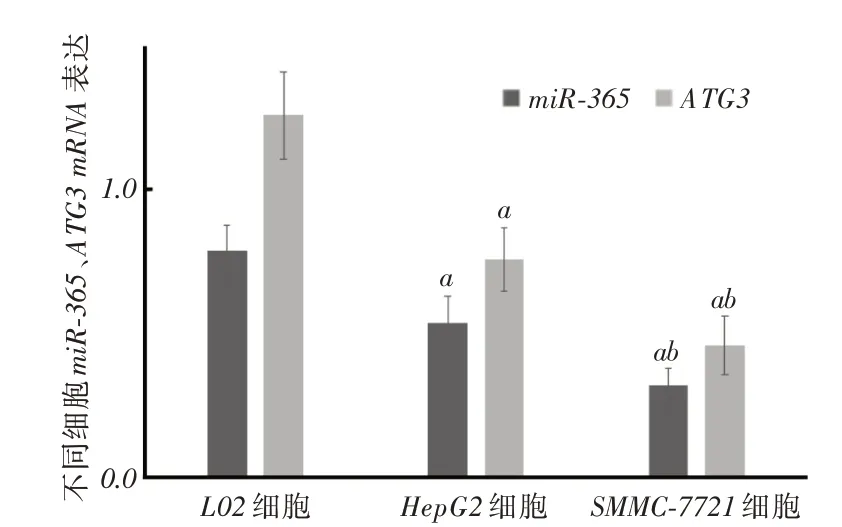
圖2 不同細胞系中miR-365、ATG3 表達情況Fig.2 The expression of miR-365 and ATG3 in different cell line
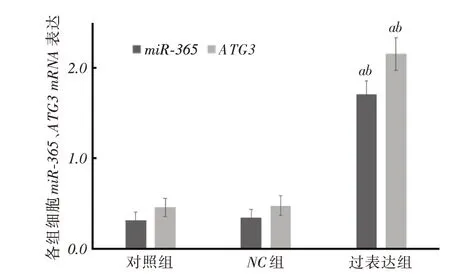
圖3 各組細胞miR-365、ATG3 相對表達量比較Fig.3 Comparison of relative expression levels of miR-365 and ATG3 in each group of cells
2.3 細胞增殖情況過表達組細胞A值明顯低于對照組、NC組(P <0.05)。見圖4。
2.4 細胞凋亡情況過表達組細胞凋亡率明顯高于對照組、NC組(P <0.05),見圖5。
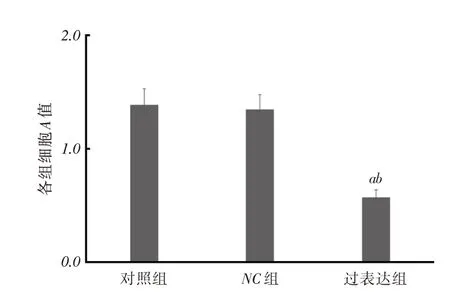
圖4 各組細胞A 值比較Fig.4 Comparison of cell A values in each group
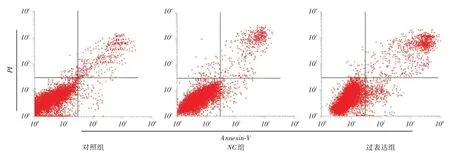
圖5 各組細胞凋亡率比較Fig.5 Comparison of cell apoptosis rate in each group
2.5 透射電鏡觀察結果透射電鏡觀察顯示,對照組、NC組內質網、溶酶體等細胞器結構正常;過表達組出現大小不一、包裹細胞器的圓形自噬泡(箭頭指示),見圖6。
2.6 細胞中ATG3、LC3-II、p62、Beclin1 蛋白相對表達量過表達組細胞中ATG3、LC3-II、Beclin1蛋白相對表達量明顯高于對照組、NC組,p62蛋白相對表達量明顯低于對照組、NC組(P <0.05),見圖7。
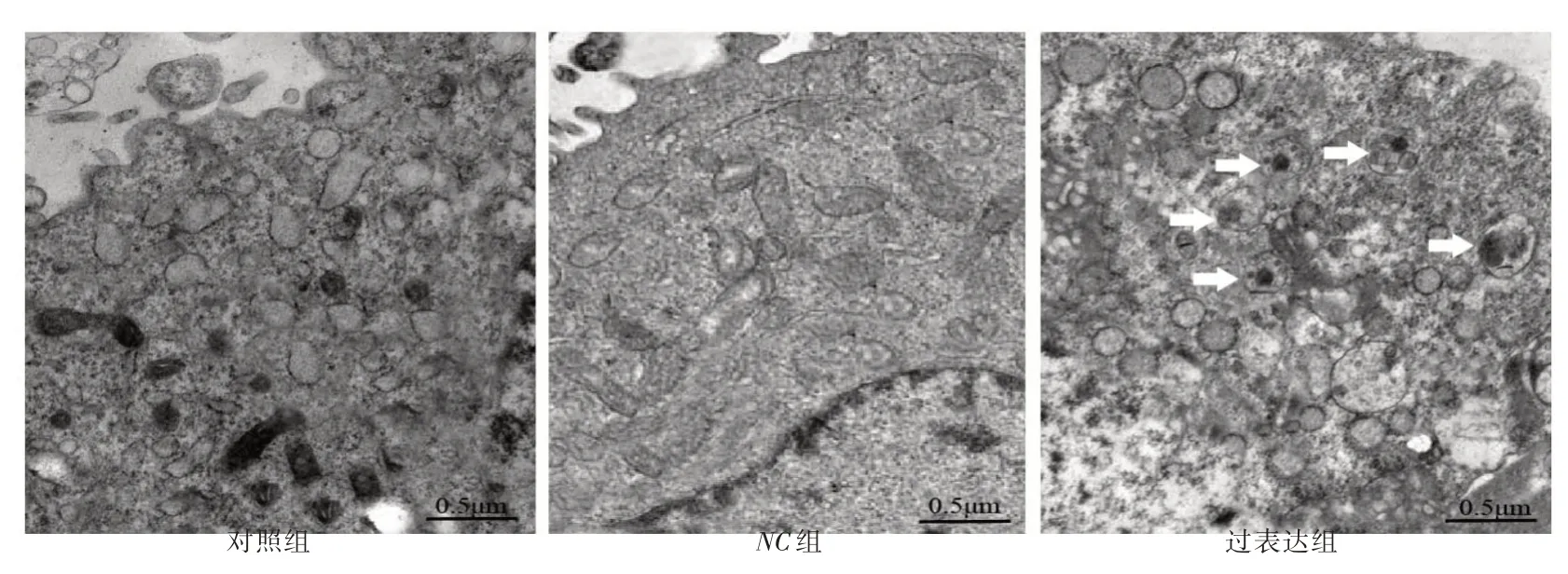
圖6 透射電鏡觀察自噬(×25 000)Fig.6 Observation of autophagy under transmission electron microscope(×25 000)
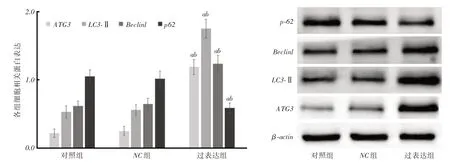
圖7 細胞中ATG3、LC3-II、p62、Beclin1 蛋白表達Fig.7 Protein expression of ATG3,LC3-II,p62,Beclin1 in cells
2.7 雙熒光素酶報告基因系統(tǒng)檢測miR-365 與ATG3 靶向性生物學信息軟件顯示,ATG3存在miR-365結合位點,見圖8A;進一步熒光素酶實驗顯示,轉染miR-365 mimics可明顯抑制野生型ATG3相對熒光素酶活性(P <0.05),而對突變型ATG3無明顯影響(P >0.05),見圖8B。
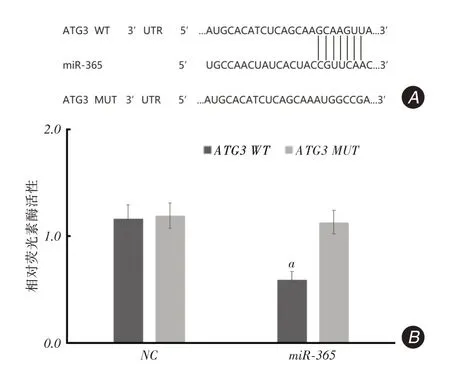
圖8 miR-365 靶向調節(jié)ATG3 表達(A:miR-365 與ATG3 存在連續(xù)結合位點;B:miR-365 靶向抑制ATG3)Fig.8 miR-365 targeted regulation of ATG3 expression(A:miR-365 and ATG3 have continuous binding sites;B:miR-365 targeted inhibition of ATG3)
3 討論
自噬與腫瘤發(fā)生發(fā)展過程關系密切,通過探討腫瘤細胞自噬的分子機制,對治療腫瘤具有重要意義[6]。自噬通過降解細胞組分,為細胞提供營養(yǎng)物質,維持細胞正常代謝,并可防止化療藥物誘導的細胞凋亡,保護細胞免受藥物作用,促進細胞耐藥;另一方面,自噬也可導致細胞死亡,通過誘導自噬促進細胞凋亡,發(fā)揮抑癌作用,在治療癌癥中具有潛在效應[7]。miRNA參與調控基因表達,通過調節(jié)自噬過程中關鍵蛋白的表達,對腫瘤細胞的增殖、凋亡、侵襲和轉移過程表現出直接或間接調控作用,從而發(fā)揮抑癌或促癌作用,為腫瘤的治療提供新靶點和新思路[8]。
miRNA在腫瘤組織中通過上調或下調下游相關基因,對腫瘤的結局和預后產生不同影響[9]。不同腫瘤組織中miR-365表達存在差異,其在皮膚鱗狀細胞癌中表達上調,在肺癌、口腔鱗狀細胞癌細胞中低表達[10-12]。HE等[13]報道顯示,miR-365在HCC癌組織表達明顯低于癌旁組織,miR-365下調可通過多種途徑促進HCC進展和轉移。本研究通過檢測HCC患者癌組織與癌旁組織中miR-365表達,結果顯示癌組織中miR-365表達顯著低于癌旁組織,與以上結果一致。為進一步證實miR-365在HCC中的表達,本研究對不同HCC細胞系及正常肝細胞系中miR-365表達情況進行檢測,結果顯示,HCC細胞系中miR-365表達明顯低于正常肝細胞,進一步驗證miR-365在HCC中低表達。為揭示miR-365在HCC中作用機制,本研究采用miR-365轉染SMMC-7721細胞,結果顯示,miR-365過表達后,細胞增殖能力降低,凋亡率升高,與JIANG等[14]研究結果一致,提示過表達miR-365可抑制HCC細胞增殖促進其凋亡。
過表達miR-365可誘導HCC細胞凋亡,阻止原發(fā)性腫瘤生長,通過誘導自噬促進HCC細胞凋亡是抑癌的重要分子機制之一[15-16]。在肥大型心肌細胞中,miR-365表達顯著上調,可負向調控心肌細胞自噬,引起自噬失調[17]。細胞自噬受機體多種基因和蛋白嚴密調控,參與調控自噬的基因統(tǒng)稱為ATG家族,其中ATG3參與調節(jié)LC3蛋白脂化系統(tǒng)[18]。LC3分為Ⅰ型和Ⅱ型,發(fā)生自噬時,Ⅰ型經泛素樣修飾轉變成Ⅱ型,LC3-Ⅱ含量與自噬泡數量成正比,是發(fā)生自噬的標志性蛋白。Beclin1是自噬啟動因子,其活性下降或缺失抑制自噬的啟動,促進腫瘤進展。p62蛋白是自噬負性調控因子,參與調節(jié)自噬降解途徑。本研究轉染miR-365后,透射電鏡提示細胞發(fā)生自噬,進一步經Western blot檢測,結果顯示過表達miR-365后,ATG3、LC3-II、Beclin1蛋白表達升高,p62蛋白表達下降,提示過表達miR-365抑制SMMC-7721細胞增殖促進細胞凋亡,可能與誘導細胞發(fā)生自噬有關。
miR-365下游有眾多靶基因,通過調節(jié)不同靶基因表達,發(fā)揮相應生物學功能[19]。本研究通過miR靶基因預測軟件預測miR-365與ATG3存在相互結合位點,經雙熒光素酶實驗驗證miR-365與ATG3之間存在靶向性,與YANG等[20]研究結果一致,由此推測,過表達miR-365可能是通過靶向促進ATG3表達,激活細胞自噬,誘導細胞凋亡,抑制細胞增殖。
綜上所示,過表達miR-365可誘導HCC細胞自噬,從而抑制細胞增殖促進其凋亡,其可能是通過靶向上調ATG3表達,調節(jié)細胞自噬水平,為臨床治療HCC提供新的治療靶點。

