豬苓多糖對LPS誘導的急性肺損傷模型大鼠炎癥因子的影響
李全有 劉海軍



【摘 要】 目的:探究豬苓多糖對LPS誘導的急性肺損傷模型大鼠炎癥因子的影響。方法:雄性SD大鼠,腹腔注射LPS(5 mg/kg)構建急性肺損傷模型,用豬苓多糖(250 mg/kg)灌胃進行處理。計算肺組織濕干重比,HE染色檢測肺組織病理學變化,ELISA檢測血清中轉化生長因子(TGF)-α、白介素-6(IL-6)、白介素-10(IL-10)和白介素-1β的水平,肺組織中丙二醛(MDA)、谷胱甘肽過氧化酶(GSH-Px)、髓過氧化物酶(MPO) 和超氧化物歧化酶(SOD)的表達水平。結果:Model組肺組織損傷嚴重,而豬苓多糖治療能夠有一定程度緩解肺損傷;與Control組相比,Model組肺組織濕干重比,TGF-α、IL-18、IL-6和IL-1β表達,以及MDA和MPO表達水平升高,而GSH-Px和SOD表達水平明顯降低,差異均具有統計學意義(P<0.05);與Model組相比,豬苓多糖組肺組織濕干重比,TGF-α、IL-18、IL-6和IL-1β表達水平,以及MDA和MPO表達水平有所降低,而GSH-Px和SOD表達水平升高,差異均具有統計學意義(P<0.05)。結論:豬苓多糖可以緩解LPS誘導的急性肺損傷模型大鼠炎癥反應。
【關鍵詞】 豬苓多糖;急性肺損傷模型大鼠;TGF-α;IL-1β;IL-18
【中圖分類號】R563.9?? 【文獻標志碼】 A??? 【文章編號】1007-8517(2021)22-0021-04
Effects of Polyporus Umbellatus Polysaccharide on Inflammatory Factors in Rats with LPS-induced Acute Lung Injury
LI Quanyou LIU Haijun
Department of pharmacy, Anyang Hospital of traditional Chinese medicine,Henan Province,Anyang 455000,China
Abstract:Objective To explore the effects of Polyporus umbellatus polysaccharide on inflammatory factors in rats with acute lung injury induced by LPS. Methods Male SD rats were purchased, LPS (5 mg/kg) was injected intraperitoneally to construct an acute lung injury model, and polyporus polysaccharide (250 mg/kg) was administered by gavage. Calculate the wet-to-dry weight ratio of lung tissue, HE staining to detect lung tissue pathological changes, ELISA to detect transforming growth factor(TGF)-α, interleukin-6(IL-6), interleukin-10(IL-10) and interleukin- 1β level, the expression level of malondialdehyde(MDA), glutathione peroxidase(GSH-Px), myeloperoxidase (MPO) and superoxide dismutase (SOD) in lung tissue.Results The lung tissue damage in the Model group was severe, and Polyporus umbellatus polysaccharide treatment could relieve the lung damage to a certain extent; compared with the Control group, the lung tissue wet-to-dry weight ratio, TGF-α, IL-18, IL-6 and IL in the Model group -1β expression, as well as the expression levels of MDA and MPO increased, while the expression levels of GSH-Px and SOD were significantly reduced(P<0.05); compared with the Model group, the lung tissue wet-to-dry weight ratio of the polyporus polysaccharide group, TGF-α, The expression levels of IL-18, IL-6 and IL-1β, as well as the expression levels of MDA and MPO decreased, while the expression levels of GSH-Px and SOD increased (P<0.05).Conclusion Polyporus umbellatus polysaccharide can alleviate the inflammatory response in rats with acute lung injury induced by LPS.
Keywords:Polyporus Umbellatus Polysaccharide;Acute Lung Lnjury Model Rat; TGF-α; IL-1β; IL-18
急性肺損傷(Acute lung injuny,ALI)是一種具有高發病率和死亡率的炎性疾病[1]。ALI或更嚴重的形式是急性呼吸窘迫綜合征(Acute respiratory distress syndrome,ARDS),其特征是嚴重的肺水腫,肺炎細胞聚集和炎性細胞因子的過量產生,導致強烈的肺部炎癥反應[2]。流行病學研究報告[3]指出,ALI仍然是世界范圍內重要的公共衛生問題,也是臨床醫生面臨的重大挑戰[3]。盡管已采取一些治療策略來改善功能結局,但ALI患者的死亡率仍然很高,故需要研究ALI的潛在機制和新的治療方法。豬苓多糖是由中藥豬苓提取的多糖類物質,能夠提高機體的細胞免疫功能[4],豬苓多糖膠囊和注射劑均已獲得中國食品藥品監督管理局(SFDA)批準,已在中國單獨或與多種臨床藥物聯合使用來治療乙型肝炎,肺癌和肝癌等疾病[5]。在肺部疾病中,豬苓多糖可以通過抑制成纖維細胞向成肌纖維細胞的轉化,抑制肺成纖維細胞的增殖和遷移而發揮有效的抗纖維化作用[6],說明了在肺部疾病中豬苓多糖可以發揮調控作用,但是在ALI中尚未有相關研究,本項目的開展可能為ALI的治療提供新的研究思路。
1 材料與方法
1.1 實驗動物 雄性SD大鼠(182~218 g),18只,購自上海Slaccas實驗動物有限公司,并以12 h光照/黑暗周期飼養在SPF實驗動物室中,實驗過程中對動物的處置均符合動物倫理學標準。[JP]
1.2 藥物和試劑 豬苓多糖(國藥準字Z10970134,廣東華南藥業集團有限公司),按劑量溶于生理鹽水;脂多糖(LPS)(北京索萊寶科技有限公司),酶聯免疫吸附法ELISA試劑盒(abcam)。
1.3 動物分組和模型制備 將18只大鼠隨機分為三組,每組各6只:Control組,生理鹽水灌胃,腹腔注射生理鹽水;Model組,生理鹽水灌胃,腹腔注射LPS(5 mg/kg);豬苓多糖組,豬苓多糖(250 mg/kg)灌胃,腹腔注射LPS(5 mg/kg)。每天灌胃一次,連續5 d,之后用腹腔注射LPS(5 mg/kg)建模。建模成功后6 h,麻醉斷頭處死,取出左肺組織稱濕重(W) ,于110 ℃烘烤24 h,稱重即為干重(D) ,計算肺組織濕干重比:W/D= W(mg) /D(mg) 。收集血清以及右肺組織進行后續試驗。
1.4 HE染色 提取肺組織,在緩沖液中保持48 h,之后進行脫水、浸蠟等操作,進行HE染色,蘇木素染細胞核,伊紅染細胞質,脫水封片,顯微鏡鏡檢,圖像采集分析。
1.5 血清炎癥因子水平檢測 收集血液,4 ℃離心分離血清,分離后的血清放置在-80 ℃保存。使用ELISA試劑盒檢測血清中轉化生長因子(TGF)-α、白介素-6(IL-6)、白介素-10(IL-10)和白介素-1β的水平。
1.6 氧化自由基相關指標檢測 根據ELISA試劑盒說明,檢測肺組織中丙二醛(MDA)、谷胱甘肽過氧化酶(GSH-Px)、髓過氧化物酶(MPO) 和超氧化物歧化酶(SOD)的表達水平。
1.7 統計學分析 采用SPSS21.0版本用于統計分析。計量數據采用Mean±SD表示,服從正態分布,多組間比較采用方差分析,兩組間比較采用t檢驗。P<0.05表示差異有統計學意義。
2 結果
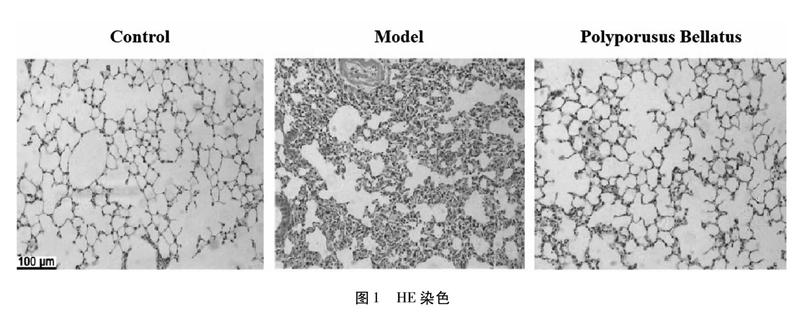
2.1 肺組織病理學觀察 如圖1顯示,Control組肺泡未見出血和水腫,細胞浸潤結構清晰;Model組炎性細胞出現浸潤,肺泡損傷明顯,肺泡、肺間質和肺毛細血管發生水腫,肺泡壁增厚;豬苓多糖組水腫程度改善,損傷程度有一定減輕,出現少量炎性細胞浸潤。
2.2 肺組織濕干重比 如表1所示,與Control組肺組織濕干重比相比,Model組肺組織濕干重比升高(P<0.05),與Model組肺組織濕干重比相比,豬苓多糖組肺組織濕干重比降低(P<0.05),說明豬苓多糖的治療能夠降低LPS誘導的急性肺損傷模型大鼠肺組織濕干重比。
2.3 各組炎癥因子水平比較 如表2所示,與Control組相比,Model組TGF-α、 IL-18、IL-6和IL-1β表達明顯升高,而與Model組相比,豬苓多糖組TGF-α、 IL-18、IL-6和IL-1β表達水平有所降低,差異具有統計學意義(P<0.05)。
2.4 氧化自由基相關指標檢測 如表3所示,與Control組相比,Model組MDA和MPO表達水平升高,而GSH-Px和SOD表達水平明顯降低,而與Model組相比,豬苓多糖組MDA和MPO表達水平有所降低,而GSH-Px和SOD表達水平升高,差異具有統計學意義(P<0.05)。
3 討論
ALI是一種進展性綜合征,其發病率和死亡率較高[7]。 ALI的生理特征是肺泡-毛細血管膜屏障的破壞,導致跨上皮炎性細胞的遷移和促炎性細胞因子的釋放顯著增加[8]。肺內皮細胞和肺泡上皮細胞均會發生損傷,導致肺功能喪失[9]。其特征在于促炎性介質的過度產生,炎性細胞的浸潤以及肺泡上皮細胞的凋亡,因此抑制失控的炎癥反應可能是治療ALI的關鍵。豬苓的使用在中國已經有2000多年的歷史,豬苓多糖是豬苓的主要成分,研究[10]表明,豬苓多糖可以通過調控有絲分裂原激活的蛋白激酶(MAPK)減輕LPS刺激的J774細胞的炎癥反應,在巨噬細胞免疫調控的研究中發現,豬苓多糖可以抑制M2巨噬細胞的黏附和偽足生成,能夠激活TLR2/TLR4-NF-κB信號通路,顯著增強免疫調節能力[11],說明了豬苓多糖能夠參與疾病炎癥反應的調控作用。
LPS是革蘭氏陰性細菌外膜的主要成分,已被廣泛用于通過氣管內插管法誘導ALI的動物模型。與Toll樣受體4(TLR4)結合后,LPS誘導下游信號傳導通路的激活,這些信號通路負責向肺內注入炎癥性細胞(即嗜中性白細胞)并產生炎癥原性細胞因子[12]。LPS與TLR4的結合還誘導IκB-α磷酸化和降解,促進核易位和NF-κB活化,并隨后導致過度釋放促炎性細胞因子,例如,腫瘤壞死因子-α (TNF-α),白介素(IL)-1β,IL-6] [13]。此外,LPS可以激活MAPK家族成員JNK,活化的JNK可以磷酸化許多線粒體蛋白,包括Bcl-2和Bcl-xl [14]。
研究通過LPS構建急性肺損傷模型大鼠進行實驗操作,用豬苓多糖處理急性肺損傷模型大鼠,檢測結果發現Model組肺組織損傷嚴重,而豬苓多糖治療能夠有一定程度緩解肺損傷;與Control組相比,Model組肺組織濕干重比,TGF-α、IL-18、IL-6和IL-1β表達,以及MDA和MPO表達水平升高,而GSH-Px和SOD表達水平明顯降低;與Model組相比,豬苓多糖組肺組織濕干重比,TGF-α、IL-18、IL-6和IL-1β表達水平,以及MDA和MPO表達水平有所降低,而GSH-Px和SOD表達水平升高。說明了豬苓多糖可以緩解LPS誘導的急性肺損傷模型大鼠炎癥反應,對于急性肺損傷的治療研究有一定的指導意義。
參考文獻
[1]羅亞嵐,許才明,李兆霞,等.NLRP3炎性小體——急性肺損傷的發病核心[J].中國急救醫學,2019,39(3):285-289.
[2]由淑萍,汪波,趙軍,等.肉蓯蓉苯乙醇總苷對脂多糖致大鼠急性肺損傷的抑制作用[J].中國藥理學與毒理學雜志,2019,33(5):347-353.
[3]陳艷,董良,朱昭瓊.急性肺損傷治療措施的研究進展[J].臨床與病理雜志,2020,40(1):157-161.
[4]黃青,李麗媛,劉晴晴,等.靈芝多糖和豬苓多糖及其復方的免疫調節作用研究進展[J].食品科學,2020,41(17):275-282.
[5]李明祥,俞維英.豬苓多糖對Lewis肺癌荷瘤小鼠抑瘤作用及外周血細胞的影響[J].中國中醫藥科技,2018,25(5):653-655.
[6]JIANG J,WANG F,LUO A,et al.Polyporus Polysaccharide Ameliorates Bleomycin-Induced Pulmonary Fibrosis by Suppressing Myofibroblast Differentiation via TGF-β/Smad2/3 Pathway[J]. Frontiers in Pharmacology, 2020,11(5):767.
[7]楊琦,曾迎楠,許永安.急性肺損傷發病與發展相關信號通路的研究進展[J].國際呼吸雜志,2020,40(24):1904-1909.
[8]韓鳳. 肺微血管內皮細胞屏障功能損傷與急性呼吸窘迫綜合征[J]. 中國急救醫學, 2015(35):1053.
[9]金善子, 胡博, 欒正剛. 高遷移率族蛋白1在膿毒癥急性肺損傷中作用的研究進展[J]. 中華急診醫學雜志, 2018(4):459-462.
[10]江澤波, 李思明, 趙晉,等. 豬苓多糖對LPS誘導的J774炎癥模型的抗炎作用及其機制[J]. 中國實驗方劑學雜志, 2015, 21(3):156-159.
[11]譚慶龍, 周昌園, 劉春萍,等. 豬苓多糖對人巨噬細胞形態及免疫功能的影響[J]. 中華中醫藥雜志, 2018, 33(5):215-220.
[12]WU X,KONG Q,ZHAN L,et al.TIPE2 ameliorates lipopolysaccharide-induced apoptosis and inflammation in acute lung injury[J]. Inflammation Research,2019,68(11):981-992.
[13]禚志紅, 張靜, 李國棟,等. 腹腔注射脂多糖對幼鼠癲癇發作及海馬TLR4/HMGB1/P-IκB-α表達的影響[J]. 中國實用神經疾病雜志, 2018(2):117-123.
[14]覃蘭惠. 在脂多糖誘導的血腦屏障破壞中p38MAPK、JNK信號通路與基質金屬蛋白酶作用機制的研究[D]. 南寧:廣西醫科大學,2015.
(收稿日期:2021-04-02 編輯:劉 斌)

