超聲造影定性及定量分析鑒別乳腺良惡性非腫塊型病變
徐 平,楊 敏,劉 勇,張 紅,吳蘭英
(首都醫(yī)科大學附屬北京世紀壇醫(yī)院超聲科,北京 100038)
乳腺非腫塊型病變(non-mass lesions, NML)[1]指超聲聲像圖未顯示明確邊界、且在2個以上不同切面上不具備空間占位效應的病變,約占全部乳腺病變的10%,常規(guī)超聲診斷特異度低[2]。近年來超聲造影(contrast-enhanced ultrasound, CEUS)用于診斷乳腺病變,可為鑒別良惡性病變提供重要依據[3-5],但觀察乳腺NML的CEUS研究較少。本研究探討CEUS定性及定量分析鑒別乳腺良惡性NML的價值。
1 資料與方法
1.1 一般資料 回顧性分析2019年1月—2020年1月57例于首都醫(yī)科大學附屬北京世紀壇醫(yī)院就診的乳腺NML患者,均為女性,年齡23~65歲,平均(42.2±9.9)歲。納入標準:①灰階超聲表現(xiàn)符合乳腺NML標準;②接受CEUS檢查;③具備病理學診斷結果;④臨床及影像學資料完整。排除圖像質量欠佳者。
1.2 儀器與方法 采用邁瑞Resona7彩色多普勒診斷儀,L11-3U探頭,頻率3~11 MHz,MI 0.07~0.08,幀頻10幀/秒。造影劑為SonoVue,以5 ml生理鹽水稀釋振蕩產生微氣泡后,抽取4.8 ml經肘靜脈團注。觀察顯示乳腺血流最豐富或有明顯粗大血管的切面,期間探頭避免施壓。
1.3 圖像分析 由具有10年以上乳腺超聲診斷經驗的副主任醫(yī)師及主治醫(yī)師各1名共同分析圖像,經討論得出結論。
1.3.1 定性分析參數 ①以周圍正常乳腺組織為參照判定病灶增強時間(早于、晚于或同步)、增強程度(高增強、等-低增強)及消退時間(晚于、早于或同步);②增強順序(向心性、非向心性)、增強均質性(均勻、不均勻);③病變范圍(擴大、無擴大),即病變增強達峰后病變范圍相比二維超聲范圍有無擴大;④周邊血管(有、無),包括放射狀灌注和穿入灌注,放射狀灌注定義為至少2個不同方向的血管樣灌注從病灶外匯集于病變邊緣,穿入灌注定義為1支或多支粗大血管從同一方向自病灶邊緣穿入病灶。
1.3.2 定量分析參數 在增強強度最高部位選取直徑約2 mm圓形ROI,繪制時間-強度曲線,記錄造影劑到達時間(arrival time, AT)、達峰時間(time to peak, TTP)、峰值強度(peak intensity, PI)、曲線下面積(area under the curve, AUC)及平均通過時間(mean transit time, MTT)。
1.4 統(tǒng)計學分析 采用SPSS 22.0統(tǒng)計分析軟件。以頻數或百分比表示CEUS定性指標,以χ2檢驗進行組間比較;以±s表示定量指標,采用t檢驗進行組間比較。使用BinaryLogistic過程對定性分析、定量分析及二者聯(lián)合分析結果進行Logistic回歸向前逐步分析,得出3種Logistic回歸方程,獲取新變量后,以受試者工作特征(receiver operating characteristic, ROC)曲線分析診斷效能。P<0.05為差異有統(tǒng)計學意義。
2 結果
57例乳腺NML中,經病理確診良性病變31例(良性組),包括18例腺病、5例導管內乳頭狀瘤、3例硬化性腺病、2例漿細胞性乳腺炎及血管平滑肌錯構瘤、導管上皮柱狀細胞病變及導管上皮不典型增生各1例;惡性病變26例(惡性組),其中導管內癌16例,浸潤性導管癌8例,浸潤性小葉癌、黏液癌各1例。
2.1 CEUS定性及定量參數比較 乳腺良性與惡性NML的增強強度、病變范圍、周邊血管及PI、AUC和MTT差異有均統(tǒng)計學意義(P均<0.05),見表1、2及圖1、2。
2.2 定性、定量分析及二者聯(lián)合分析的Logistic回歸分析結果 將表1、2中差異有統(tǒng)計學意義的指標納入多因素分析,結果顯示定性分析中的增強強度、病變范圍,定量分析中PI、AUC以及二者聯(lián)合分析中的病變范圍、PI均為鑒別乳腺良惡性NMLs的獨立因子(P均<0.05),見表3。將上述獨立因子納入回歸方程,得到3個回歸方程,即定性分析回歸方程:P=1/[1+e-(1.188+0.882X1+0.891X2)],其中X1為增強強度,X2為病變范圍;定量分析回歸方程:P=1/[1+e-(0.322+0.09Y1+0.034Y2)],其中Y1為PI,Y2為AUC;聯(lián)合分析回歸方程:P=1/[1+e-(-1.466+0.901X2+0.101Y1)]。
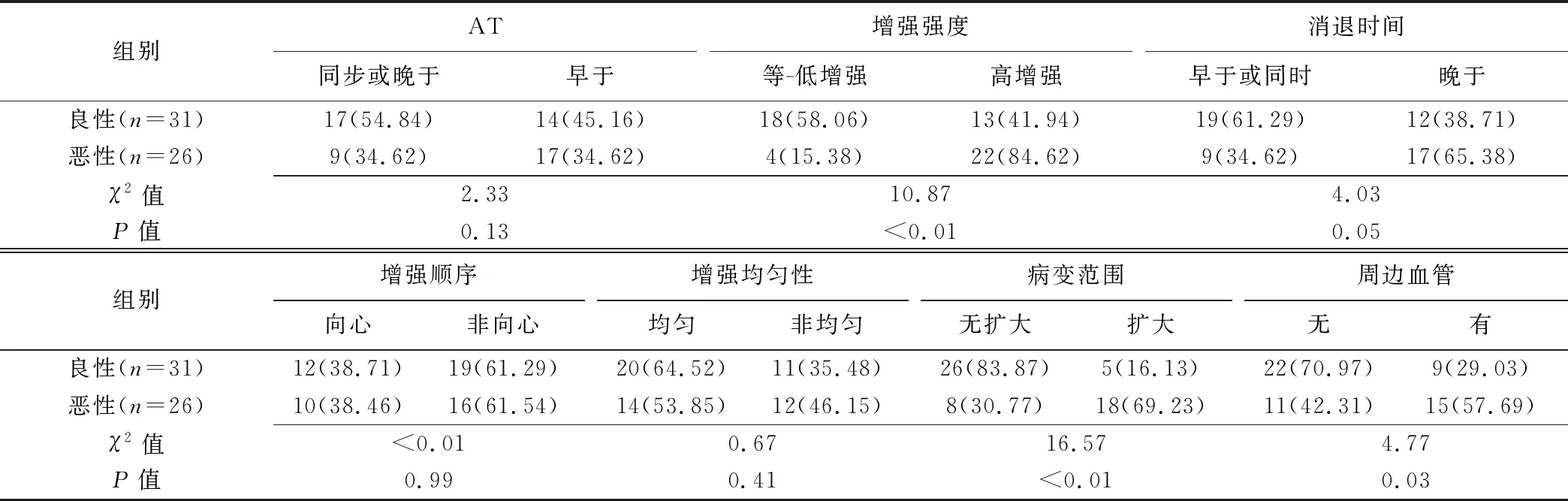
表1 乳腺良惡性NML的CEUS定性指標比較[個(%)]
表2 良惡性乳腺NML的CEUS定量指標比較(±s)
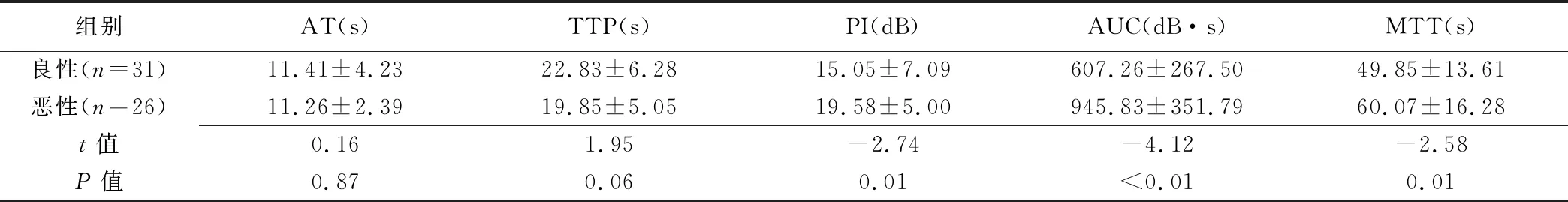
表2 良惡性乳腺NML的CEUS定量指標比較(±s)
組別AT(s)TTP(s)PI(dB)AUC(dB·s)MTT(s)良性(n=31)11.41±4.2322.83±6.2815.05±7.09607.26±267.5049.85±13.61惡性(n=26)11.26±2.3919.85±5.0519.58±5.00945.83±351.7960.07±16.28t值0.16 1.95 -2.74 -4.12 -2.58P值0.87 0.06 0.01 <0.010.01
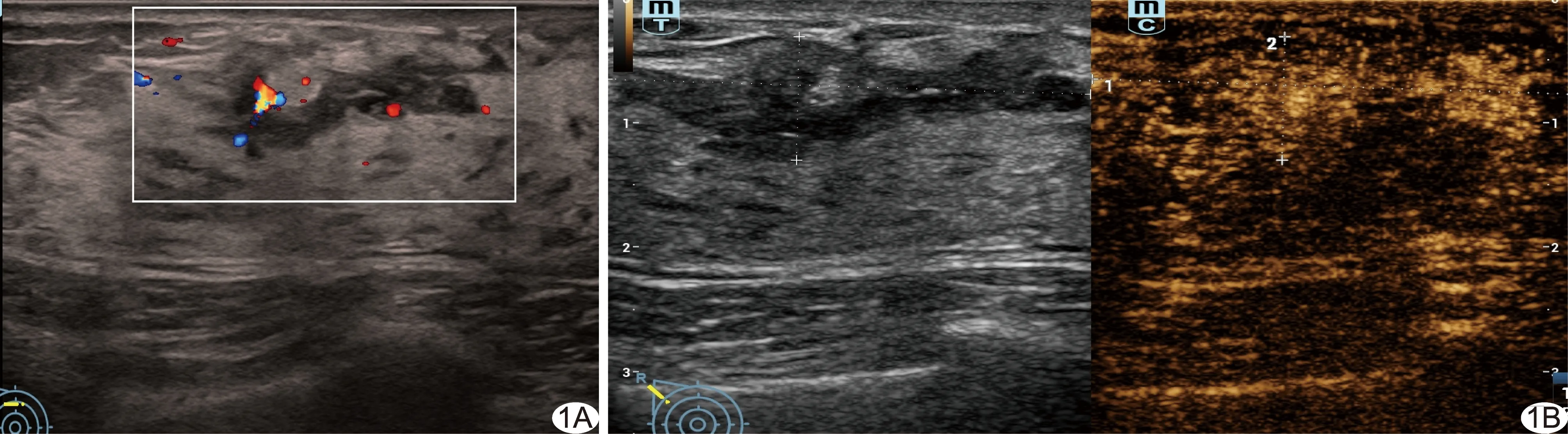
圖1 患者女,39歲,右乳NML,病理診斷為腺病 A.常規(guī)灰階超聲聲像圖示病變邊界及形態(tài)不確定,導管增寬,無微鈣化,無后方回聲衰減,CDFI示其內血流信號較豐富; B.CEUS定性分析示病變早增強、高增強,CEUS所示范圍無擴大,與周邊腺體同步消退,造影劑分布不均勻,可見穿入灌注;定量分析示PI=11.44 dB,TTP=17.20 s,AT=10.00 s,AUC=532.53 dB·s,MTT=29.90 s
圖2 患者女,41歲,左乳NML,病理示浸潤性導管癌 A.常規(guī)灰階超聲聲像圖示病變邊界及形態(tài)不確定,導管增寬,無微鈣化,無后方回聲衰減,CDFI示內部血流較豐富; B.CEUS定性分析示早增強、高增強,病變范圍擴大,周邊可見放射狀增強;定量分析示PI=13.33 dB,TTP=10.20 s,AT=9.60 s,AUC=633.87 dB·s,MTT=37.20 s
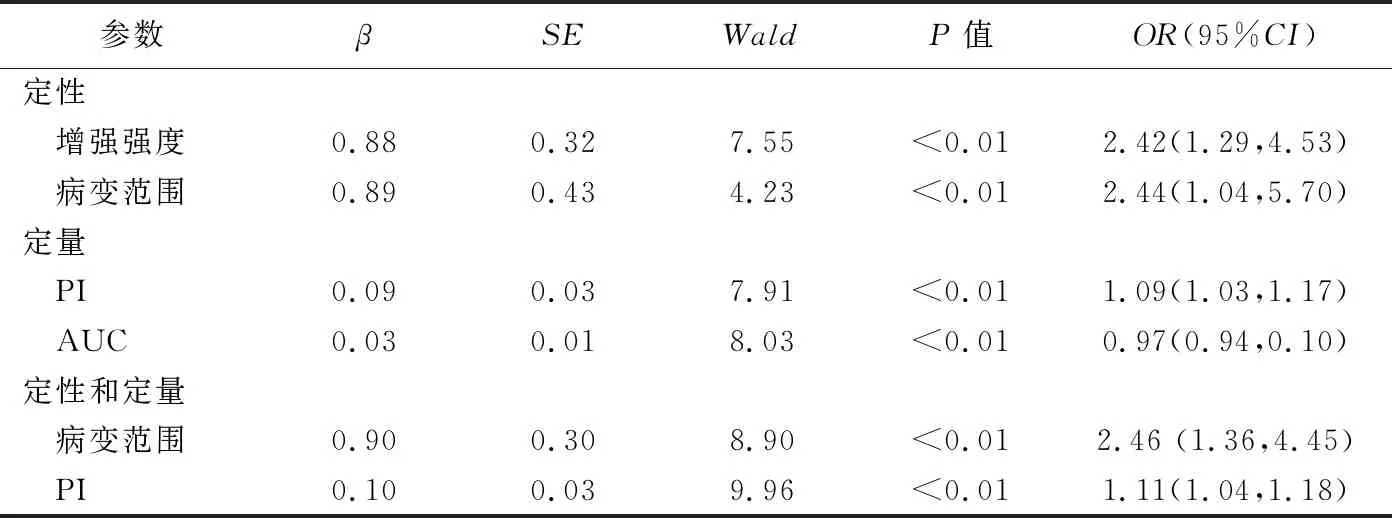
表3 CEUS定性、定量分析及二者聯(lián)合診斷乳腺良惡性NML的多因素分析結果
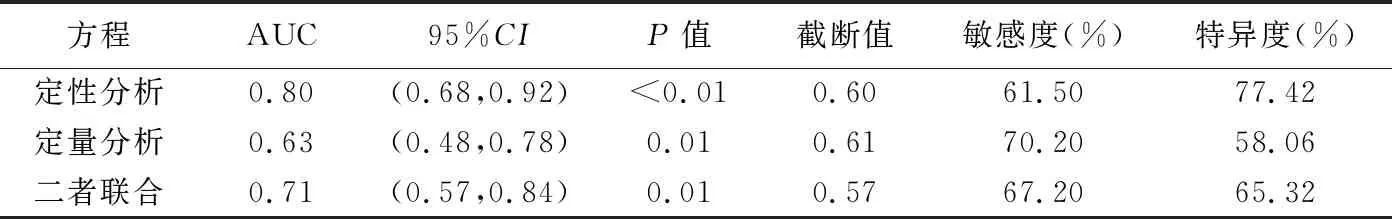
表4 CEUS定性、定量分析及二者聯(lián)合診斷乳腺良惡性NML的ROC曲線分析結果
2.3 診斷效能 定性、定量及二者聯(lián)合分析回歸方程預測乳腺惡性NML的AUC分別為0.80、0.63及0.71,定性分析優(yōu)于定量分析(Z=-3.02,P=0.00),而與聯(lián)合分析間差異無統(tǒng)計學意義(Z=-0.10,P=0.54),見表4及圖3。
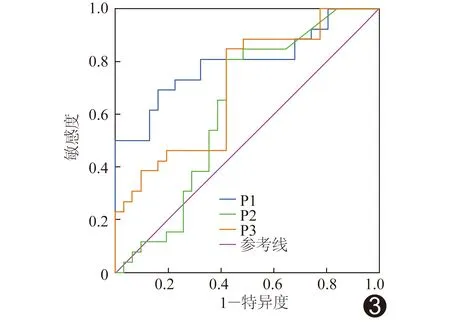
圖3 CEUS定性、定量及二者聯(lián)合分析回歸方程診斷乳腺良惡性NML的ROC曲線 P1:定性分析回歸方程; P2:定量分析回歸方程; P3:二者聯(lián)合分析回歸方程
3 討論
常規(guī)超聲診斷乳腺NML特異度低,導致增加不必要的活檢。CEUS定性及定量分析可為鑒別乳腺良惡性病變提供依據,但目前關于NML的CEUS研究較少。
本研究結果顯示,CEUS定量及定性分析均可用于鑒別診斷乳腺良惡性NML,尤以定性指標中的增強強度和病變范圍、定量指標中的PI和AUC鑒別診斷價值較高。惡性NML可分泌大量血管內皮生長因子,在病變內部及周邊形成大量微小血管,致其CEUS呈高增強,PI增高[6];同時單位時間內通過病變的血流量增加,AUC增大,造影后病變周邊微小血管顯影,表現(xiàn)為病變范圍擴大。以上結果與ZHANG等[7]的結果基本相符,而與部分定性及定量分析乳腺腫塊型病變研究結果[8-9]存在差異,可能原因如下:①NML多與正常腺體實質混合生長,常規(guī)超聲及CEUS均為無明確邊界及固定形態(tài),導致增強邊界及增強形態(tài)對于鑒別良惡性病變不具參考意義;②NML與正常腺體實質混合生長,測量AT、TTP難以避免受正常腺體實質影響;③研究方法不同也可能導致結果存在差異,如ROI選取、造影劑用量、心率、血管彈性和檢查時患者精神狀態(tài)等均可影響定量指標測值[10-11]。
本研究結果顯示,相比CEUS定量分析,定性分析鑒別乳腺良惡性NML的效能更優(yōu),與既往研究[3,9,12]基本相符。定性及定量分析均可反映病變的微循環(huán)狀況,但存在差異,定性指標中的造影前后病變范圍變化可為診斷惡性NML提供重要依據。既往研究[13-14]顯示灰階超聲常低估乳腺癌病灶大小、尤其是導管內癌,而CEUS所測病變范圍更接近術后病理標本實測值,即造影所示病變大小及形態(tài)更為真實。大部分NML與正常腺體混雜存在,灰階超聲易識別病變的低回聲部分;造影狀態(tài)下,腺體的基線回聲被屏蔽,惡性NML表現(xiàn)為增強后范圍擴大,而除炎性病變外,良性NML一般無改變。CEUS定性指標中,周邊病理血管形成具有重要輔助診斷價值。惡性NML細胞分泌大量血管內皮生長因子,誘導病變周邊大量異常血管生成,CEUS可顯示異常穿支及放射狀血管,多數學者[15]認為這是惡性病變的特異性征象,可提高診斷乳腺癌的準確率,而現(xiàn)有定量指標無法反映上述病理變化。此外,測定定量指標受多因素影響,目前尚無統(tǒng)一測量標準,亦影響其診斷效能。
綜上所述,CEUS定性及定量分析均有助于鑒別診斷乳腺良惡性NML,且定性分析的診斷效能優(yōu)于定量分析。本研究樣本量較小,有待大樣本、多中心研究進一步觀察CEUS鑒別乳腺良惡性NML的價值。

