結直腸黏液腺癌的形態學分類及其臨床病理意義
張 前,茍思琪,李志文,楊路路,王勁松,黃文斌
結直腸癌是消化系統常見的惡性腫瘤之一,隨著飲食結構的改變,結直腸癌的發病率逐漸增高且呈年輕化。黏液腺癌(mucinous adenocarcinoma, MA)是結直腸癌最常見的亞型,占結直腸癌的5%~20%,定義為腫瘤由惡性上皮和細胞外黏液池組成,而且黏液池成分占腫瘤區域的50%以上,黏液池內漂浮的惡性上皮細胞可形成腺泡狀、條索狀或單個散在存在,腫瘤細胞形態多樣包括印戒樣細胞等[1]。結直腸MA的預后文獻報道不一,提示MA內不同形態學特征可能具有不同的臨床病理意義[2-5]。目前結直腸MA內漂浮的腫瘤細胞形態學特征與臨床病理特征及預后的關系報道較少,其形態學分類也不一致,導致研究結果也不相同。本文觀察80例結直腸MA的病理形態學特征,將結直腸MA分為分化型、漂浮型和印戒細胞型3種組織學類型,分析不同組織學類型與結直腸MA臨床病理學特征的關系,旨在進一步認識結直腸MA的異質性,探討結直腸MA進一步分型的可能性,從而更加精準地指導臨床治療。
1 材料與方法
1.1 臨床資料收集2013年1月1日~2018年12月31日南京醫科大學附屬南京醫院(南京市第一醫院)存檔的80例結直腸MA手術切除標本,所有病例術前均未行新輔助治療。其中男性44例,女性36例,男女比約1.2 ∶1;年齡41~96歲,平均65.53歲。腫瘤直徑≤5 cm者31例,>5 cm者49例;右半結腸癌42例,左半結腸和直腸38例;腫瘤侵及固有肌層2例,漿膜下層74例,漿膜外層4例;有脈管侵犯者15例,無脈管侵犯者65例;有神經周圍侵犯者11例,無神經周圍侵犯者69例;有淋巴結轉移者38例,無淋巴結轉移者42例;pTNM分期:Ⅰ期1例,Ⅱ期41例,Ⅲ期37例,Ⅳ期1例。
1.2 方法所有病例均為手術切除標本,并經10%中性福爾馬林固定,常規石蠟包埋,5 μm厚切片,分別行HE染色和免疫組化染色。免疫組化染色采用EnVision法,切片常規脫蠟,梯度乙醇脫水,3%H2O2內源性生物素滅活,高溫高壓抗原修復,抗原修復液為枸櫞酸鈉緩沖液(pH 6.0),隨后在Dako Autostainer Link48全自動免疫組化儀上進行染色,具體操作步驟嚴格按試劑盒說明書進行。MLH1、MSH2、MSH6、PMS2購自福州邁新公司,D2-40、CD31和S-100抗體購自北京中杉金橋公司,均為即用型,二抗及檢測試劑盒均購自Dako公司。
1.3 結果判斷
1.3.1形態學分類 所有病例均由病理科兩名高年資主治及以上職稱醫師復核。MA的形態學分型根據黏液湖內有無腫瘤細胞以及漂浮的腫瘤細胞形態分為分化型、漂浮型和印戒細胞型。當MA中印戒癌樣細胞≥10%為印戒細胞型MA,當黏液湖中漂浮的腫瘤細胞(非印戒細胞癌形態)≥10%為漂浮型MA,而印戒癌樣細胞和(或)漂浮的癌細胞<10%,或者無兩種結構時為分化型MA。
1.3.2免疫組化 D2-40、CD31和S-100分別標記淋巴管、血管和神經,當標記的淋巴管、血管和神經內見有癌細胞時則分別判讀為淋巴管、血管和神經侵犯。MLH1、MSH2、MSH6、PMS2均定位于細胞核,當上述4種錯配修復(mismatch repair, MMR)蛋白均表達時判定為錯配修復基因完整(proficient mismatch repair, pMMR),而當4種MMR蛋白中至少1種蛋白失表達時判定為錯配修復蛋白表達缺陷(deficient mismatch repair, dMMR)。陽性對照以腫瘤間質內淋巴細胞作為陽性對照,以PBS代替一抗作為陰性對照。
1.4 統計學分析采用SPSS 26.0軟件進行統計學分析。MA的3種形態學分類和臨床病理特征的關系采用χ2或Fisher確切概率法,不同形態學分類MA中微衛星不穩定性(microsatellite instability,MSI)狀態采用Fisher確切概率法,以P<0.05為差異有統計學意義。
2 結果
2.1 結直腸MA 3種組織學亞型的形態學特征80例MA中,分化型MA 40例,占50%,其組織學特征表現為腫瘤性腺體襯覆于黏液池周邊,腺上皮分化良好,黏液池內幾乎無腫瘤細胞,或漂浮著單個腫瘤細胞或散在的腫瘤細胞巢(圖1A);漂浮型MA 19例,占23.8%,其組織學特征表現為黏液池內漂浮著多量微乳頭或篩狀腫瘤細胞巢,胞質明顯嗜酸性,細胞核間變較明顯(圖1B、C);印戒細胞型MA 21例,占26.2%,其組織學特征為黏液池中漂浮的腫瘤細胞呈明顯的印戒樣,可呈彌漫或成簇分布(圖1D)。
2.2 結直腸MA 3種組織學亞型與臨床病理特征的關系結直腸MA 3種組織學亞型與患者發病年齡、性別、腫瘤部位、腫瘤最大徑和浸潤深度均無關(P>0.05),而與淋巴結轉移、脈管侵犯、神經周圍侵犯以及pTNM分期有關(P<0.05,表1)。進一步分析顯示,漂浮型和印戒細胞型MA中淋巴結轉移陽性率明顯高于分化型MA(P<0.05),但淋巴結轉移率在漂浮型和印戒細胞型之間差異無顯著性(P>0.05);pTNM分期中Ⅲ+Ⅳ期更多見于漂浮型和印戒細胞型MA,而分化型MA更多為Ⅰ+Ⅱ期,差異有顯著性(P<0.05),但漂浮型和印戒細胞型之間差異無顯著性(P>0.05)。
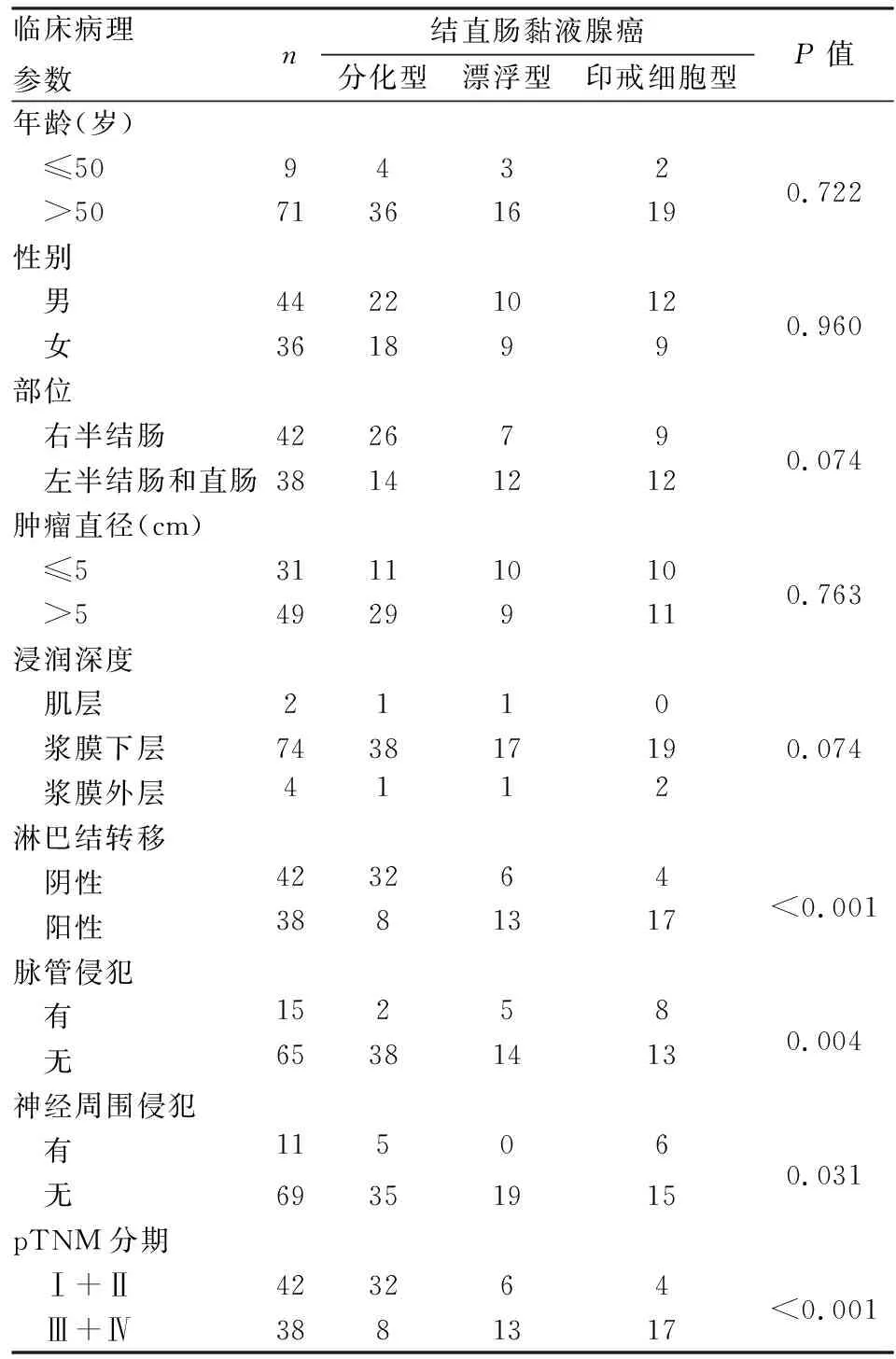
表1 結直腸黏液腺癌3種組織學亞型與臨床病理特征的關系
2.3 結直腸MA不同組織學亞型中MMR蛋白表達4種MMR蛋白(MLH1、MSH2、MSH6和PMS2)均定位于腫瘤細胞核(圖2)。MLH1、MHS2、MSH6和PMS2在結直腸MA 3種組織學亞型的表達差異均無統計學意義(P>0.05)。根據MLH1、MHS2、MSH6和PMS2等4種基因表達情況將MMR分為dMMR和pMMR,它們在結直腸MA 3種組織學亞型的分布,差異無統計學意義(P>0.05,表2)。
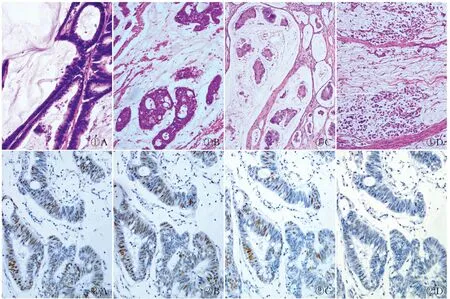
圖1 結直腸黏液腺癌的3種組織學形態特征:A.分化型,腫瘤性腺上皮襯覆于黏液池周邊;B.飄浮型,腫瘤性腺體呈篩狀漂浮于黏液池內;C.飄浮型,腺癌細胞呈微乳頭狀漂浮于黏液池內;D.印戒細胞型,黏液湖內漂浮著印戒細胞癌成分 圖2 結直腸黏液腺癌中4種MMR蛋白表達:A.癌組織中MLH1陽性,EnVision法;B.癌組織中MSH2陽性,EnVision法;C.癌組織中MSH6陽性,EnVision法;D.癌組織中PMS2陽性,EnVision法

表2 結直腸黏液腺癌3種組織學亞型中MMR蛋白的表達
3 討論
MA是結直腸腺癌常見的一種組織學類型,該類型腺癌具有獨特的臨床病理學特征,如患者發病年齡較輕,常見于近端結腸,診斷時多處于進展期以及常伴有遺傳性非息肉病性結直腸癌,但其預后文獻報道不一[2,6]。
結直腸MA不同的預后除了其固有的分子生物學特征外,可能還與其具有不同的形態學改變有關。Kondo等[7]將33例MA分為乳頭管狀型(22例)和黏液細胞型(11例),分析其臨床病理學特征及微衛星改變,結果發現兩者在淋巴管侵犯、淋巴結轉移、腹膜轉移和Dukes分期差異有顯著性,高度MSI在乳頭管狀型明顯高于黏液細胞型,乳頭管狀型MA患者的5年生存率也高于黏液細胞型,作者認為結直腸MA由于存在明顯的臨床病理學特征、MSI以及預后差異而應進一步分為上述2型。Ikeda等[8]將MA分為固定型和漂浮型,發現固定型和漂浮型MA在發病年齡、性別、臨床分期以及部位上無明顯差異,KRAS基因突變和β-catenin蛋白表達雖然固定型高于漂浮型,但差異無統計學意義。p53蛋白表達在飄浮型高于固定型,生存分析顯示,5年生存率漂浮型明顯低于固定型(21.4%vs68.4%),該研究不僅提示MA不同形態學類型預示不同的預后,而且腫瘤發生機制上可能也存在不同,即固定型MA類似于非MA,而飄浮型則可能通過另外機制發生。Song等[9]根據黏液池內腫瘤細胞形態將結直腸MA分為條帶為主型、群集為主型、混合印戒細胞型和印戒細胞為主型,結果顯示條帶或群集為主型MA主要見于老人,混合印戒細胞型或印戒細胞為主型更常見于左側結腸,條帶為主型MA有高分化非MA成分,而混合印戒細胞型或印戒細胞為主型MA顯示差分化腺癌或印戒細胞癌。淋巴血管侵犯、神經周圍侵犯、局部淋巴結分期和TNM分期在印戒細胞為主型MA中明顯高于其他類型MA,而患者性別、T分期、遠處轉移和MSI狀態在不同類型MA之間均無明顯差異。生存分析顯示印戒細胞為主型MA預后最差,其次為混合印戒細胞型,作者認為MA應根據腫瘤細胞形態進一步分型,其中印戒細胞為主型應歸為印戒細胞癌。國內周良銳等[10]將結直腸MA分為無印戒細胞分化和有印戒細胞分化,結果發現有印戒細胞分化的腫瘤體積較小,患者年齡較小,好發于近端結腸以及分期較高,分子生物學分析顯示KRAS/NRAS突變的頻率在不伴印戒細胞分化的病例中顯著高于伴印戒細胞分化,提示兩者具有不同的臨床特征和分子基礎。
MA不同的形態學分型導致研究結果不一致性。Kondo等[7]和Ikeda等[8]分類未能將黏液池內非印戒細胞癌和印戒細胞癌成分區分,而周良銳等[10]根據有無印戒細胞癌分化進行分類,但忽略了MA的黏液池內漂浮非印戒細胞癌的病例,導致這部分病例未能準確分類使研究結果可能出現偏倚。本組根據MA中腫瘤細胞生長方式和細胞形態分為分化型、漂浮型和印戒細胞型。分化型表現為腫瘤性腺體襯覆于黏液池周邊,腺上皮分化良好,黏液池內幾乎無或者漂浮著少量單個腫瘤細胞或散在的腫瘤細胞巢;漂浮型類似于乳腺富于細胞型黏液癌,其組織學特征表現為黏液池內漂浮著多量腫瘤細胞巢,呈篩狀或實性巢狀分布,胞質嗜酸性,核間變較明顯;印戒細胞型病理學特征為黏液池中彌漫或成簇漂浮著印戒細胞癌成分。
本組實驗結果顯示,MA的組織學分類與淋巴血管侵犯、神經周圍侵犯、淋巴結轉移和pTNM分期均有關,而與患者發病年齡、性別、腫瘤部位、腫瘤最大徑和浸潤深度均無關。進一步分析顯示,淋巴血管侵犯、神經周圍侵犯、淋巴結轉移和pTNM分期在漂浮型和印戒細胞型MA中明顯高于分化型,但所有臨床病理特征在漂浮型和印戒細胞型之間差異無顯著性。本組實驗結果提示,結直腸MA具有高度異質性,其中漂浮型和印戒細胞型具有侵襲性臨床生物學行為,建議注明在病理報告中。另外,本組實驗結果支持Kondo等[7]和Ikeda等[8]的分類,但與周良銳等[10]的分子研究結果不符,具體的分型還需要從形態學和分子遺傳學上進一步研究。
MMR蛋白和MSI檢測對于結直腸癌患者是否獲益于5-FU治療、預后評估以及Lynch綜合征篩查具有重要價值,近年研究發現高度MSI可以預測免疫檢查點抑制劑的療效[11-13]。MMR蛋白免疫組化檢測與MSI檢測具有高度的一致性[14-15]。因此,國內外一些指南均推薦結直腸癌進行MMR蛋白免疫組化檢測。有研究發現MMR缺陷型結直腸癌組織學多為MA[16-17]。然而,在MA的亞型分型中研究相對較少。Kondo等[7]研究發現黏液細胞型MA中,高度MSI 2例,低度MSI 7例,微衛星穩定(microsatellite stability, MSS)2例,而乳頭管狀型MA中,高度MSI 12例,低度MSI 3例,MSS 7例,黏液細胞型中高度MSI明顯低于管狀乳頭狀型。Leopoldo等[18]根據MSI狀態將結直腸MA分為MSS型和MSI型,結果發現MSI型MA常位于近端結腸和分化差,腫瘤復發率和患者生存期明顯高于MSS型MA。Song等[9]采用單因素和多因素生存分析顯示,缺乏MSI的MA患者預后差。本實驗發現結直腸MA中MMR蛋白表達缺失主要以MLH1/PMS2為主,缺失率占23.8%,而MSH2/MSH6僅有1例缺失,MLH1/PMS2缺失病例中,MLH1和PMS2共同缺失7例,PMS2單獨缺失2例,MSH2和MSH6共同缺失。4種MMR蛋白缺失和dMMR在結直腸MA 3種組織學分型的分布中未見明顯差異,與Kondo等[7]報道不一致,可能是由于本組病例未能進行MSI檢測,以及病例數量較少有關,尚待以后進一步積累病例進行深入研究。
總之,MA雖是結直腸癌的一種組織學亞型,但其組織學形態具有高度異質性,不同形態學特征的MA具有不同的臨床病理學特征和生物學行為。根據本實驗結果和文獻復習,MA可以進一步行組織學分類和分子分型,但具體組織學分類和分子分型目前文獻尚未統一,還需積累更多病例并結合分子病理學進行深入研究。作者認為在結直腸MA的病理報告中,應注明黏液湖中腫瘤細胞類型及比例,以利于更好地指導臨床治療和預后判斷。

