降結腸轉移性腎癌1例
葛 嫻,潘 云,李正金,趙立仙,王 敏,李躍康
患者男性,75歲。因腹瀉1個月余就診,10余年前曾因腎透明細胞癌行左腎根治性切除術。查體:貧血貌,左側腹部可見一長約15 cm手術切口瘢痕。左側腹部輕壓痛,無反跳痛。糞便常規:紅色水樣便,RBC滿視野/HP。腹部CT檢查:(1)降結腸團塊狀占位,考慮降結腸癌;(2)腹膜后多發團塊狀占位,多為淋巴結轉移;(3)脾臟內類圓形低密度影,不除外轉移瘤。(4)左腎缺如。電子腸鏡示:乙狀結腸增殖樣病變,活檢標本為少量黏膜上皮,未見腫瘤。考慮降結腸占位擬行左半結腸癌切除術,術后標本送病理檢查。
病理檢查眼觀:送檢(左半結腸切除標本)腸管一段,長41 cm,直徑3~6 cm,距一側周徑斷端11 cm處見一大小9.5 cm×8 cm×3 cm的隆起型腫物,腫物切面呈淡黃、暗紅色,實性質中,侵及腸壁全層,腸系膜內查見結節12枚,直徑0.3~1.4 cm。鏡檢:腫瘤細胞多呈實性巢索狀,部分呈管狀、腺泡狀或乳頭狀排列。間質富有毛細血管(圖1)。癌細胞體積較大,呈立方形。胞質透明,有的可見嗜酸性顆粒狀胞質。細胞核圓形或卵圓形,核仁可見,核分裂象偶見(圖2)。免疫表型:CD10(圖3)、CKpan、MLH1、MSH2、MSH6、PMS2、vimentin(圖4)均陽性,CK20、CK7、villin、CD117均陰性,Ki-67增殖指數約5%。
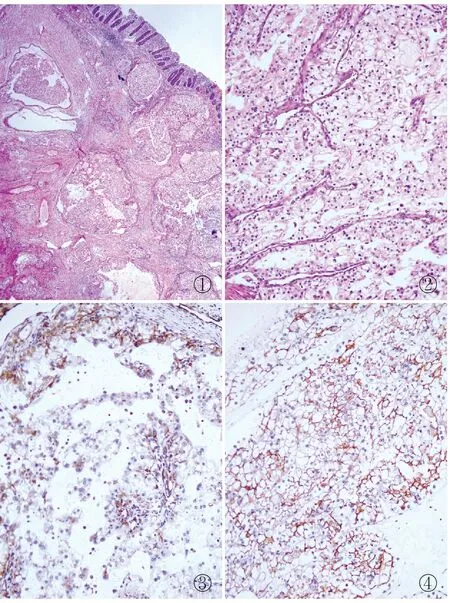
①②③④
病理診斷:降結腸轉移性腎透明細胞癌,WHO/ISUP Ⅲ級。
討論腎細胞癌(renal cell carcinoma, RCC)是起源于腎小管上皮的惡性腫瘤,占成人惡性腫瘤的2%~3%[1-2]。最常見的亞型是透明細胞RCC,約占RCC的80%[2],其次為乳頭狀RCC及嫌色細胞癌,集合管癌和髓質癌等較為少見。RCC發病相對隱匿,20%~30%的患者初診時已為轉移性RCC,超過20%的局限性RCC患者接受手術后仍會發生轉移。轉移性RCC的預后較差,中位生存期僅為13個月,5年生存率不足10%[3]。RCC轉移最常見的部位是肺、骨、肝、腦和淋巴結;亦有轉移至甲狀腺、乳腺、胃等部位的報道[4-6];罕見有轉移至結腸的報道。晚期復發是RCC特有的生物學行為,尤其是罕見部位的轉移更為常見。有5年以上RCC病史的患者一旦被發現臨床可疑腫瘤時,首先應考慮晚期復發的可能[7]。本例為降結腸轉移的晚期復發RCC病例,提示RCC復發可轉移至全身各處。
結腸轉移性RCC起病隱匿,臨床無明顯癥狀,轉移灶的發現可在腎臟切除術后數年甚至數十年后發生,因此遇有結直腸腫物即使RCC病史較長者也應警惕轉移的可能性。本例患者肺、肝等常見部位未出現轉移,影像學顯示脾臟、胰腺、腹腔淋巴結腫大以及降結腸占位預示腫瘤晚期,但患者仍處于亞臨床狀態,直至出現間歇性腹痛、腹瀉和便血等消化道癥狀。迄今為止,尚未有特異性實驗室指標或診斷性生物標記能提示結直腸腫瘤轉移,CT或MRI尤其是增強掃描的影像學檢查是相當重要的診斷性檢查項目。結腸內鏡活檢可確定和顯示結直腸腫塊的組織學性質。
需與轉移性RCC鑒別診斷是原發性結直腸透明細胞腺癌(clear cell adenocarcinoma, CCA),這是一種十分罕見的腫瘤實體,首次報道于1964年。CCA多見于成年男性,平均發病年齡56歲,常見部位為遠端結腸[8]。其發病機制尚不明確,因其是經典腺瘤或腺癌的一部分,且CCA常發生于普通腺瘤/癌中或與之相鄰。鏡下見腫瘤細胞呈腺管狀或篩狀結構排列,部分瘤巢中央可見壞死,腫瘤細胞胞界清楚,長柱狀或多邊形,胞質透明,細胞核多位于基底部,細胞核卵圓形或多角形,部分可見核仁。王云帆等[9]結合文獻總結14例結直腸原發性CCA中CEA(10/10)、EMA(7/7)、CK20(5/6)、β-catenin(2/2)陽性。另外陰性指標有CK7(6/7)、vimentin(2/2),而透明細胞RCC多呈實性片狀排列,常無真正的腺管結構,并且間質富有毛細血管;免疫組化標記RCCa、CD10、PAX2、PAX8陽性,CK20陰性。
轉移性RCC是一種預后不良且對放、化療均不敏感的腫瘤。對于孤立性RCC轉移病灶應積極手術治療,但對于多處轉移性患者,手術僅能減少腫瘤負荷,改善癥狀。以細胞因子為基礎的非特異性免疫治療是轉移性RCC全身治療的主要手段。IL-2和IFN-α兩種細胞因子在臨床中療效穩定,應用廣泛。隨著分子生物學的不斷發展,與RCC發生相關的VEGF通路和mTOR通路已成為治療的關鍵靶點,以索拉非尼、替西羅莫司為代表,聯合免疫檢查點抑制劑如PD-1/PD-L1抑制劑、CTLA-4抑制劑等,拓展了治療手段,給患者帶來希望。本例患者術后未給予任何輔助治療,隨訪5個月,一般情況良好。

