臨床藥物不良事件主動監(jiān)測與智能評估警示系統Ⅱ的研發(fā)
姚 翀,劉東杰,郭代紅,劉思源,孔祥豪,3,于承暄,朱 雨(.解放軍總醫(yī)院醫(yī)療保障中心藥劑科,北京 00853;.北京康聯達軟件有限公司,北京 0008;3.重慶醫(yī)科大學藥學院,重慶 40006)
藥物不良事件(adverse drug event,ADE)是指藥物治療過程中所發(fā)生的任何不幸的醫(yī)療事件,其中也包括藥品不良反應(adverse drug reaction,ADR)。對ADE進行監(jiān)測是保障公共安全用藥的重要手段,其目的是盡早檢出涉藥安全問題、鑒定和量化風險因素,進而采取必要措施防止患者受到不必要的傷害。本團隊前期基于軍衛(wèi)1號醫(yī)院信息系統(hospital information system,HIS),采用觸發(fā)器原理和文本識別技術,設計并開發(fā)了住院患者ADE主動監(jiān)測與智能評估警示系統(active surveillance and assessment system of adverse drug event, ADE-ASAS)[1-2];經多年實踐應用已經完成了住院人群20余種重點藥物ADE自動監(jiān)測與智能評估警示[3-5]。本研究是結合近年來真實世界研究(real world study,RWS)的理論方法,在前期研究基礎上,進一步研發(fā)的新型臨床藥物不良事件主動監(jiān)測與智能評估警示系統(ADE-ASAS-Ⅱ)。ADE-ASAS-Ⅱ是對ADE-ASAS的補充而不僅是簡單的替換升級,能夠提供涉及醫(yī)療數據全部指標監(jiān)測與評估的支持,為高效精準低成本的開展藥物上市后評價研究提供實用的分析工具。
1 資料與方法
1.1 設計思路
ADE-ASAS-Ⅱ是基于最真實的、未經干預的原始醫(yī)療數據的分析,設計重點是解決數據的規(guī)范采集,對數據分析的高度靈活性以及高效率的支持,以及對病歷評價簡捷快速的閱讀檢索支持和提示。系統采用業(yè)務邏輯分層開發(fā)模式,每層都能夠進行獨立開發(fā)、且層間相互依賴的程度低,降低了系統整體開發(fā)難度,同時提高了系統擴展性和穩(wěn)定性。具體分為四層,見圖1。
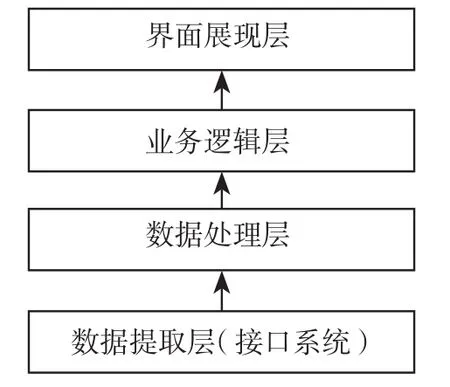
圖1 系統分層示意圖Fig 1 System stratification diagram
界面展現層:負責界面展示,用表格、圖形、文本的方式將經過邏輯處理的數據展現給用戶。該層屬于前端開發(fā)技術,數據動態(tài)加載,通過WebAPI技術從業(yè)務邏輯層獲取數據;可以按照用戶使用習慣或者研究目的靈活修改,更換簡單。
業(yè)務邏輯層:負責業(yè)務邏輯組合,可以選擇任意指標進行排列組合分析,例如生化指標、生命體征、病程文本等。業(yè)務邏輯層承載著本系統的核心算法,不直接訪問數據庫,只負責處理數據。通過調用數據處理層獲取數據并以WebAPI的方式提供給界面展現層。臨床藥師可以參與邏輯設計,根據科研需要提出自己的需求和想法。
數據處理層:負責根據業(yè)務邏輯的設定從數據庫中進行數據查詢檢索,并將數據提供給業(yè)務邏輯層;然后執(zhí)行業(yè)務邏輯層的請求,對數據進行保存。本層還負責數據的標準化,設計有一個通用標準數據模型,定義了各類信息的標準表結構以及字段要求,并兼容國家ADR中心的數據、ICH的藥品基礎信息、ICD10診斷名稱、ICH的ADR名稱等。軍隊各醫(yī)院的藥品編碼、檢查檢驗指標、診斷名稱等基礎數據必須經過標準化后才能進行多中心的自動化監(jiān)測,因此本接口系統提供了編碼對照功能,將醫(yī)院各自編碼與標準庫編碼做一對一唯一對照匹配。
數據提取層:屬于HIS接口,從各種數據源中獲取數據并存儲在緩存庫中,屬于原始數據。
1.2 系統開發(fā)
ADE-ASAS-Ⅱ采用B/S架構,服務器(虛擬機)配置為Intel至強處理器十核及以上,內存64 G及以上,硬盤空間2 T可用,操作系統Windows Server 2016簡體中文企業(yè)版,數據庫管理系統為Microsoft SQL SERVER 2016;客戶端瀏覽器建議為最新版的火狐瀏覽器。
ADE-ASAS-Ⅱ編程開發(fā)工具為Microsoft Visual Studio 2017 C#,ASP.Net Core 3.0。
1.3 數據接口
數據提取層負責數據的采集(見圖2),可兼容不同HIS系統。ADE-ASAS-Ⅱ目前有兩個數據來源,在用庫和歷史庫,在用庫是正在運行的HIS數據,包含近一年來的醫(yī)療數據,歷史庫是近10余年的電子醫(yī)療數據。
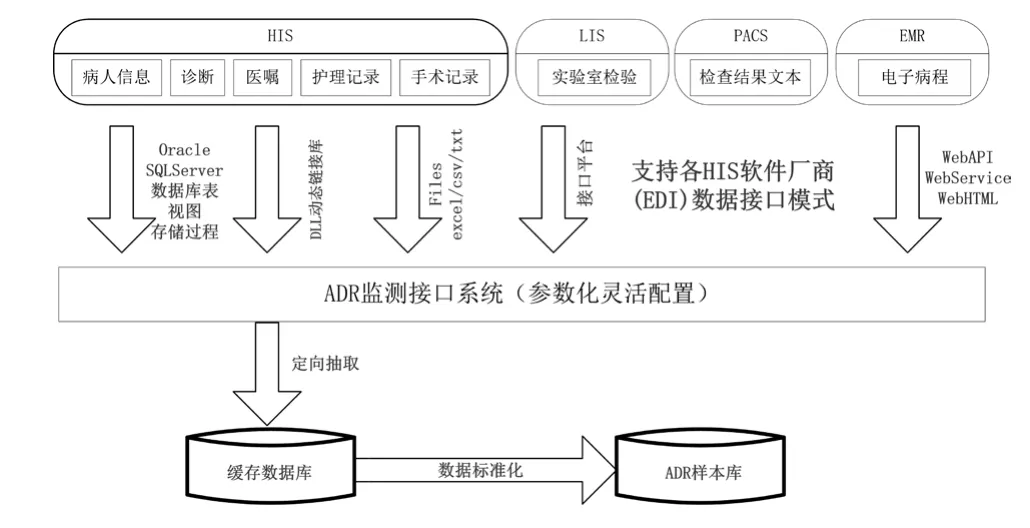
圖2 數據接口與采集示意圖Fig 2 Data interface and collection diagram
2 系統功能與特點
系統開發(fā)基于圍繞臨床海量電子醫(yī)療數據開展真實世界研究需求設計,具有多種藥物對應同一種不良事件的自動監(jiān)測與智能分析警示功能,借助人工智能技術分析相關數據信息篩選陽性預警病例,為研究者的后期人工評價甄別減免了大量信息篩查與數據分析工作,能夠幫助醫(yī)療機構高效、快捷、低儉地開展臨床用藥風險大樣本、長時程的前瞻/回顧性主動監(jiān)測與評價工作,為重點監(jiān)測品種的風險管控提供科學可信的精準數據。主要功能與特點見圖3。
3 系統應用
3.1 監(jiān)測計劃
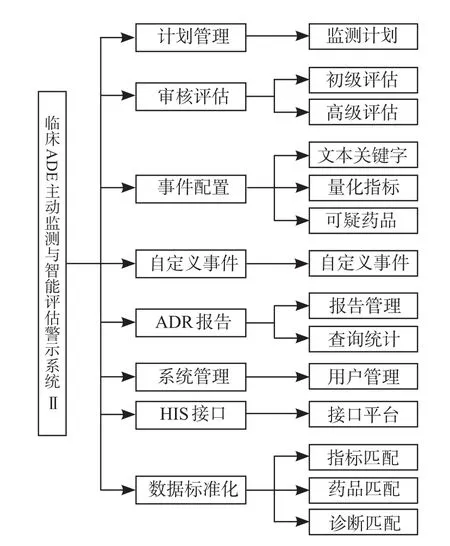
圖3 ADE-ASAS-Ⅱ主要功能示意圖Fig 3 Schematic diagram of the main functions for ADE-ASAS-Ⅱ
ADE-ASAS-Ⅱ根據設定計劃執(zhí)行監(jiān)測。每個計劃執(zhí)行的監(jiān)測指標、識別的不良事件以及納入人群特征等,都需要根據監(jiān)測的藥品或者監(jiān)測目的不同而單獨設置(見圖4)。系統允許更改設置、刪除設置以及立即執(zhí)行計劃、停止執(zhí)行計劃。
新增計劃包括基本信息(主要定義計劃性質,若是回顧性分析需要設置監(jiān)測時間段)、待監(jiān)測的藥品、選擇關注的不良事件、監(jiān)測的病區(qū)范圍。待監(jiān)測藥品直接選取HIS接口的藥品字典,允許選擇多個藥品。
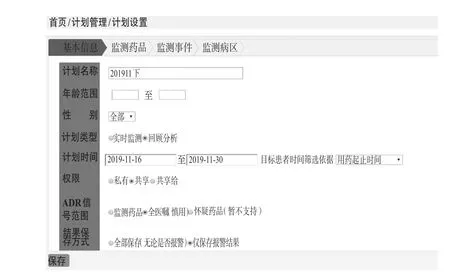
圖4 ADE-ASAS -Ⅱ監(jiān)測的計劃設置Fig 4 Settings of monitoring plan for ADE-ASAS-Ⅱ
監(jiān)測事件是系統的核心算法,由自定義事件功能模塊創(chuàng)建,并允許在特定計劃中修改事件的參數(見圖5)。而監(jiān)測病區(qū)允許用戶選擇特定病區(qū)進行監(jiān)測,如果不選擇指定的病區(qū),系統默認監(jiān)測醫(yī)院所有的病區(qū)。
3.2 事件配置管理
用戶可創(chuàng)建不良事件監(jiān)測觸發(fā)器算法,事件的配置包含納入標準、排除標準、嚴重程度定義和其他共四個選項卡(見圖6)。
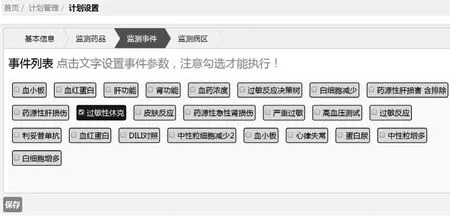
圖5 ADE-ASAS-Ⅱ監(jiān)測事件Fig 5 Monitoring events of ADE-ASAS-Ⅱ
納入標準又分為三個主要指標:①實驗室檢驗(laboratory information system,LIS)指標,LIS指標絕大多數都屬于數字類型,也稱之為量化指標,因此每個LIS指標有大于、大于等于、等于、小于、小于等于的操作。納入指標可以是多個指標的組合。②文本檢索,設定檢索關鍵字或者關鍵字組合,系統將檢索符合檢索條件的所有病人的所有入院記錄、出院記錄、查房記錄、會診記錄等電子病程文檔。③解救藥品。
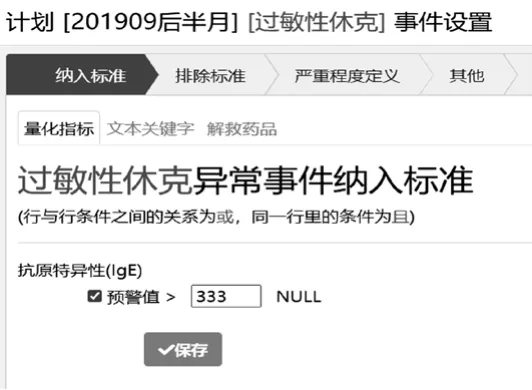
圖6 ADE-ASAS-Ⅱ監(jiān)測事件配置參數Fig 6 Configuration parameters of monitoring events for ADE-ASAS-Ⅱ
3.3 病歷審核評估
計劃的默認執(zhí)行時間為凌晨03:00,是為了避免影響HIS系統的性能。
評估模塊把一個病人的所有在院信息用八個模塊集中展示,方便臨床藥師從整體到局部的排查。八個模塊包括:基本信息、診斷、醫(yī)囑、LIS、PACS、手術、護理(生命體征)、電子病程。在評估界面的最上部分是系統自動監(jiān)測的預警結果,多個預警結果按照數字順序列出。查看電子病程時,會自動對疑似報警關鍵字進行高亮標紅顯示,讓用戶能夠快速定位關鍵字,提高閱讀速度以節(jié)省評估時間。
病人信息的下方為關聯性評價選項。關聯性評價包括:肯定、很可能、可能、可能無關、無法評價等選項,并可以錄入評價的理由。
3.4 ADR報告統計分析
統計評價為肯定、很可能、可能的病例,分析其人口學特征、發(fā)生率、發(fā)生規(guī)律。
新系統可實現重點病例關注、上報,疑難病例討論等功能,為臨床藥師日常工作、藥學專業(yè)人員學習、臨床重點藥品監(jiān)測、醫(yī)院藥學科研、流行病學調查等提供了強有力的技術支持。
4 討論
4.1 自動監(jiān)測模式與路徑需要與時俱進
ADR監(jiān)測是保障公眾安全用藥的重要手段,目前我國ADR監(jiān)測的模式主要為自發(fā)報告(被動監(jiān)測)與主動監(jiān)測(集中監(jiān)測),與全球其他國家采用的基本方法相似,但耗時長、效率低。近年來,美國、歐盟、英國等國家和地區(qū)圍繞電子醫(yī)療數據庫開展的ADR主動監(jiān)測,已有多項研究與實踐[6-7]。國內我們團隊2012年自行研發(fā)成功的自動監(jiān)測專項軟件ADEASAS,基于觸發(fā)器原理和文本識別技術在國內率先實現了醫(yī)療機構重點用藥品種ADE主動監(jiān)測與智能評估警示,能夠實現十多種常見ADE(血小板、紅細胞、白細胞減少及粒細胞減少、肝功能、腎功能、血糖、胰酶異常、皮膚損害、過敏性休克、過敏樣反應、心電異常)的重點品種自動監(jiān)測、并具有較好的陽性報警率。經過多年來的不斷優(yōu)化,既能夠與HIS在用數據庫對接開展實時監(jiān)測,亦可與HIS歷史數據庫對接完成大樣本用藥人群的回顧性監(jiān)測研究[2,8-9]。但囿于當時環(huán)境條件和人工智能算法制約,采用了以重點監(jiān)測藥物為坐標的自動監(jiān)測,其監(jiān)測路徑相對較為固定,必須是通過以HIS中的某一藥物為出發(fā)點,關聯性提取自動監(jiān)測智能評估需要的相關電子醫(yī)療信息,監(jiān)測模式局限于重點藥品/重點事件的一對一和一對多。隨著硬件支持條件的改善和軟件開發(fā)技術的進步,近2年來,我們依托新的算法開展了以ADE為出發(fā)點的自動監(jiān)測評估研究,拓展了監(jiān)測模式,增加了重點藥品/重點事件多對一、進而發(fā)展為多對多的選擇。
4.2 自動監(jiān)測軟件的功能應該持續(xù)拓展
在前期研究的基礎上,我們團隊繼續(xù)深化研發(fā)的ADE-ASAS-Ⅱ,基于圍繞臨床海量電子醫(yī)療數據開展真實世界研究需求設計,具有可一次性實現多種藥物對應同一種ADE的自動監(jiān)測與智能分析警示功能。系統采用的是B/S系統架構,各模塊通過API接口實現互聯,降低了模塊相互依賴的程度,提高了系統擴展性和穩(wěn)定性。研究模式由ADE-ASAS的“模塊確定研究”轉變?yōu)椤把芯看_定模塊”,研究人員基于HIS中的量化指標和文本信息,即可自定義ADR模塊;關鍵詞法可靈活的適用于任意模塊,更可酌情更改報警規(guī)則;系統界面集成性更強,可以在同一界面調取患者的病歷文本、檢驗指標、檢查報告、護理記錄等各種信息,提高了信息查閱、數據提取以及病例評價的效率;開展超大樣本量研究時仍然可選擇性保存報警結果或全部結果,從而盡可能滿足用戶不同目標設計的真實世界研究需求。系統借助人工智能技術分析相關數據信息篩選陽性預警病例,幫助醫(yī)療機構高效、快捷、低儉地開展臨床用藥大樣本、長時程的前瞻/回顧性主動監(jiān)測與評價工作,為重點監(jiān)測品種的風險管控提供科學可信的精準數據。
4.3 自動監(jiān)測軟件的應用前景可期
近年來美國、英國、法國、德國在利用真實世界證據取代傳統臨床試驗的擴大適應癥研究及審批方面,均肯定了真實世界證據(real world evidence,RWE)的價值與意義。我國相關部門也出臺了系列政策,如2019年4月3日衛(wèi)健委發(fā)文《關于開展藥品使用監(jiān)測和臨床綜合評價工作的通知》、2020年1月3日藥監(jiān)局發(fā)文《真實世界證據支持藥物研發(fā)與審評的指導原則(試行)》,鼓勵相關機構利用RWE開展藥物評價研究。醫(yī)療機構的HIS中積累有海量的電子醫(yī)療信息,借助人工智能技術實施大樣本用藥人群的真實世界評價研究具有顯著的自身優(yōu)勢,尤其適用于用藥患者分散在不同病區(qū)、用藥例次數相對較少、因而依靠人工難以收集足夠多完整病例的重點監(jiān)測藥品的評價研究[3-5]。ADE-ASAS-Ⅱ研發(fā)完成后,依托與HIS的適應性對接,高效的實現了ADR發(fā)生率較低、涉及用藥品種眾多的大樣本真實世界藥物安全性評價[10];還可以根據研究需要自動監(jiān)測并篩選獲取所需病例的全部真實世界數據,高效快捷的開展真實世界藥物評價研究[11],成本消耗低、數據可溯源、結果可信、研究質量有保證。ADE-ASAS-Ⅱ不是ADE-ASAS簡單的升級,目前兩者的自動監(jiān)測功能是相互補充的關系,無法完全替換,還有待今后繼續(xù)完善歸一。

