Sb2O3/Sb 鋰離子電池負極材料的制備及電化學性能
張豪杰, 胡業旻
(上海大學材料科學與工程學院, 上海 200444)
近年來, 持續增長的能源需求使得開發高能量密度、清潔的儲能裝置成為研究的熱門, 鋰離子電池體系由于具有高能量密度而備受研究者的關注[1-2].傳統的鋰離子電池負極是石墨,這是因為石墨負極的能量密度為372 mAh·g?1, 且具有良好的循環穩定性和倍率性能.由于消費電子產品的迅速更迭, 新能源汽車以及其他智能設備的發展對儲能裝置提出了更高的要求,傳統的石墨負極很難滿足日益高漲的需求.因此, 開發高能量密度負極材料成為了亟待解決的問題[3-4].
金屬負極通常具有高的理論容量, 例如硅[5]、錫、銻[6]等.銻的理論容量為660 mAh·g?1,儲量豐富且具有較低的放電電壓, 成為一種潛在的鋰離子電池負極材料[7].但是, 銻負極在充放電過程中會發生合金化-脫合金化反應, 在獲得高容量的同時面臨著巨大體積膨脹(290%)的問題.巨大的體積膨脹導致電極材料的破碎粉化, 使電池的循環性能迅速衰減[7-8].解決體積膨脹問題的一種有效途徑是設計復合結構, 如設計合適妥當, 復合物中物相可以優勢互補達到良好的綜合性能[6,9-11].Sb2O3理論容量是1 102 mAh·g?1, 首次放電過程中發生轉化反應生成Li2O, Li2O 充當緩沖相阻止金屬顆粒團聚[10].由于氧化物通常導電性能較差, 在大電流充放電時, 氧化物電極電子傳輸速度差, 從而得到較差的倍率性能.因此, 我們設計了Sb2O3/Sb 復合材料, 其中銻能改善復合物的電子傳輸能力, 而銻的體積膨脹問題能借助轉化反應生成的Li2O 得到改善.
1 實 驗
1.1 三氧化二銻/銻復合物的制備
本工作中使用的原料為實驗室制備的多孔銻.由銻的熱重圖譜可知, Sb 發生明顯氧化的溫度在400?C 附近.因此, 選擇溫度區間300~450?C, 以50?C 的溫度梯度分別對多孔銻進行空氣退火1 h 處理, 加熱速率為5?C/min, 所得樣品分別記為Sb-300、Sb-350、Sb-400、Sb-450, 并分別對其進行掃描電鏡表征.根據不同溫度對形貌的破壞程度, 選定樣品保持最好的350?C 為微氧化溫度.在350?C 下對樣品分別進行空氣退火4、8、12、24 h 處理, 樣品分別記為Sb-350-4、Sb-350-8、Sb-350-12、Sb-350-24, 然后分別對其進行表征與電化學性能測試.
1.2 電池裝配及電化學測試
首先將制備的樣品、導電劑(乙炔黑)、粘接劑(黃原膠)按照8∶1∶1 制備漿料, 再加入適量去離子水混合攪拌均勻后, 用涂膜機在銅箔上進行涂膜, 最后將膜放在真空干燥箱(80?C)中干燥12 h.干燥后的電極片用裁片機裁成直徑為12 cm 的電極片, 再放于手套箱(水蒸氣和氧氣的質量分數均小于10?7)中, 使用鋰金屬片作為對電極, 六氟磷酸鋰作為電解液封裝電池.封裝好的電池放置12 h 后進行恒電流充放電測試, 電化學窗口為0~3 V, 循環伏安(cyclic voltammetry, CV)測試的電壓窗口為0~3.0V, 掃速為0.1 mV·s?1.
1.3 材料的表征
使用X 射線衍射(X-ray diffraction, XRD)對材料的物相進行表征.材料的微觀形貌使用掃描電鏡(scanning electron microscope, SEM)和透射電子顯微鏡(transmission electron microscope, TEM)進行表征.采用差熱-熱重分析法(thermogravimetric analysis-differential thermal analysis, TG-DTA)對Sb2O3/Sb 復合材料中Sb2O3的含量進行定量分析.
2 結果與討論
2.1 結構與形貌
圖1 和2 分別為實驗室制備的多孔銻和Sb2O3/Sb 復合材料的XRD 圖譜和SME 圖.由圖1 可知: 樣品多孔銻的峰位與標準PDF 卡85-1322 吻合, 確定此物相為Sb;其他樣品中除了含有Sb 外, 還含有另外一種相, 對照標準PDF71-0365 證明其為Sb2O3.隨著氧化時間的延長,發現在2θ=27.8?、32.2?、46.2?處峰信號的強度逐漸增強, 可知Sb2O3取向生長在進一步增加.
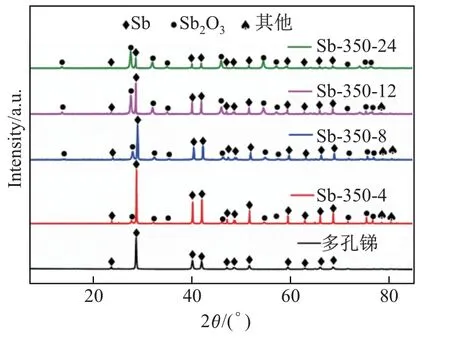
圖1 多孔銻和Sb2O3/Sb 復合材料的XRD 圖譜Fig.1 XRD pattern of porous Sb and Sb2O3/Sb composites
由圖2(a)可知, 多孔銻顆粒大小均勻, 為10μm 左右的金屬塊, 孔徑連通, 分布均勻.由圖2(b)可知, Sb-300 形貌基本與多孔銻一致, 未發生變化, 這可能是因為溫度太低, 銻的氧化速率極慢.圖2(e)中樣品部分泛白, 這是因為此部分不導電, 表明此位置發生了燒結, 溫度太高, 氧化反應劇烈.因此, 考慮樣品制備的效率, 本工作中微氧化溫度選擇350?C.圖2(f)中樣品仍具有多孔結構.圖3(g)中樣品表面有明顯的顆粒狀起伏出現, 這可能是存在新生的Sb2O3.圖2(h)與圖2(g)類似, 均有球形顆粒生成.圖2(i)中樣品整個顆粒更加密實, 孔徑只存在樣品表面, 這可能是微氧化時間過長所致.

圖2 多孔銻和Sb2O3/Sb 復合材料的掃描電鏡圖Fig.2 SEM images of porous Sb and Sb2O3/Sb composite
圖3 為Sb-350-8 樣品的氮氣吸脫附曲線和孔徑分布.由圖3 可以看出, Sb-350-8 樣品的氮氣吸脫附曲線屬于Ⅳ型吸脫附等溫線.通過BET(Brunauor-Emmett-Teller)方法計算, 可知Sb-350-8 樣品的比表面積為3.55 m2/g.另外, 由圖3(c)可知, Sb-350-8 樣品的孔徑集中分布在2~15 nm, 保持了較好的孔徑結構.
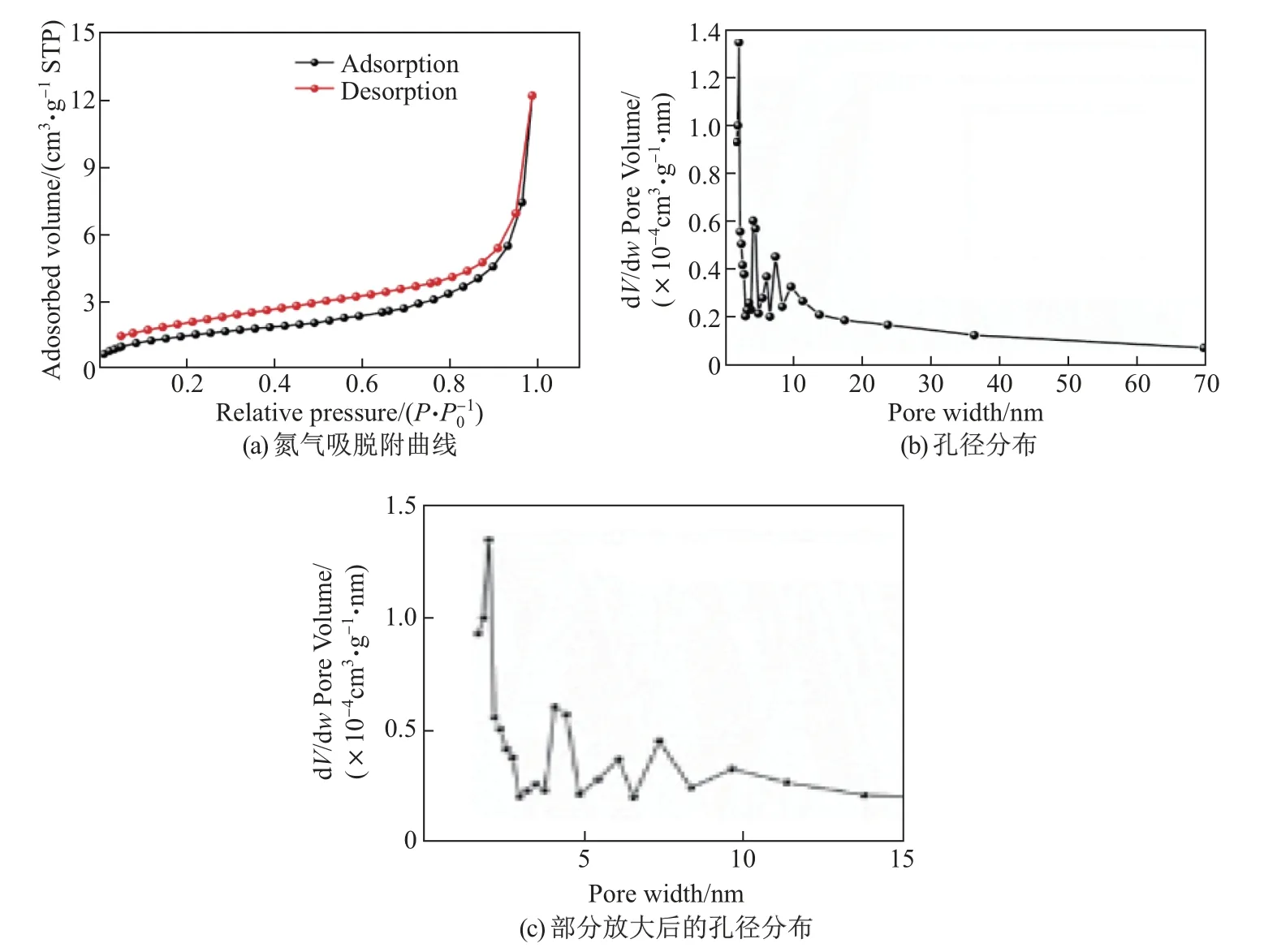
圖3 樣品Sb-350-8 的N2 吸脫附曲線和孔徑分布Fig.3 N2 adsorption-desorption isotherms and pore distribution of Sb-350-8 sample
圖4 為Sb-350-8 樣品的透射電鏡圖.由圖4(a)可以看出: 經過微氧化處理后的樣品仍然維持堅固的銻骨架(深色部分), 新生的Sb2O3相鄰生長, 形成了一種獨特的孔徑結構;區域1(見圖4(b))的晶格條紋間距為3.10 nm, 與Sb(012)的晶面間距相吻合, 該區域的傅里葉變換圖為周期性排列的點, 說明了Sb 為單晶形態;區域2(見圖4(b))的晶格條紋間距為2.79 nm,與Sb2O3(400)的晶面間距相吻合, 該區域的傅里葉變換圖為衍射環, 說明了Sb2O3是多晶形態.圖5 為Sb-350-8 樣品的面掃描能譜圖.可以看出, 銻與氧元素均勻地分布在樣品表面, 說明在樣品的表面很可能形成了Sb2O3的包裹層.
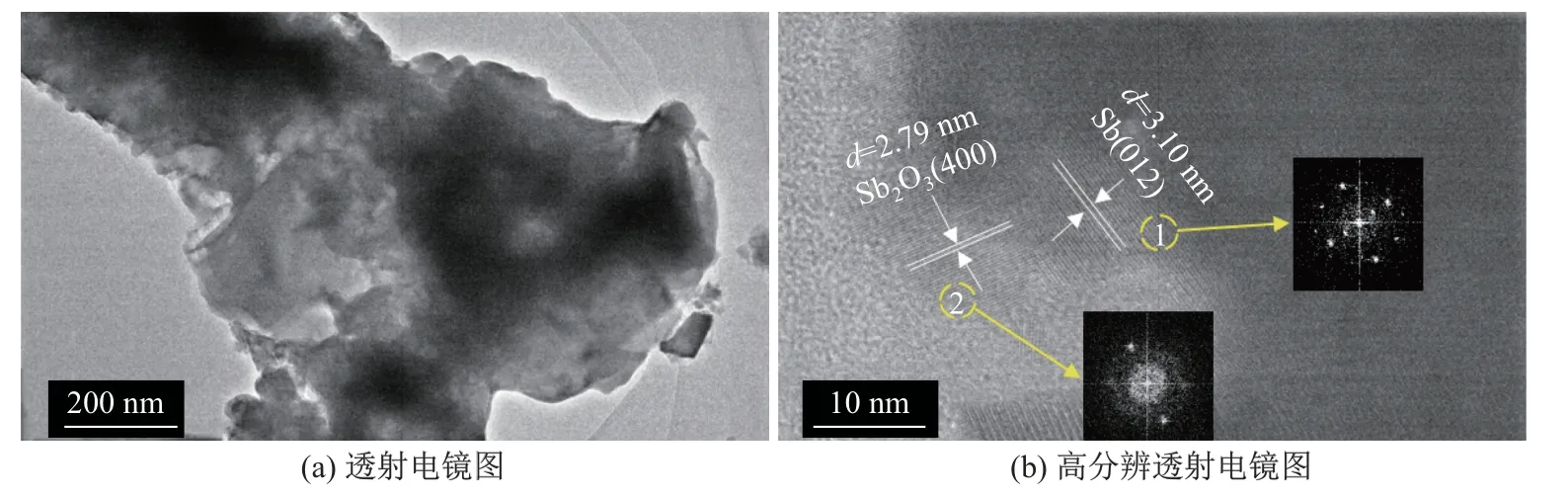
圖4 Sb-350-8 樣品的透射電鏡圖Fig.4 TEM and HR-TEM of Sb-350-8 sample

圖5 Sb-350-8 樣品的面掃描能譜圖Fig.5 Elemental pattern of Sb, O of the Sb-350-8 sample
為了定量表征不同樣品中Sb2O3的含量, 分別對樣品Sb-350-4、Sb-350-8、Sb-350-12、Sb-350-24 進行TG-DTA 分析, 并由樣品Sb-350-4 來說明樣品中Sb2O3的含量.圖6 為多孔銻和Sb2O3/Sb 復合材料樣品的TG-DTA 曲線, 從圖中6(a)可以看出: 在0~200?C 時樣品的質量一直在減小, 這可能是樣品中水分的揮發造成的[12];樣品的增重階段為370~560?C, 對應Sb 的氧化反應, 該階段出現兩個放熱峰, 分別是457 和553?C, 這是Sb 的多步氧化(Sb→Sb2O3→Sb2O4)所致[8];560?C 之后質量保持恒定, 說明此時氧化過程已經完成.Sb-350-4 的組成為Sb 和Sb2O3, 由于370~560?C 對應著樣品的氧化過程, 560?C 后的產物為Sb2O4.由圖6(b)可知, 樣品質量的增加?m= 19.7%, 由反應前產物可知, 樣品的變化為Sb-350-4 中Sb 得兩個O, Sb2O3得一個O 所致, 因此可以計算出Sb-350-4 中Sb2O3的質量分數為30.3%.圖6(c)、(d)、(e)中, ?m分別為11.3%、10.7%、10%, 對應樣品中Sb2O3的質量分數分別為70.5%、74.9%、78.3%.由4 個樣品中Sb2O3的含量可知, 350?C 時, 隨著反應時間的延長, Sb2O3含量增加速率越來越緩慢, 這可能是因為新生的Sb2O3覆蓋在Sb 上, 使內部的Sb 更難接觸到空氣中O2, 從而減緩了反應的速度.
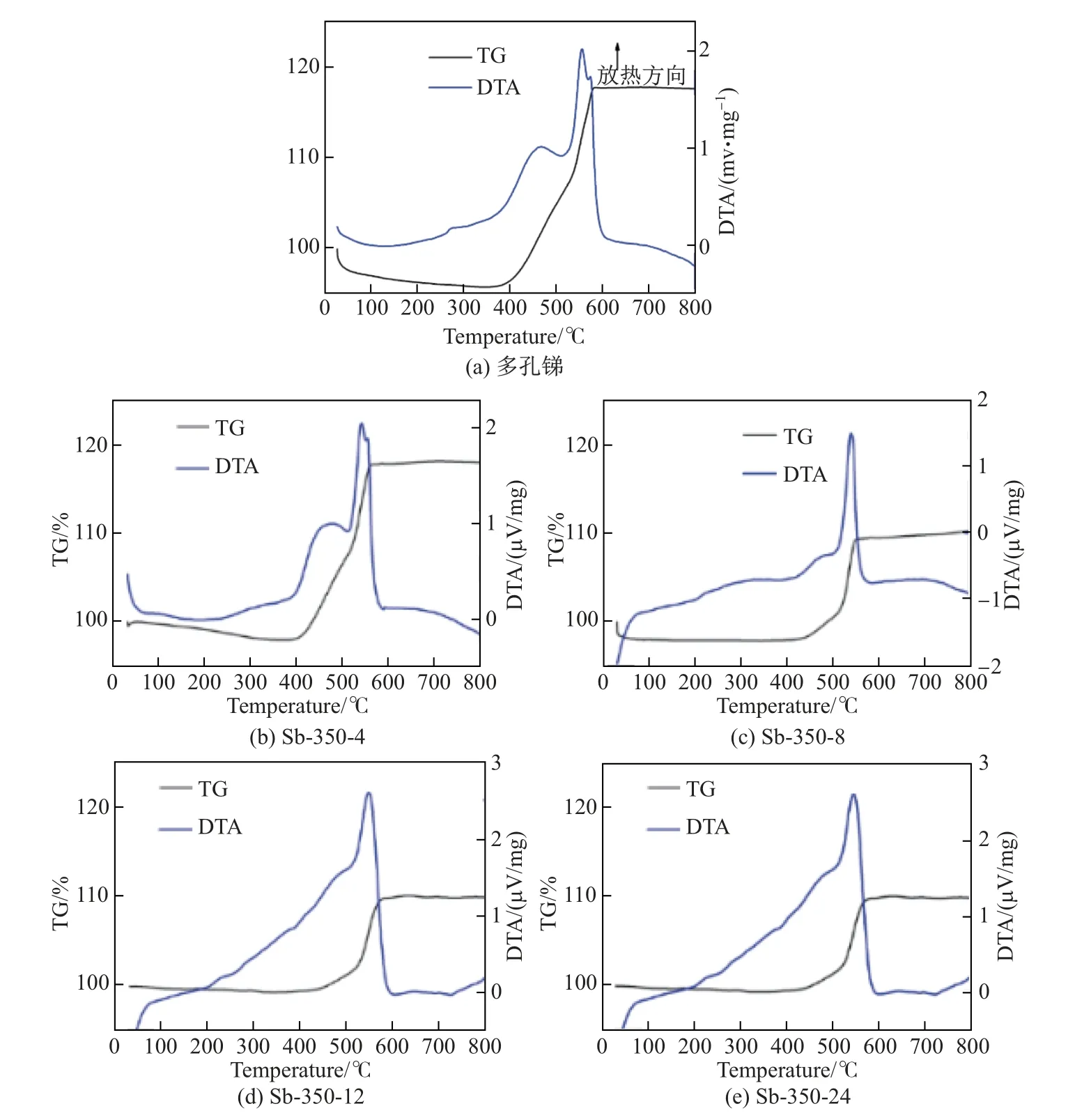
圖6 多孔銻和Sb2O3/Sb 復合材料的TG-DTA 圖Fig.6 TG-DTA diagrams of porous Sb and Sb2O3/Sb composites
2.2 電化學性能
圖7(a)為Sb-350-8 的循環伏安曲線.可以看出: 在首次掃描中1.03 V 處出現了一個較寬的還原峰, 0.61 V 處出現了第二個尖銳的還原峰, 分別對應著Sb2O3+Li→Sb+Li2O,Sb+Li→Li3Sb 反應;在隨后的反掃過程中, 1.03 V 附近的還原峰消失, 說明了轉化反應的不可逆性;在1.20 V 的掃描中, 氧化還原峰位穩定, 說明了電極具有良好的可逆性.圖7(b)為電流密度為200 mA·g?1時Sb-350-8 的充放電曲線.可以看出: 在1.2 V 處出現了放電平臺,對應著Sb2O3與Li 發生轉化反應生成Li2O, 在0.82 V 處出現了放電平臺, 這是Sb 與Li 生成Li3Sb 所致[10];在隨后的充放電曲線中, 1.2 V 的平臺消失, 說明了轉化反應的不可逆性, 而這與CV 的結果相對應.Sb-350-8 電極的首次放電比容量為1 272.1 mAh·g?1, 首次充電比容量為994.7 mAh·g?1, 首次庫倫效率為78.2%.圖8(a)為電流密度為200 mA·g?1時Sb2O3/Sb 樣品的循環性能圖.經過100 圈循環后Sb-350-4、Sb-350-8、Sb-350-12、Sb-350-24 的容量剩余分別為481.2、729.6、552.0、563.67 mAh·g?1.Sb-350-4 雖然具有較好的循環能力, 但是由于Sb2O3的含量較低(30.3%), 故容量較低.Sb-350-12、Sb-350-24 雖然初始容量較高, 但是穩定性較差, 這可能由于Sb2O3的含量過高使得復合物電子傳輸能力急劇下降, 顆粒破碎嚴重最終導致樣品的循環性能急劇下降.Sb-350-8 容量剩余729.6 mAh·g?1, 容量保持為73.34%,遠高于多孔銻(426 mAh·g?1), 這得益于該復合物中Sb2O3含量適中, 新生的Sb2O3形成了不同于多孔銻的獨特孔結構, 以及Sb2O3與Sb 的協同效應[10].圖8(b)為樣品Sb-350 的倍率性能測試圖, 電流密度為50、100、200、500、1 000、2 000、3 000、5 000、10 000 mA·g?1時,Sb-350-8 的容量分別為954、890、850、787、726、653、570、420、203 mAh·g?1.在電流密度重置為100 mA·g?1時, 容量回復至820 mAh·g?1, 表現了良好的可逆性, 并且在各個電流密度下, 其容量均是樣品中最高的.Sb-350-8 號樣品表現了優秀的電化學性能, 這是由于其獨特的Sb2O3/Sb 結構設計.在Sb2O3/Sb 復合材料中, Sb2O3在提供高容量的同時, 在首次放電Sb2O3發生轉化反應, 生成的一部分不可逆Li2O 可以阻止因巨大的體積膨脹而造成Sb 破碎引起的團聚現象, 緩解內部應力, 而Sb 可以加速電子傳導, 增加復合材料的導電性, 從而加速電化學反應, 有利于循環性能的提升.Sb2O3與Sb 之間的這種協同效應使Sb-350-8 表現了優異的電化學性能[8,10,13].為了進一步評價Sb-350-8 的儲鋰性能, 采用商業磷酸鐵鋰[14]作為全電池的正極, Sb-350-8 復合物作為負極, 全電池的電壓窗口為2.5~4.0 V, Sb-350-8 復合物電極在全電池封裝前進行預鋰化處理.圖9 為全電池的充放電曲線和循環性能.由圖9 可見,放電平臺在2.2 V 左右、電流密度為200 mA·g?1時, 循環30 圈后, 電池容量為90 mAh·g?1, 庫倫效率為97.1%, 展現了較好的循環性能.
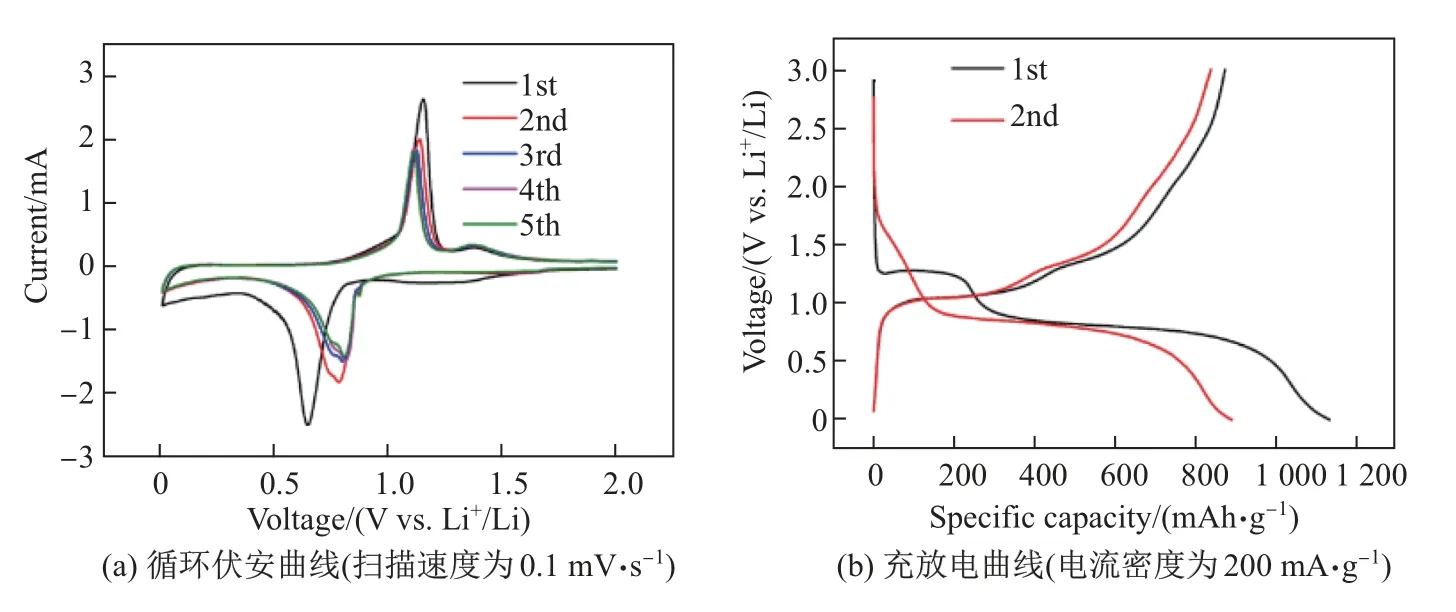
圖7 樣品Sb-350-8 的循環伏安曲線和充放電曲線Fig.7 CV curve and charge-discharge curve of Sb-350-8 sample
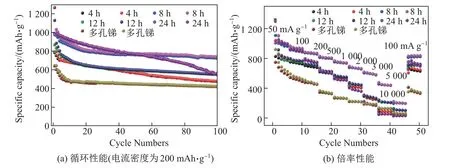
圖8 多孔銻和Sb-350 復合材料的循環性能和倍率性能Fig.8 Cycle performance and rate performance of porous Sb and Sb-350 samples
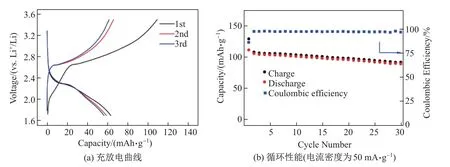
圖9 LiFePO4-Sb2O3/Sb 全電池的充放電曲線和循環性能Fig.9 Charge-discharge diagram and cycle performance of LiFePO4-Sb2O3/Sb full cell
3 結束語
本工作通過梯度試驗確定微氧化溫度, 通過控制氧化時長來控制Sb2O3的含量, 制備了Sb2O3/Sb 復合物材料, 并對樣品進行了SEM、XRD、TEM, TG-DTA 表征和電化學性能測試.經過350?C 微氧化8 h 的樣品中Sb2O3的含量為70.5%, 其中新生的相鄰的Sb2O3之間接觸形成了多孔結構, 整體具有密實的結構.Sb2O3/Sb 復合材料表現出了優秀的電化學性能,電流密度為200 mA·g?1時首次庫倫效率為78.2%, 循環100 圈后容量高達729.6 mAh·g?1, 電流密度為10 000 mA·g?1時,容量仍有203 mAh·g?1.Sb2O3/Sb 復合材料表現出優異的電化學性能, 歸因于Sb2O3與Sb 形成的協同效應: Sb2O3提供高容量;基于轉化反應生成的Li2O 組織Sb 團聚, 緩解應力;Sb 提高材料的電子傳輸能力, 提高電化學反應動力, 有利于電化學反應的進行.Sb2O3/Sb 復合材料的制備為制備其他高性能金屬-氧化物型復合材料提供了一個良好的思路.

