金屬有機骨架衍生雙金屬氧化物的鋰離性能
張燕鋒, 蔡 昌, 談馨怡, 孫煒偉
(上海大學環境與化學工程學院, 上海 200444)
隨著人類社會經濟全球化的不斷發展, 能源危機和環境污染等問題日趨嚴重, 使得人類不斷面臨新的挑戰.清潔、可再生能源的研究越來越受到關注.鋰離子電池是一種重要的綠色能源儲存裝置.與傳統的二次電池(鉛酸電池、鎳鎘電池、鎳氫電池等)相比, 鋰離子電池具有工作電壓高、能量密度大、循環壽命長、無污染、無記憶效應等特點, 因此成為了未來高性能電池的主要發展方向[1-2].電極材料是鋰離子電池的關鍵組成部分, 其電化學性能對高性能鋰離子電池的進一步發展有決定性作用.探索研發新型高性能的電極材料將有助于加速鋰離子電池的發展.目前, 金屬氧化物Co3O4, CoO, NiO, Fe2O3, CuO, MnO2等是鋰離子電池負極材料的研究熱點, 這類金屬氧化物材料用作鋰離子電池負極材料時表現出高的理論比容量[3-10].但這類金屬氧化物的電子電導率差[11].另外, 這類金屬氧化物在充放電過程中存在與金屬單質的來回轉換, 由于二者的尺寸大小差距比較明顯, 使得金屬氧化物電極材料的體積變化較大, 從而容易導致材料粉化、團聚, 嚴重影響電極材料的可逆容量和循環壽命.為了更有效地提升金屬氧化物的儲鋰性能, 常通過構筑特殊的微觀形貌如立體結構、多孔結構、空心結構等[12-17], 或通過與含碳材料復合的方式[18-20]來改善其結構穩定性, 從而提升其電化學性能.值得一提的是, 金屬有機骨架作為前驅體衍生得到的金屬氧化物電極材料因大多可以延承金屬有機骨架的特殊形貌和多孔特性而具有明顯改善的電化學性能, 得到了研究者的廣泛關注.本工作以雙金屬有機骨架為前驅體合成得到Co/Zn 雙金屬氧化物材料, 并將其用作鋰離子電池負極材料進行電化學性能測試.
1 實驗部分
1.1 雙金屬有機骨架的制備
稱取一定量的六水合硝酸鈷Co(NO3)2·6H2O、六水合硝酸鋅Zn(NO3)2·6H2O 和2,5-二羥基對苯二甲酸(2,5-dihydroxyterephthalic acid, DOBDC), DOBDC 與混合金屬離子的摩爾比為3∶1.首先, 將兩種反應物混合后溶于N,N-二甲基甲酰胺(dimethyl formamide, DMF)、乙醇和水(質量比為1∶1∶1)組成的混合溶液, 攪拌均勻后, 轉移到微波玻璃管中; 然后, 放進微波合成儀, 設定130°C, 保溫1 h, 反應完成后得到黃紅色沉淀; 將所得的沉淀離心, 乙醇洗7 次后, 再在真空干燥箱中60°C 干燥12 h, 得到的黃紅色粉末即為雙金屬有機骨架Co/Zn-MOF-74, 收集待用.通過類似的合成方法, 只添加鈷源, 沒有鋅源, 可以制備得到單金屬有機骨架Co-MOF-74.
1.2 雙金屬氧化物的制備
將制備好的Co/Zn-MOF-74 雙金屬有機骨架材料放入石英舟, 再將石英舟放入管式爐中,以2°C/min 的速率升溫至500°C, 保持2 h, 最后冷卻得到的黑色粉末即為Co-Zn-O 雙金屬氧化物.選擇單金屬有機骨架材料Co-MOF-74 作為前驅體, 通過類似的煅燒方法可以得到對比產物二元金屬氧化物Co3O4.
1.3 材料表征和測試儀器
采用日立公司的Rigaku D/max-2550 V 型X 射線衍射(X-ray diffraction, XRD)儀對所得的樣品進行物相分析, 測試條件如下: 輻射源為CuKα 射線,λ= 0.154 18 nm, 入射狹縫寬度為0.05 mm, 接收狹縫寬度為0.15 mm, 掃描速度為8(°)/min, 掃描角度為2θ= 5°~85°,工作電壓為18 kV, 電流為30 mA.采用JEOL 公司的JSM-6700F 場發射掃描電鏡(scanning electron microscope, SEM)觀測粉末試樣的表面形貌, 加速電壓為15 kV.采用JEOL 公司的JEM-200CX 型透射電鏡(transmission electron microscope, TEM)、JEM-2010F 型高分辨透射電鏡觀察樣品的大小、形態和晶格結構.采用Micromeritics Instrument Corp 的ASAP2020 M+C 型分析儀在77 K 下進行N2吸脫附等溫線的測量.測量前, 樣品需要在150°C 真空預處理5 h.循環伏安測試采用CHI660D 型電化學工作站, 掃描速度為0.1 mV/s.電化學測試在藍電CT2001A 電池測試儀上進行, 將裝配好的電池靜置3 h 后進行電化學性能測試, 充放電電壓窗口為0.005~3.0 V, 室溫測試, 充放電測試的電流密度為100 mA/g.
2 結果與討論
制備雙金屬有機骨架材料常用的方法之一是先制備一種單金屬有機骨架結構, 然后將其與另外一種金屬的鹽溶液混合, 通過離子交換獲得[21-22].這樣制備得到的雙金屬有機骨架結構傾向于形成核殼結構, 兩種不同的金屬離子在整個骨架結構及其衍生結構中呈現不均勻分布.本工作選擇一步微波合成法成功制備了具有棒狀形貌的Co/Zn 雙金屬有機骨架材料,在空氣中500°C 煅燒2 h 后, 得到了由納米粒子組成的Co-Zn-O 雙金屬氧化物多孔微米棒.圖1 為金屬有機骨架Co/Zn-MOF-74 和Co-MOF-74 的XRD 圖譜.從圖中可以看出, 兩種金屬有機骨架結構均具有很好的結晶度, 其特征峰也可以很好地重合, 從而證明了雙金屬有機骨架結構的成功合成.圖2 為Co/Zn-MOF-74 前驅體在空氣中煅燒后得到的雙金屬氧化物Co-Zn-O 的XRD 圖譜.由圖2 可以看出, 18.9°, 31.1°, 36.7°, 38.4°, 44.6°, 55.4°, 59.1°, 65.0°,68.3°, 77.4°處的特征衍射峰與ZnCo2O4(PDF#23-1390)或Co3O4(PDF#43-1003)的特征峰一致, 說明Co-Zn-O 是由ZnCo2O4或Co3O4或兩種物質混合組成.
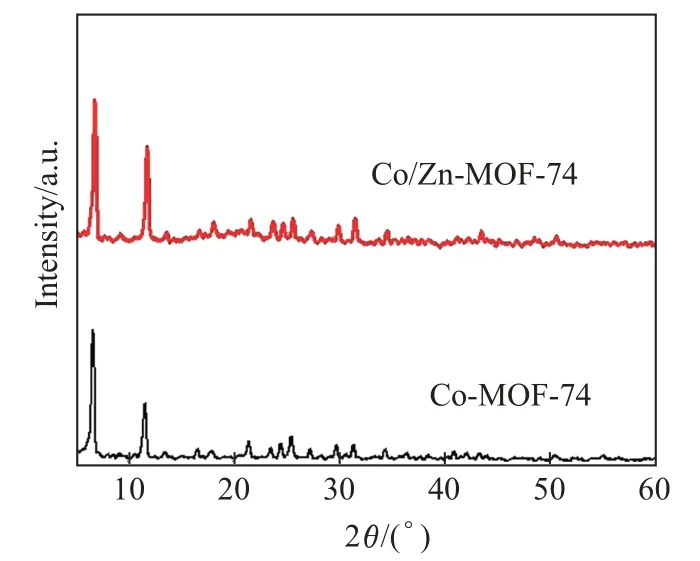
圖1 Co/Zn-MOF-74和Co-MOF-74的XRD圖譜Fig.1 XRD patterns of Co/Zn-MOF-74 and Co-MOF-74

圖2 Co-Zn-O和Co3O4的XRD圖譜Fig.2 XRD patterns of Co-Zn-O and Co3O4
圖3 為Co-Zn-O 的能量色散光譜(energy-dispersive spectrometry, EDS)圖.由圖3 可知, Co-Zn-O 由Co, Zn, O 3 種元素組成.經過計算可知, Co-Zn-O 中Co, Zn 原子的比例約為9.2∶1.0, 這與合成雙金屬有機骨架前驅體時兩種不同金屬鹽的投料比基本一致.由此可以推斷, 雙金屬氧化物Co-Zn-O 是ZnCo2O4和Co3O4組成的混合物.

圖3 Co-Zn-O 的EDS 圖Fig.3 EDS spectrum of Co-Zn-O
對一步微波法得到的Co/Zn-MOF-74 和其衍生的Co-Zn-O 雙金屬氧化物進行形貌表征,結果如圖4 和5 所示.由圖4 可以看出, Co/Zn-MOF-74 前驅體具有微米棒的形貌, 表面較為光滑.而由圖5(a)可以看到,Co-Zn-O 材料呈現多孔的微米棒形貌,該微米棒具有粗糙的表面.由圖5(b)可以清晰看出, Co-Zn-O 微米棒是通過納米粒子致密交聯而形成的, 這種納米粒子交聯形成的結構具有更好的結構穩定性.圖5(c)是煅燒Co-MOF-74 得到的對比產物Co3O4的SEM 圖.由圖5(c)可以看出, Co3O4也呈現出由納米粒子構成的多孔微米棒形貌.

圖4 Co/Zn-MOF-74 的SEM 圖Fig.4 SEM image of Co/Zn-MOF-74

圖5 Co-Zn-O 的TEM 圖, Co-Zn-O 和Co3O4 的SEM 圖Fig.5 TEM image of Co-Zn-O, and SEM images of Co-Zn-O and Co3O4
圖6 是Co-Zn-O 微米棒在77 K 下氮氣的吸脫附曲線和孔徑分布, 其中圖6(b)中V為體積,D為孔徑.通過計算可知, Co-Zn-O 微米棒的比表面積為20.3 m2/g, 孔徑分布為10~15 nm.
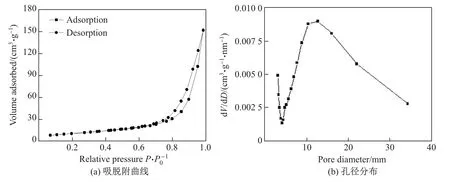
圖6 Co-Zn-O 在77 K 下氮氣的吸脫附曲線和孔徑分布Fig.6 Nitrogen adsorption-desorption isotherm and pore size distribution of Co-Zn-O
為了研究Co-Zn-O 雙金屬氧化物的儲鋰性能, 測試Co-Zn-O 作為鋰離子電池負極材料的電化學性能.Co-Zn-O 雙金屬氧化物前三圈的CV 和充放電曲線如圖7 所示.由圖7(a) 可以看出, 0.82 V 處出現一個較長的平臺, 是因為歸屬于Co-Zn-O 中的氧化鈷被還原為Co 單質以及固體電解質界面(solid electrolyte interface, SEI) 膜的形成, 而0.39 V 處的峰歸屬為LiZn 合金的形成, 1.55 V 和2.04 V 的峰分別對應Zn 和LiZn 變為ZnO 以及Co的氧化.后續的兩圈0.82 V 處的峰轉移到了1.01 V 處.而由圖7(b) 可以明顯地看到分別歸屬于Co 和Zn 的兩個平臺, 這與CV 曲線的結果是一致的.圖8 為主產物Co-Zn-O 和對比產物Co3O4在100 mA·g?1電流密度下的循環性能.由圖8 可知: Co3O4微米棒電極材料首圈放電比容量與充電比容量分別為1 522 和1 098 mA·h·g?1, 經過100 圈的循環, 充電比容量僅為560 mA·h·g?1; 相比而言, 主產物Co-Zn-O 雙金屬氧化物展現出了更高的比容量和更優異的循環性能, Co-Zn-O微米棒的首圈放電比容量與充電容量分別為1 620 和953 mA·h·g?1, 庫侖效率為59%, 經過100 圈的充放電循環后, 其充電比容量上升至1 137 mA·h·g?1.隨著循環圈數增加, 電極材料比容量增加, 這種現象在過渡金屬氧化物中是很常見的[23-27], 主要是由于隨著循環的增加, 材料不斷被活化, 從而提高了鋰離子擴散的動力學性能.

圖7 Co-Zn-O 微米棒前三圈的循環伏安和充放電曲線Fig.7 First three cyclic voltammetry curves and discharge/charge curves of Co-Zn-O microrod
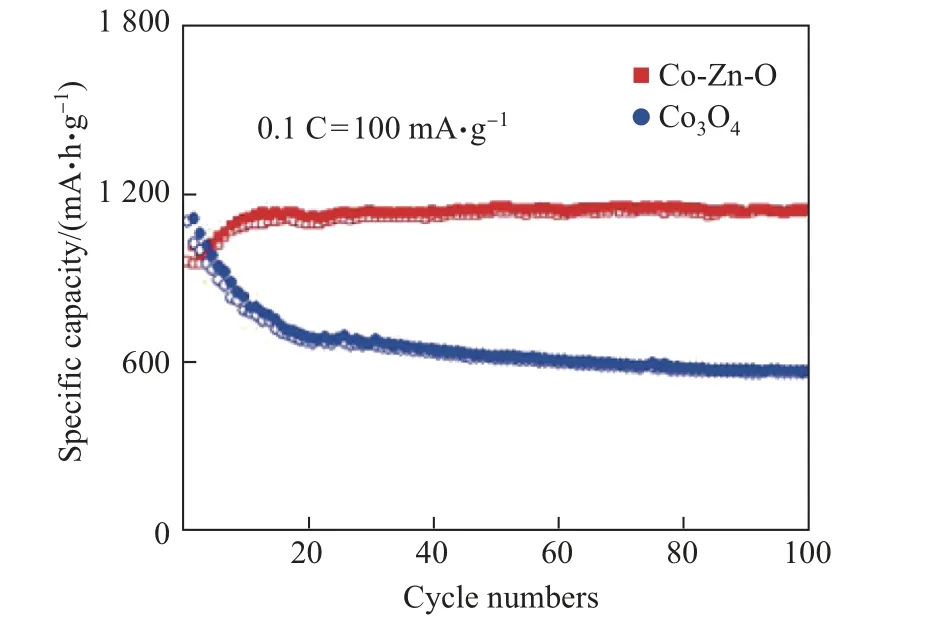
圖8 Co-Zn-O 和Co3O4 在100 mA·g?1 電流密度下的循環性能Fig.8 Cycling performances of Co-Zn-O and Co3O4 at 100 mA·g?1
圖9 是氧化物Co-Zn-O 和Co3O4的交流阻抗和等效電路模型.圖9(b)中Re表示高頻區電解質和電極的歐姆電阻,Rct表示中頻區電荷轉移電阻,Zw表示與低頻區離子擴散有關Warburg 阻抗, 常相位角元件(constant phase angle element, CPE)表示雙層電容和鈍化膜電容.從圖9(a)中可以看出, 在中頻區域中顯示的Co-Zn-O 比Co3O4具有更小的半周期, 表明由Co-Zn-O 的獨特結構帶來的更小的電荷轉移電阻以及增強的電荷轉移效率.圖10 是Co-Zn-O電極循環100 圈后的TEM 圖.由圖10 可以看出, 循環后的材料基本保持了微米棒的形貌, 說明該材料具有較好的結構穩定性.

圖9 Co-Zn-O 和Co3O4 的Nyquist 圖和等效電路模型Fig.9 Nyquist plots and the equivalent circuit model of Co-Zn-O and Co3O4

圖10 Co-Zn-O 電極在循環100 圈后的TEM 圖Fig.10 TEM image of Co-Zn-O electrode after 100 cycles
綜上所述, 本工作中由雙金屬有機骨架為前驅體衍生獲得的Co-Zn-O 雙金屬氧化物具有高的比容量以及優秀的循環性能, 主要歸因于:
(1) Co-Zn-O 雙金屬氧化物很好地繼承了雙金屬有機骨架前驅體的微米棒形貌與多孔特性.煅燒后的多孔結構可以使材料更好地與電解液接觸, 提供更大的活化面積和更多的嵌鋰電位, 大孔結構則可以加快電解液的傳輸.同時, 孔內間隙和材料多層間的間隙空間可以對鋰離子嵌脫過程中材料的體積變化進行緩沖來保持結構的穩定性.
(2) Co-Zn-O 雙金屬氧化物中氧化鈷與氧化鋅有不同的嵌鋰平臺, 這就使得氧化鈷的嵌鋰還原的過程中, 氧化鋅在此電壓下還沒有活化, 其可以充當緩沖物質來緩沖氧化鈷嵌鋰還原過程中的體積膨脹.而在氧化鋅嵌鋰還原為鋅單質的過程中, 氧化鈷已經還原為鈷單質, 此時的鈷單質也可以緩沖氧化鋅嵌鋰過程中的體積膨脹.
3 結束語
本工作以六水合硝酸鈷為鈷源、六水合硝酸鋅為鋅源、2,5-二羥基對苯二甲酸為有機配體制備了含有Co 和Zn 的雙金屬有機骨架材料, 并以此為前驅體煅燒制備得到由納米粒子組裝形成的雙金屬氧化物Co-Zn-O 多孔微米棒材料.雙金屬氧化物Co-Zn-O 作為鋰離子電池負極材料時, 較二元氧化物材料表現出了更高的比容量與更優異的循環穩定性, 主要可以歸因于該材料具有的多孔棒狀構型及兩種不同金屬組分之間的協同儲鋰作用.

