貝伐珠單抗聯合化療治療晚期乳腺癌療效及安全性的Meta分析
杜林娟,劉 霜,李 明,王春光
2018年全球新發癌癥1 810萬例,統計數據顯示女性患者乳腺癌發病率最高,約占總數的1/4,同時也是癌癥死亡的主要原因[1]。2015年,中國惡性腫瘤流行分析結果顯示,乳腺癌新發病例為30.4萬例,死亡為7萬例,發病率及死亡率呈逐年上升趨勢[2]。乳腺癌儼然已成為危害女性健康的一大公敵。晚期轉移性乳腺癌治療較棘手,已知常規治療手段為內分泌及化療等全身治療,治愈可能性小。血管內皮生長因子(vascular endothelial growth factor,VEGF)是血管生成過程中的關鍵信號分子,阻斷該通路是公認的腫瘤治療靶點[3],貝伐珠單抗是一種可與VEGF結合的人源化單克隆抗體。為此全球展開了多項貝伐珠單抗聯合化療治療晚期乳腺癌的臨床研究。2項隨機對照試驗AVF2119g研究[4]及E2100研究[5]結果顯示,聯合治療可改善患者客觀緩解率(objective response rate,ORR),然而對于中位無進展生存期(median progression free survival,mPFS)結果仍存在爭議。其后,E2100研究[5]直接促進2008年美國食品藥品監督管理局(food and drug administratin,FDA)加快批準貝伐單抗聯合化療用于人類表皮生長因子受體2(human epidermal growth fctor recptor-2,HER-2)陰性晚期轉移性乳腺癌的一線治療,但由于后來對安全性的擔憂以及隨機臨床試驗中總體生存率缺乏改善,該批準在2010年被撤銷[6]。因此,本研究通過納入多項隨機對照研究以系統評價貝伐珠單抗聯合化療治療晚期乳腺癌的療效及安全性,以期為晚期乳腺癌的臨床治療提供更多的循證醫學證據。
1 資料與方法
1.1 文獻檢索
計算機檢索PubMed、The Cochrane Library、EMbase、CNKI、維普和萬方等數據庫中化療聯合貝伐珠單抗治療晚期乳腺癌的隨機對照臨床試驗(randomized controlled trial,RCT)。英文檢索詞包括“chemotherapy”、“metastatic breast cancer”、“bevacizumab”、“clinical trial”、“breast cancer”和“avastin”;中文檢索詞包括“晚期乳腺癌”、“聯合化療”、“貝伐珠單抗”、“臨床試驗”、“療效評估”、“安維汀”和“抗血管生成抑制劑”,并根據入選文獻的參考文獻進一步擴大檢索相關數據庫如MEDLINE和SpringerLink,檢索時限均為各數據庫建庫起至2020年9月。
1.2 文獻納入與排除標準
1.2.1 納入標準
研究類型:國內外公開發表的隨機對照臨床試驗,語種限制為中文和英文。研究對象:(1)病理及影像學確診的Ⅳ期乳腺癌患者;(2)存在可測量病灶者;(3)按美國東部腫瘤協作組(Eastern Cooperative Oncology Group,ECOG)體力狀況評分標準評為0~2分者,無其他化療禁忌癥,可耐受相關治療;(4)種族、年齡和性別不限。
治療方法:(1)試驗組為各種靜脈及口服化療藥聯合貝伐珠單抗;對照組為單用各種靜脈及口服化療藥。劑量、用法按照說明書及專家共識推薦為準。
結局指標及療效判定:結局指標包括(1)ORR;(2)中位總生存期(median overall survival,mOS);(3)mPFS;(4)安全性和耐受性評估根據常見不良事件評價標準(National Cancer Institue-Common Terminology Criteria AdverseEvents,NCI-CTCAE)評估其嚴重程度。療效判定:依據實體腫瘤療效評價標準(Response E-valuation Criteria in Solid Tumors,RECIST)進行療效判定。
1.2.2 排除標準
(1)相關結局指標缺失;(2)重復發表的文獻;(3)非隨機對照臨床試驗。
1.3 文獻篩選、資料提取及質量評價
由2名研究者獨立按照文獻納入排除標準閱讀文獻題目及摘要,排除不具備納入標準的文獻,通過閱讀全篇文獻,確定納入的文獻,并提取相關數據,對存在分歧的地方進行討論并由第3名研究員判定。如有需要,通過郵件、電話聯系原始作者獲取未確定但對本研究重要的信息。納入的文獻采用Cochrane Hand book 5.1.0推薦的偏倚風險評估工具評價納入研究質量。如遇分歧通過討論或參考第3位研究者意見決定。
1.4 統計學方法
采用RevMan 5.3軟件進行Meta分析。結局指標ORR及不良反應事件以比值比(odds ratio,OR)及其95%可信區間(confidence interval,CI)為效應量,mOS和mPFS以風險比(hazard ratio,HR)及95%CI為效應量。首先分析各納入研究的臨床異質性,采用I2檢驗分析其統計學異質性。當P>0.1,I2<50%時可認為多個同類研究間具有同質性,選用效應固定模型進行分析;當P<0.1,且I2≥50%時,選用效應隨機模型合并分析。
2 結果
2.1 納入文獻結果
初檢出文獻179篇,經逐層篩除最終納入10篇文獻,共計5 210例患者。篩選過程見圖1,納入研究基本信息見表1,質量評價表2。
2.2 Meta分析結果
2.2.1 ORR
共納入了9項[4-5,7-11,13-14]研究,共計4 231例患者。結果(圖3)顯示,2組之間I2檢驗P=0.35,I2=10%,異質性小,選用固定效應模型分析。2組患者間的ORR存在顯著差異,有統計學意義(OR=1.79,95%CI為1.56~2.05,P<0.000 01)。
2.2.2 mPFS
共納入了9項[4-5,7-11,13-14]研究,ROBERT等[8]研究因化療方案不同又將試驗組分為卡培他濱組及紫杉類/蒽環類組,分別與對照組的mPFS進行比較,得出不同HR值及95%CI,故將數據分列2組(a組和b組)再進行合并。結果(圖4)顯示,I2檢驗提示異質性較大(P=0.03,I2=50%),應用隨機效應模型分析。2組患者的mPFS間差異有統計學意義(HR=0.70,95%CI為0.63~0.78,P<0.000 01)。敏感性分析發現,剔除MILLER等[5](E2100研究)文獻后,異質性降低(P=0.73,I2=0%),Meta分析結果仍顯示試驗組mPFS優于對照組,差異有統計學意義(HR=0.73,95%CI為0.68~0.79,P<0.000 01)。
2.2.3 mOS
共納入了5項[7-8,10-11,14]研究,異質性分析顯示2組的P=0.94,I2=0%,無異質性,選用固定效應模型分析。Meta分析結果(圖5)顯示,最終2組的mOS間差異無統計學意義(HR=0.94,95%CI為0.84~1.05,P=0.28)。

Fig.1 Literature scanning process.OS:Overall survival;PFS:Progression-free survival;DFS:Diseasefree surviva;RCT:Randomized controlled trial.圖1 文獻篩選流程
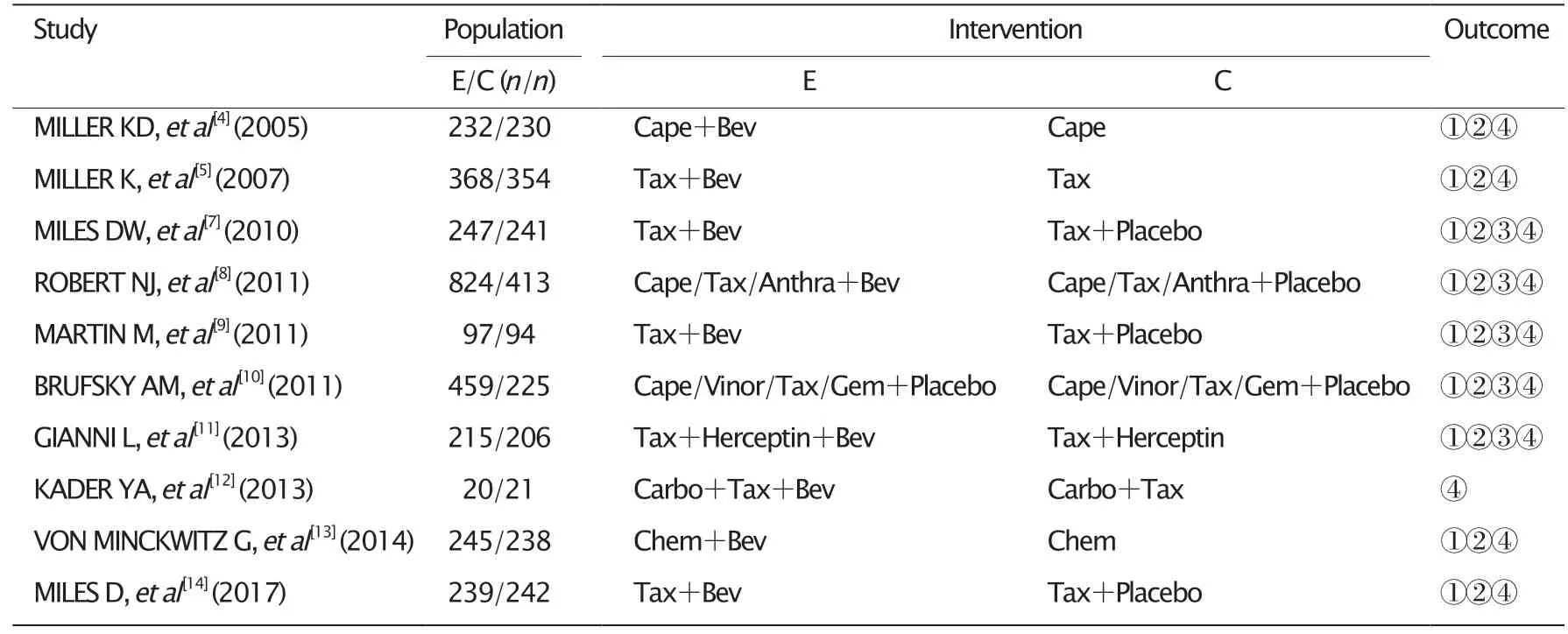
表1 納入研究基本信息表Table 1 Basic characteristics of the articles included in this study

Fig.2 Quality assessment of included studies.圖2 納入研究的質量評價結果

Fig.3 Forest plot of objective response rate (ORR).OR:Odds ratio;CI:Confidence interval.圖3 ORR的森林圖
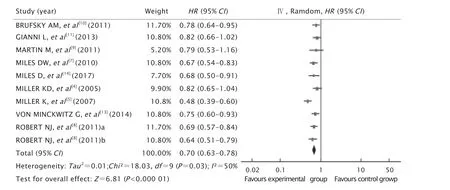
Fig.4 Forest plot of progression-free survival (mPFS).HR:Hazard ratio;CI:Confidence interval.圖4 mPFS的森林分析結果圖
Fig.5 Forest plot of median overall survival (mOS).HR:Hazard ratio;CI:Confidence interval.圖5 mOS期的森林分析結果圖
2.2.4 不良反應
根據常見不良事件評價標準評估≥3級不良反應,Meta分析結果(表2)顯示,試驗組中高血壓(OR=8.39,95%CI為3.56~19.78,P<0.000 01)、蛋白尿(OR=10.87,95%CI為4.68~25.22,P<0.000 01)和神經毒性(OR=1.36,95%CI為1.03~1.79,P=0.03)的發生率高于對照組。而在出血事件及粒細胞減少方面,試驗組并未顯示更高的風險[(OR=1.95,95%CI為0.96~3.95,P=0.07)和(OR=1.25,95%CI為0.95~1.65,P=0.11)]。
2.3 發表偏倚
以mPFS繪制漏斗圖評價發表偏倚,結果(圖6)顯示倒漏斗圖左右基本對稱,提示發表偏倚可能性較小。

表2 不良反應的Meta分析結果Table 2 Meta-analysis of adverse event
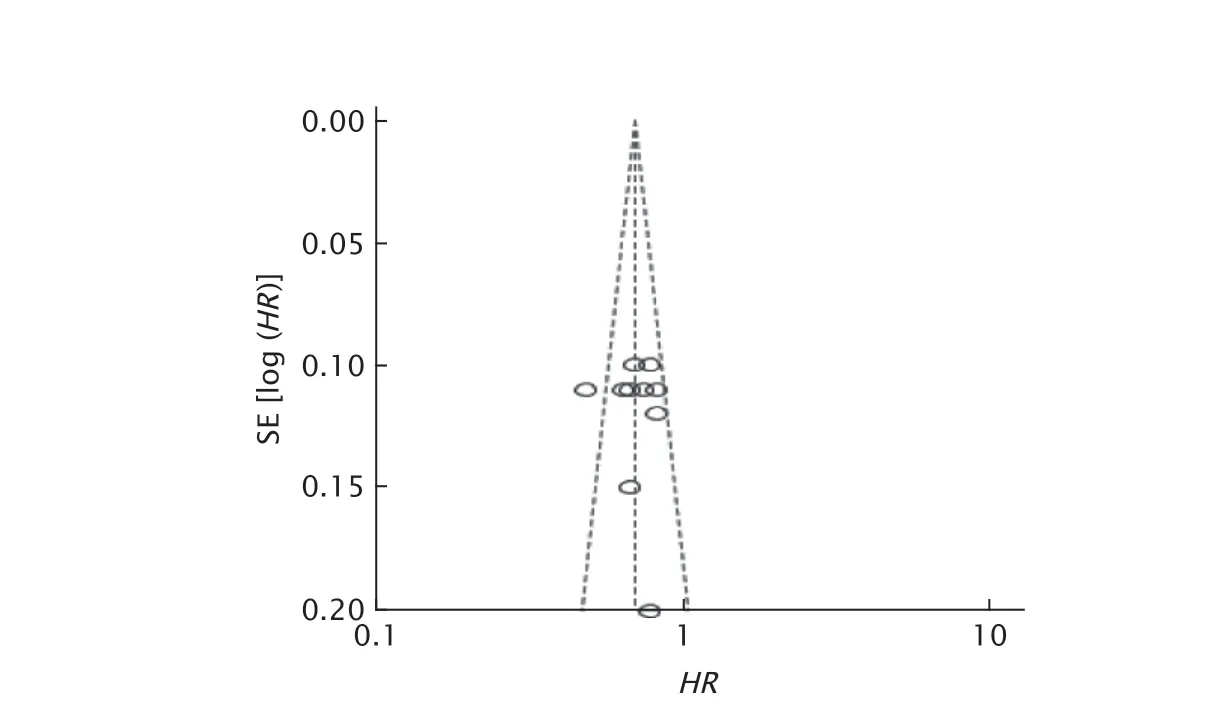
Fig.6 Funnel plot of median progression-free survival (mPFS).SE:standard error;HR:Hazard ratio.圖6 mPFS的漏斗圖
3 討論
抗血管生成治療主要是通過使腫瘤組織異常的脈管系統正常化,改善化學藥物和抗腫瘤藥物從血液循環到腫瘤組織的運輸,以達到增加腫瘤組織內藥物濃度、增強抗腫瘤作用的目的[15]。目前抗血管生成藥物種類繁多,貝伐珠單抗作為第一個問世的抗血管生成靶向藥物[16],其適應癥不斷拓寬。其在晚期轉移性乳腺癌治療中扮演的角色存在爭議,本篇系統評價提取合并10篇隨機對照試驗數據,結果顯示聯合治療組可顯著改善ORR及mPFS,而2組患者的mOS差異無統計學意義。≥3級不良反應中,聯合治療組在高血壓、蛋白尿、粒細胞減少及周圍神經毒性方面發生率更高,出血事件風險未見明顯增加。進一步閱讀相關的非隨機對照試驗發現不同結果,日本的一項單臂臨床試驗[17]結果顯示,貝伐珠單抗聯合紫杉醇治療晚期轉移性乳腺癌療效卓越,mOS達到35.8月、1年總生存率為88.9%,且耐受性好,由此貝伐珠單抗獲得晚期轉移性乳腺癌的適應癥。近期一項在日本開展的包括301例HER-2陰性晚期轉移性乳腺癌患者的回顧性研究[18]結果公布,無肝轉移晚期患者亞組分析,貝伐珠單抗聯合化療對比傳統化療顯著改善患者mOS(48.0個月vs27.3個月),差異有統計學意義(P=0.015)。此外,一項從法國流行病學策略和醫學經濟學(French Epidemiological Strategy and Medical Economics,ESME)數據庫獲取的紫杉醇聯合貝伐珠單抗對比紫杉醇單藥治療共計5 553名HER-2陰性晚期轉移乳腺癌患者的回顧性研究[19]結果顯示,聯合治療組mOS(27.7個月vs19.8個月)(HR=0.672,95%CI為0.601~0.752)及mPFS(8.1個月vs6.4個月)(HR=0.739,95%CI為0.672~0.813)延長。考慮到回顧性研究存在的偏倚,2者可比性降低,研究結論不如嚴格隨機對照試驗嚴謹可靠。回顧貝伐珠單抗在晚期結直腸癌和肺腺癌中的成功應用,三陰性乳腺癌惡性程度高,治療手段較匱乏,聯合抗血管生成治療也是一種新的探索。貝伐珠單抗在晚期轉移性乳腺癌治療中的角色仍有待挖掘。本篇系統評價結果還需更大樣本量及質量更高的臨床試驗加以驗證。
本研究局限性在于:(1)納入的研究雖都為隨機對照試驗,但部分研究未明確提及隨機分配方法;納入文獻時間跨度較大,安全性和耐受性評價標準及實體腫瘤的療效評價標準不同版本內容有所更新,可能影響結果的可靠性及穩定性;(2)納入研究中貝伐珠單抗用量均為推薦劑量15 mg/kg每3周1次或10 mg/kg 2周1次,試驗及對照組中余化療方案盡可能保持相同,但各項研究中患者前期治療不盡相同,可能是影響結果的一個因素。

