不溶性腐植酸的制備及吸附Cr(VI)條件的優化
廖 孜,郭雅妮,胥文敬,惠 璠
(1.西安工程大學 環境與化學工程學院,陜西 西安 710048;2.陜西省現代建筑設計研究院,陜西 西安 710048)
0 引 言
由于工業的迅猛發展,水污染問題在環境治理中早已成為重中之重。水污染導致的生態環境惡化,已嚴重威脅人類的生產和生活。在軍工業、航天、醫藥等領域的發展中,對重金屬的需求愈來愈大,大量的重金屬廢水也隨之產生。因此,大量的Cr(VI)以各種方式排入環境,Cr(VI)在環境中不斷富集,尤其與水環境中的氯離子、HA等物質絡合生成更具毒性的有機化合物,一旦進入人體,將導致人體器官衰竭、誘發癌癥等,故鉻污染已成為世界重金屬污染的主要問題。目前常用的處理Cr(VI)方法主要有離子交換法、氧化還原法、化學沉淀法等[1-2],但這些方法存在技術缺陷和成本過高的缺點,而吸附法具有可回收、高效、污染小、容量大等特點,對Cr(VI)有良好的吸附效果。對于吸附法本身而言,吸附劑性能的好壞直接影響吸附效果,所以制備低成本、高性能的新型吸附劑用于吸附廢水中鉻離子具有重要意義。
HA是天然有機物,經過動植物尸體堆積反應形成[3]。廣泛存在于褐煤、泥炭以及風化煤[4]中,是無定形、棕褐色或棕黑色的有機膠體[5],具有弱酸、親水、熱解、光化學活性及氧化還原等性質,比表面積大,黏度高,吸附能力強[6]。由于其分子結構復雜,含有羧基、羥基、醇羥基及羰基等活性官能團[7],故HA可通過離子交換、疏水連接等作用與金屬離子結合,具有吸附、絡合[8]、螯合的能力[9]。因此,HA廣泛應用于工業[10-11]、農業[12]、環保、醫藥[13]以及化妝品領域[14]。
HA溶于堿而不溶于酸[15]。因此,在堿溶液中能與重金屬離子形成螯合物,但當pH<3.5時,HA易溶解,達不到吸附重金屬離子的效果[16],需要將HA制成IHA。
魏云霞等將HA改性為IHA,以殼聚糖和IHA為原料,采用滴加成球法制備殼聚糖交聯IHA為吸附劑,分析其在水中對Pb(Ⅱ)的吸附作用[17]。陳榮平等通過加熱HA并在CaCl2中浸泡,將HA改性為鈣型IHA,探討改性前后HA表面結構和物理化學性質的變化[18]。本文通過儲量極高且無燃燒價值的風化煤,提取HA[19]用于重金屬廢水的處理,經過高溫鈣化法[20-21]將其制成IHA,分析IHA吸附Cr(VI)的影響因素。
1 實 驗
1.1 材料、試劑和儀器
1.1.1 材料 以陜西黃陵風化煤為原料,研磨過80目篩,70 ℃條件下于恒溫鼓風干燥箱內烘干,采用文獻[22]堿溶酸析法確定最佳條件,提取HA備用。
1.1.2 試劑與儀器 試劑:硝酸鈉(NaNO3,天津市河東區紅巖試劑廠);氯化鈣(CaCl2,天津市科密歐化學試劑有限公司);氫氧化鈉(NaOH,鄭州派尼化學試劑廠);硝酸(HNO3,西安三浦化學試劑有限公司);鹽酸(HCl,西安三浦精細化工廠);氯化鈉(NaCl,天津市北方天醫化學試劑廠),以上均為分析純;重鉻酸鉀(K2Cr2O7,天津市科密歐化學試劑有限公司),優級純。儀器:集熱式恒溫加熱磁力攪拌器(DF-101S,鞏義市予華儀器有限責任公司);水浴恒溫振蕩器(SHA-C,金壇市天竟實驗儀器廠);低速離心機(80-1A,北京時代北利離心機有限公司);恒溫鼓風干燥箱(智能型電熱,上海瑯玕實驗設備有限公司);電子天平(ESJ120-4,沈陽龍騰電子有限公司);優普系列超純水機(UPD-1-201,成都超純科技有限公司);數控超聲波清洗器(KQ5200DE,昆山市超聲儀器有限公司);BET測試儀(Quanta450-FEG,美國FEI公司)。
1.2 實驗方法
1.2.1 IHA制備 稱取一定量HA放入馬弗爐中,加熱使其脫水,用一定濃度的CaCl2溶液浸泡,再用硝酸和蒸餾水反復洗滌,最后用適當濃度的NaNO3溶液浸泡適當時間,然后在80 ℃條件下干燥,得到IHA,密封保存備用。
1.2.2 比表面積分析方法 采用BET測試儀對HA和IHA進行比表面積測定。
1.2.3 Cr(VI)吸附實驗 取不同質量的吸附劑,放入一定體積和濃度的Cr(VI)溶液中吸附一定時間,分析吸附劑投加量對吸附性能的影響。取0.1 g HA、IHA分別置于250 mL錐形瓶中,在不同pH、初始Cr(VI)溶液濃度和浸泡時間、溫度及攪拌速度條件下,測定0.1 g HA、IHA吸附劑在體積20 mL、質量濃度5 mg/L的溶液內對Cr(VI)吸附性能的影響。
吸附量Q和去除率E分別由式(1)和(2)計算:
(1)
(2)
式中:Q為吸附達到平衡的吸附量,mg/L;V為溶液體積,L;C0、Ct為吸附前后Cr(VI)質量濃度,mg/L;m為HA、IHA加入量,g。
2 結果與討論
2.1 IHA制備
采用正交試驗,選取高溫時間、CaCl2濃度、CaCl2浸泡時間和NaNO3濃度等4個影響因素,設計四因素三水平,考察不同因素對IHA產率的影響,并確定最佳制備工藝條件。高溫鈣化法制備IHA實驗設計見表1。
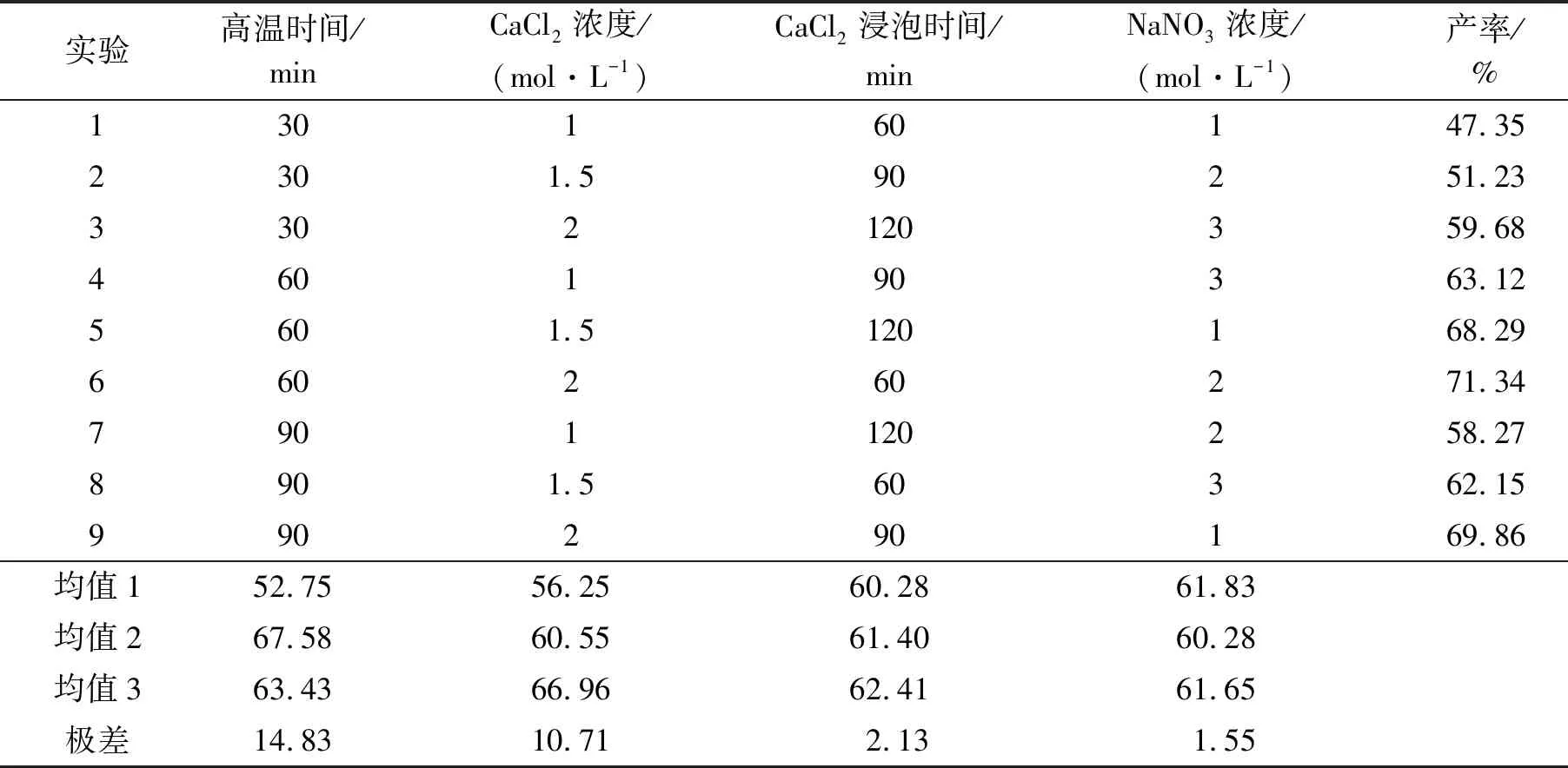
表 1 高溫鈣化法制備IHA實驗設計Tab.1 Experimental design of preparation of IHA by high-temperature calcification
從表1可以看出,4種因素對產率的影響大小依次為高溫時間、CaCl2濃度、CaCl2浸泡時間、NaNO3濃度,在4種影響因素下IHA的產率在41.35%~71.34%范圍內。經過3次平行實驗驗證,得出最佳制備條件為高溫時間60 min,CaCl2濃度為2 mol/L,CaCl2浸泡時間60 min,用于洗滌的NaNO3濃度為2 mol/L,在此條件下,IHA產率最高為74.21%。
2.2 HA和IHA吸附參數比較
由比表面積分析儀測定得到HA與IHA性能比較見表2。從表2可以看出,HA平均孔徑和累計吸附孔容偏小,比表面積較小,而改性后的IHA孔徑增大,累計吸附孔容提高,比表面積增加了近1倍,表明改性為IHA后吸附性能明顯改善。

表 2 HA和IHA性能比較Tab.2 Characteristic comparison between HA and IAH
2.3 吸附Cr(VI)操作條件優化
2.3.1 pH值 用0.1 mol/L HCl和0.1 mol/L NaOH調節pH,測定pH對HA和IHA吸附Cr(VI)的影響,結果如圖1所示。
從圖1可以看出,HA和IHA 2種吸附劑對Cr(VI)吸附量隨pH升高而減小。在pH相同條件下,對Cr(VI)吸附效果IHA好于HA。在酸性條件下(pH<5)時,2種吸附劑隨pH的升高,吸附量也呈升高的趨勢,但不明顯;在5≤pH<8時,HA、IHA 2種吸附劑的下降趨勢均較為緩慢;而在pH=5時,HA 、IHA Cr(VI)吸附量均為最高,分別為0.477 mg/g和0.693 mg/g;在堿性條件下(pH>8)時,隨著pH的升高,2種吸附劑對Cr(VI)的吸附量急劇下降,HA較快,IHA次之。可以看出IHA耐酸能力優于HA。
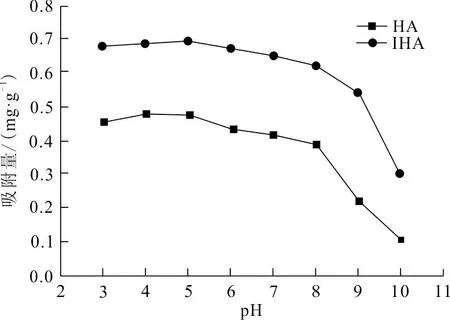
圖 1 pH對吸附Cr(VI)的影響Fig.1 Effect of pH on adsorption of Cr (VI)
2.3.2 溫度 在pH=5條件下,分別取0.1 g HA、IHA 2種吸附劑測定不同溫度對Cr(VI)的影響,結果如圖2所示。
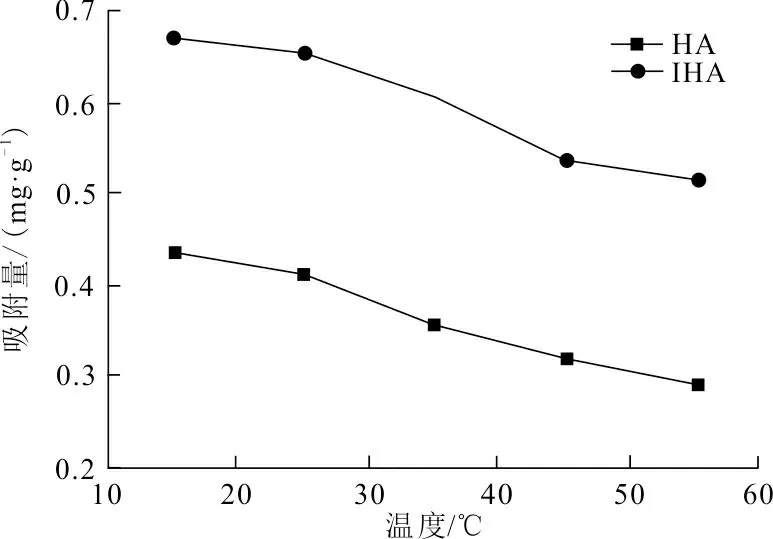
圖 2 溫度對吸附Cr(VI)的影響 Fig.2 Effect of temperature on adsorption of Cr (VI)
從圖2可以看出,隨著溫度的升高(15~55 ℃),吸附劑的吸附量隨之下降,HA吸附量由0.438 mg/g下降到0.289 mg/g,IHA吸附量由原來的0.675 mg/g下降到0.515 mg/g。但總體來說,同一溫度下2種吸附劑的吸附效果始終為IHA好于HA,即IHA的吸附性能始終優于HA。因為IHA經過高溫鈣化后,比HA更耐高溫,性質也較為穩定。溫度在15~30 ℃時,IHA吸附量均高于0.6 mg/g,表明IHA在常溫下適用性很好,有利于實際應用。
2.3.3 初始濃度和時間 分別取0.1 g HA、IHA,溫度為25 ℃、pH=5條件下分別放入20 mL初始質量濃度分別為1、2、3、4、5 mg/L的Cr(VI)溶液中,分別測定0、0.2、1.0、1.5、2.0、2.5、3 h吸附時間下HA、IHA對Cr(VI)的吸附量及去除率,結果如圖3所示。
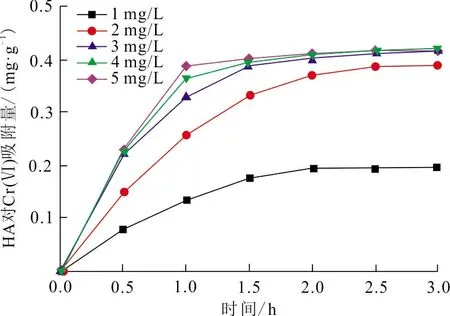
(a) HA吸附量

(b) HA去除率
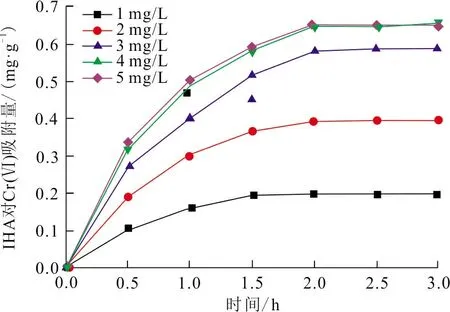
(c) IHA吸附量

(d) IHA去除率圖 3 初始濃度和吸附時間對IHA 吸附Cr(VI)的影響Fig.3 Effects of initial concentration and adsorption time on the adsorption of Cr (VI) by IHA
從圖3可以看出,HA、IHA 2種吸附劑隨著時間的變化,對Cr(VI)的吸附趨勢相似,均可以分為3個階段。第一階段為Cr(VI)快速吸附期。吸附量隨著時間的增加快速增加,因為吸附位點充足,主體溶液與溶液濃度梯度較大,加快Cr(VI)從溶液擴散到吸附劑表面的速度;第二階段為Cr(VI)緩慢吸附期。由于吸附劑表面有效吸附位點減少,溶液的濃度梯度降低,故Cr(VI)的吸附速度變緩,但仍處于上升階段;第三階段為吸附平衡期。吸附劑上的吸附位點幾乎處于飽和狀態,達到吸附平衡,因此,Cr(VI)的吸附量基本保持不變。從整體比較可以看出,HA吸附曲線比IHA的吸附曲線更快地達到吸附平衡,說明經過改性的IHA吸附位點多于HA的吸附位點,2種吸附劑對Cr(VI)的吸附效果為IHA比HA的吸附能力更強。
同樣,以去除率E為指標可以看出,在低濃度Cr(VI)溶液(1~2 mg/L)中,2種吸附劑對Cr(VI)的去除率相當,而在高濃度Cr(VI)溶液(3~5 mg/L)中,IHA比HA能夠保持良好的去除率。可見,IHA的吸附能力明顯優于HA,較高的Cr(VI)濃度下優勢更明顯。
2.3.4 吸附劑投加量 分別投加0.05、0.1、0.2、0.3、0.4、0.5 g HA和IHA,在溫度為25 ℃、pH=5、吸附時間2 h時,測定吸附劑對Cr(VI)的吸附,結果如圖4所示。
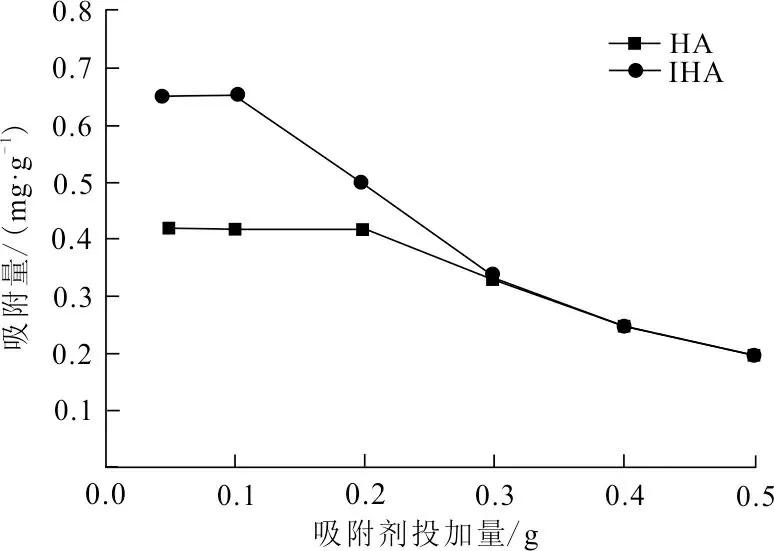
(a) HA、IHA吸附量
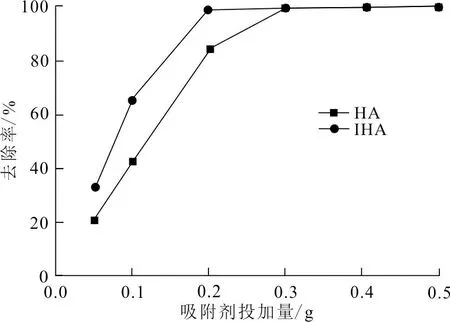
(b) HA、IHA去除率圖 4 投加量對吸附Cr(VI)的影響Fig.4 Effect of adsorbent dosage on adsorption of Cr(VI)
從圖4可以看出,在投加的吸附量小于0.2 g時,HA和IHA都能保有比較良好的吸附量,因為相對于吸附劑投加量而言,溶液中的Cr(VI)含量充足,投加的吸附劑的吸附位點能達到飽和狀態,但HA與IHA相比,遠不如IHA對Cr(VI)的吸附量,且吸附劑投加量為0.2 g時,IHA對Cr(VI)去除率能達到100%。改性后IHA的吸附孔容、平均孔直徑以及比表面積均高于HA。在溶液中,高容量、高比表面積有益于IHA與溶液接觸,使吸附劑的吸附位點增多且利用率提高。因此當投加的吸附劑量增多即吸附位點的增多時,吸附劑對Cr(VI)的螯合能力、離子交換能力及靜電吸附作用均有所增加,但溶液中Cr(VI)含量有限,無法滿足所有的吸附位點,吸附達不到飽和,對Cr(VI)的吸附量不增反減;當投加量較少時,吸附位點無法滿足Cr(VI)含量,因此去除率較低;當吸附劑投加量逐漸增加,吸附劑的吸附位點增多,能吸附更多Cr(VI),吸附位點量甚至能夠完全滿足溶液中Cr(VI)時,Cr(VI)幾乎能被完全去除,去除率趨近100%。因此,實際應用中根據水中Cr(VI)含量掌握好投加比例,不僅可以保證吸附效果,而且不會造成IHA的浪費。
2.3.5 攪拌速度 在pH=5、溫度25 ℃條件下,分別取0.1 g HA、IHA 2種吸附劑測定不同攪拌速度對HA、IHA吸附Cr(VI)的影響,結果如圖5所示。
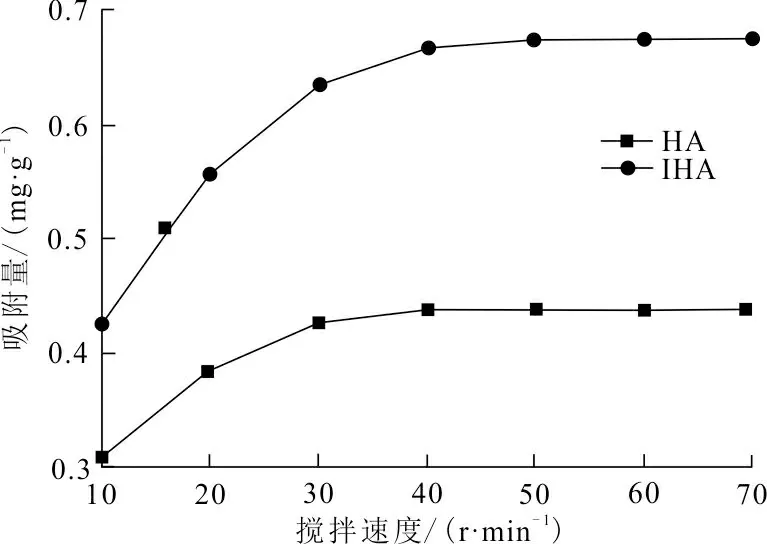
圖 5 攪拌速度對吸附Cr(VI)的影響Fig.5 Effect of stirring speed on adsorption of Cr (VI)
從圖5可以看出,HA、IHA對Cr(VI)的吸附量隨著攪拌速度的增加,變化趨勢相似。同一攪拌速度下IHA的吸附量明顯高于HA,因為HA本身較IHA可溶性強。在攪拌時,使吸附劑與溶液充分接觸的同時,也加速了HA在溶液中的溶解,因此在吸附過程中HA的吸附量更低。對于同一種吸附劑而言,在攪拌速度低于40 r/min時,吸附量隨著攪拌速度的提高逐漸增大,當攪拌速度達到40 r/min以后,吸附量基本不變。因為在攪拌過程中,速度越快,吸附劑與溶液的接觸越徹底,使得吸附位點的利用率得以提高,則吸附量也提高;也說明攪拌速度達到40 r/min時可以使吸附劑與溶液完全混合,此時再提高攪拌速度對吸附效率無影響。
3 結 論
1) IHA制備的最佳條件為高溫時間60 min,CaCl2濃度2 mol/L,CaCl2浸泡時間60 min,洗滌所用的NaNO3溶液濃度2 mol/L。
2) BET分析結果表明,經高溫鈣化后IHA孔容增大,比表面積增加,吸附性能明顯改善,有利于實際應用。
3) IHA吸附Cr(VI)的效果明顯優于HA,適用性更強;吸附Cr(VI)的最佳操作條件為室溫、pH=5、吸附時間2 h、攪拌速度40 r/min,適當比例投加條件下去除率為99%以上。

