中醫藥治療肝豆狀核變性痰瘀互結證用藥規律研究*
宋成瑋,韓輝,忻凌,詹敏,麻雨弟
1 安徽中醫藥大學 安徽合肥 230012
2 安徽中醫藥大學第一附屬醫院腦病二科 安徽合肥 230031
肝豆狀核變性 (hepatolenticular degeneration,HLD),即Wilson 病(Wilson’s disease,WD),是由于致病基因ATP7B 突變引起的常染色體隱性單基因遺傳病,是隱性遺傳病中是最常見的疾病之一[1]。Wilson 病為慢性遺傳病,治療主要以藥物排銅、飲食控制等,患者需長期服藥,一旦停藥錐體外系癥狀易反復發作并加重,影響患者預后。中醫藥在治療肝豆狀核變性患者的作用逐漸被重視,其不良反應較少,療效較好,有利于減輕癥狀并且改善預后。韓輝[2]等發現,痰瘀互結證是Wilson 病最常見的證候之一。本研究采用數據挖掘技術,探索安徽中醫藥大學第一附屬醫院腦病科治療Wilson 病痰瘀互結證的用藥規律,為制定和優化中西醫結合個體化治療方案奠定基礎。
資料與方法
1 診斷標準
西醫診斷標準符合《肝豆狀核變性診療方案》[3]。中醫診斷標準根據其癥狀可辨病為“肝風”“痙證”“顫證”“黃疸”“鼓脹”“積聚”和 “癇病”等[4]。
2 入組標準
2.1 納入標準 ①符合西醫Wilson 病診斷標準;②中醫辨證為痰瘀互結證;③完整方藥信息;④中藥湯劑或復方顆粒內服治療;⑤UWDRS 量表評分提示療效較前改善(P<0.01)。
2.2 排除標準 ①中醫辨證非痰瘀互結證;②未服用中藥;③未采用內服法應用中藥;④UWDRS 量表評分未提示療效較前改善的患者。
3 一般資料
應用HIS 系統收集安徽中醫藥大學第一附屬醫院腦病科2013 年2 月—2018 年12 月肝豆狀核變性痰瘀互結證住院患者病歷資料。符合本研究要求的患者共4835 例,年齡12 ~57 歲,平均年齡(25.1±10.4)歲;其中男性3223 例,女性1612 例,男女比例約為1.5 ∶1。
4 數據分析方法
將HIS 系統中符合納入標準的數據導入Excel 2010 建立數據庫,應用SPSS Statistics 22.0 對數據庫進行分析,分析藥物使用頻次,高頻藥物性味歸經。采用SPSS Clementine 11.1 軟件進行 Aprior 模塊分析,探討中藥之間的相互關系。設置支持度≥30%, 置信度≥80%。
結 果
1 中藥的藥性統計
本研究涉及380 味中藥,寒(87.46%)、溫(72.96%)、平(51.43%)性藥物是使用頻率前三的藥物,見表1。
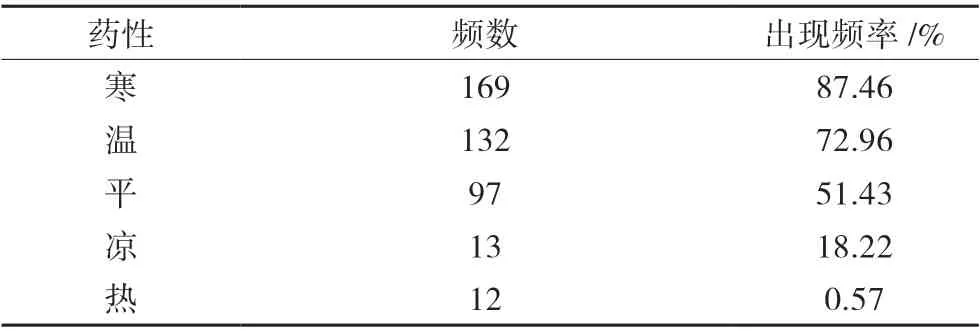
表1 中藥藥性情況
2 中藥的藥味統計
研究得出,味苦(97.30%)、甘(91.01%)、辛(78.43%)的中藥是使用頻率前三的藥物,見表2。
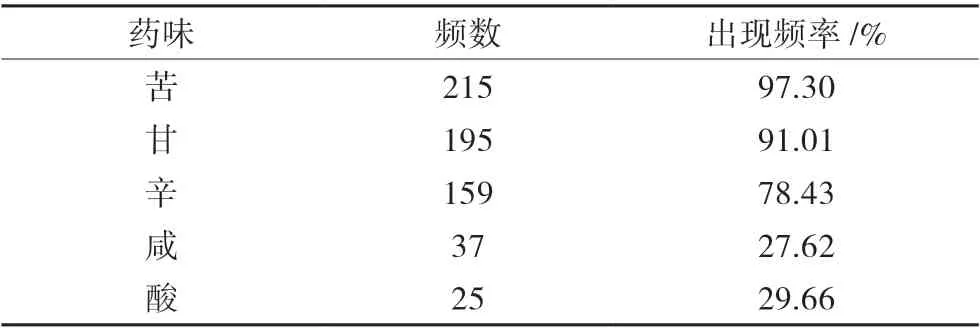
表2 中藥藥味情況
3 中藥的歸經統計
研究涉及380 味中藥中大多歸于肝(53.19%)、胃(35.70%)、脾(32.62%)經。
4 藥物使用情況分析
研究發現,高頻中藥的使用頻率及功效、性味歸經,見表3。
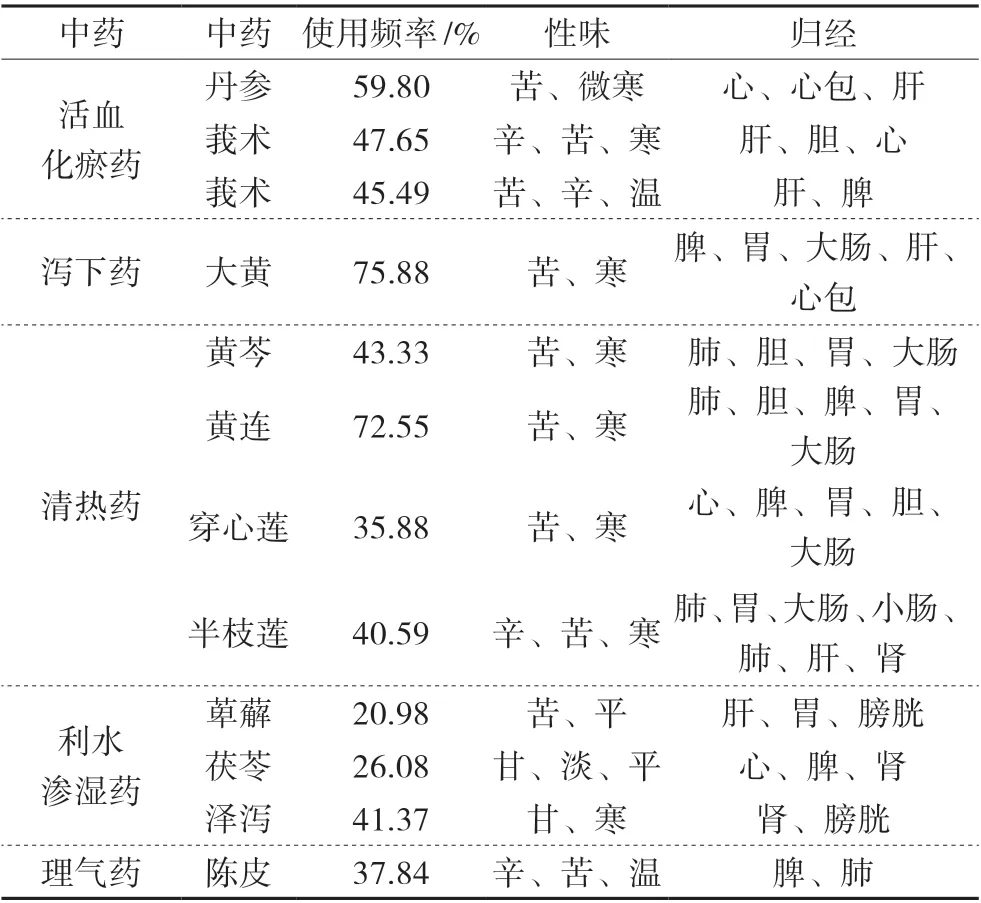
表3 常用中藥分類及性味歸經
5 核心處方分析
本研究通過復雜核心網絡分析圖,可看出本院腦病科治療肝豆狀核變性痰瘀互結證的核心處方是:茯苓、黃芩、澤瀉、丹參、黃連、陳皮、莪術、大黃、萆薢、郁金、穿心蓮、半枝蓮,見圖1。
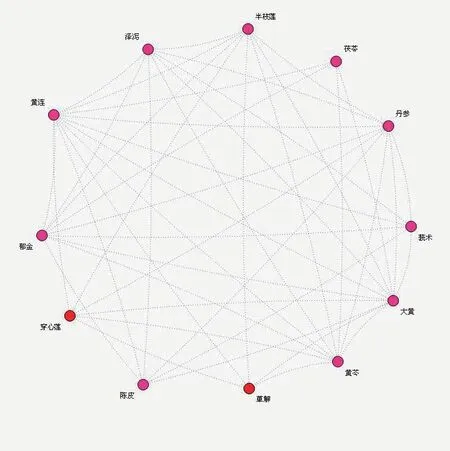
圖1 核心用藥分析
6 關聯規則分析
運用SPSS Clementine 11.1 軟件進行 Aprior 模塊分析,設置支持度≥30%, 置信度≥80%。支持度越高,表明規則出現的頻率越高,可得出治療Wilson 病痰瘀互結證常見的藥對,共得到11 條規則,見表4;以及常見的藥組,共得到29 條規則,見表5。
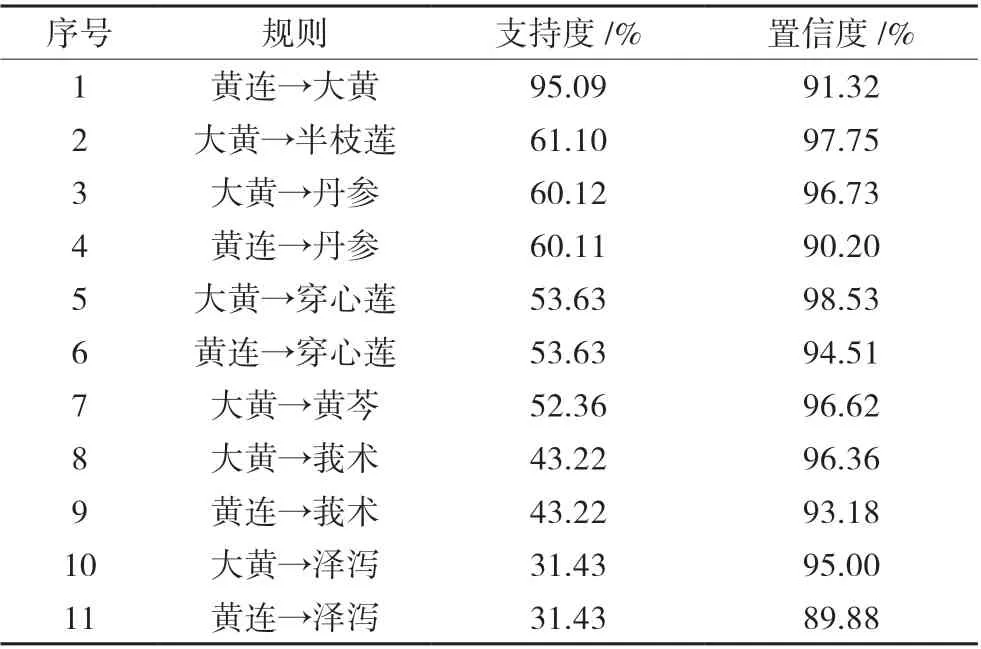
表4 常用藥對關聯規則分析(支持度≥30%)
7 主成分因子分析
將高頻藥物數據放入SPSS Statistics 25 進行降維運算,進行Bartett 球形檢驗,得出F=731.536,P = 0<0.05,KMO 為0.69>0.6,表明可以進行主成分因子分析運算。總方差解釋得出累計貢獻率為67.583%,可提取5 個公因子,見表6。
討 論
Wilson 病患者體內銅轉運障礙,體內過多的銅可從糞、尿中排出,導致糞銅、尿銅增高[4-5]。中醫學可將其歸于肝風,黃疸,痙證,顫證,鼓脹,積聚,癇病等范疇。中醫認為其本質是稟賦不足、銅毒內生[6],體內元氣充足則銅毒邪氣被正氣壓制不易發病,若體內元氣損傷和銅毒積聚到一定程度時,則發為本病。而痰瘀互結證多見于Wilson 病的后期,是疾病發展后期的一種主要表現。由于痰來自水液化生,濕易阻滯氣機,氣滯不易化水,水聚而成痰。血行不暢,則血滯,聚而為瘀;熱邪積聚則煉液為痰,煎熬血成瘀,發為痰瘀互結。表現以屈伸不利,言語謇澀,肌膚甲錯,舌質暗淡或有瘀斑,苔薄膩,脈弦滑為主[7]。一項關于證型與UWDRS 量表相關性研究顯示[8],痰瘀互結證的UWDRS 量表的神經功能評分要高于其他證型,其主要原因可能與疾病發展到中后期,病程越長,痰瘀癥狀越明顯。故本文著力于探討WD 痰瘀互結證的相關問題。汪美霞等[9]認為痰瘀既是人體新陳代謝的產物,又是致病因素。方淑珍等[10]認為銅在生理上屬于津液和血液,痰瘀是由于津液和血液在體內聚集日久而成,銅毒也隨即在體內聚集,并隨津血的運動停于不同的臟腑,引起相應的臨床癥狀。血液的運行與五臟密切相關,故瘀血在不同臟腑則引起不同癥狀[11]。
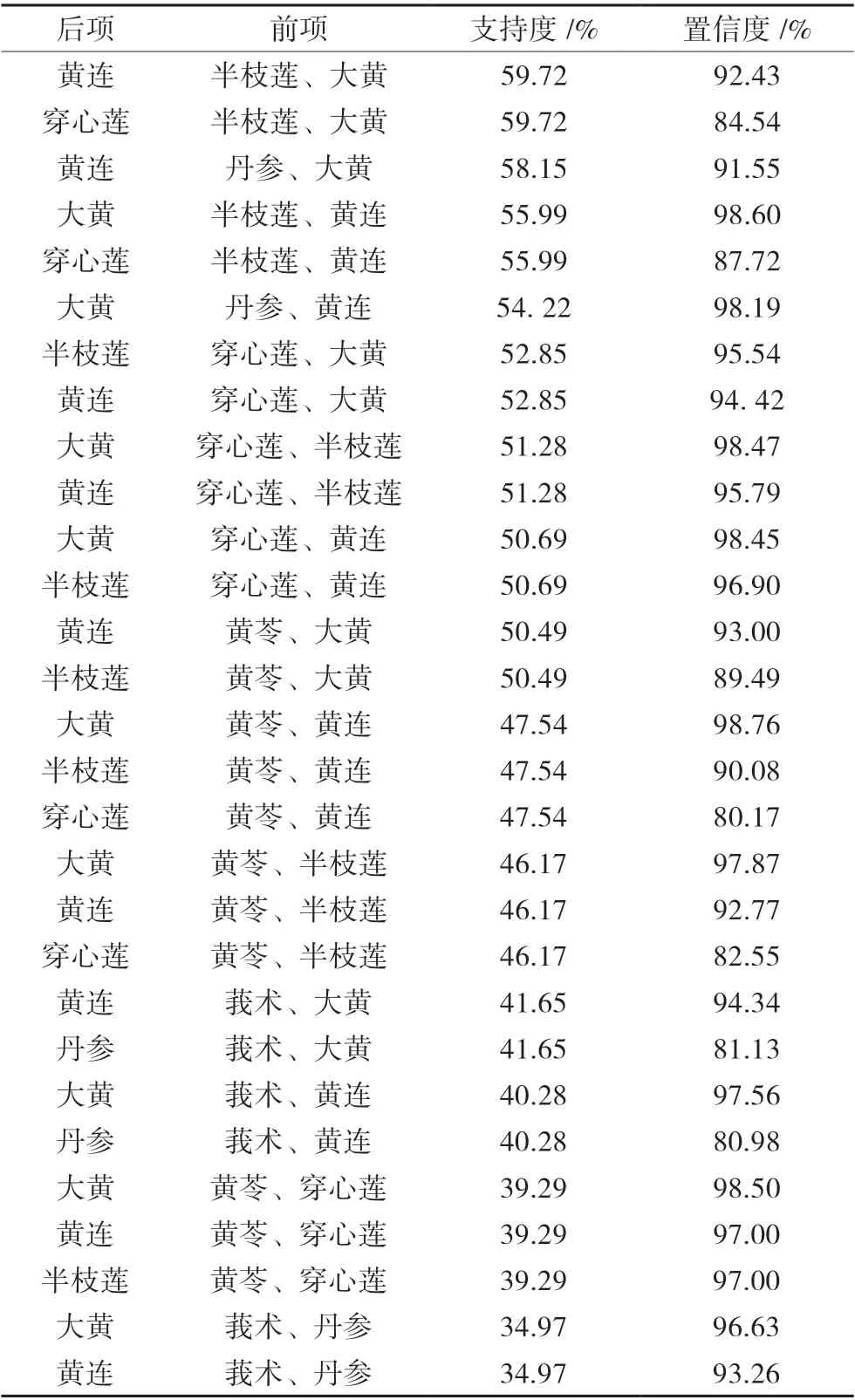
表5 三項關聯規則分布

表6 高頻藥物主成分因子分析
西醫主要應用保肝排銅的藥物治療,這些藥物需長期服用,藥物副作用大,部分患者因各種原因無法按時服用藥物而不能達到預期療效。故我們通過祖國醫藥方面入手[12],探尋適合Wilson 病患者的最佳治療方案,中藥毒副作用小,運用中醫藥綜合治療除可幫助排銅外,還有一定的保肝護腦等綜合作用,具有扶正祛邪之功,顯示出中藥治療Wilson 病的整體優勢,具有良好的研究價值和應用前景。
從中藥的歸經分析,肝、胃、脾經最為常見。從中醫診斷分析,Wilson 病可屬于肝風、顫病、鼓脹、積聚的范疇。肝風即肝風內動,由體內陽氣亢逆變動引起。顫病以肢體動搖不定,相當于以錐體外系癥狀為主要表現的患者。鼓脹表現為腹大脹滿、繃急如鼓,皮色蒼黃,可見于Wilson 病肝硬化失代償期的患者,以肝硬化腹水、肝性腦病等為主要表現,病情危重。肝氣不疏、脾運失職、肝脾不調致有形實邪停于腹中而形成“積聚”。常可于腹部觸及包塊。韓輝[13]等發現化痰祛瘀法中藥有益于Wilson 病神經功能的改善。因患者體內的銅主要通過二便排出,尤大便為主,治療使應以瀉下通便為主要目的,協助排銅。選方以大黃瀉下攻積,丹參、姜黃、郁金、莪術佐以活血化瘀,澤瀉、金錢草、茯苓、萆薢、半枝蓮、黃芩、黃連、穿心蓮清熱燥濕作為核心處方,適當增加補氣健脾藥物,可在祛除痰、瘀、濕等邪氣的同時扶助正氣、滋養先天,其余根據辨證論治可適當增加開竅藥、平肝熄風藥等治療有痰濁蒙竅、肢體顫動等表現的患者。研究表明,通過使用中藥可增加銅離子從二便排出,促進膽道排銅,可抗肝纖維化,延緩肝硬化進程[14],從而減少并發癥。如丹參具有抗肝纖維化活性,減少炎性因子生成,同時可以增強自由基清除酶的活性,間接發揮抗纖維化作用[15]。如郁金對急性肝損傷有一定的防治作用[16]。大黃中的大黃素具有抗氧化應激的作用,清除氧自由基,增強肝臟活性,保護肝臟細胞[17]。金錢草對于急性黃疸型肝炎具有良好效果,故對合并黃疸的WD 患者可使用[18]。萆薢具有抗骨質疏松的作用,對于WD 患者長期排銅引起鈣降低的患者具有較好的效果,可輔助鈣片起到防止鈣質流失的作用[19]。
我院腦病科常用治療肝豆狀核變性痰瘀互結證核心處方藥物可分為:活血化瘀藥、瀉下藥、清熱藥、利水滲濕藥、理氣藥。通過核心處方分析,我們發現這些藥物主要起到活血化瘀、清熱利濕、瀉下通便、行氣導滯的作用,部分行氣藥中頁有扶助正氣、補氣的作用,這也與我們的治療原則相符合。本研究對中醫藥治療Wilson 病痰瘀互結證的核心處方進行關聯規則分析,在研究中發現,藥對的使用對方劑的加減具有良好的作用。如研究中大黃與黃連,大黃與半枝蓮,大黃與丹參關聯度較高,體現出瀉下藥與清熱藥及活血化瘀藥之間的相互應用,而這些置信度≥80%的藥對中的藥物均為核心處方中的關鍵藥物,證明其應用的廣泛性,形成Wilson 病痰瘀互結證中藥治療的基本框架。藥組配對以黃連、半枝蓮和大黃的配對最多見,由藥組藥對的配伍可得出,大黃、黃連兩味藥是核心處方中的用藥核心,藥物的配伍均以二味藥為主,起到主要作用。張山等[20]認為大黃本身有活血化瘀、清熱瀉下的功效,再與清熱、活血之劑配伍可相須為用,加強藥效。曹富等[21]認為大黃黃連相配伍,還具有抗菌、增強機體免疫功能的作用,既可驅邪又扶正。
主成分因子分析中可以看出:F2 黃連和大黃可單獨成組,這與核心處方分析結果相類似,體現二味藥的關鍵作用。F1 中半枝蓮、穿心蓮、黃芩、丹參、莪術5 味藥配伍,共同起到活血化瘀,清熱利濕,行氣導滯之用。F3 澤瀉與萆薢相配伍,利水滲濕,泄熱,利濕去濁。F4 茯苓與陳皮利水滲濕,理氣行滯。F5 郁金理氣解郁,起到輔助作用。
綜上所述,本院腦病科在治療肝豆狀核變性痰瘀互結證時,多選用活血化瘀、清熱利濕、瀉下通便、扶助正氣的藥物。通過運用數據挖掘方法,探討肝豆狀核變性痰瘀互結證患者用藥規律,為進一步優化治療方案及改善患者的生活質量奠定基礎。

