介入治療中藥物涂層球囊長度與冠心病患者臨床結局的關系
楊廣興,楊利果,弓向榮
(鄭州大學第一附屬醫院 a.心血管內科;b.內分泌科,河南 鄭州 450052)
近年來,隨著介入技術的迅速發展,藥物洗脫支架(drug eluting stent,DES)成為冠心病患者經皮冠脈介入治療的標準方案之一[1]。然而,DES并不能降低冠心病患者的病死率,支架內血栓形成、心肌梗死(myocardial infarction,MI)和反復血運重建仍然是冠脈支架植入術后難以避免的常見并發癥[2]。有研究表明支架內血栓形成與死亡風險之間呈正相關[3]。支架長度是發生嚴重主要不良心血管事件(major adverse cardiac events,MACE)的一個獨立危險因素,并與支架內血栓形成、心肌梗死、靶病變血運重建(target lesion revascularization,TLR)及死亡有關[4-5]。除急性不良事件外,在支架植入后,由內膜增生引起的再狹窄也是一個主要問題[6]。10%接受DES治療的患者和20%~30%接受裸金屬支架治療的患者在5 a后會出現支架內再狹窄(in-stent restenosis,ISR),需要再次血運重建[7-8],目前,藥物涂層球囊(drug-coated balloon,DCB)已成為介入治療的一項新手段,DCB通過將表面攜帶的抗增生藥物釋放到血管內壁,不僅可以抑制內膜增生,還可有效地抑制平滑肌細胞的遷移。有研究表明,DCB治療ISR的效果優于DES及普通球囊成形術[7-8],但是迄今為止關于DCB的長度與臨床結局的關系尚無定論。基于此,本研究探討DCB的長度和臨床結局的關系。
1 資料與方法
1.1 研究對象及分組回顧性分析2017年6月至2018年6月在鄭州大學第一附屬醫院分別使用15 mm DCB(Sequent?PREE,B.Braun Melsungen)和30 mm DCB治療的249例冠心病患者的臨床資料。依據置入的DCB長度分為15 mm組(155例)和30 mm組(94例)。依據249例患者DCB擴張后是否發生夾層分為夾層組和無夾層組。排除標準:(1)近期有活動性出血;(2)對對比劑或紫杉醇過敏;(3)存在急性心衰或嚴重瓣膜疾病;(4)存在嚴重感染。本研究經鄭州大學第一附屬醫院醫學倫理委員會批準,所有患者均在術前簽署介入手術知情同意書。
1.2 資料搜集通過查閱電子病歷收集患者的臨床資料,包括年齡、性別、相關病史、冠心病危險因素、左室射血分數及胸痛情況。穩定型心絞痛、ST 段抬高型和非ST段抬高型急性冠脈綜合征的診斷依據《中國經皮冠狀動脈介入治療指南(2016)》[9]。
1.3 DCB操作流程和病變定義DCB手術遵循《藥物涂層球囊臨床應用中國專家共識》[10]。患者術前均接受標準的雙聯抗血小板治療(阿司匹林每天100 mg,氯吡格雷每天75 mg,或阿司匹林每天100 mg,替格瑞洛每天180 mg)。導絲通過病變后,使用順應性球囊預擴張靶血管病變處,若預擴張不滿意,則根據病變情況使用非順應性球囊、切割球囊或棘突球囊等充分預擴張靶病變。選擇的DCB直徑與靶血管直徑的比值為0.8~1.0∶1.0,且DCB的長度比處理后的病變兩端各長2~3 mm,避免地理缺失。DCB在8~14 atm(1 atm=1.01×105Pa)下擴張并維持50~80 s。球囊撤壓后,冠狀動脈造影確定無C型及以上夾層且心肌梗死溶栓治療(thrombolysis in myocardial infarction,TIMI)血流分級3級、殘余狹窄≤30%,即手術成功。若不滿足上述標準則進行補救性支架植入。冠狀動脈夾層分型依據美國心肺血液研究中心分型標準[11]。靶病變在造影時鈣化嚴重程度依據Tsuchihashi等[12]提出的半定量評分,評分3分為重度鈣化病變。分叉病變為主支、分支血管分別或同時存在的嚴重狹窄病變。所有患者圍手術期除接受標準的雙聯抗血小板治療外,無禁忌證者均服用他汀類藥物、血管緊張素轉換酶抑制劑/血管緊張素Ⅱ受體拮抗劑和β受體阻滯劑。
1.4 介入治療預后評價觀察指標為出院后2 a內的MACE,即由心源性死亡、心肌梗死及TLR構成的復合指標。患者出院后通過電話詢問及門診復診的方式隨訪MACE發生情況。
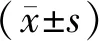
2 結果
2.1 臨床基線資料本研究共入選249例患者,年齡38~72歲,平均(54.16±11.09)歲,男182例,女67例。兩組靶病變部位分布情況差異無統計學意義(P>0.05)。兩組在年齡、性別、體質量指數(body mass index,BMI)、冠心病危險因素、相關病史和左心室功能等方面,差異無統計學意義(P>0.05)。見表1。

表1 兩組患者臨床基線資料比較
2.2 手術相關資料240例(96.39%)患者在預處理后單獨置入DCB,另外9例(3.61%)患者因DCB術后出現C型及以上夾層而補救性植入支架,15 mm組分叉病變率(14.19%)高于30 mm組(2.13%),差異有統計學意義(P<0.05)。兩組DCB擴張后夾層發生情況見表2,15 mm組DCB擴張后夾層發生率(7.74%)低于30 mm組(17.02%),差異有統計學意義(P<0.05),見表3。兩組在DCB直徑、擴張壓力及擴張時間方面,差異無統計學意義(P>0.05),見表4。

表2 兩組DCB擴張后夾層發生情況[n(%)]

表3 兩組患者發生分叉、鈣化病變、DCB擴張后夾層、 補救性植入支架比較[n(%)]
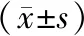
表4 兩組患者DCB直徑、擴張壓力、擴張時間比較
2.3 隨訪及預后所有患者均完成隨訪,無失訪病例。兩組患者隨訪期間MACE發生率比較,差異無統計學意義(P>0.05),其中30 mm組出現1例心源性死亡,見表3。15 mm組與30 mm組生存曲線比較,差異無統計學意義(P>0.05),夾層組與無夾層組生存曲線差異無統計學意義(P>0.05),見圖1~2。

表5 兩組患者2 a隨訪期間MACE發生率比較[n(%)]

圖1 249例患者依據DCB長度分組的Kaplan-Meier曲線

圖2 249例患者依據術中是否發生夾層分組的 Kaplan-Meier曲線
3 討論
近年來,隨著介入技術及藥物涂層技術的發展,DCB在冠心病的介入治療中取得重要地位。從德國學者Scheller等[13]首次證明DCB在預防ISR方面的安全性和有效性,到獲得歐洲心臟病學會證據等級ⅠA和《藥物涂層球囊臨床應用中國專家共識》的推薦,DCB已成為支架內再狹窄的標準治療方案之一[14]。有研究結果顯示DCB在小血管及分叉病變治療上具有優勢[15]。DCB通過貼壁釋放抗增殖藥物至血管內膜,不僅有效減少靶血管的炎癥反應,同時可加快動脈內皮愈合進程,但對于DCB長度是否與MACE發生率有關尚無明確定論。本研究發現,30 mm組患者較15 mm組DCB術后出現夾層率更高,兩組患者在隨訪期間MACE發生率相似,差異無統計學意義。目前,普遍認為冠狀動脈支架長度是ISR的獨立危險因素之一[4-5]。支架長度增加與血管損傷、血小板活化和支架內血栓形成風險相關[16]。在臨床實際工作中接受30 mm DCB治療的患者存在更廣的病變范圍,故接受較長DCB治療的患者預后更差。在臨床工作中也觀察到接受更長的DCB治療的患者MACE發生率可能更高。有研究顯示,接受較長DCB治療的患者MACE發生率更高[17]。本研究顯示,30 mm組在DCB術后較15 mm組存在更高的冠脈夾層發生率,表明30 mm組DCB術后存在更多的血管損傷及炎癥反應。
本研究結果顯示接受不同長度DCB治療的患者住院期間及2 a隨訪期間MACE發生率差異無統計學意義,與先前研究結果不一致[17]。在球囊成形術時代,“治療性夾層”這一觀念被廣泛認可,認為夾層對減少再狹窄至關重要。夾層是一把雙刃劍,嚴重的冠脈夾層會導致諸如急性心肌梗死或緊急冠狀動脈搭橋術等不良事件[18-19]。有研究顯示,DCB術后夾層組與非夾層組MACE事件發生率及隨訪期間的最小管腔面積比較,差異無統計學意義。夾層并不會影響DCB對靶病變的治療,即使存在嚴重的夾層也是如此[20]。同樣,既往研究顯示,盡管近1/3的患者術中出現冠脈夾層,但大多數(94%)患者在隨訪中完全愈合[21]。重要的是,這些夾層并未增加不良心血管事件的發生率。Funatsu等[22]研究顯示,盡管80%的病變合并冠脈夾層,但急性期和中期的臨床療效仍較好。DCB的療效取決于進入血管壁的抗增生藥物的作用面積和量。有研究顯示,輕微的夾層有助于內膜對DCB所攜帶藥物的攝取,促進藥物在冠脈內膜及中膜的滲透,增強DCB的療效[23]。本研究中夾層組與無夾層組患者生存曲線差異無統計學意義。基于本研究得出假設:更長的DCB可能釋放更多的藥物以抵消更廣泛的冠脈病變及血管損傷。本研究術中嚴格遵循《藥物涂層球囊臨床應用中國專家共識》的操作流程,僅有9例患者因DCB后出現C型以上夾層而補救性植入支架,這與先前研究結果[24]相似。本研究中術后有3例(1.20%)發生早期缺血驅動的靶血管血運重建事件,較Byrne等[25]報道的早期血運重建發生率低,這可能是由于近年來術中更多的切割球囊及腔內影像的應用進一步減少了急性缺血事件的發生。
本研究存在一定的局限性。首先,本研究是單中心回顧性研究,患者數量較少。其次,本研究入選患者并未常規接受冠脈造影定量分析,只進行了臨床事件的隨訪,因此無法對患者置入前、置入即刻及隨訪時的病變進行定量分析,缺乏DCB置入后遠期管腔數據。此外,患者在術中并未常規接受血管內超聲或光學相干斷層掃描等對造影結果及治療后靶血管情況進行評價。因此,本研究結果需要大樣本的臨床隨機試驗和薈萃分析進一步驗證。
綜上所述,接受更長DCB治療的患者更容易出現冠脈夾層,但DCB長度并不影響臨床預后。

