胎膜早破極早產兒的臨床特征和主要不良結局的預測因素分析
董會敏 宋娟 決珍珍 位樂樂 李文冬 周竹葉
(鄭州大學第三附屬醫院新生兒科/河南省小兒腦損傷重點實驗室/河南省兒科疾病臨床醫學研究中心,河南鄭州 450052)
胎膜早破 (prelabor rupture of membranes,PROM)被定義為臨產前發生的胎膜破裂,其中妊娠37周之前發生的胎膜早破被稱為未足月胎膜早破 (preterm prelabor rupture of membranes,PPROM)[1]。研究顯示妊娠<37周PPROM的發生率為2%~3%,妊娠<34周PPROM發生率低于1%[1-3]。PPROM主要引起早產兒宮內感染,也是早產兒發生呼吸道或神經系統并發癥和死亡的危險因素[4]。既往研究表明,胎齡越小,出生體重越輕,生后72 h內發生早發型敗血癥(early-onset sepsis,EOS)的風險和病死率越高[5-9]。本研究回顧性分析了PROM極早產兒的臨床資料,評估PROM極早產兒的臨床特征及其發生EOS和死亡的預測因素,旨在為PROM極早產兒主要不良結局的臨床防治提供循證醫學依據。
1 資料與方法
1.1 研究對象
收集2018年1月至2020年5月我院新生兒重癥監護室收治的PROM且胎齡<32周的早產兒的臨床資料,除外疑似先天性染色體或遺傳代謝性疾病、出生后因非感染性疾病3 d內放棄治療和臨床資料不完整的患兒,最終共399例患兒納入研究。根據胎膜破裂至分娩的時間不同分為4組:PROM<18 h(107例)、PROM 18 h~<3 d(111例)、PROM 3 d~<14 d(144例)和PROM≥14 d(37例)。另外根據生后72 h內是否發生EOS分為EOS組(42例)和非EOS組(357例);根據出生后3個月內存活與否分為存活組(359例)和死亡組(40例)。
該研究已獲得鄭州大學第三附屬醫院醫學倫理委員會批準[(2020)醫倫審第38號]及患兒家屬的知情同意。
1.2 診斷標準
PPROM的診斷標準參考《最新未足月胎膜早破臨床指南解讀》[2]。新生兒敗血癥的診斷標準參考《新生兒敗血癥診斷及治療專家共識(2019年版)》[10],確診診斷需要滿足血培養或腦脊液培養中發現致病細菌。臨床敗血癥的診斷要求有臨床異常表現的情況下滿足下列條件中任何一項:(1)血液非特異性檢查≥2項陽性;(2)腦脊液檢查呈化膿性腦膜炎改變。根據發生敗血癥的日齡,生后72 h內發生的為EOS,超過72 h發生的為晚發型敗血癥(late-onset sepsis,LOS)。
化膿性腦膜炎、新生兒肺炎、Ⅱ~Ⅲ期壞死性小腸結腸炎(necrotizing enterocolitis,NEC)、腦室內出血(intraventricular hemorrhage,IVH)、腦室周圍白質軟化(periventricular leukomalacia,PVL)、支氣管肺發育不良(bronchopulmonary dysplasia,BPD)、早產兒視網膜病變(retinopathy of prematurity,ROP)的診斷均參考第5版《實用新生兒學》[11]。
1.3 資料收集
收集所納入早產兒的臨床資料,包括母孕期一般情況:發生PROM時孕周、PROM時間、羊水情況、胎盤早剝、前置胎盤、妊娠期合并癥、胎盤病理檢查等;新生兒一般情況:性別、胎齡、出生方式、出生體重、窒息史、宮內窘迫、機械通氣史等;以及患兒住院期間并發癥/合并癥等。
1.4 統計學分析
采用SPSS 21.0統計軟件進行分析。正態分布的計量資料用均數±標準差(-x±s)表示,組間比較采用兩樣本t檢驗。偏態分布的計量資料以中位數(四分位數間距)[M(P25,P75)]表示,組間比較采用Mann-WhitneyU檢驗。計數資料用頻數及百分率(%)表示,組間比較采用χ2檢驗、連續性校正χ2檢驗或Fisher確切概率法。應用多因素logistic回歸分析PROM極早產兒發生EOS和死亡的預測因素。P≤0.05為差異有統計學意義。
2 結果
2.1 PROM極早產兒的臨床特征分析
共納入符合入選標準的早產兒399例,其中男224例,女175例;胎齡25~31+6周,平均胎齡(29.8±1.5)周;出生體重700~2 490 g,平均出生體重(1 380±289)g。死亡40例,其中因RDS死亡16例,因肺出血死亡6例,因敗血癥死亡6例,因重癥肺炎死亡1例,因重度窒息死亡2例,因重度IVH死亡2例,因持續性肺動脈高壓死亡1例,因預后較差放棄治療后死亡6例。
399例患兒中,較常見的并發癥依次為:新生兒肺炎(126例,31.6%)、新生兒窒息(112例,28.1%)、BPD(73例,18.3%)、Ⅲ~Ⅳ級RDS(56例,14.0%)、血小板減少癥(46例,11.5%)、IVH(45例,11.3%)、LOS(44例,11.0%)、EOS(42例,10.5%)、Ⅱ~Ⅲ期NEC(39例,9.8%)、化膿性腦膜炎(14例,3.5%)、ROP(12例,3.0%)和PVL(10例,2.5%)。
PROM<18 h、PROM 18 h~<3 d、PROM 3 d~<14 d及PROM≥14 d 4組間新生兒期各并發癥發生率和病死率的比較差異均無統計學意義(P>0.05),見表1。
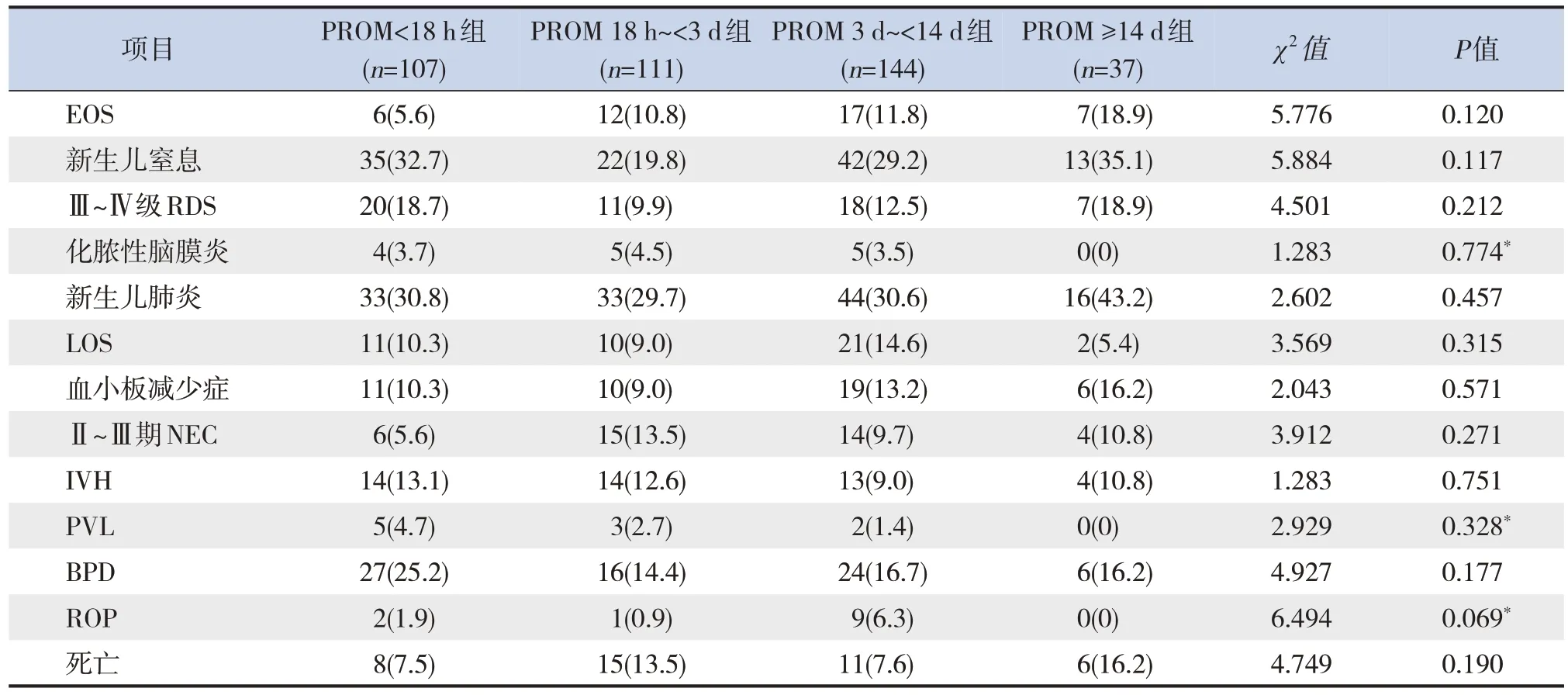
表1 PROM不同時間各組的臨床特征比較 [n(%)]
2.2 PROM極早產兒發生EOS的單因素分析
單因素分析顯示,與非EOS組相比,EOS組患兒胎齡較小,出生體重較低,Ⅲ度羊水污染比例較高,新生兒窒息和Ⅲ~Ⅳ級RDS的發生率較高,差異均有統計學意義(P<0.05),見表2。
2.3 PROM極早產兒死亡預測因素的單因素分析
單因素分析顯示,與存活組患兒相比較,死亡組患兒出生胎齡較小,出生體重較低,新生兒窒息、Ⅲ~Ⅳ級RDS及新生兒敗血癥的發生率較高,機械通氣≥7 d的比例較高,差異均有統計學意義(P<0.05),見表3。
2.4 PROM極早產兒發生EOS的多因素logistic回歸分析
將單因素分析中有統計學意義的變量(胎齡、出生體重、Ⅲ度羊水污染、新生兒窒息和Ⅲ~Ⅳ級RDS)進行多因素logistic回歸分析,顯示出生體重<1 000 g、Ⅲ度羊水污染和Ⅲ~Ⅳ級RDS是PROM極早產兒發生EOS的預測因素 (P<0.05),見表4。
2.5 PROM極早產兒死亡預測因素的多因素logistic回歸分析
將單因素分析中有統計學意義的變量(胎齡、出生體重、Ⅲ~Ⅳ級RDS、新生兒窒息、新生兒敗血癥、機械通氣≥7 d)進行多因素logistic回歸分析,顯示出生體重<1 000 g、出生體重1 000~1 499 g、Ⅲ~Ⅳ級RDS及新生兒敗血癥是PROM極早產兒死亡的預測因素(P≤0.05),見表5。
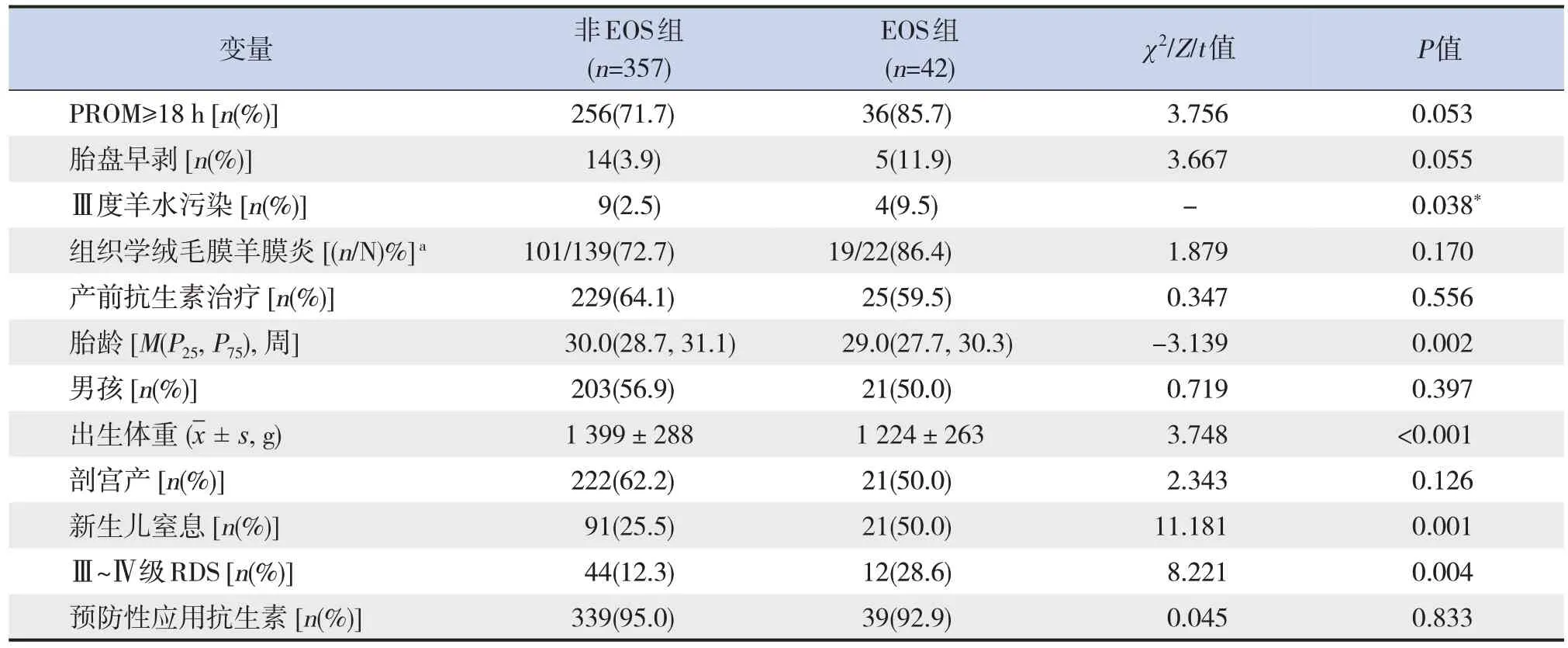
表2 PROM極早產兒發生EOS的單因素分析
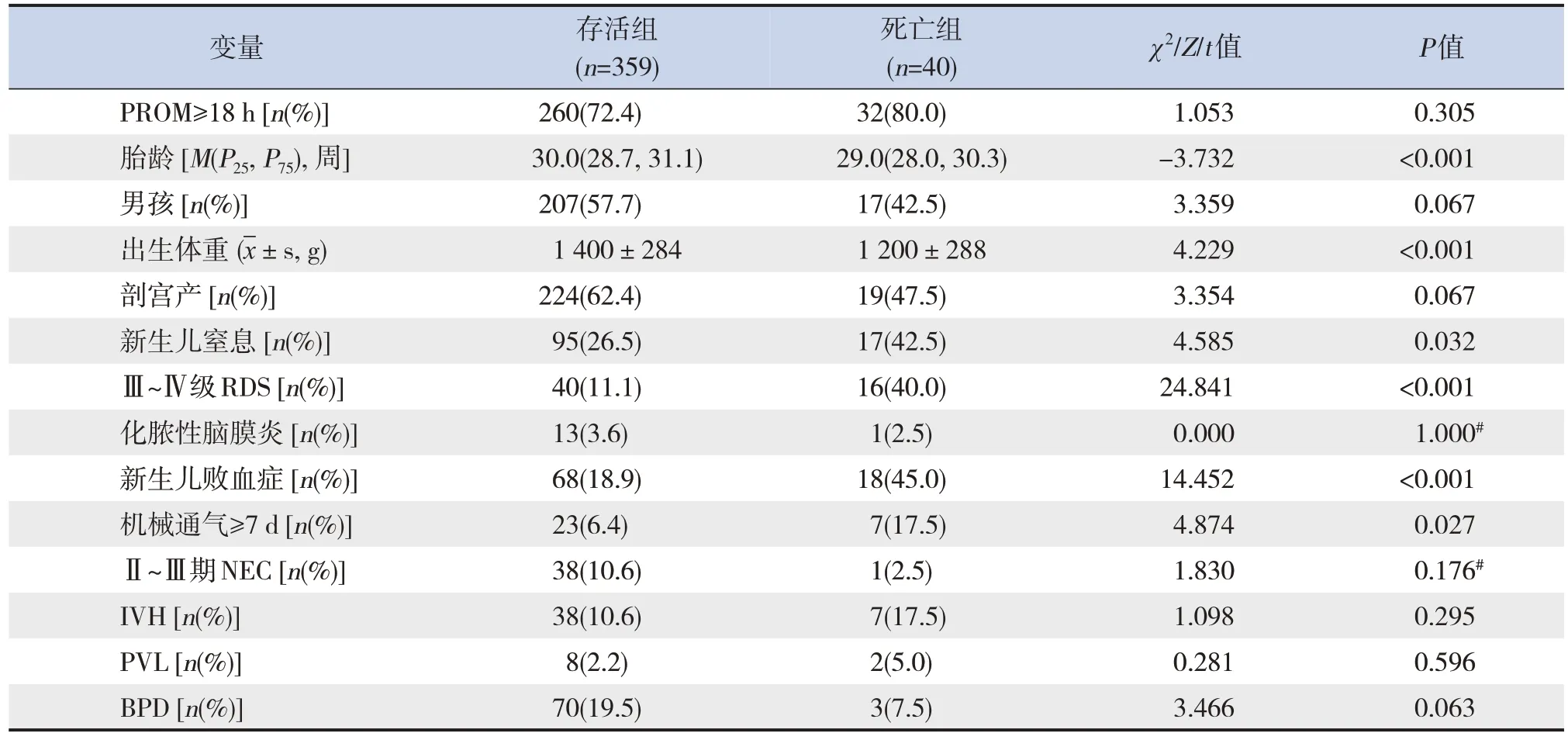
表3 PROM極早產兒死亡預測因素的單因素分析
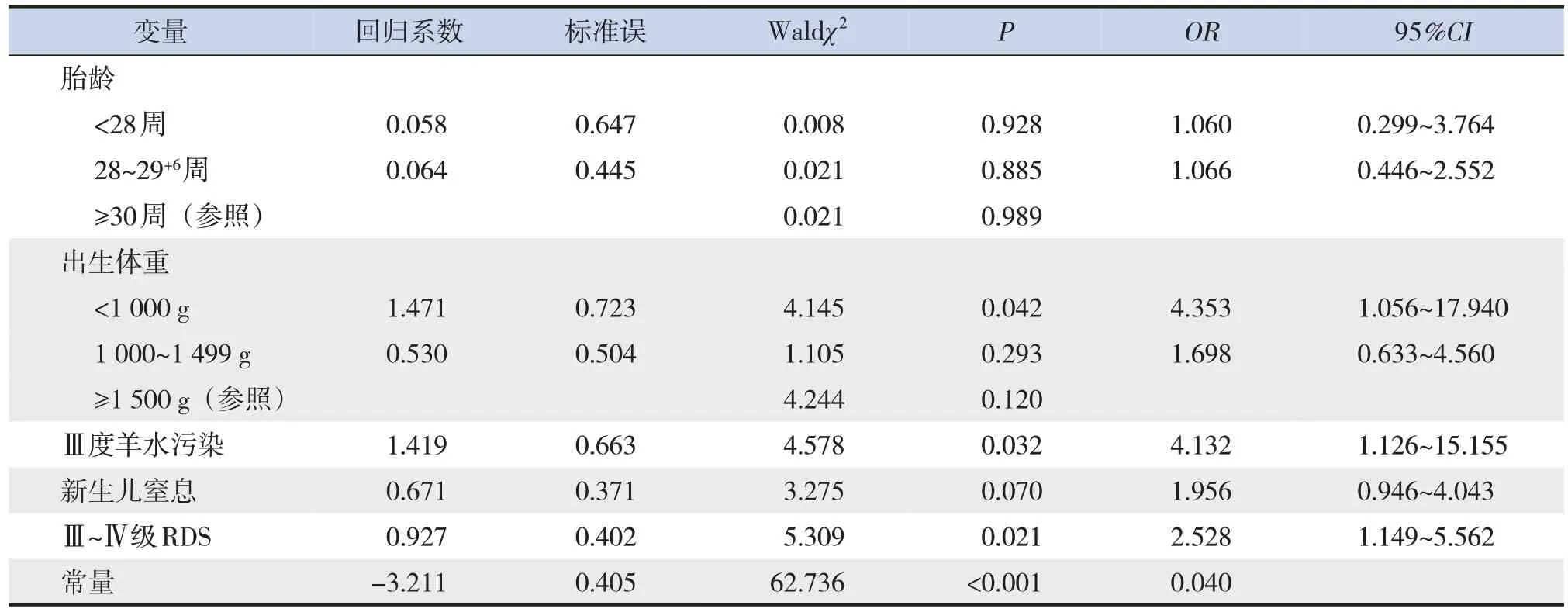
表4 PROM極早產兒發生EOS的多因素logistic回歸分析
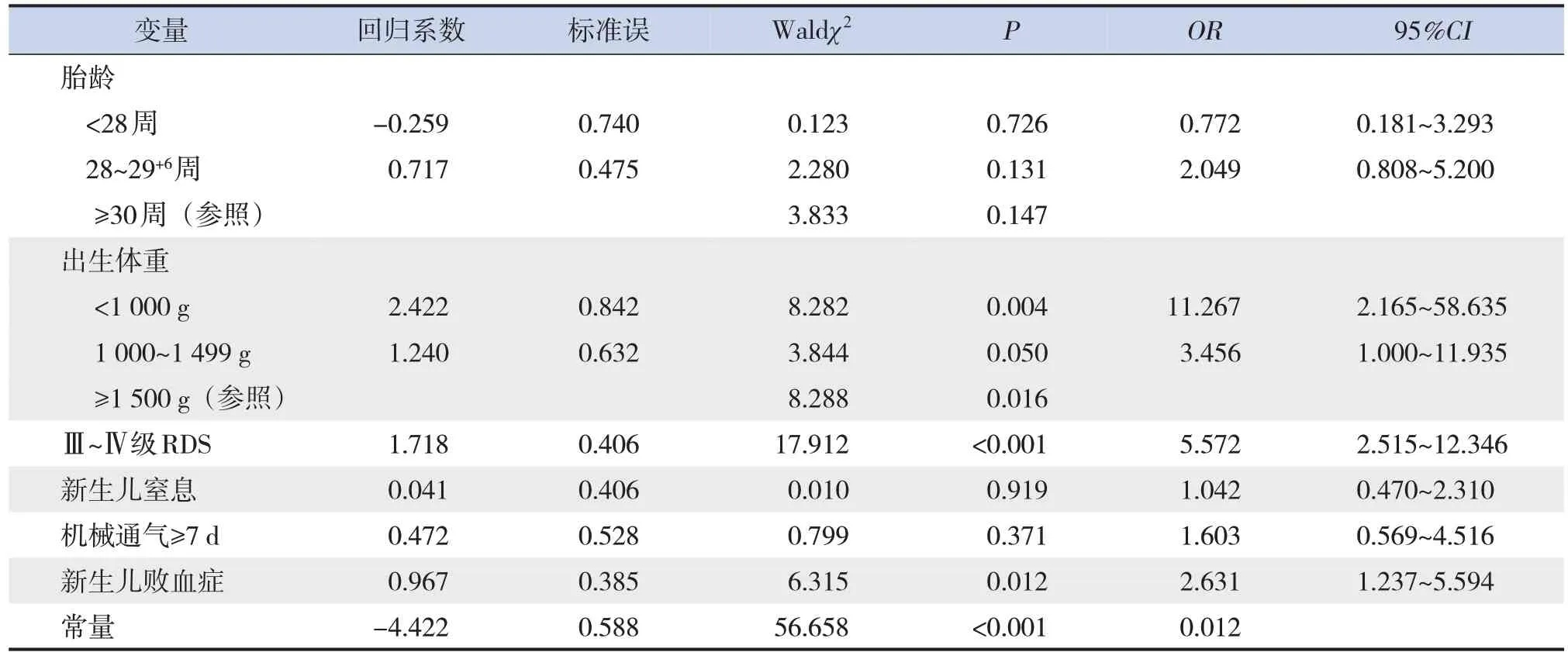
表5 PROM極早產兒死亡預測因素的多因素logistic回歸分析
3 討論
本研究顯示,PROM極早產兒中,新生兒肺炎(31.6%)是最常見的并發癥,其次是新生兒窒息(28.1%)、BPD(18.3%)、Ⅲ~Ⅳ級RDS(14.0%)、血小板減少癥(11.5%)、IVH(11.3%)、LOS(11.0%)、EOS(10.5%)等。吳甜等[12]研究顯示,331例PROM早產兒(胎齡<37周)中,肺炎發生率為51.1%,RDS為15.1%,窒息為14.2%,EOS為5.7%,BPD為2.4%。段順艷等[13]的一項多中心研究顯示,在2 889例PROM早產兒中,合并RDS 15.5%,敗血癥3.4%,BPD 2.9%。與之相比較,本研究中新生兒窒息、BPD及敗血癥的發生率較高,可能與研究對象納入標準不同及區域差異有關。Ye等[14]研究顯示,323例伴有PROM的24~34周的早產兒中,19.2%(62/323)合并有早產兒敗血癥,本研究結果與其一致。國外Gezer等[15]對288例PROM早產兒研究發現,在胎齡29~32周的早產兒中,RDS發生率為27.7%,敗血癥為10.8%,IVH為9.6%,病死率為8.4%;在胎齡≤28周的早產兒中,RDS發生率為75.0%,敗血癥為33.9%,IVH為26.8%,病死率為53.6%,可見隨著胎齡的降低,PROM早產兒的并發癥的發生率及病死率隨之增加。因此,提示臨床醫生應加強PROM早產兒住院期間管理,特別關注胎齡較小的極早產兒或超早產兒,盡可能減少嚴重并發癥及不良結局的發生。
另外,本研究發現PROM時間延長并不增加極早產兒的新生兒期并發癥和死亡的發生率,與既往報道一致[16-17]。Lorthe等[16]通過對胎齡24~32的PROM早產兒的全國性調查,發現PROM時間延長并不惡化新生兒預后;Manuck等[17]也研究了306例胎齡22~33周的PROM的早產兒,發現PROM時間與圍生期不良結局無相關性。此外,有學者認為PROM新生兒的不良結局很大程度上取決于胎齡[18],因此需要權衡早產與PROM時間延長帶來的風險,在應用抗生素防治感染的同時,合理應用宮縮抑制劑,并給予糖皮質激素促進胎肺成熟,以期延長孕周,改善早產兒預后[2]。
本研究多因素logistic回歸分析顯示,超低出生體重、Ⅲ度羊水污染與Ⅲ~Ⅳ級RDS是PROM極早產兒發生EOS的預測因素。Palatnik等[19]研究發現,較低的出生體重是極早產兒發生EOS或死亡的獨立危險因素,本研究結果與其相一致。吳芳芳等[20]研究顯示,羊水污染是新生兒EOS的危險因素之一,可能的原因為羊水受到胎糞污染后,胎兒長時間處于污染的羊水中,增加了其宮內感染的發生。Baizat等[21]研究發現早產兒應用肺表面活性物質是EOS的預測因素,而肺表面活性物質為RDS的有效替代治療方法,因此RDS與早產兒EOS的發生有一定的相關性。可能的原因是早產兒肺部發育不成熟,易引起肺部局部感染,因早產兒免疫系統欠完善,最終導致EOS的發生。
本研究多因素logistic回歸分析顯示,極低出生體重、Ⅲ~Ⅳ級RDS、新生兒敗血癥是PROM極早產兒發生死亡的預測因素,這與一項前瞻性研究[22]結果一致。早產所致的較低出生體重兒因全身各個臟器未發育成熟,功能不完善,其與死亡的相關性已成為共識[19,22]。國內吳繁等[23]與張雨生[24]的研究表明RDS是引起早產兒死亡的主要原因。張素娥等[25]對179例超早產兒的研究發現,PROM者使用肺表面活性物質的比例偏低,可能的原因是PROM引起宮內絨毛膜羊膜炎的發生率增高,宮內炎癥反應有利于刺激胎肺成熟[25-26]。因此PROM一定程度上降低了RDS的發生,但是伴有PROM的早產兒,一旦發生嚴重的RDS,加上感染的潛在因素,可能會導致較嚴重的不良結局[27]。因此,合理應用產前糖皮質激素和生后外源性肺表面活性物質促進肺成熟,能夠改善PROM早產兒RDS的嚴重程度,降低病死率[28]。此外,PROM被認為是引起早產兒宮內感染的主要因素,產婦生殖道細菌,如大腸埃希菌、鏈球菌等可通過上行性感染進入羊膜腔,刺激單核-巨噬細胞分泌炎性因子,誘發炎癥反應,增加宮內感染的風險[29-30]。國外Corchia等[27]對意大利地區2 974例極早產兒的研究表明,PROM增加了因新生兒感染導致早產兒死亡的風險。可見,早產兒敗血癥也是引起早產兒死亡的主要原因之一[31]。針對合并PROM的早產兒,我國《新生兒敗血癥診斷和治療專家共識(2019年版)》[10]推薦對PROM≥18 h或母親確診絨毛膜羊膜炎的新生兒預防性使用抗生素。本研究為單中心回顧性分析,且樣本量有限,對研究結果可能會造成一定的偏倚。因此,有必要采用多中心的前瞻性隊列研究來驗證相關因素對疾病發生的風險。
綜上所述,本研究顯示,PROM時間延長不會增加極早產兒新生兒期并發癥和死亡的發生率,但仍要高度重視PPROM對早產兒帶來的潛在感染風險。極早產兒不良結局,如EOS和死亡的發生與較低的出生體重、肺發育不成熟和全身感染有著密切的關系,臨床上對于有發生極早產風險的PROM產婦應在控制感染的同時,適當延長孕周,并促胎肺成熟,減少早產兒并發癥和不良結局的發生。針對存在高危因素的患兒應早期識別并采取有效措施早期干預,提高早產兒生存率。

