替普瑞酮治療老年HP陽性慢性萎縮性胃炎臨床效果分析
吳 晉
(遼寧中醫藥大學附屬第四醫院藥劑科,遼寧 沈陽 110024)
慢性萎縮性胃炎是常見消化道疾病,多發于老年人群。目前其發病機制尚未完全探明,但研究[1]表明幽門螺旋桿菌(Helicobacter pylori,HP)感染為其主要致病機制之一。目前老年HP陽性慢性萎縮性胃炎多采用質子泵抑制劑、抗生素進行HP根治治療。近年研究[2-3]顯示,葉酸作為水溶類維生素可促進胃黏膜修復,與HP根治療法聯用可促進病情歸轉,為慢性萎縮性胃炎的常用治療方案,但耐藥仍普遍存在。替普瑞酮為萜烯類藥物衍生物,可為萎縮胃黏膜組織提供磷脂質[4]。目前替普瑞酮聯合葉酸及HP根治療法治療老年HP陽性慢性萎縮性胃炎的相關研究較少,治療機制也尚未明確。本研究旨在觀察替普瑞酮聯合葉酸、HP根治療法治療老年HP陽性慢性萎縮性胃炎患者的臨床效果,現報告如下。
1 資料與方法
1.1 一般資料 納入2019年2月至2020年3月我院收治的老年HP陽性慢性萎縮性胃炎患者132例,采用隨機數字表法分為對照組和觀察組,各66例。對照組男性36例,女性30例;病程1~7年,平均(3.01±1.25)年;年齡60~78歲,平均(68.33±4.62)歲;體重指數(BMI)19~26 kg/m2,平均(22.02±1.12)kg/m2;胃黏膜萎縮程度[5]中,Ⅰ度20例,Ⅱ度27例,Ⅲ度19例。觀察組男性33例,女性33例;病程1~7年,平均(3.13±1.41)年;年齡60~79歲,平均(67.42±4.77)歲;BMI 19~25 kg/m2,平均(22.16±1.32)kg/m2;胃黏膜萎縮程度中,Ⅰ度18例,Ⅱ度28例,Ⅲ度20例。兩組患者性別、病程、年齡、BMI及胃黏膜萎縮程度比較無統計學差異(均P>0.05)。病例納入標準:①慢性萎縮性胃炎診斷符合《中國慢性胃炎共識意見(2017年,上海)》[6]中標準;②既往無胃腸道及腹部手術治療史;③HP經呼氣試驗診斷為陽性;④心、肝、腎等重要臟器功能正常,無精神障礙、語言障礙等。排除標準:①對替普瑞酮、葉酸及HP根治療法治療有禁忌證;②合并自身免疫缺陷性疾病、嚴重感染性疾病;③合并膽道梗阻、消化道潰瘍及消化道梗阻等疾病;④病理組織學檢查提示萎縮性胃炎組織有惡變傾向。研究對象均對本研究知情同意。本研究實驗設計經本院醫學倫理委員審批。
1.2 治療方法
1.2.1 對照組:接受葉酸及HP根治療法治療。口服葉酸片(國藥準字H21020966,5 mg/片),10 mg/次,3次/d;埃司美拉唑腸溶片(國藥準字H20203298, 20 mg/片),20 mg/次,2次/d;阿莫西林膠囊(國藥準字H23020415,0.25 g/片),1 g/次,2次/d;克拉霉素膠囊(國藥準字H19990221,0.125 g/粒),0.5 g/次,2次/d。治療3個月。
1.2.2 觀察組:在對照組基礎上口服替普瑞酮膠囊(國藥準字H20093656,50 mg/粒),50 mg/次,3次/d。治療3個月。
1.3 觀察指標
1.3.1 胃蛋白酶原(PG)水平:治療前后抽取患者空腹清晨靜脈血3 ml,3000 r/min離心10 min后取上層血清,通過酶聯免疫吸附試驗(ELISA)分析血清胃蛋白酶原Ⅰ(PGⅠ)和胃蛋白酶原Ⅱ(PGⅡ),并計算PGⅠ/PGⅡ(PGR)。
1.3.2 胃腸道激素水平:治療前后采用免疫比濁法檢測血清降鈣素基因相關肽(CGRP)、生長抑素(SS)和表皮生長因子(EGF)水平。血液采集及血清制備同1.3.1。
1.3.3 炎癥因子水平:治療前后,通過ELISA檢測兩組血清白介素(IL)-8、IL-11水平,通過化學發光免疫分析法檢測血清腫瘤壞死因子-α(TNF-α)水平。血液采集及血清制備同1.3.1。
1.3.4 內鏡病理評分[7]:包括黏膜炎癥(黏膜炎性細胞浸潤程度)、炎癥活動度(黏膜充血、水腫情況)、腺體及腸上皮化生(腺體數量減少,胃黏膜上皮組織轉變為腸道黏膜上皮組織情況),根據嚴重程度計0~4分,得分越高表示病理程度越高。
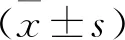
2 結 果
2.1 兩組患者治療前后血清PG水平比較 見表1。治療后,兩組血清PG Ⅰ、PG Ⅱ、PGR水平升高,且觀察組PG Ⅰ、PGR水平高于對照組(均P<0.05)。
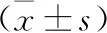
表1 兩組患者治療前后血清PG水平比較
2.2 兩組患者治療前后血清胃腸道激素水平比較 見表2。治療后,兩組血清EGF水平較治療前降低,且觀察組低于對照組(均P<0.05);CGRP、SS水平較治療前升高,且觀察組高于對照組(均P<0.05)。
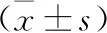
表2 兩組患者治療前后血清胃腸道激素水平比較
2.3 兩組患者治療前后血清炎癥因子水平比較 見表3。治療后,兩組血清炎癥因子水平降低,且觀察組低于對照組(均P<0.05)。

表3 兩組患者治療前后血清炎癥因子水平比較(ng/L)
2.4 兩組患者治療前后內鏡病理評分比較 見表4。治療后,兩組黏膜炎癥、炎癥活動度、腺體及腸上皮化生評分降低,且觀察組低于對照組(均P<0.05)。

表4 兩組患者治療前后內鏡病理評分比較(分)
3 討 論
固有腺體減少或消失為老年HP陽性慢性萎縮性胃炎的主要特征。研究[8]顯示,慢性萎縮性胃炎發病率可達10%以上,而隨訪10年遠期癌變率為3%~6%,臨床需引起重視。目前老年HP陽性慢性萎縮性胃炎尚無特效治療方案,葉酸及HP根治療法為常規治療方案。HP根治療法中,埃司美拉唑為質子泵抑制劑,可抑制胃酸分泌;阿莫西林和克拉霉素為抗生素,可殺滅HP,共同起到根治HP的作用;葉酸可提供組織生長必需的甲基供體,促進胃黏膜恢復,一定程度上改善腺體萎縮情況。但HP根治療法起效慢,對疾病進程逆轉作用不強,臨床亟需探索新的治療方案。
研究[9-11]顯示,替普瑞酮具有廣譜抗潰瘍作用,且不會影響胃腸道正常功能。替普瑞酮屬萜烯類藥物衍生物,不僅可以促進胃黏膜微粒體中糖脂質中間體的生物合成,進而提高胃黏膜中磷脂質的含量,最終促進胃黏膜細胞再生,還可以改善胃黏膜局部微循環,提高磷脂流動性而激活磷脂酶A2,從而提高前列腺素的合成作用,促進損傷胃黏膜的修復過程,抑制損傷胃黏膜分泌與釋放致炎因子,進而促進胃鏡病理狀況改善。本研究中,治療后觀察組血清IL-8、IL-11、TNF-α水平,以及黏膜炎癥、炎癥活動度、腺體及腸上皮化生評分均低于對照組,提示替普瑞酮聯合葉酸及HP根治療法可降低老年HP陽性慢性萎縮性胃炎患者炎癥反應及胃黏膜損傷。
PGⅠ、PGⅡ均為胃黏膜腺體分泌的胃蛋白酶原。老年HP陽性慢性萎縮性胃炎患者存在黏膜腺體萎縮,可導致兩者血清水平下降,但由于PGⅡ腺體在胃黏膜內比例更高,PGⅡ變化較PGⅠ更小,故而PGR出現下降[12-13]。SS為神經內分泌因子,可感知胃酸分泌水平,從而調節胃酸對消化道黏膜的損傷。CGRP主要分布于血管神經纖維內,可改善胃腸黏膜微循環供血[14]。EGF可促進上皮細胞、成纖維細胞增殖,參與損傷胃黏膜的重建過程,在老年HP陽性慢性萎縮性胃炎的發生與發展中發揮重要作用[15-16]。本研究中,治療后觀察組血清PGⅠ、CGRP、SS、PGR水平高于對照組,而血清EGF水平低于對照組,提示替普瑞酮聯合葉酸及HP根治療法可調節神經內分泌激水平,進而促進HP陽性慢性萎縮性胃炎患者胃黏膜再生,增加其分泌功能。其原因可能為:①替普瑞酮可提高胃壁黏液中的磷脂質濃度,增強胃黏膜防御作用,降低胃黏膜損傷,促進損傷重建過程[17];②替普瑞酮可保持胃黏膜細胞增殖區的穩定性,促進壞死組織代謝、修復,提高胃黏膜完整性,促進血管神經纖維分泌CGRR[18];③替普瑞酮可促進高分子糖蛋白的生物合成,加速黏膜修復因子的合成,進而促進胃黏膜血管、上皮、分泌腺的修復[19-20]。
綜上所述,替普瑞酮聯合葉酸、HP根治療法可降低老年HP陽性慢性萎縮性胃炎患者血清EGF水平,提高血清CGRP、SS水平,改善腸道激素及PG分泌,抑制炎癥反應,進而改善胃鏡病理情況。

