雪蓮細胞培養物的質量標準研究
張敏 張雪松 劉雅萍

摘要 目的:建立雪蓮細胞培養物的質量標準。方法:參照《中華人民共和國藥典》2020年版附錄,分別建立雪蓮細胞培養物的一般檢查項目及定性定量指標。以蘆丁為對照品,利用紫外分光光度法建立雪蓮細胞培養物總黃酮成分含量的測定方法;利用高效液相色譜(HPLC)法同時測定綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸成分含量,并建立其特征圖譜,采用2012版《中藥色譜指紋圖譜相似度評價系統》對特征圖譜進行相似度分析。結果:15批次雪蓮細胞培養物總黃酮類成分含量10.0%~11.0%;綠原酸含量0.86%~1.09%;紫丁香苷含量0.34%~0.48%;1,5-二咖啡酰奎尼酸含量3.20%~3.75%。15批雪蓮細胞培養物指紋圖譜相似度大于0.9,特征圖譜中呈現10個特征峰,指認峰2為綠原酸、峰4為紫丁香苷、峰7為1,5-二咖啡酰奎尼酸。結論:本研究建立了雪蓮細胞培養物的質量標準,建議醇溶性浸出物不得低于29.4%;雪蓮細胞培養物中的總黃酮類成分含量不得低于10.0%,綠原酸、紫丁香苷、1,5-二咖啡酰奎尼酸的含量應分別不得低于0.86%、0.34%、3.20%,為天山雪蓮藥制品的工業化生產提供了參考。
關鍵詞 雪蓮細胞培養物;定性定量;總黃酮;綠原酸;紫丁香苷;1,5-二咖啡酰奎尼酸;特征圖譜;質量標準
Abstract Objective:To establish the quality standard of Saussurea involucrata cell cultures.Methods:According to the appendix of Chinese Pharmacopoeia (2020 edition),the general examination items and qualitative and quantitative indexes of S.involucrata cell cultures were established.The content of total flavonoids in Saussurea involucrata cell culture was determined by ultraviolet spectrophotometry with rutin as the control substance; the content of chlorogenic acid,syringin and 1,5-dicaffeoylquinic acid was determined by HPLC simultaneously,and the characteristic chromatogram was established.The similarity of characteristic chromatogram was analyzed by the software Chinese Medicine Chromatographic Fingerprint Similarity Evaluation system(2012 edition).Results:The total flavonoid content of 15 batches of S.involucrata cell cultures was between 10.0% and 11.0%; the content of chlorogenic acid was between 0.86% and 1.09%; the content of syringin was between 0.34% and 0.48%; 1,5-The content of dicaffeoylquinic acid was between 3.20% and 3.75%.The similarity of fingerprint patterns of 15 batches of S.involucrata cell cultures was greater than 0.9,and there were 10 characteristic peaks in the characteristic pattern.Peak 2 was chlorogenic acid,peak 4 was syringin,and peak 7 was 1,5-dicaffeoylquinic acid.Conclusion:In this study,the quality standard of S.involucrata cell cultures is established,and it is suggested that the alcohol soluble extract should not be less than 29.4%; the content of total flavonoids in S.involucrata cell cultures should not be less than 10.0%,and the content of chlorogenic acid,syringin and 1,5-dicaffeoylquinic acid should not be less than 0.86%,0.34% and 3.20%,respectively,which provides a reference for the industrial production of S.involucrata medicinal products.
Keywords Cell cultures of Saussurea involucrata; Qualitative and quantitative indicators; Total flavonoids; Chlorogenic acid; Syringin; 1,5-dicaffeoylquinic acid; Characteristic chromatogram; Quality standard
中圖分類號:R284.1文獻標識碼:Adoi:10.3969/j.issn.1673-7202.2021.07.001
天山雪蓮[Saussurea involucrate(Kar.et Kir.)Sch.Bip]又稱雪蓮、雪蓮花、新疆雪蓮,為菊科風毛菊屬多年生草本植物,主要分布于新疆天山、昆侖山及阿爾泰山區終年積雪不化的地帶,是一種高山稀有的名貴藥用植物[1]。其入藥始載于公元8世紀的藏藥典《月王藥診》,并在之后多部著名醫藥典籍中出現,如《四部醫典》《本草綱目拾遺》等,至今已有上千年的用藥歷史。天山雪蓮具有活血通經、散寒除濕、強筋助陽的功效[2],漢族人民多視其為治療風濕關節炎之珍品,維吾爾族、哈薩克族則將其作為治療痛經、月經不調的婦科良藥,故民間有“東北人參,新疆雪蓮”之說。現代研究表明,天山雪蓮主含黃酮類、倍半萜類、香豆素類、生物堿類等活性成分,具有抗炎鎮痛、抗疲勞、抗衰老等作用[3],其對人體的調理保健作用受到普遍關注。
由于天山雪蓮生長環境獨特,生長周期長,人工栽培困難,加之亂采濫挖,過度開發,野生資源瀕臨滅絕,已被列為國家二級瀕危植物,難以滿足日益增長的市場需求。而在人工控制的條件下,對天山雪蓮進行細胞培養,可在短時間內獲取大量細胞產物,并能保證產品質量穩定、藥效成分高,實現大規模工業化生產,從而解決雪蓮藥材短缺的問題[4-6]。有研究表明,雪蓮細胞培養物與野生植株存在相似的化學成分及藥效,富含黃酮類化合物,且綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸的含量遠高于天然植物,具有重要的應用價值[7-8]。目前,已有大量以雪蓮細胞培養物為原料的營養保健品上市[9-10]。鑒于雪蓮細胞培養物與植物在生長周期、生長環境及外觀性狀等方面存在明顯差異,需針對其特點進行質量研究。
我們首次對雪蓮細胞培養物的水分、灰分、酸不溶性灰分及醇溶性浸出物進行測定,并以蘆丁為對照,建立紫外分光光度法測定總黃酮成分含量,建立高效液相色譜(HPLC)法同時測定綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸成分含量,并在此基礎上規定其活性成分的含量限度,同時建立對照特征圖譜,為雪蓮培養物的質量控制提供參考。
1 儀器與試藥
1.1 儀器
紫外分光光度計(島津企業管理有限公司,型號:UV-1900I);高效液相色譜儀(安捷倫科技公司,美國,型號:Agilent 1260);色譜柱(4.6 mm×250 mm,5 μm)(安捷倫科技公司,美國,型號:Agilent ODS C18);電子天平(上海精科天美儀器有限公司,型號:FA2204B)。
1.2 試劑
甲醇(色譜級,Merck,德國,批號:JA090530);乙腈(色譜級,Spectrum Chemical,美國,批號:3IA0017);其他試劑均為分析純,水為去離子水。蘆丁標準品(純度98%,北京北納創聯生物技術研究院,批號:153-18-4);綠原酸標準品(純度98%,中國藥品生物制品檢定所,批號:110753-200413);紫丁香苷標準品(純度98%,中國藥品生物制品檢定所,批號:111574-200205);1,5-二咖啡酰奎尼酸標準品(純度98%,北京北納創聯生物技術研究院,批號:19040105)。
1.3 分析樣品
15批雪蓮培養物由大連普瑞康生物技術有限公司提供,以野生天山雪蓮[S.involucrate(Kar.et Kir.)Sch.Bip.]的種子萌發的無菌葉片為種源,誘導產生愈傷組織進行繼代培養,即得紫紅色團狀細胞培養物,編號S1~S15。
2 方法與結果
2.1 雪蓮培養物的水分、灰分和酸不溶性灰分測定
按照《中華人民共和國藥典》(2020年版)(以下簡稱《藥典》)通則0832第二法測定雪蓮培養物中的水分:含水量為4.6%~7.0%。按照《藥典》通則2302測定雪蓮培養物中的總灰分:總灰分為7.0%~9.8%。按照《藥典》通則2302測定雪蓮培養物中的酸不溶性灰分:酸不溶性灰分為0.15%~0.23%。具體結果見表1。
2.2 雪蓮培養物中浸出物測定
根據《藥典》通則2201醇溶性浸出物測定法項下的熱浸法測定,以70%乙醇作溶劑,對雪蓮培養物的浸出物進行檢查,得浸出物含量為29.40%~32.40%,平均浸出物為30.94%。具體結果見表1。
2.3 雪蓮培養物中總黃酮成分含量測定
2.3.1 對照品溶液的制備
取蘆丁對照品適量,精密稱定,加甲醇溶解,制成每1 mL含蘆丁0.4 mg的溶液,作為對照品溶液。
2.3.2 供試品溶液的制備
取本品0.1 g,精密稱定,加甲醇適量,超聲處理30 min,放冷,轉移至50 mL容量瓶,定容,搖勻。并按亞硝酸鈉-硝酸鋁法[11]進行處理。
2.3.3 線性關系考察
分別精密量取對照品溶液1、2、3、4、5、6 mL,置25 mL量瓶中,加水至6.0 mL,加5%亞硝酸鈉溶液1 mL,混勻后靜置6 min;加10%硝酸鋁溶液1 mL,混勻后靜置6 min;加4%氫氧化鈉溶液10 mL,加蒸餾水定容至刻度,混勻后在510 nm波長處測定吸光度。以吸光度(A)為縱坐標,濃度(μg/mL)為橫坐標繪制標準曲線,得回歸方程y=80.912x-0.109 3,R2=0.999 9。
2.3.4 精密度試驗
取對照品溶液,連續測定6次。測定其吸光度,得到RSD值為0.09%,表明精密度良好。
2.3.5 中間精密度試驗
不同實驗人員進行“2.3.4”項下試驗。測定其吸光度,得到RSD值為1.04%,表明中間精密度良好。
2.3.6 穩定性試驗
取3組供試品溶液,分別于0 h、0.5 h、1.0 h、1.5 h、2.0 h、2.5 h、3.0 h時進行測定,計算3組總黃酮類成分的RSD值分別為0.81%、0.73%和0.67%,說明供試品溶液3 h內穩定。
2.3.7 重復性試驗
精密稱取雪蓮培養物0.1 g共6份,按“2.3.2”項下方法制備供試品溶液。測定其吸光度,得到RSD值為0.80%,表明本方法重復性良好。
2.3.8 回收率試驗
取雪蓮培養物0.05 g與定量的蘆丁對照品溶液混合進行超聲提取,制備供試品溶液。平行6次,測定總黃酮含量,計算方法的回收率為99.60%,RSD%為1.42%,表明方法的準確度較好。
2.3.9 樣品測定結果
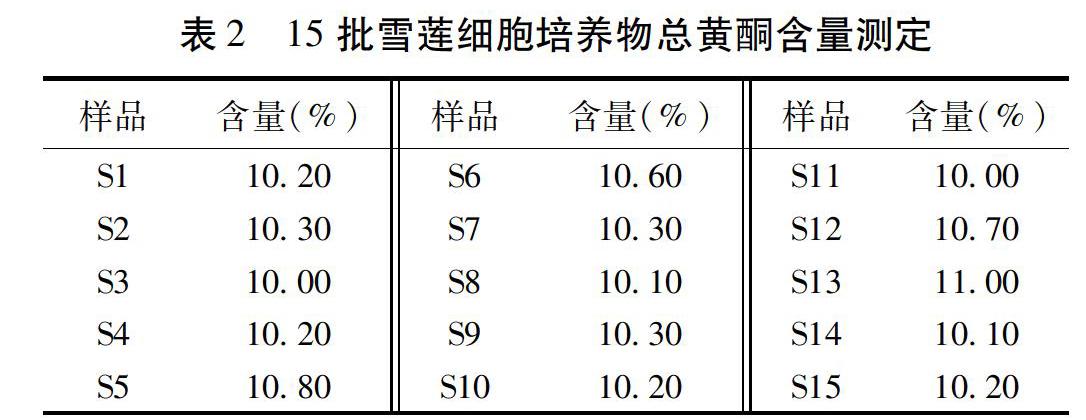
取各批次雪蓮細胞培養物,測定總黃酮含量。測得雪蓮總黃酮含量為10.0%~11.0%,平均值為10.33%。見表2。
2.4 雪蓮培養物中綠原酸、紫丁香苷、1,5-二咖啡酰奎尼酸含量的測定
2.4.1 色譜條件
安捷倫1200液相系統,Agilent ODS C18色譜柱(4.6 mm×250 mm,5 μm);以乙腈流動相為A,以0.02M磷酸二氫鉀溶液為流動相B,梯度洗脫(0~20 min,8%~10% A;20~50 min,10%~30% A);柱溫30 ℃;流速為1.0 mL/min;檢測波長265 nm;進樣量為20 μL。
2.4.2 對照品溶液的制備
取綠原酸、紫丁香苷、1,5-二咖啡酰奎尼酸標準品適量,加10%乙腈溶液,配制含量分別為0.01 mg/mL、0.005 mg/mL、0.025 mg/mL的混合標準品溶液。
2.4.3 供試品溶液的制備
取本品0.1 g,加10%乙腈水溶液100 mL,超聲提取30 min,取上清液過濾膜,待測。
2.4.4 專屬性試驗
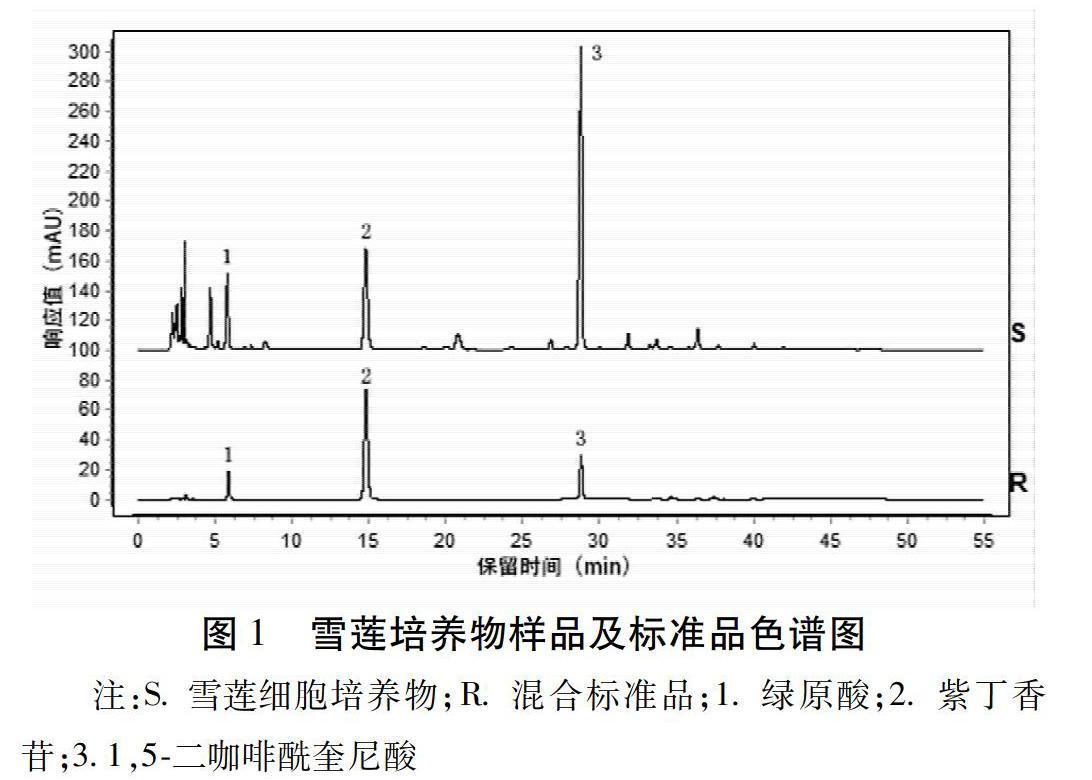
精密量取供試品溶液、混合對照品溶液各20 μL,注入液相色譜儀,按2.4.1色譜條件下進樣檢測,結果見圖1。結果表明,本方法可正確檢測綠原酸、紫丁香苷、1,5-二咖啡酰奎尼酸色譜峰,專屬性良好。
2.4.5 線性關系考察
取標準品溶液,在進樣量分別為4 μL、10 μL、16 μL、20 μL、40 μL、60 μL條件下測定峰面積,折算進樣量20 μL進行測定。以質量濃度(μg/mL)為縱坐標,峰面積(AU×S)為橫坐標,繪制各成分標準曲線。綠原酸y=0.069 18x+0.098 47(R2=1),線性范圍為2.3~34.5 μg/mL;紫丁香苷y=0.021 30x+0.006 75(R2=1),線性范圍為0.992~14.88 μg/mL;1,5-二咖啡酰奎尼酸y=0.063 82x+0.085 31(R2=1),線性范圍為5.0~75.0 μg/mL。
2.4.6 精密度試驗
取綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸混合對照品,連續測定6次。計算峰面積RSD,得到RSD值分別為0.16%、0.77%和0.11%,說明精密度良好。
2.4.7 中間精密度試驗
不同研究人員采用不同儀器取同一批次樣品0.1 g,按照“2.4.3”項下制備供試品溶液,進樣測定,得到中間精密度RSD值分別為0.36%、1.01%、1.20%,表明中間精密度良好。
2.4.8 穩定性試驗
取雪蓮培養物0.1 g,按2.4.3制備供試品溶液,分別在0、1、2、3、4、5 h進樣。計算峰面積RSD值小于2%,結果表明,供試品溶液在5 h內穩定性良好。
2.4.9 重復性試驗
按“2.4.6”項下方法,計算對照品溶液中綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸的峰面積,得到RSD值分別為1.04%、0.91%和0.73%,說明方法的重復性良好。
2.4.10 回收率試驗
精密稱定雪蓮培養物0.05 g,定量加入一定濃度的混合標準品溶液,制備供試品溶液,平行六次測定,得到綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸回收率均值分別為101.97%、100.18%、100.66%,RSD值分別為1.68%、1.76%、2.44%。1,5-二咖啡酰奎尼酸回收率的RSD值偏大,推測與1,5-二咖啡酰奎尼酸穩定性有關,其樣品溶液配制時間過長導致含量降低,回收率測定結果偏差較大。
2.4.11 樣品測定結果
取15個批次的雪蓮細胞培養物,進行含量測定,得到綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸平均含量分別為0.99%、0.38%、3.45%,RSD值分別為6.01%、10.37%、5.03%。見表3。
2.5 特征圖譜的建立
2.5.1 供試品溶液的制備 同“2.4.3”項下。
2.5.2 對照品參照物溶液的制備 同“2.4.2”項下。
2.5.3 色譜條件建立 同“2.4.1”項下。
2.5.4 精密度試驗
取雪蓮培養物樣品,按“2.5.1”項下制備供試品溶液,按“2.5.3”項下色譜條件方法,連續進樣6次。以紫丁香苷峰為參照峰S,計算各共有峰的相對保留時間。結果各色譜峰相對保留時間RSD為0.31%~1.59%,表明精密度良好。
2.5.5 穩定性試驗
取雪蓮培養物樣品,按“2.5.1”項下制備供試品溶液,按“2.5.3”項下色譜條件方法,連續進樣6次。以紫丁香苷峰為參照峰S,計算各共有峰的相對保留時間。結果各色譜峰相對保留時間RSD為0.16%~1.21%,表明穩定性良好。
2.5.6 重復性試驗
取雪蓮培養物樣品,平行6份,按“2.5.1”項下制備供試品溶液,按“2.5.3”項下色譜條件方法,進樣測定。以紫丁香苷峰為參照峰S,計算各共有峰的相對保留時間。結果各色譜峰相對保留時間RSD為0.18%~1.55%,表明重復性良好。
2.5.7 對照特征圖譜的建立
取15批雪蓮培養物,按“2.5.1”項下制備供試品溶液,按“2.5.3”項下色譜條件方法進樣檢測。采用2012版《中藥色譜指紋圖譜相似度評價系統》軟件對15批雪蓮細胞培養物色譜峰進行校正,以中位數法生成對照特征圖譜(R),確立10個共有特征峰。見圖2。與對照品比對,指認其中峰2為綠原酸、峰4為紫丁香苷、峰7為1,5-二咖啡酰奎尼酸。見圖3。15批次雪蓮培養物與對照特征圖譜的相似度均大于0.9,表明各批次的雪蓮培養物質量一致性較好。見表4。
3 討論
天山雪蓮是典型的珍稀瀕危藥用植物,市場上價格高、需求量大,植物細胞培養是解決供需矛盾的有效途徑[12]。20世紀90年代開始,就出現雪蓮組織培養的相關報道[13-14]。以野生天山雪蓮種子萌發后的無菌苗葉片為原料,在培養基進行誘導產生愈傷組織,經繼代培養產生穩定的天山雪蓮細胞系,篩選高產細胞系,在特定條件下培養,即可獲得雪蓮細胞培養物。在不同培養條件下,天山雪蓮愈傷組織的形態及次生代謝產物存在明顯差異,其中,以在MS培養基上誘導產生的紫紅色團粒狀的愈傷組織生長旺盛,且總黃酮類成分含量高[15-16]。
2010年,原衛生部批準雪蓮培養物為植物類新資源食品,對其性狀(鮮品:紫紅色團塊顆粒;干品:紫灰色粉末)、蛋白質含量(鮮品:≥1%;干品:≥7%)、總黃酮含量(鮮品≥0.4%;干品:≥7%)均做要求,可應用于生產保健食品[17]。但至今尚未有雪蓮培養物的藥用標準。雪蓮細胞培養物中除與原植物藥材相似富含以蘆丁為主的黃酮類成分,其綠原酸、紫丁香苷和1,5-二咖啡酰奎尼酸的含量也很高[18-19],可達到培養物干重的0.862%、3.20%、0.335%,遠高于原植物藥材。綠原酸具有抗炎、抗高血糖和抗乙型肝炎病毒的作用,是眾多藥材抗菌解毒、消炎利膽的主要成分[20];紫丁香苷具有抗炎鎮痛、抗高血糖、抗抑郁、抗腫瘤活性,在《中華人民共和國藥典》中是天山雪蓮、刺五加等藥材及相關制劑的定性和定量指標[21];1,5-二咖啡酰奎尼酸具有良好的抗氧化、治療糖尿病和抗艾滋病的作用[22]。與原植物藥材相比,雪蓮細胞培養物具有更強的抗氧化和抗病毒活性。故本研究選擇總黃酮成分及綠原酸、1,5-二咖啡酰奎尼酸和紫丁香苷成分含量為定量指標,對天山雪蓮培養物進行質量研究。
本研究以15批次天山雪蓮細胞培養物為研究對象,測定指標成分總黃酮類及綠原酸、1,5-二咖啡酰奎尼酸和紫丁香苷成分的含量,建立相應的含量測定方法及特征指紋圖譜,且方法學考察符合要求,可全面反映雪蓮細胞培養物化學組分信息,為雪蓮細胞培養物的質控和評價提供參考。
參考文獻
[1]中國科學院中國植物志編輯委員會.中國植物志[M].北京:科學出版社,2002:35.
[2]國家藥典委員會.中華人民共和國藥典(一部)[M].北京:中國醫藥科技出版社,2020:55-56.
[3]尹輝.雪蓮化學成分、藥理活性及臨床應用研究[J].齊齊哈爾醫學院學報,2013,34(7):1010-1012.
[4]荊甜蕊,徐思雅,倪亦飛,等.天山雪蓮生物技術研究進展[J].基因組學與應用生物學,2016,35(8):2201-2210.
[5]劉曉鵬,王鋒,趙黎明,等.藥用植物組織培養研究進展[J].湖北民族學院學報:自然科學版,2019,37(1):13-18.
[6]賈麗華,郭雄飛,賈曉光,等.天山雪蓮的開發與應用[J].新疆中醫藥,2016,34(1):126-128.
[7]鄒曉偉.雪蓮細胞培養物成分及新型循環色譜的研究[D].大連:大連理工大學,2014.
[8]劉雅萍.雪蓮培養物的抗輻射抗疲勞抗氧化功能評價[D].大連:大連理工大學,2012.
[9]廉翠翠,查圣華,王俊亮,等.雪蓮培養物保健食品的抗氧化功能研究[J].食品研究與開發,2020,41(13):43-49.
[10]楊夢楠,趙曉枚.雪蓮培養物紅景天膠囊的保健功效綜述[J].科技資訊,2018,16(27):224-226.
[11]付婉藝,李厚華,李玲,等.天山雪蓮懸浮培養細胞總黃酮提取純化工藝研究[J].西北農林科技大學學報:自然科學版,2013,41(8):175-181.
[12]王娟,李金鑫,李建麗,等.植物組織培養技術在中藥資源中的應用[J].中國中藥雜志,2017,42(12):2236-2246.
[13]趙德修,喬傳令,汪沂.水母雪蓮的細胞培養和高產黃酮細胞系的篩選[J].植物學報,1998,16(6):3-5.
[14]趙德修,趙敬芳.水母雪蓮的細胞培養[J].應用基礎與工程科學學報,1997,5(4):363-368.
[15]賈景明,吳春福,吳立軍,等.天山雪蓮愈傷組織培養與次生代謝物形成的研究[J].中藥研究與信息,2005,7(7):11-15.
[16]丁黛靈,陳蕓,魏炯河,等.天山雪蓮組織培養體系的優化[J].甘肅農業科技,2019,57(6):25-29.
[17]中華人民共和國衛生部公告2010年第9號[J].中國食品衛生雜志,2010,22(4):380.
[18]李燕,郭順星,王春蘭,等.天山雪蓮細胞培養物與原藥材中紫丁香苷含量的比較[J].中國藥學雜志,2008,43(10):737-739.
[19]陳日道,劉曉,鄒建華,等.天山雪蓮懸浮培養細胞中紫丁香苷、綠原酸和1,5-二咖啡酰奎尼酸的生物合成調控[J].中國中藥雜志,2014,39(12):2275-2280.
[20]嚴永旺,肖蘭,周旭,等.綠原酸的藥理作用及藥用研發對策[J].中國藥房,2017,28(19):2729-2732.
[21]汪琢,姜守剛,祖元剛,等.刺五加中紫丁香苷的提取分離及抗腫瘤作用研究[J].時珍國醫國藥,2010,21(3):752-753.
[22]趙昱,趙軍,李湘萍,等.咖啡酰奎尼酸類化合物研究進展[J].中國中藥雜志,2006,31(11):869-874.
(2021-03-05收稿 責任編輯:徐穎)

