結(jié)直腸癌中VASP表達(dá)及與轉(zhuǎn)移關(guān)系研究
黨運(yùn)芝 于嬌 趙淑紅 金龍 任曉躍 王青
結(jié)直腸癌(colorectal cancer,CRC)是消化道最常見的惡性腫瘤之一,在全球范圍內(nèi)發(fā)病率位列第三,死亡率位列第三[1]。手術(shù)切除是CRC最有效的治療方式,但是復(fù)發(fā)和轉(zhuǎn)移仍是手術(shù)治療失敗的主要原因[2]。另外,約20%的結(jié)直腸癌患者在診斷時(shí)已出現(xiàn)了轉(zhuǎn)移[3]。盡管近年來CRC治療方法取得了顯著進(jìn)步,但轉(zhuǎn)移性CRC可選擇的有效治療方式仍較少[4-5],目前關(guān)于CRC轉(zhuǎn)移的機(jī)制仍不清楚,亟待進(jìn)一步研究。VASP是Ena/VASP家族的一個(gè)重要成員,可調(diào)節(jié)actin細(xì)胞骨架運(yùn)動(dòng)及細(xì)胞遷移[6-8]。過表達(dá)的VASP可促進(jìn)多種腫瘤的侵襲和遷移,且與差的預(yù)后呈正相關(guān)[9-11]。但關(guān)于VASP在結(jié)直腸癌中的表達(dá)和功能報(bào)道較少。本研究檢測(cè)了VASP表達(dá),并分析了VASP表達(dá)量與結(jié)直腸癌預(yù)后的關(guān)系。通過體外細(xì)胞實(shí)驗(yàn)及裸鼠體內(nèi)實(shí)驗(yàn)探索了VASP在CRC轉(zhuǎn)移中的作用。
材料與方法
一、細(xì)胞系和人組織標(biāo)本
人結(jié)腸永生化細(xì)胞CRL1 790,人結(jié)直腸癌細(xì)胞系SW480、S1226、DLD-1、RKO、Caco-2、SW620、LoVo、SW48、T84和Colo201引自美國(guó)模式菌種細(xì)胞庫(kù)(ATCC),由陜西省人民醫(yī)院實(shí)驗(yàn)室組織細(xì)胞庫(kù)保存。
二、熒光定量PCR
用Takara試劑盒提取新鮮組織的RNA,用Takara試劑盒逆轉(zhuǎn)錄成cDNA,后行熒光定量PCR。反應(yīng)程序如下:95°C,15s;55-60 °C,15s;72°C,15 s共45個(gè)循環(huán)。用如下公式計(jì)算樣本的表達(dá)量:2–ΔΔCt(ΔΔCt=ΔCtTumor– ΔCtNontumor)。
VASP的引物序列如下:
正向:5'-ATGGCAACAAGCGATGGCT-3'
反向:5'-CGATGGCACAGTTGATGACCA-3'
三、免疫組化
結(jié)腸癌及癌旁組織芯片,65℃烤片3~4 h,常規(guī)脫蠟水化,檸檬酸鈉(pH=6.0)高壓修復(fù)2 min,冷卻至室溫后于3%H2O2封閉15 min。加入VASP(abcam,ab229624)一抗,4℃孵育過夜。第二天PBS漂洗3次×5 min后,滴加二抗,室溫孵育30 min。PBS漂洗3次×5 min后,滴加辣根過氧化物酶,室溫孵育30 min。PBS漂洗3次×5 min,DAB顯色,脫水透明,中性樹脂封片。
免疫組化評(píng)分由兩位病理科醫(yī)生獨(dú)立完成,免疫染色強(qiáng)度分為0~3分:0(陰性),1(弱陽(yáng)性),2(中度陽(yáng)性),3(強(qiáng)陽(yáng)性)。細(xì)胞陽(yáng)性率分5個(gè)級(jí)別:0(陰性),1(1%~25%),2(26%~50%),3(51%~75%),4(76%~100%)。最終得分為免疫染色強(qiáng)度與細(xì)胞陽(yáng)性率的乘積。其中0~3為陰性,4~12分為陽(yáng)性。
四、蛋白免疫印跡
用中等強(qiáng)度的細(xì)胞裂解液(含蛋白酶及磷酸酶抑制劑)提取細(xì)胞蛋白,用SDS-PAGE凝膠電泳1.5~2.0 h,轉(zhuǎn)至PVDF膜上(恒壓25 V,30 min),10%牛奶室溫封閉1 h。一抗VASP(abcam,b229624)孵育,4℃過夜。第二天,TBST漂洗5 min×3次,二抗室溫孵育30 min。采用Bio-Rad公司的ChemiDocXRS凝膠成像儀成像。
五、Transwell侵襲和遷移實(shí)驗(yàn)
選用corning公司24孔小室(直徑為8 μm)。在遷移實(shí)驗(yàn)中,5×105細(xì)胞種植在無血清的上室內(nèi);在侵襲實(shí)驗(yàn)中,5×105細(xì)胞被種植在無血清且基質(zhì)膠包被的上室,下室均加入600 μL含20%血清的培養(yǎng)基。24~48 h后分別取出小室,用4%多聚甲醛固定10 min,7%的結(jié)晶紫染色10 min,倒置顯微鏡拍照,分析細(xì)胞侵襲和轉(zhuǎn)移的數(shù)目。
六、裸鼠尾靜脈肺轉(zhuǎn)移實(shí)驗(yàn)
BALB/C裸鼠,雄性,4~6周齡,購(gòu)自北京維通利華公司,飼養(yǎng)在SPF級(jí)別動(dòng)物房中。將相應(yīng)細(xì)胞培養(yǎng)至對(duì)數(shù)期,收取細(xì)胞并計(jì)數(shù)。將裸鼠隨機(jī)分組(n=10),每只裸鼠尾靜脈注射200 μL細(xì)胞懸液(約5×105個(gè)細(xì)胞),后每周行活體成像,9周后處死全部小鼠。
七、數(shù)據(jù)分析
采用SPSS 20.0進(jìn)行數(shù)據(jù)統(tǒng)計(jì)分析,數(shù)值均記為平均值±標(biāo)準(zhǔn)差(SD)。數(shù)值變量采用Student t檢驗(yàn),分類變量采用卡方(χ2)檢驗(yàn),P<0.05時(shí)認(rèn)為差異有統(tǒng)計(jì)學(xué)意義。
結(jié) 果
一、VASP高表達(dá)與結(jié)直腸癌較差的預(yù)后相關(guān)
我們首先用實(shí)時(shí)定量PCR方法檢測(cè)了VASP在20例正常腸上皮組織及110例配對(duì)的癌旁及CRC組織中的表達(dá)水平,發(fā)現(xiàn)VASP的表達(dá)水平在CRC組織中較癌旁及正常組織明顯升高。進(jìn)一步分析發(fā)現(xiàn)VASP的表達(dá)水平在復(fù)發(fā)CRC(n=59)的表達(dá)較沒有復(fù)發(fā)的CRC(n=51)升高更為顯著。在轉(zhuǎn)移的CRC(n=53)較無轉(zhuǎn)移CRC(n=45)的升高更為顯著(圖1A)。在20對(duì)配對(duì)的標(biāo)本中,VASP在轉(zhuǎn)移性CRC中的表達(dá)明顯高于原發(fā)性CRC(圖1A~1B)我們進(jìn)一步用免疫組化方法分析了VASP在222對(duì)配對(duì)CRC組織與癌旁組織中的表達(dá)。我們選取了222例均接受手術(shù)切除的結(jié)直腸癌患者,其中130例患者只接受了手術(shù)治療;60例患者接受了手術(shù)+化療;32例患者接受了手術(shù)+放療+化療。發(fā)現(xiàn)VASP主要為胞質(zhì)著色,且VASP在CRC中的表達(dá)明顯高于癌旁(圖1C)。VAS與腫瘤大小、腫瘤分化、神經(jīng)侵犯、淋巴結(jié)轉(zhuǎn)移、遠(yuǎn)處轉(zhuǎn)移、AJCC分期呈正相關(guān)(表1)。COX多因素分析表明VASP的表達(dá)是結(jié)直腸癌患者復(fù)發(fā)及死亡的獨(dú)立預(yù)測(cè)因素之一(表2)。而生存分析發(fā)現(xiàn),過表達(dá)的VASP與短的總體生存(χ2=62.4,P<0.001)及高的復(fù)發(fā)率呈正相關(guān)(χ2=66.9,P<0.001)(圖1D)。
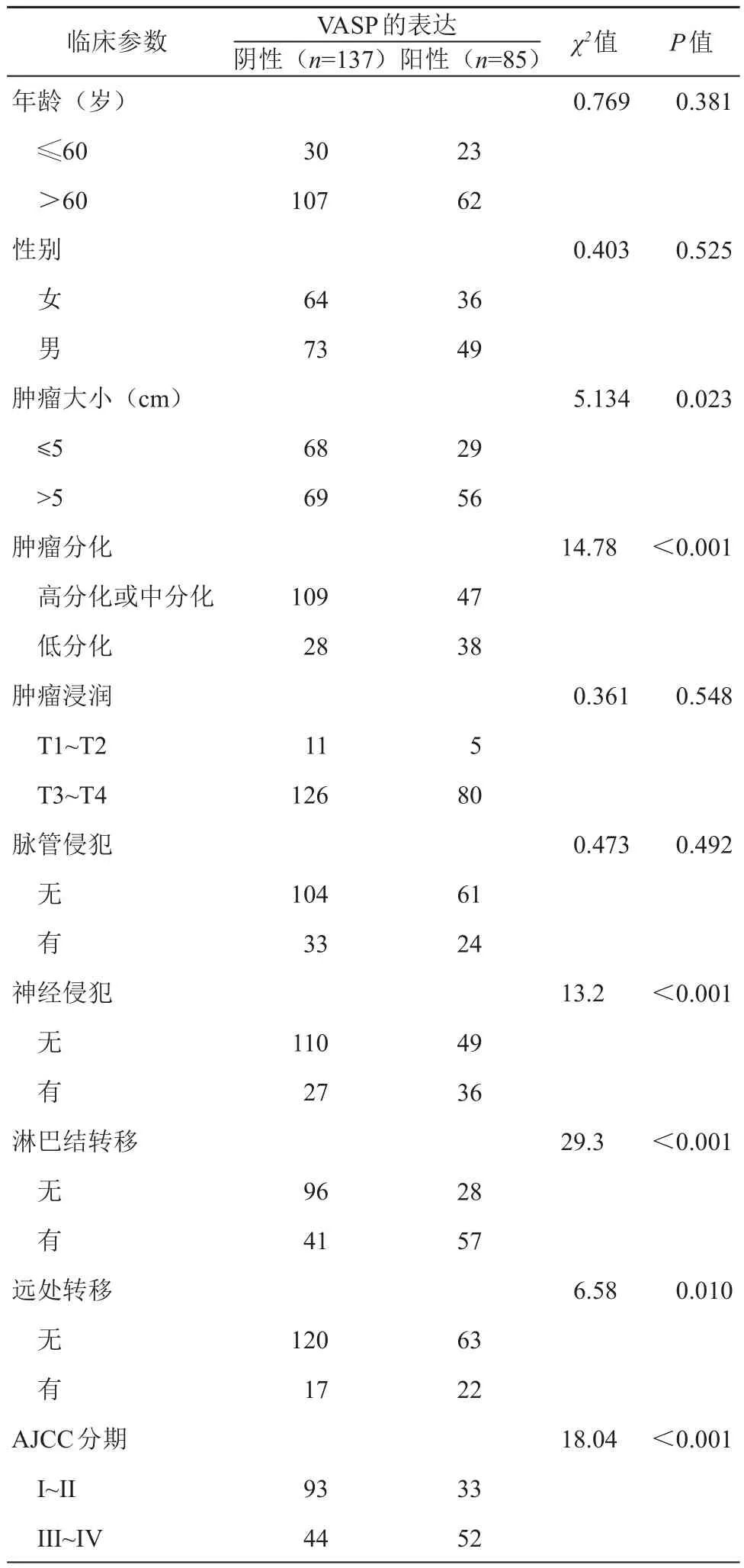
表1 結(jié)直腸患者中VASP的表達(dá)與臨床參數(shù)的相關(guān)性
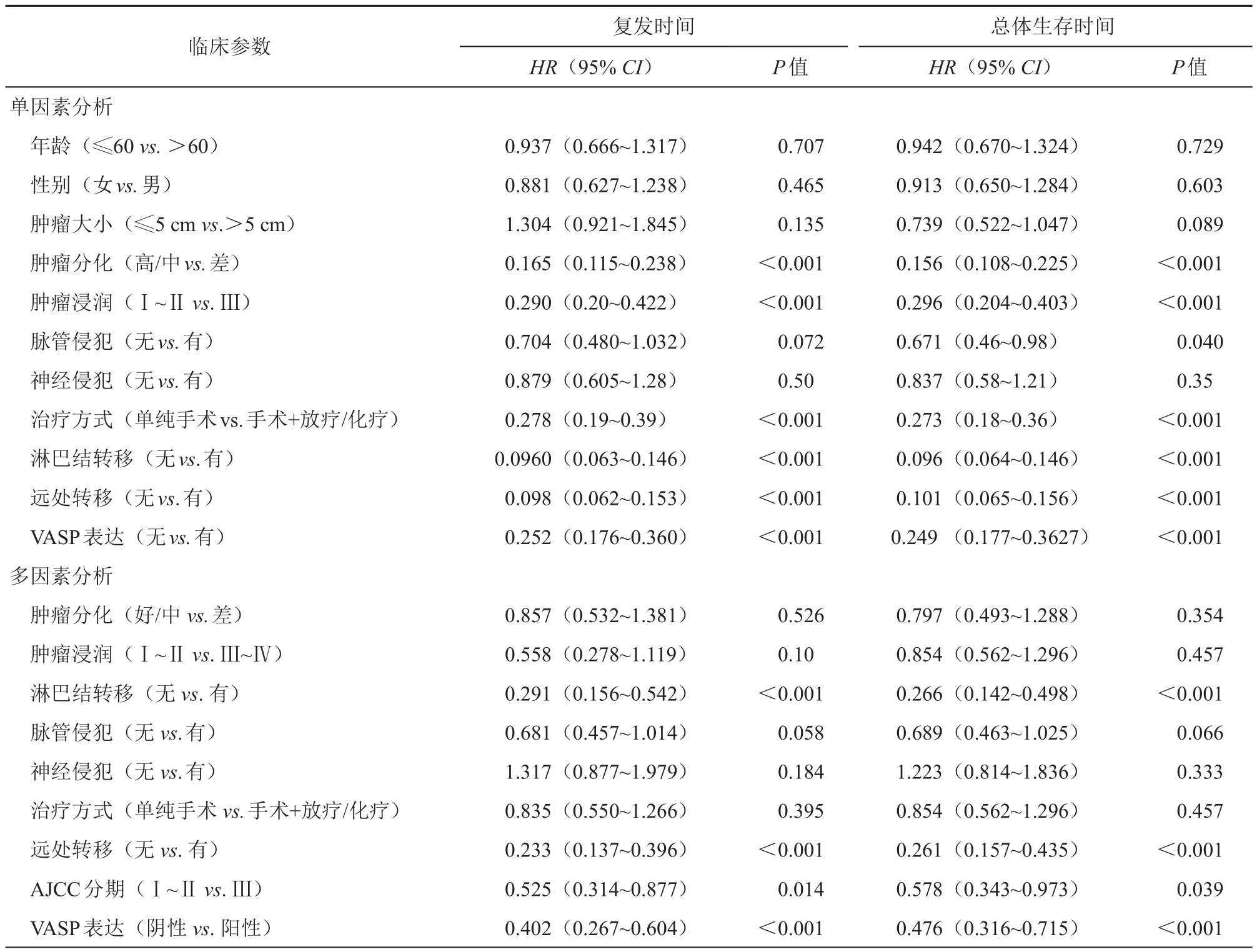
表2 VASP的表達(dá)是結(jié)直腸癌患者復(fù)發(fā)及死亡的獨(dú)立預(yù)測(cè)因素

圖1 VASP在結(jié)直腸癌中的表達(dá)。1A:實(shí)時(shí)定量PCR方法分析正常腸上皮組織、癌旁及CRC組織中VASP mRNA的表達(dá)水平;復(fù)發(fā)與未復(fù)發(fā)CRC患者VASP mRNA的表達(dá);轉(zhuǎn)移與未轉(zhuǎn)移CRC患者VASP mRNA的表達(dá);20對(duì)配對(duì)的正常腸上皮組織、原發(fā)CRC及轉(zhuǎn)移CRC中VASP mRNA的表達(dá)。1B:IHC檢測(cè)VASP在20例配對(duì)的癌旁,原發(fā)性CRC及遠(yuǎn)處轉(zhuǎn)移CRC的表達(dá)情況。1C:IHC染色分析VASP在癌旁及CRC的蛋白表達(dá)情況及IHC評(píng)分情況。1D:Kaplan-Meier方法分析VASP的表達(dá)與復(fù)發(fā)及生存的關(guān)系。低倍鏡圖中bar值代表250 μm,高倍鏡圖中bar值為50 μm。*P<0.05
二、VASP過表達(dá)促進(jìn)CRC細(xì)胞的侵襲和遷移
為進(jìn)一步研究VASP在CRC中的功能,我們首先檢測(cè)了正常腸上皮、結(jié)腸永生化細(xì)胞及10種CRC細(xì)胞系中VASP的表達(dá),發(fā)現(xiàn)SW620細(xì)胞中VASP的表達(dá)最低,而SW480細(xì)胞中VASP的表達(dá)最高(圖2A)。因此,我們用慢病毒感染的方法建立兩個(gè)穩(wěn)定的細(xì)胞株:SW480-VASP和SW620-shVASP(圖2B)。體外細(xì)胞實(shí)驗(yàn)發(fā)現(xiàn),與對(duì)照組細(xì)胞相比,上調(diào)VASP表達(dá)可促進(jìn)SW480細(xì)胞侵襲和遷移能力,而下調(diào)VASP的表達(dá)可以抑制SW620細(xì)胞的侵襲和遷移(圖2C)。

圖2 VASP可促進(jìn)結(jié)直腸癌細(xì)胞的侵襲和遷移。2A:VASP在正常腸上皮、結(jié)腸永生化細(xì)胞及10種CRC細(xì)胞系中的表達(dá);2B:慢病毒轉(zhuǎn)染后VASP在相應(yīng)細(xì)胞中的表達(dá);2C:Transwell實(shí)驗(yàn)分析SW480-VASP,SW620-shVASP與相應(yīng)對(duì)照組細(xì)胞的侵襲和遷移能力
三、裸鼠體內(nèi)實(shí)驗(yàn)VASP過表達(dá)可促進(jìn)CRC細(xì)胞系的肺轉(zhuǎn)移
為進(jìn)一步研究VASP在CRC中的功能,我們將SW480-VASP及SW620-shVASP細(xì)胞及其相應(yīng)對(duì)照組細(xì)胞分別注射到小鼠的尾靜脈,并每周成像一次。生物活體成像發(fā)現(xiàn)VASP過表達(dá)可增加SW480細(xì)胞的信號(hào)強(qiáng)度,而下調(diào)VASP的表達(dá)可降低SW620細(xì)胞的信號(hào)強(qiáng)度(圖3A~3B)。HE染色發(fā)現(xiàn)VASP過表達(dá)可以增加SW480細(xì)胞肺臟轉(zhuǎn)移的發(fā)生率及轉(zhuǎn)移灶數(shù)目,而下調(diào)VASP的表達(dá)則可以降低SW620細(xì)胞肺臟轉(zhuǎn)移的發(fā)生率及轉(zhuǎn)移灶數(shù)目(圖3C~3E)。而生存分析發(fā)現(xiàn)VASP過表達(dá)可以降低小鼠總體生存時(shí)間,而下調(diào)VASP的表達(dá)則可以延長(zhǎng)小鼠總體生存時(shí)間(圖3F)。
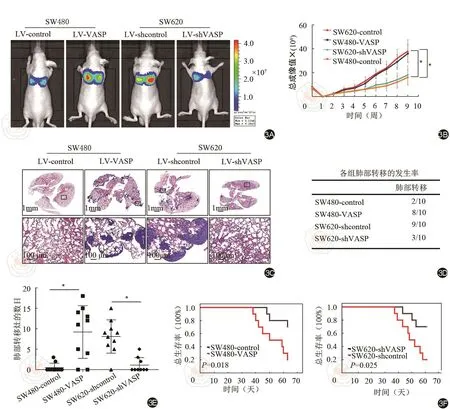
圖3 VASP可促進(jìn)結(jié)直腸癌細(xì)胞的肺轉(zhuǎn)移。3A:生物發(fā)光成像顯示各組裸鼠體內(nèi)轉(zhuǎn)移情況;3B:各組裸鼠尾靜脈注射后0~9周活體成像的信號(hào)值;3C:各組裸鼠肺部代表性的HE圖像;3D:各組裸鼠肺轉(zhuǎn)移發(fā)生率;3E:各組裸鼠肺臟轉(zhuǎn)移灶的數(shù)目;3F:各組裸鼠的總體生存。*P<0.05
討 論
Ena/VASP蛋白是一個(gè)保守的actin調(diào)節(jié)蛋白家族,由EVH1、EVH2和一個(gè)富含脯氨酸蛋白的區(qū)域組成。近年來的研究表明,VASP在多種腫瘤中亦具有重要作用。在肝細(xì)胞癌中,VASP的表達(dá)水平明顯升高,與門靜脈癌栓形成及不良預(yù)后呈正相關(guān)[12]。肝臟是結(jié)腸癌最常見的轉(zhuǎn)移器官,在小鼠肝臟轉(zhuǎn)移模型及腫瘤患者中,結(jié)腸癌細(xì)胞到達(dá)肝竇并上調(diào)肝臟星形細(xì)胞的VASP表達(dá),VASP促進(jìn)肝臟星形細(xì)胞向腫瘤相關(guān)肌成纖維細(xì)胞轉(zhuǎn)化[9]。乳腺癌中,Wnt/β-catenin信號(hào)通路與VASP形成正反饋環(huán)路,促進(jìn)乳腺癌細(xì)胞增殖和轉(zhuǎn)移[13]。在我們前期研究中發(fā)現(xiàn),VASP在肝細(xì)胞癌中表達(dá)明顯升高,轉(zhuǎn)錄因子HOXC10通過上調(diào)VASP的表達(dá)促進(jìn)肝細(xì)胞癌的轉(zhuǎn)移[14]。而食管癌中,VASP的239位點(diǎn)磷酸化則可抑制腫瘤的侵襲和遷移[15]。
臨床病理學(xué)特征在預(yù)測(cè)結(jié)直腸癌預(yù)后,選擇合理治療方案上具有重要作用[16]。但目前關(guān)于VASP在結(jié)直腸癌中表達(dá)報(bào)道還較少,且結(jié)論相互矛盾。在既往的文獻(xiàn)中[17]發(fā)現(xiàn)VASP的過表達(dá)及磷酸化與CRC疾病的復(fù)發(fā)呈正相關(guān)。另外,在60例結(jié)腸癌中VASP的過表達(dá)與不良預(yù)后呈正相關(guān)[18]。但另一篇只有20例CRC的研究中則發(fā)現(xiàn)VASP及兩種磷酸化VASP的表達(dá)水平在癌組織顯著低于癌旁組織[19]。本研究通過實(shí)時(shí)定量PCR及免疫組化染
色的方法發(fā)現(xiàn)VASP在CRC中的表達(dá)較癌旁明顯升高。VASP與AJCC分期及淋巴結(jié)轉(zhuǎn)移呈正相關(guān),是CRC患者復(fù)發(fā)及死亡的獨(dú)立預(yù)測(cè)因素之一。另外,在20例配對(duì)的樣本中,我們發(fā)現(xiàn)VASP在轉(zhuǎn)移性CRC組織中的表達(dá)顯著高于原發(fā)CRC組織中的表達(dá),基于此我們對(duì)VASP在CRC轉(zhuǎn)移中的作用進(jìn)行了進(jìn)一步探索。首先體外細(xì)胞Transwell實(shí)驗(yàn)發(fā)現(xiàn)上調(diào)VASP的表達(dá)可促進(jìn)CRC細(xì)胞的侵襲和遷移,而下調(diào)VASP的表達(dá)則可以抑制CRC細(xì)胞的侵襲和遷移。體內(nèi)的裸鼠尾靜脈實(shí)驗(yàn)中,過表達(dá)的VASP可以促進(jìn)CRC細(xì)胞的侵襲和轉(zhuǎn)移,是促進(jìn)CRC進(jìn)展的重要分子。
綜上,本研究發(fā)現(xiàn)VASP在CRC中表達(dá)升高與差的預(yù)后呈正相關(guān)。體內(nèi)外實(shí)驗(yàn)表明VASP可促進(jìn)CRC的侵襲和轉(zhuǎn)移。本研究明確了VASP在CRC中的表達(dá)和功能,為臨床治療CRC轉(zhuǎn)移提供潛在的靶點(diǎn),但VASP促進(jìn)CRC轉(zhuǎn)移的機(jī)制仍需進(jìn)一步的研究。
- 中華結(jié)直腸疾病電子雜志的其它文章
- 直腸癌術(shù)后肛門功能康復(fù)的研究進(jìn)展
- 第六屆中國(guó)醫(yī)師協(xié)會(huì)結(jié)直腸腫瘤專業(yè)委員會(huì)年會(huì)暨國(guó)家癌癥中心結(jié)直腸癌國(guó)際高峰論壇、第五屆國(guó)際NOSES學(xué)術(shù)云會(huì)議、第十一屆中國(guó)中青年結(jié)直腸腫瘤專家論壇
- 結(jié)直腸癌類器官生物樣本庫(kù)的建立和應(yīng)用研究進(jìn)展
- 中國(guó)闌尾腫瘤多學(xué)科綜合治療專家共識(shí)(2021版)
- 2013年~2017年黑龍江省腫瘤登記地區(qū)結(jié)直腸癌發(fā)病趨勢(shì)與死亡分析
- 聯(lián)合無痛胃腸鏡檢查患者的腸道準(zhǔn)備策略

