SARS CoV-2特征和可能對泌尿及男性生殖系統侵害的研究進展
李天杰,崔慶鵬,劉浩林,雷 銀,吳汶釗,陶搏宇,劉孝東
2019冠狀病毒病(coronavirus disease 2019, COVID-19)[1],由新型冠狀病毒 (SARS CoV-2)引起。該疾病的部分危重患者可出現蛋白尿、腎功能不全等表現。本文對SARS CoV-2結構、生物學特點及其可能侵襲泌尿及男性生殖系統進行分析綜述。
1 病毒特性及可能在體內播散路徑
SARS CoV-2屬于β屬冠狀病毒,有包膜,顆粒呈圓形或橢圓形,常為多形性,直徑60~140 nm[2]。經測序顯示,該病毒與SARS-CoV的基因序列相似性為75.0%~80.0%[3-5]。研究表明,SARS CoV-2通過結合人體內血管緊張素轉化酶2(angiotensin converting enzyme 2,ACE2)進入靶細胞,ACE2很可能是SARS CoV-2感染的重要受體[6-8]。
SARS CoV-2從呼吸道進入肺部引起肺部感染后,全身其他器官系統相關表現及具體致病機制尚未闡明。病毒若進入血液,繼而隨著血液循環播散至消化系統、泌尿系統等全身其他系統可引發相關病變。早期研究表明SARS-CoV可進入血液中,感染循環免疫細胞,后者再將病毒攜帶至其他器官系統中[9]。現研究也顯示,在SARS CoV-2感染患者血液、尿液和糞便中檢測到病毒[10-13]。SARS CoV-2極有可能類似SARS-CoV的途徑:飛沫傳播-呼吸系統-血液和循環免疫系統-播散至泌尿系統及男性生殖系統。
2 ACE2在泌尿和男性生殖系統中表達及作用
在人類蛋白質表達圖譜(The human protein atlas,HPA) 數據庫中對正常人體組織ACE2 mRNA和蛋白表達進行分析,結果顯示,ACE2 mRNA和蛋白均在小腸、十二指腸等消化道器官中表達最多。ACE2 mRNA在泌尿生殖系統中表達前五位依次為:腎臟、睪丸、附睪、輸精管、精囊腺,肺臟位于其后(見圖1);ACE2 蛋白在泌尿生殖系統中的表達依次為:腎臟、睪丸、腎上腺、精囊腺,肺臟位于其后(見圖2)。其中腎臟和睪丸中ACE2 mRNA和蛋白質水平均位于人體所有組織中表達前五位。肺臟組織中ACE2水平遠低于部分消化系器官,以及腎臟和睪丸等部分泌尿生殖器官。

圖1 HPA數據庫人體組織中ACE2 mRNA表達
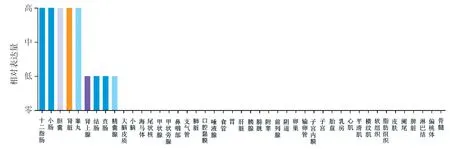
圖2 HPA數據庫人體組織中ACE2蛋白表達
Donoghue等[14]研究顯示:ACE2蛋白在腎臟血管內皮細胞和腎小管上皮細胞及中等大小血管的平滑肌細胞中表達,且具有調節腎血流分布及水、電解質平衡的功能。研究發現,ACE2表達于人睪丸的間質細胞和支持細胞,認為ACE2是成熟睪丸間質細胞的產物,不受激素調節,以未知的機制參與對睪丸功能的控制[15]。盡管ACE2蛋白在腎上腺中同樣高表達,但其生理作用及具體機制尚不明確。可見ACE2在腎臟和睪丸中高表達對維持腎功能穩定,調控腎素-血管緊張素-醛固酮系統平衡至關重要,在男性生殖系統中也發揮著重要作用。
3 SARS-CoV和SRAS CoV-2侵害泌尿及生殖系統
在早期關于SARS-CoV感染與人體腎臟、腎上腺、睪丸相關研究中,Gu等[9]對SARS患者進行尸體解剖,在確診患者遠端腎小管上皮細胞中檢測到SARS-CoV病毒顆粒簇,并且8例確診SARS男性患者中7例睪丸顯示發生局灶性萎縮,在遠端腎小管中發現SARS-CoV感染,表明腎小管上皮細胞容易感染SARS-CoV,也為在尿液中病毒檢出提供了解釋。趙景民等[16]和Ding等[17]也分別通過病理解剖證實腎上腺實質細胞中存在SARSCoV,腎上腺表現為局限性出血壞死性炎[18]。Xu等[19]則通過6例確診SARS-CoV感染死亡患者睪丸病理變化研究,所有患者睪丸均顯示出廣泛的生殖細胞破壞,生精小管中幾乎沒有精子,基底膜增厚和白細胞浸潤。SARS患者睪丸可能受到損傷,猜測睪丸炎是SARS并發癥,從而影響生精。既往病毒性睪丸炎的研究表明,人類免疫缺陷病毒、乙肝病毒、腮腺炎病毒可能會進入睪丸細胞引起睪丸炎,病毒引起的睪丸組織損傷可能會引起男性不育和腫瘤[20]。然而,同時存在相反的研究結果和觀點,Ding等[21]研究表明,盡管ACE2在睪丸組織中表達水平很高,但睪丸細胞不能被SARS-CoV感染。Song等[22]也認為睪丸炎主要與患者持續的高燒和SARS-CoV引起的自身免疫反應相關,因此無法確定SARS-CoV是否會直接攻擊睪丸引起睪丸炎。進行相關文獻搜索,尚未發現SARS-CoV感染精囊腺等其他泌尿生殖系器官的報道及研究。
雖然現暫無證據直接明確SARS CoV-2直接感染攻擊腎臟、腎上腺、睪丸等泌尿和男性生殖器官,但最近Fan等[23]研究認為,SARS CoV-2有引起潛在睪丸損傷可能,其通過研究發現ACE2在腎小管細胞、睪丸間質細胞、睪丸生精管細胞中高表達,且睪丸炎可能是SARS CoV-2感染的晚期并發癥。Wang等[24]的研究同樣表明,ACE2除了主要富集在生殖系統睪丸間質細胞和睪丸支持細胞中,還富集在精原細胞中,而ACE2表達陽性的精原細胞占人所有精原細胞的1.28%,還發現用于病毒啟動的絲氨酸蛋白酶TMPRSS2表達集中在精原細胞和精子細胞中,人睪丸中SARS CoV-2感染的可能性很高,病毒可能直接靶向感染ACE2陽性精原細胞并破壞精子生成。人腎臟和睪丸可能是SARS CoV-2感染的潛在靶標,從而影響血壓、電解質、腎功能等腎素-血管緊張素-醛固酮系統相關指標,以及影響男性患者生殖功能,甚至引發腫瘤、腎功能衰竭等惡性后果。
以上研究為SARS CoV-2感染泌尿及男性生殖器官提供了理論依據,也證明了泌尿及男性生殖系統可能成為SARS CoV-2感染的理論傳播途徑。現已報告發現從患者糞便、尿液和血液中檢出并分離出病毒[10-13],且現有SARS CoV-2感染患者病理解剖發現腎上腺局灶性壞死[2]。雖然無法明確腎上腺的病理表現是否為病毒感染相關的損害表現,仍需警惕SARS CoV-2感染腎上腺,引起腎上腺皮質和髓質激素不足,甚至引起腎上腺危象等危急情況和不良后果。最近首次有報道顯示在患者精液中檢測到SARS CoV-2,通過檢測38例證實為SARS CoV-2感染患者的精液標本,最終4例急性期和2例康復期患者精液標本中SARS CoV-2陽性[25]。其認為當血睪屏障功能障礙特別是存在全身性炎性反應時,SARS CoV-2便有可能傳播到男性生殖道中,即使SARS CoV-2不能在男性生殖道中復制擴增,也可能長期持續存在于男性生殖道中。之前的研究也認為在病毒大量入血情況下,血睪屏障并不能完全阻隔病毒,病毒可能進入到男性生殖道中[26]。另一項研究則為SARS CoV-2感染男性生殖系統提供了間接的證據,其通過比對COVID-19患者和健康男性的激素水平,發現血清促黃體生成素水平顯著升高,而睪丸激素和促黃體生成素的比例顯著降低,認為在性腺功能受損減退早期,睪丸激素生產受損會刺激促黃體生成素的釋放增多,短暫地維持睪丸激素在正常水平[27]。
然而另一些相反的研究結果和觀點則顯示,在COVID-19急性期和康復期患者精液和睪丸中都未檢測到SARS CoV-2,認為SARS CoV-2可能不會直接感染睪丸和男性生殖道,病毒通過精液和性行為傳播的可能性非常低[22,28-29]。從ACE2在泌尿和男性生殖系統器官及肺臟中表達中分析,盡管ACE2在泌尿和男性生殖系統器官中相對高表達,但此次SARS CoV-2感染患者中仍然以肺部表現為主。這可能與人體泌尿系統和生殖系統免疫保護有關,或者ACE2并非SARS CoV-2感染人體的唯一受體,又或者SARS CoV-2通過直接結合ACE2感染人體后發揮作用的途徑中存在其他影響因素。雖然現報道從患者尿液和精液中都檢測到SARS CoV-2,但是由于男性泌尿道和生殖道的重疊,若無法排除尿液和精液經過同一管道排泄的干擾,檢測到的SARS CoV-2并不能確切證明其來源。
現關于SARS CoV-2的致病機制尚未完全清楚,其侵害泌尿和男性生殖器官的相關研究仍然十分稀缺,現有部分小樣本量的單中心研究和實驗顯示出相反的結果,但缺乏大樣本量的權威多中心研究結果。總之從現有為數不多的研究證據來看,尚無可靠的證據直接明確或否定SARS CoV-2直接攻擊感染腎臟、腎上腺、睪丸等泌尿和男性生殖器官,但泌尿及男性生殖系統的多個器官中ACE2表達遠遠高于肺臟,據此必須關注SARS CoV-2可能對泌尿和男性生殖系統侵害及其侵襲路徑、病理機制,為疾病的預防及治療提供線索。

