化學發光免疫法在腫瘤生物標志物檢驗中的應用
王劭
(欽州市靈山縣人民醫院 檢驗科,廣西 欽州 535400)
0 引言
目前,人類已經探明的惡性腫瘤疾病已經超過100余種,此類疾病一般是指身體細胞發生突變后,會不受身體控制地不斷分裂、擴大、轉移,最終侵蝕機體健康細胞和組織,使患者在承受巨大痛苦后死亡。盡管現代醫學的發達程度正在逐漸提升,但對于很多中晚期惡性腫瘤疾病仍然無法根治,如人們熟知的肝癌、骨髓癌、肺癌等,發展至終末期后只能采取保守治療,盡量維持延長患者的生命。為了提高疾病診斷的準確率,檢驗過程旨在檢測腫瘤標生物標志物是否存在。腫瘤生物標志物是由腫瘤細胞直接產生或由肺腫瘤細胞經過腫瘤細胞誘導后產生的物質,對其進行檢測后,可對腫瘤是否存在、發病過程及預后作出判斷[1]。不同的檢測方式在檢測準確性方面也存在一定的差異。本研究旨在分析化學發光免疫法應用于腫瘤生物標志物檢驗時的效果,現對研究過程進行梳理。
1 資料與方法
1.1 一般資料。選取2019年1月至2021年2月在欽州市靈山縣人民醫院進行治療,經過病理檢測確診為原發性單一惡性腫瘤疾病的患者60例,將之納入觀察組;選取同期在本院接受體檢的健康人群60例納入觀察組。觀察組:①性別分布:男33例,女27例;②年齡34~68歲,平均(51.45±2.48)歲;③原發性腫瘤疾病分布:胃癌10例、肺癌7例、卵巢癌10例、肝癌5例、胰腺癌8例、乳腺癌5例、子宮肌瘤6例、其他9例。對照組:①性別分布:男32例,女28例;②年齡33~69歲,平均(51.52±2.54)歲。經比對兩組受檢人群的性別及年齡分布情況均差異無統計學意義(P>0.05),具有可比性。
納入標準:①經病理檢測,已經確診為原發性惡性腫瘤疾病的患者;②單一原發性惡性腫瘤疾病患者;③病情尚未發展至晚期的患者;④本次研究符合醫學倫理、患者知情同意。排除標準:①病情已發展至終末期,癌細胞已經發生遠端轉移,預計生存期不足3個月的患者;②病歷資料完善程度不符合本研究要求的患者。
1.2 研究方法簡析。抽取兩組人群的靜脈血,基于化學發光免疫檢測法進行腫瘤生物標志物檢驗,具體流程如下:
(1)采血前的準備工作:①由醫護人員與受檢者進行耐心、細致地溝通,針對受檢者提出的一切問題進行詳細解答,避免受檢者因緊張、恐懼等消極心緒而影響采血;②制定應急處理預案,主要針對受檢者在采血期間可能出現的暈針、暈血現象進行緊急處理。如受檢者發生眩暈情況時,如果穿刺針已經插入受檢者體內,則醫護人員應該立刻拔出針頭,對穿刺點位進行止血處理,幫助受檢者調整至平臥姿勢,通過吸入芳香酊、按壓人中穴位的方式,使其盡快蘇醒。此外,可叮囑受檢者準備一些牛奶、香蕉等食品(抽血室可準備一些葡萄糖溶液),當受檢者因靜脈采血后出現低血糖現象時可及時補充營養。
(2)采血流程。①要求受檢者檢測日前夜晚10時候禁食,檢測日清晨7時前往醫院,在空腹狀態下自手肘處抽取5 mL靜脈血;②將血液標本放入無抗凝劑的紅帽試管中,密封保存;③將受檢者血液標本送入檢驗室,通過全自動化學發光免疫分析儀對患者進行檢測;④本院選用的設備型號為深圳邁瑞生物醫療電子股份有限公司生產的CL-6000i免疫分析系統,采用微粒子酶促發光原理,分立一體模塊化設計。采用更穩定的增強型化學發光底物AMPPD,檢測靈敏度高達10~21 mol/L。此外,CL-6000i分析速度單模塊為480測試/小時,目前醫院配置兩個模塊組成CL-6000iM2流水線,雙模塊速度為960測試/小時,試劑位置為72個,試劑盤為圓盤式,溫度控制在2℃~8℃,采用托盤式裝載樣品架,可以同時裝載兩個托盤,每個托盤可以裝15個樣本架,每個樣本架可以裝10個樣本,可以一次上兩托盤樣本(300個標本),加上樣本處理系統緩沖位置290個樣本位,10個急診位置,這個檢測系統一次性可上600個樣本。可以同時裝載2瓶(每瓶500T)發光底物液。系統突出優勢為試劑、清洗液等消耗品,系統均可以在不停機狀況下添加;⑤樣本離心處理要求:離心轉速4000 r/min,持續時長為10~15 min,完全按照化學發光免疫法的操作步驟依次執行。
1.3 觀察指標界定。比對兩組受檢者的腫瘤生物標志物陽性檢出情況,具體指標為:①CA125,糖類抗原125;②CA153,糖類抗原153;③CA199,糖類抗原199④AFP,甲胎蛋白;⑤CEA,癌胚抗原。
評估檢測結果是否為陽性的一般標準為:①CA125含量超過35U/mL(參考范圍:0~35 U/mL);②CA199含量超過35 U/mL(參考范圍:0~30 U/mL);③CA153含量超過35 U/mL(參考范圍:0~15 U/mL);④AFP含量超過20 ng/mL(參考范圍:0~7 ng/mL);⑤CEA含量超過5 ng/mL(參考范圍:0~4.5 ng/mL)
1.4 統計學分析。本研究產生的所有數據均納入SPSS 23.0統計學軟件進行分析。其中,針對計量資料行“t”檢驗,所有結果均以“±s”的形式予以呈現;針對計數資料行“χ2”檢驗,相關結果以“n(%)”的形式呈現;當P<0.05時,表明組間差異具有統計學意義。
2 結果
觀察組原發性腫瘤疾病患者的CA125、CA199、CA153、AFP、CEA5項腫瘤生物標志物的陽性檢出率均顯著高于對照組健康受檢人群,差異具有統計學意義(P>0.05),見表1。
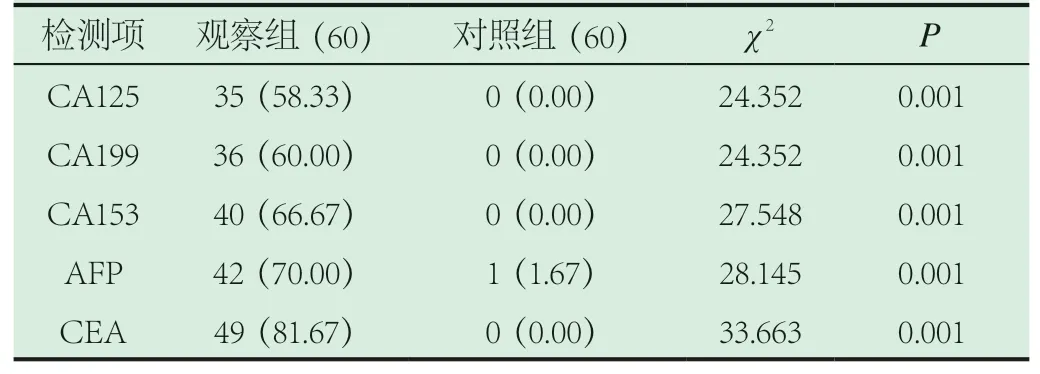
表1 兩組受檢者腫瘤生物標志物陽性檢出情況對比[n(%)]
3 討論
化學發光免疫分析技術,英文全稱chemi luminesce nce immuno assay,簡稱CLIA,是指將具有高靈敏度的化學發光測定技術與具有高特異性的免疫反應相結合,可應用于多種抗原、半抗原、抗體、激素、酶、脂肪酸、維生素、藥物等的檢測[2]。該技術是繼放射性免疫分析、酶免分析、熒光免疫分析、時間分辨熒光免疫分析技術之后發展而成的最新免疫測定技術。目前,化學發光免疫分析法已經成為公認的腫瘤標志物和各種激素最精確、最成熟的檢測方法之一。從檢測準確度層面來說,化學發光免疫分析法與放射免疫法不相上下;但從成本及實用性方面來說,放射免疫分析法的靈敏度雖然較高,但卻存在放射性防護和同位素污染的問題,加之試劑價格昂貴、保質期較短,無法在基層醫療機構普及。化學發光免疫分析技術不僅繼承了傳統放射免疫檢測技術的所有優點,還克服了傳統技術的缺點。該技術的作用原理為:分為兩個部分,分別為免疫反應系統和化學發光分析系統[3]。其中,前者是將發光物質(即在反應劑的激發下,生成一種激發態的中間體)直接標記在化學發光免疫分析抗原或免疫化學發光分析抗體、作用于發光底物的酶上;后者是指利用化學發光物質(經過催化劑的催化以及氧化劑的氧化,同樣能夠形成一個激發態中間體)。當上述激發態中間體從“亢奮狀態”回轉到穩定的基本狀態時,會向外發射光子;此時,檢驗人員可借助發光信號測量儀對光量子的產生額度進行測定,進而確定受檢物質的含量[4]。
綜上所述,化學發光免疫分析法因標記方式的不同可分為兩種類型:其一,化學發光標記免疫分析法;其二,酶標記、以化學發光底物作為信號試劑的化學發光酶免疫分析法。前者是用化學發光劑直接標記抗原或抗體的免疫分析方法。常用于標記的化學發光物質有吖啶酯類化合物;后者屬酶免疫分析,只是酶反應的底物是發光,操作步驟與酶免分析完全相同。通過此種方式對受檢者的靜脈血液標本進行檢測時,通過添加反應劑,將目標腫瘤生物標志物作為目標檢測對象;在對光量子的產生額度進行確定的過程中,檢測人員可清晰獲取每一種腫瘤生物標志物在受檢者血液內的含量[5]。由于不同受檢者個體存在差異,單一腫瘤生物標志物的檢測結果并不能說明問題,故需同時列出多個腫瘤生物標志物,根據整體檢測結果評估患者是否患有惡性腫瘤疾病。本研究結果顯示,原發性惡性腫瘤疾病患者的腫瘤生物標志物陽性檢出率較高;而健康人群的腫瘤生物標志物陽性檢出率整體為“零”,表明此種方式準確性高。

