牙周炎伴慢性阻塞性肺疾病急性加重期患者相關牙周指標和齦溝液指標的研究
莊賢文,陳展澤,蘭 倩,羅海玲
1.廣東省佛山市口腔醫院(佛山市牙病防治指導中心)檢驗科,廣東佛山 528000;2.廣東省佛山市第一人民醫院檢驗科,廣東佛山 528000;3.廣東省佛山市口腔醫院(佛山市牙病防治指導中心)牙周病科,廣東佛山 528000
慢性阻塞性肺疾病(COPD)是較為常見的一種呼吸系統疾病,具有不完全可逆、進行性加重的特點[1],可進一步發展為肺源性心臟病和呼吸衰竭。全球每年約300萬人死于COPD,約占全球總死亡人數的5%[2],目前我國COPD患病率約占40歲以上人群的13.7%,位列全球死亡原因的第4位[3]。牙周炎是由牙菌斑中細菌侵犯牙周組織引起的一種慢性破壞性疾病[4],可與全身疾病相關,研究表明牙周炎對COPD發病、發展有一定的促進作用[5-6],牙周狀況較差的患者COPD急性發作的頻率會升高[7]。本研究通過檢測牙周炎伴慢性阻塞性肺疾病急性加重期(AECOPD)患者相關的牙周指標和齦溝液指標,探討其臨床診治意義,現報道如下。
1 資料與方法
1.1一般資料 選取2019年1-12月到廣東省佛山市口腔醫院(以下簡稱該院)就診的30例單純慢性牙周炎(CP)患者作為CP組,其中男18例、女12例,平均(37.5±13.2)歲;選取同期到佛山市第一人民醫院就診的30例單純AECOPD患者作為AECOPD組,其中男16例、女14例,平均(40.2±10.3)歲;選取同期到該院和佛山市第一人民醫院就診的30例中重度CP伴AECOPD患者作為CP+AECOPD組,其中男18例、女12例,平均(39.2±12.4)歲;另選取同期到該院檢查的30例全身及牙周健康體檢者作為對照組,其中男15例、女15例,平均(36.3±9.5)歲。入選標準:(1)所有AECOPD患者符合中華醫學會呼吸病學分會修訂的《慢性阻塞性肺疾病診治指南(2013年版)》中COPD的相關診斷標準[8];(2)所有CP患者臨床診斷為中重度CP,全口余留牙≥20個;(3)患者及其家屬對本研究知情并同意。排除標準:(1)合并有嚴重器質性疾病如心、肝、腎功能不全者或內分泌、血液疾病者;(2)有其他可能與牙周炎有關的全身性疾病;(3)3個月內使用抗菌藥物或含漱液者,6個月內進行牙周治療者。各組研究對象的年齡、性別差異無統計學意義(P>0.05),有可比性。
1.2方法 對所有研究對象的4個牙(12、11、21、22)進行牙周檢查和齦溝液采集,記錄牙周指標包括出血指數(BI)、探診深度(PD)、臨床附著喪失(CAL)、菌斑指數(PLI)。將待取樣牙的齦上菌斑和軟垢清除并待牙面吹干后,用Whatman濾紙(2 mm×10 mm)插入齦溝底30 s進行標本采集,取出濾紙浸入含0.2 mL 磷酸鹽緩沖液(PBS)的EP管中充分振蕩搖勻,以3 000 r/min離心10 min取上清液[9]備用,使用酶聯免疫吸附試驗檢測齦溝液中白細胞介素(IL)-6、IL-8、C反應蛋白(CRP)和腫瘤壞死因子-α(TNF-α)。IL-6、IL-8、TNF-α使用羅氏診斷產品有限公司提供的全自動免疫分析儀及配套試劑盒進行檢測,CRP使用深圳國賽生物技術有限公司提供的特定蛋白分析儀(Astep PLUS)及配套試劑盒進行檢測。所有操作均嚴格按照試劑盒說明書操作方法進行,并采用同一批號的試劑檢測,排除非特異性干擾,以保證檢測結果的穩定性和可比性。采用基于16S rRNA基因的高通量測序方法檢測CP組和CP+AECOPD組各30份標本的細菌組成。將所有標本送至深圳華大基因股份有限公司進行檢測,獲得兩組標本的細菌分析數據。
1.3觀察指標 分別對所有研究對象的齦溝液炎癥因子(IL-6、IL-8、TNF-α、CRP),以及牙周指標(BI、PD、CAL、PLI)和細菌群落相對豐度進行檢測。

2 結 果
2.1各組牙周指標比較 與對照組比較,CP組和CP+AECOPD組BI、PD、CAL、PLI明顯升高,差異均有統計學意義(P<0.05);與CP組比較,CP+AECOPD組PLI明顯升高,差異有統計學意義(P<0.05)。見表1。
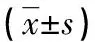
表1 各組牙周臨床檢測指標對比
2.2各組齦溝液中的炎癥因子對比 與對照組比較,CP組和CP+AECOPD組CRP、TNF-α、IL-6、IL-8水平顯著升高,差異均有統計學意義(P<0.05);與CP組比較,CP+AECOPD組CRP、TNF-α、IL-6、IL-8水平明顯升高,差異均有統計學意義(P<0.05)。見表2。
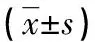
表2 各組齦溝液中的炎癥因子比較
2.3兩組患者齦溝液在門水平細菌群落的相對豐度比較 在門水平,CP+AECOPD組在厚壁菌門、擬桿菌門、梭桿菌門和變形菌門的相對豐度明顯高于CP組,差異均有統計學意義(P<0.05)。見表3。

表3 兩組患者齦溝液在門水平細菌群落的相對豐度比較[ M(P25~P75)]
2.4兩組患者齦溝液在屬水平細菌群落的相對豐度比較 在屬水平,CP+AECOPD組在纖毛菌屬、棒桿菌屬、鏈球菌屬和普氏菌屬的相對豐度顯著高于CP組,差異有統計學意義(P<0.05)。見表4。

表4 兩組患者齦溝液在屬水平細菌群落的相對豐度比較[ M(P25~P75)]
3 討 論
CP主要通過以下方式影響COPD患者的疾病進展[10]:(1)牙周組織是炎性介質儲存庫;(2)齦下菌斑是細菌儲存庫;(3)CP和COPD危險因素相似。同時,牙周炎和COPD在疾病發展過程中會釋放多種炎性介質,如IL-6、IL-8等,各種炎性介質相互影響,在疾病發生、發展過程中發揮作用[11-12]。本研究通過檢測CP伴AECOPD患者相關牙周指標和齦溝液炎癥因子及細菌指標水平,探討其臨床診治意義。
CP患者普遍發生牙齦出血、牙齒松動及附著喪失等情況,本研究中CP組和CP+AECOPD組患者BI、PD、CAL、PLI顯著高于對照組,差異均有統計學意義(P<0.05);CP+AECOPD組和CP組患者BI、PD、CAL相比差異均無統計學意義(P>0.05),CP+AECOPD組PLI高于CP組,差異有統計學意義(P<0.05)。研究表明,COPD患者口腔健康狀況較差,COPD和CP之間存在一定相關性,隨著牙周附著喪失的增加,COPD患者肺功能逐漸減弱[13]。
CP不僅與糖尿病、心腦血管疾病、類風濕關節炎、肥胖、早產低出生體質量兒有密切關系,與呼吸系統疾病的關系也日益受到關注[14]。IL-6、IL-8等炎癥因子相互作用,在CP和COPD兩者的發生、發展中相互影響,IL-6、IL-8等炎癥因子在呼吸系統炎癥過程中過度產生與聚集,通過氣道及血源等途徑進入口腔,加劇牙周組織破壞[15]。本研究中,CP組和CP+AECOPD組齦溝液CRP、TNF-α、IL-6、IL-8水平明顯高于對照組,差異均有統計學意義(P<0.05);CP+AECOPD組齦溝液CRP、TNF-α、IL-6、IL-8水平均顯著高于CP組,差異均有統計學意義(P<0.05)。其中,在啟動和加劇炎性反應過程中IL-6和IL-8起關鍵作用,兩者均參與牙槽骨的破壞和吸收,減弱牙周組織修復能力,而且過度產生的IL-8會激活大量粒細胞,進一步破壞牙周組織并影響炎性反應進程。IL-6和IL-8作為遠端細胞因子,在近端細胞因子刺激肺泡巨噬細胞時大量產生,可導致瀑布式炎性反應,最終造成肺過度損傷[16-17]。COPD患者體內細菌或病毒中所含抗原及代謝產物激活局部肺泡巨噬細胞,生成TNF-α等炎癥因子,而TNF-α反作用于COPD患者誘導產生中性粒細胞,提高蛋白溶解酶活性。
口腔菌群不僅數量巨大,而且種類十分豐富,由于口腔與呼吸道相通,研究發現健康人群肺部菌群與口腔菌群具有高度的相似性,在牙周常規檢出的細菌也可出現在下呼吸道中[18]。有研究表明,感染是COPD急性加重的主要原因,其中細菌感染最常見[4]。本研究中發現,在CP+AECOPD患者齦溝液中細菌的主要門類為厚壁菌門、擬桿菌門、梭桿菌門和變形菌門,主要屬類為纖毛菌屬、棒桿菌屬、鏈球菌屬和普氏菌屬,與相關研究結果相類似[19]。從研究結果上看,CP+AECOPD組患者的部分細菌門類、屬類群落相對豐度均高于CP組,但不同患者間的細菌門類、屬類分布仍存在較大差異,需要擴大樣本量,減少取樣偏差再次分析。
綜上所述,牙周炎伴AECOPD患者牙周損傷程度高于單純牙周炎患者,CRP、TNF-α、IL-6、IL-8等炎癥因子水平增高以及細菌種類與牙周炎存在密切關系,可為牙周炎患者診治提供重要依據。通過檢測上述指標可對治療方案進行優化調整。本研究存在一定的局限性,樣本量相對較少,且AECOPD的影響因素較多。在后續研究中將進一步加大樣本量,根據牙周及齦溝液陽性指標構建相關預測模型,用于臨床危險評估干預。

