使用一次性硬膜外麻醉導管進行無創小鼠氣管插管的方法建立
趙聰慧王 妍周 禹袁曉紅*
(1.首都醫科大學附屬北京口腔醫院病理科,北京 100050;2.山西醫科大學第一醫院,太原 030001;3.山西醫科大學肝病與器官移植研究所,太原 030001;4.中國醫學科學院藥物研究所,北京 100050)
肺疾病為常見的呼吸系統疾病,極大損害了人類健康,對社會造成勞動力和醫療資源損失。通過構建動物肺部疾病模型,可以直觀研究疾病發病機制,動態演變以及評估藥物治療效果。由于小鼠肺部疾病模型造模指向性強,需要直接將造模藥物均勻輸送到肺組織中。因此包括哮喘模型[1],肺纖維化模型[2],急性肺組織損傷模型[3],病毒感染模型[4]等肺部疾病模型均使用氣管插管法造模。小鼠體型較小,呼吸道狹窄,不易發現氣管入口。霧化吸入是常用的方法之一,操作簡便,可批量處理。但是,此方法存在藥品消耗大,每只動物吸入劑量不可控等缺點。滴鼻法操作簡便,但是藥物部分進入食道,造成不同動物之間實際給藥劑量差異。并且,研究表明經口鼻吸入法造模效果不及氣管插管法[5]。目前為止,多種小鼠氣管插管技術已被報道,可以歸類為“有創法”、“無創直接法”和“無創輔助法”,這些方法各有優勢,但仍存在不足。有創小鼠氣管插管技術雖然經過優化將動物損傷降到最低,但是仍不利于小鼠長期生存和多次給藥[6-8];無創輔助法通過使用輔助工具,例如使用光源[9-12]或者光源和纖維引導絲組合[13],從而直接可視化小鼠氣管入口并將插管引入氣管。但是,由于小鼠氣管狹窄,入口仍然不便直接觀察,且對于實驗器材獲取和實驗人員經驗技術要求較高;無創直接法也稱為“盲插法”,此方法不使用任何輔助,直接經小鼠口腔插入氣管,操作最為簡便,但手法難以掌握,并且成功插入與否難以把控。
綜合目前已經報道的小鼠氣管插管技術,同時參考大鼠氣管插管技術,結合實際在構建小鼠肺部疾病模型經驗,我們建立了一套操作簡單,成本低廉,重復性好,對操作要求較低的小鼠氣管插管方法。并總結出本方法訓練方法。本方法立足于無創“盲插”法,組裝包括一次性硬膜外麻醉導管,1 mL注射器,10μL移液器槍頭在內的常見實驗耗材作為氣管插管工具,并總結出插入氣管的判斷依據。使用本方法給藥,過程舒緩程度可控,一名操作人員即可快速完成實驗。本方法將有助于小鼠肺部疾病模型的研究。
1 材料和方法
1.1 實驗動物
SPF級C57BL/6小鼠,雌性,20只,6周齡,體重18~22 g。購于北京華阜康生物科技有限公司[SCXK(京)2019-0023],于中國醫學科學院藥物研究所動物房中飼養[SYXK(京)2019-0023],光照黑暗交替照明(12 h/12 h),自由飲水,進食,溫度22℃左右,相對濕度50%左右。本實驗已通過中國醫學科學院藥物研究所動物倫理委員會審批批準(00005199),實驗過程中遵循3R原則并對動物給予人道主義關懷。
1.2 主要試劑與儀器
1%戊巴比妥鈉;臺盼藍染液;1 mL注射器(BD);胰島素注射針(BD);一次性硬膜外麻醉導管;10μL移液器槍頭;縫合線;移液器架;眼科剪;眼科鑷。
1.3 實驗方法
1.3.1 小鼠氣管插管簡易裝置制作
小鼠氣管插管簡易裝置組成如圖1A所示,一次性硬膜外麻醉導管1支,10μL移液器槍頭若干,1 mL注射器一支,胰島素注射針1支。首先將硬膜外麻醉導管軟管對折,從中間剪開,插管時使用其中一半即可,將其中一端側面開口剪去(硬膜外麻醉導管的一端為側面開口),改為頂端開口。將處理好的軟管與進藥裝置組合,并旋緊螺絲扣。使用胰島素注射針吸取給定劑量藥物(此處為臺盼藍染液或PBS),將其通過進藥裝置注入軟管內。需要說明的是,使用的胰島素注射針與硬膜外麻醉導管的進藥口必須緊密對接,并且該注射器沒有死腔,有利于精確控制給藥劑量。建議每次只吸取1只小鼠的劑量。將藥物注入導管完畢后,使用1 mL注射器將針頭棄去不用,將注射器調整至最大量程處,與進藥口緊密對接,此處注射器當作“氣筒”使用。小心調節注射器,觀察軟管中液平面,將其控制在距離軟管出口處3~5 cm左右位置,以便于觀察。將軟管出口處套入10μL移液器槍頭內,以液體不外露為準,如圖1B所示。氣管插管裝置和藥物準備完成。

圖1 小鼠氣管插管簡易裝置Note.A,Tools for tracheal intubation.B,Assembled tracheal intubation tools for mice.Figure 1 Simple tracheal intubation tools for mice
1.3.2 實驗動物準備
1%戊巴比妥鈉深度麻醉小鼠,麻醉過淺在插管時會產生嘔吐反射,不利于找到氣管位置。小鼠以使用鑷子夾住四肢無反應,雙眼濕潤,呼吸規律且較為深長為佳。使用縫合線,將小鼠懸掛于移液器架上。
1.3.3 小鼠氣管插管過程
使用縫合線將小鼠懸空掛于移液器架上,高度以操作人員舒適為準。使用眼科鑷小心將小鼠舌頭拔出。如圖2所示,左手大拇指放在小鼠頸前部,指肚緊貼小鼠頸部(重要),其余手指置于小鼠后頸部固定小鼠,以免搖晃。右手手持套入軟管的移液器槍頭,沿小鼠下顎,抵住小鼠舌頭緩緩插入小鼠口中,在抵達小鼠會厭部時,會感受到阻力,這是小鼠會厭軟骨所造成,此時不可用蠻力向下,以免傷及小鼠。將槍頭稍稍回撤,而后將槍頭下端向小鼠頸部腹側反方向向下一小段距離(此時操作員面對小鼠,小鼠頸部腹側正對操作員臉部),而后轉向頸部腹側表皮方向輕輕挑一下,同時將槍頭向下,目的為挑過會厭軟骨將槍頭送入小鼠氣管。當感覺槍頭越過阻礙后,將槍頭抵住左手拇指肚,輕柔地上下摩擦,注意動作輕柔。此時如果插入氣管,應感覺到移液器槍頭與氣管軟骨摩擦“一楞一楞”的感覺,這個感覺就是成功插入小鼠氣道的判斷依據,同時也是本技術的重點,如果插入食道則左手拇指肚感受到平滑感。此時觀察軟管中的液面,如果插入氣管中,液面應該波動并向小鼠方向移動。當成功插入氣管后,左手把住槍頭,右手持注射器,緩慢推進,直至軟管內液體全部進入后繼續打入0.5 mL刻度的氣體,迅速拔掉槍頭。

圖2 小鼠氣管插管手法Figure 2 Schematic diagrams of tracheal intubation by epidural anesthesia catheter
小鼠懸掛30 s后即可取下。若插管成功,小鼠呼吸應該從麻醉的深長呼吸狀態變為短促呼吸狀態,此狀態會維持數分鐘,直至漸漸變為規律的深長呼吸,此時呼吸聲音明顯增加。
1.3.4 注意事項
(1)小鼠麻醉程度要控制得當,麻醉淺小鼠會出現掙扎情況,麻醉過深則容易窒息死亡;(2)給藥體積控制在每只小鼠30~50μL,少于30μL不利于藥物均勻分布,多于50μL則容易造成小鼠窒息死亡;(3)插管的深度不宜過深,應控制在氣管中上部分,不宜過度接近氣管分支部分,以免造成藥物偏向一側肺組織;(4)氣管插管過程中,由于小鼠個體差異和狀態不同,不同小鼠插管的難易程度略有不同,建議連續2~3次插管不成功(遇到阻力,回撤再向下為一次)將小鼠取下休息一段時間,并且過程一定要輕柔,以免損傷小鼠或者造成窒息;(5)插管成功的依據是左手拇指有“一楞一楞”的感覺,因此應保持左手拇指的位置正確和敏感性,少部分情況即使成功插入氣管,軟管中液面的波動亦不明顯;(6)此方法雖然簡單,但是需要操作人員有一定的練習,可采用先將小鼠解剖,完全暴露小鼠頸部組織結構,體會槍頭插入的位置和程度;(7)我們使用的是10μL移液器槍頭,這個部分可以換做任何可以與導管頭接合的器具,以使用順手為目的,原則是足夠細,并且不會傷及小鼠;(8)推入液體時速度應保持中速和穩定,確定將液體全部推入后,應繼續進氣0.5 mL左右,以保證液體進入肺組織深部。有文章提出,補氣有助于滴注物擴散,防止動物窒息,但由于小鼠肺總容量小,補氣量為0.6~0.8 mL[14]。
1.4 統計學方法
實驗數據采用GraphPad Prism 8.0進行統計分析,計數數據采用Two-way ANOVA檢驗,P<0.05、P<0.01以及P<0.001為差異有統計學意義。
2 結果
如圖3所示,通過氣管插管給予小鼠臺盼藍染液,可見小鼠肺組織均勻藍染,同時胃中沒有藍色,證明染液均勻分布于肺組織中。通過氣管插管給予PBS組小鼠,在麻醉劑作用失效后,存活情況良好,無小鼠死亡。證明上述操作安全可靠。使用上文所述小鼠氣管插管方法,我們已經完成多種、多次小鼠肺部疾病模型造模,包括IL-33誘導的小鼠哮喘模型,博來霉素誘導的小鼠肺纖維化模型,以及LPS引發的急性肺損傷模型。對于氣管插管造模的成功率,我們以博來霉素誘導的肺纖維化為例,如圖4所示。相比于對照組,模型組小鼠體重有顯著下降,并且數據變異度小,證明模型發病率高,造模方法穩定。如圖5A所示,使用此方法構建博來霉素誘導的肺纖維化模型28 d后,安樂死小鼠取肺組織,進行病理學分析,HE染色顯示對照組小鼠肺組織肺泡結構清晰,肺泡間無雜質,無炎性細胞浸潤,模型組小鼠肺泡組織結構消失,原本肺泡組織被大量細胞外基質填充,可見炎性細胞浸潤。Masson染色顯示相比對照組,模型組小鼠肺組織著色顯著。同時如圖5B所示,免疫組化染色表明,肺纖維化標志αSMA、Collagen I和Vimentin在模型組顯著表達增高。綜上,病理分析表明小鼠肺纖維化模型成功。
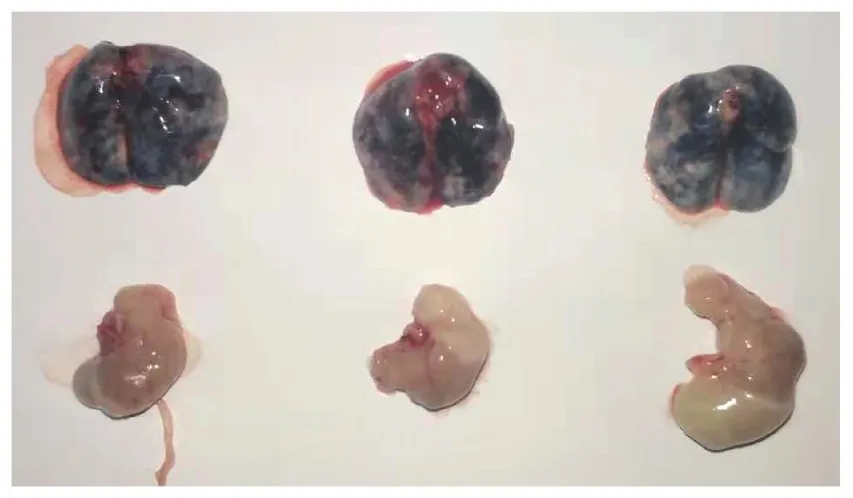
圖3 氣管插管給予小鼠臺盼藍染液后,肺組織和胃染色情況Figure 3 Trypan blue staining of mouse lung and stomach after intratracheal intubation
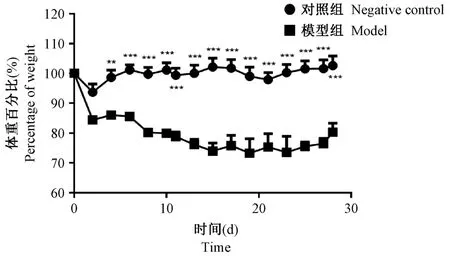
圖4 經氣管插管使用博來霉素小鼠肺纖維化造模后小鼠體重變化統計(n=7)Note.Compared with the control group,**P<0.01,***P<0.001.Figure 4 Body weights(%)of animals after bleomycin intratracheal intubating
小鼠氣管插管過程中,由于個別小鼠較為敏感或者手法問題,會出現小鼠因窒息死亡現象。具體表現為,小鼠眼球突出眼眶,出現身體蜷曲張口深大呼吸等呼吸困難表征,此為小鼠窒息前兆,如無此現象小鼠不會窒息死亡。通過手法逐漸熟練和給與的液體量減少,小鼠死亡現象顯著下降。
3 討論
小鼠肺部疾病模型需要將造模藥物直接并且均勻輸送到肺組織中,口服,靜脈/腹腔/皮下注射等造模方式不能完全滿足需求。張曉曄等[15]比較經尾靜脈和經氣管進行小鼠肺纖維化造模,結果表明動物肺纖維化程度尾靜脈造模組低于氣管造模組(但未見統計學差異),且小鼠肺組織病變部位二者存在顯著差異。由于小鼠體積較小,口腔空間狹窄,導致難以準確找到氣管開口位置。因此掌握成熟、穩定的氣管插管技術就顯得尤為重要。
由于大鼠也常被用于構建肺部疾病模型,因此大鼠的氣管插管方法也可參考[16-17]。已報道的各類方法可分為“有創性插管”,“使用輔助工具無創性插管”和“無創性直接插管”(也被稱作“盲插”)。有創性插管采用暴露部分氣管,將藥物注射入動物氣管內。此方法經過多次改良,力求盡可能減少對動物損傷,但是依舊易導致動物死亡,并且不利于多次干預。使用輔助工具無創性插管的改進在于使用光源,或光源與體試鏡,導引絲結合,在無創條件下將氣管入口可視化,提高插管成功率。有報道分別使用小鼠和大鼠比較了經口直視插管組和經頸透照直視插管的優劣,認為經頸透照直視插管可靠性更佳[18-19]。使用輔助工具無創性插管準確性高,對動物傷害小,但是仍有不足。一方面對于操作人員技術要求較高或者需要兩人一起操作,另一方面需要購買或自制相關設備。相比之下“盲插”具有成本低廉,上手較快等優點。但是,此方法具有無法準確判定是否進入氣管,插管手法難以掌握這兩大缺點。王凱等[20]在比較不同方法建立大鼠間質性肺炎模型中摸索出一套切實可用的大鼠氣管“盲插”手法。但是提及的“輕微阻力”和“摩擦感”兩個插入氣管的特征,并不能準確判定工具進入氣管。而且小鼠相比于大鼠,由于體積更小,氣管更加狹窄,不利于插管。因此有必要改進“盲插”法以更好的適應小鼠實驗。
本文立足于“盲插”法,使用硬膜外麻醉導管,移液器槍頭,注射器等常用實驗耗材,并通過手指的感覺確定進入氣管,給藥過程可控制速度,且藥物可均勻分布到肺組織中。器材選用方面,已報道的方法多使用滯留針,穿刺針和移液器槍頭等。相比于鐵質針頭,移液器槍頭不易損傷組織。通過比較不同氣管插管方法造小鼠肺纖維化模型的情況,提出插管深度對藥物分散和造模效果直接相關[21]。10μL移液器槍頭可滿足進入氣管一定深度。連接硬膜外麻醉導管后,可將推注使用的移液器放置于合適位置,有助于控制推注過程。本方法操作手法需要一定的練習,可先在解剖條件下觀察插管時槍頭在小鼠咽喉部的位置,記住在何處有阻力,如何避開會厭軟骨隔擋。在熟練掌握手法后,每只小鼠插管給藥時間可控制在1~2 min內,并且在50μL以內的給藥體積小鼠被直接嗆死的比例小于10%。使用本方法,我們已經建立了IL-33誘導的小鼠哮喘模型,LPS誘導的小鼠急性肺損傷模型,博來霉素誘導的小鼠肺纖維化模型。模型成功率接近100%,并且出模率穩定。通過更換所使用的工具,以相同的判定方式和手法,本方法也可適用于大鼠氣管插管給藥。
綜上,我們在無創無可視輔助工具的條件下,經過改良和創新,建立了一套成本低廉,原料易得,上手容易,并且高效,穩定的小鼠氣管插管方法,此方法將有助于更多小鼠肺組織疾病模型研究。

