circRNA CDR1as靶向miR-876-5p調控肝癌細胞的增殖、遷移和侵襲
李沛 李穎 劉宇
(南華大學附屬第一醫院 1檢驗科,湖南 衡陽 421001;2急診科)
雖然針對肝癌的治療研發水平不斷提高,但其預后并未得到明顯的好轉,因此,開拓新的治療方案具有重要意義〔1,2〕。環狀RNA(circRNA)是一類長的非編碼RNA分子,其形成共價閉合的連續環,不存在5′-3′極性且不含polyA尾。CircRNA在真核轉錄組中表達高度組織特異性〔3〕。最新研究發現,數千種內源性circRNA存在于哺乳動物細胞中,它們通過與微小RNA或其他分子結合,以抑制其功能,在轉錄或轉錄后水平調控基因的表達。此外,circRNA在多種類型的癌癥中表現出異常表達,包括肝癌〔4〕,由此可見,circRNA是診斷或治療腫瘤生物標志物的新希望。小腦退化相關蛋白1反義RNA (CDR1as)是一種致癌環狀RNA,參與人類腫瘤的發生,其在肝癌中表達失調〔5,6〕,CDR1as在肝癌中作用的分子機制尚不清楚。miRNA作為circRNA的調控因子之一,其確實對circRNA的功能具有很大的作用。miR-876-5p在肝癌中發揮抑制癌癥進一步惡化的作用〔7〕,但是其是否與CDR1as在肝癌中的功能具有相關性尚且未知。本研究擬以肝癌細胞為研究對象,檢測其中CDR1as、miR-876-5p的表達,觀察敲減CDR1as、過表達miR-876-5p對肝癌細胞增殖、遷移和侵襲的影響,揭示其機制可能與CDR1as靶向miR-876-5p有關,將為CDR1as在肝癌的診斷、治療中的研究提供參考依據。
1 材料與方法
1.1材料 正常肝細胞L02和肝癌細胞Huh-7、Hep-3B均購自ATCC;實驗動物SPF級BALB/C裸鼠(18~20 g)30只,購自湖南斯萊克實驗生物有限公司,遵守實驗動物管理和倫理委員會章程對動物進行飼養和相關實驗;胎牛血清(FBS)購自杭州四季青;DMEM培養基購自美國Hyclone;CCK-8試劑盒購自美國Apexbio;LipofectamineTM2000、逆轉錄試劑盒、熒光定量試劑盒購自大連Takara公司;雙熒光素酶報告基因檢測試劑盒購自美國Promega公司;Transwell小室購自美國Corning。
1.2方法
1.2.1細胞培養 將正常肝細胞L02和肝癌細胞Huh-7、Hep-3B,用含有10%FBS的DMEM培養基進行常規培養。
1.2.2細胞轉染與分組 將正常肝細胞L02和肝癌細胞Huh-7、Hep-3B分別標記為L02組、Huh-7組、Hep-3B組;將培養24 h 的Huh-7隨機分為si-NC組(轉染si-NC)、si-CDR1as組(轉染si-CDR1as)、miR-NC組(轉染miR-NC)、miR-876-5p組(轉染miR-876-5p mimics)、anti-miR-NC組(轉染anti-miR-NC)、anti-miR-876-5p組(轉染anti-miR-876-5p)、si-CDR1as+miR-NC組(共轉染si-CDR1as和miR-NC)、si-CDR1as+miR-876-5p組(共轉染si-CDR1as和miR-876-5p mimics),各組細胞用LipofectamineTM2000試劑盒說明要求操作進行轉染,轉染48 h后,用實時熒光定量-聚合酶鏈式反應(qRT-PCR)檢測轉染效率,轉染成功后用于后續試驗。
1.2.3qRT-PCR檢測細胞中CDR1as、miR-876-5p的mRNA的相對表達水平 取充分研磨腫瘤組織或細胞,用Trizol法提取總RNA,使用微量核酸蛋白測定儀檢測RNA濃度和純度。調整RNA樣品濃度,使用TaKaRa反轉錄試劑盒和熒光定量試劑盒分別將RNA反轉錄為cDNA,并配制反應體系,以U6為內參進行擴增。實驗結果采用2-△△Ct法進行分析。引物信息如下:CDR1as:上游引物5′-GTGTCTCCAGTGTATCGGCG-3′,下游引物 5′-TACTGGCACCACTGGAAACC-3′;miR-876-5p:上游引物 5′-TGAAGTGCTGTGGATTTCTTTGTG-3′,下游引物 5′-TGAATTACTTTGTAAACCACCACCA-3′。
1.2.4CCK-8法檢測細胞的增殖 調整細胞至1×105個/ml,取100 μl/孔接種至96孔板,37℃、5%CO2培養24 h。每組設5個重復,加入20 μl的CCK-8溶液,490 nm波長檢測吸光度(OD490值)。細胞的增殖能力與細胞的吸光度呈正比。
1.2.5Transwell小室檢測細胞的遷移和侵襲 通過Transwell小室檢測細胞的遷移和侵襲,不同之處在于,檢測細胞侵襲的小室的聚碳酸酯膜上表面需要鋪有一層基質膠,模擬人體的細胞外基質,細胞需要消化基質后才能進行穿膜。操作方法為:首先將細胞用無血清培養基培養24 h,調整至5×105/ml,取100 μl加入小室上室的聚碳酸酯膜上,取600 μl含血清的培養基加入下室,將小室放在37℃、5%CO2的細胞培養箱中進行培養48 h,取出小室。用棉簽小心擦去上室聚碳酸酯膜下表面的細胞,用甲醇固定,結晶紫染色,在顯微鏡下用400倍視野觀察細胞的數量,取5個視野進行拍照計算,取平均值。
1.2.6雙熒光素酶報告基因檢測實驗檢測細胞的熒光活性 將含有CDR1as-WT(含CDR1as野生型片段)和CDR1as-MUT(含CDR1as突變體片段)克隆至pGL3報告熒光素酶載體,標記為pGL3-CDR1as-WT、pGL3-CDR1as-MUT,將其分別于miR-NC、miR-876-5p、anti-miR-NC、anti-miR-876-5p共轉染48 h,通過螢火蟲熒光素酶和海腎熒光素酶的熒光活性的比值表示熒光素酶的活性。
1.2.7裸鼠成瘤實驗 將30只裸鼠隨機分為Blank組、si-NC組、si-CDR1as組,每組10只。Blank組裸鼠,不進行任何處理,正常飼養;si-NC組、si-CDR1as組裸鼠分別接種轉染si-NC、si-CDR1as的Huh-7細胞,用1 ml注射器吸取0.2 ml的1×106個/ml細胞,接種在裸鼠左前肢,在SPF條件下飼養裸鼠,第3天開始,每周用直尺測量腫瘤的長和寬(cm),計算腫瘤的體積。至第60 天腫瘤生長到足夠大,斷頸法處死裸鼠,小心剝離腫瘤,稱量重量(mg),取平均值。
1.3統計學方法 采用GraphPad Prism6.0軟件進行單因素方差分析、Bonferroni校正的t檢驗。
2 結 果
2.1CDR1as、miR-876-5p在肝癌細胞中的表達 與L02組相比,Huh-7、Hep-3B組細胞中CDR1as表達均顯著升高,miR-876-5p表達均顯著降低(P<0.05)。見表1。

表1 CDR1as、miR-876-5p在肝癌細胞中的表達
2.2敲減CDR1as對肝癌細胞增殖、遷移和侵襲的影響 與si-NC組相比,si-CDR1as組細胞中CDR1as表達顯著降低,在48、72 h時,細胞增殖顯著降低,遷移細胞數和侵襲細胞數均顯著降低(P<0.05)。見表2、圖1。
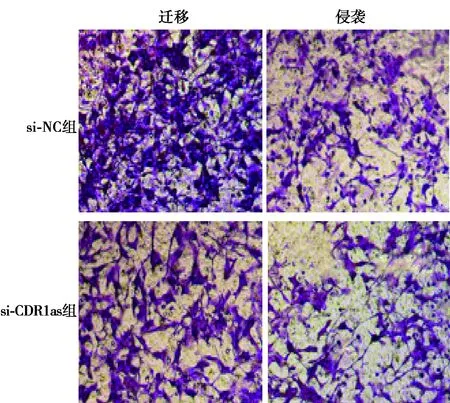
圖1 敲減CDR1as的肝癌細胞的遷移侵襲(結晶紫染色,×200)

表2 敲減CDR1as對肝癌細胞增殖、遷移和侵襲的影響
2.3CDR1as靶向miR-876-5p 通過生物信息學在線預測網站Target Scan(http://www.targetscan.org/vert_71/)預測到CDR1as與miR-876-5p之間存在15個互補的靶向結合位點見圖2。雙熒光素酶報告基因檢測實驗顯示,與miR-NC組相比,miR-876-5p組CDR1as表達顯著升高,WT-CDR1as細胞的熒光活性顯著降低,MUT-CDR1as細胞的熒光活性差異不明顯,與anti-miR-NC組相比,anti-miR-876-5p組CDR1as表達顯著降低,WT-CDR1as細胞的熒光活性顯著升高,MUT-CDR1as細胞的熒光活性差異不明顯(P<0.05)。見表3。
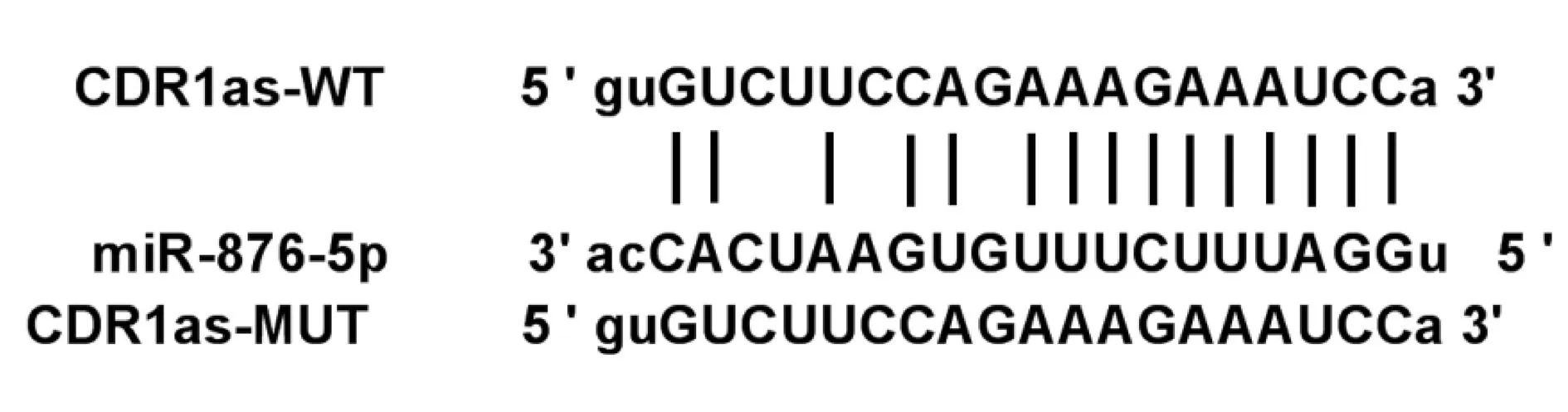
圖2 circ RNA CDR1as與miR-876-5p之間存在互補的結合位點

表3 雙熒光素酶報告實驗結果
2.4過表達miR-876-5p對肝癌細胞增殖、遷移和侵襲的影響 與miR-NC組相比,miR-876-5p組細胞中miR-876-5p表達顯著升高,在48、72 h時,細胞增殖顯著降低,遷移細胞數和侵襲細胞數均顯著降低(P<0.05)。見圖3、表4。

表4 過表達miR-876-5p對肝癌細胞增殖、遷移和侵襲的影響
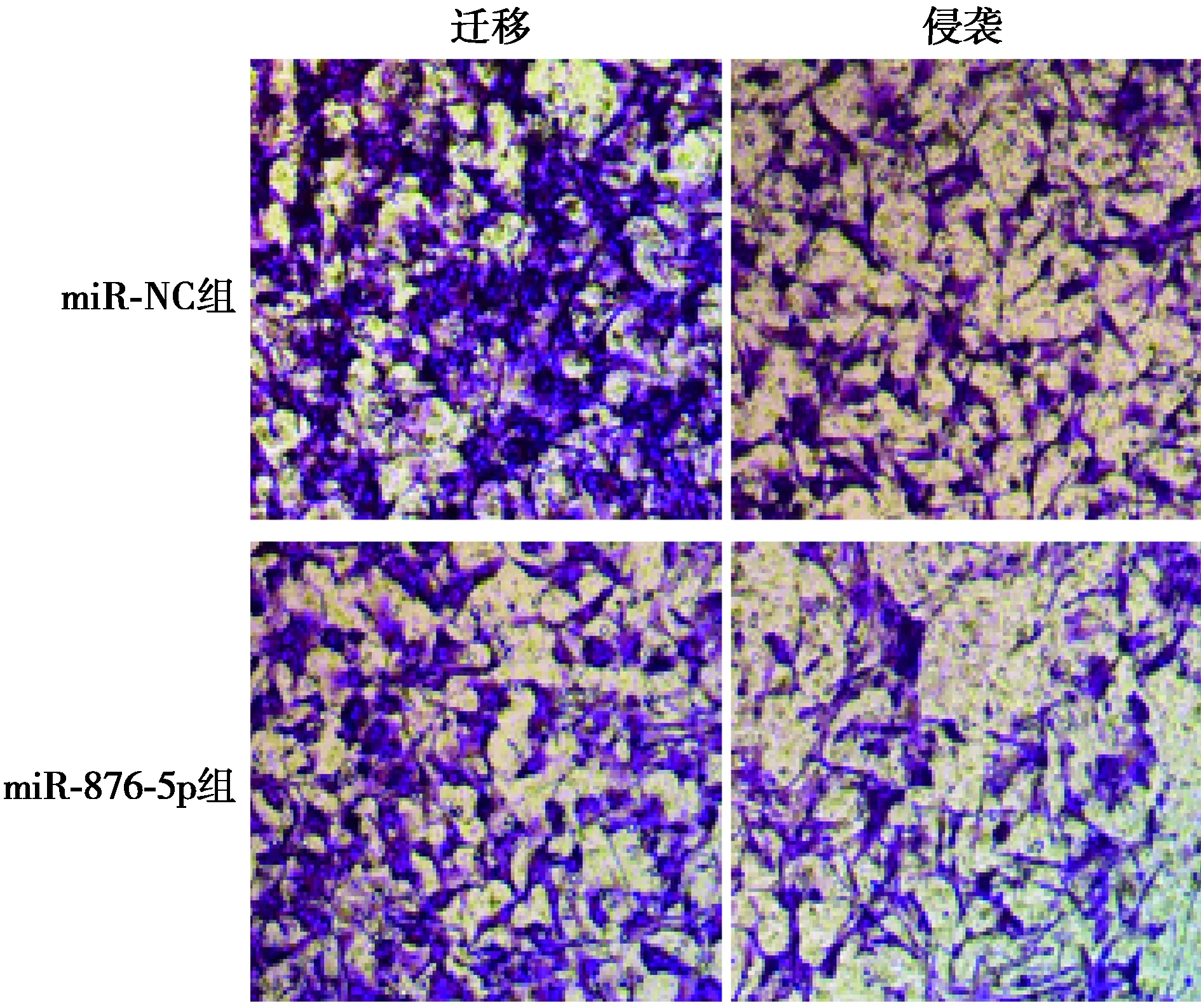
圖3 過表達miR-876-5p的肝癌細胞的遷移侵襲(結晶紫染色,×200)
2.5抑制miR-876-5p逆轉了敲減circRNA CDR1as對肝癌細胞增殖、遷移和侵襲的抑制 與si-CDR1as+miR-NC組相比,si-CDR1as+miR-876-5p組細胞中CDR1as表達顯著升高,在48、72 h時,細胞增殖顯著升高,遷移細胞數和侵襲細胞數均顯著升高(P<0.05)。見表5。

表5 抑制miR-876-5p逆轉了敲減circRNA CDR1as對肝癌細胞增殖、遷移和侵襲的抑制作用
2.6敲減circRNA CDR1as對裸鼠成瘤的影響 與si-NC組相比,si-CDR1as組裸鼠成瘤的平均重量和體積均顯著降低,腫瘤組織中CDR1as的表達顯著降低,miR-876-5p的表達顯著升高(P<0.05)。見表6。

表6 敲減circRNA CDR1as的裸鼠成瘤及CDR1as、miR-876-5p mRNA的表達
3 討 論
circRNA是一類內源性RNA,通過與其他分子或微小RNA相互作用調節轉錄后或轉錄水平的基因表達。circRNA在生物學過程中起著至關重要的作用。circRNA被證明是許多疾病(包括癌癥)的潛在生物標志物〔8〕。研究表明CDR1as的表達明顯發生升高,其表達與miR-7之間呈靶向負調控的關系,且敲減CDR1as可抑制肝癌細胞的增殖和侵襲,提示CDR1as在肝癌新療法中的巨大潛力〔9,10〕。Yang等〔11〕發現CDR1as在肝癌細胞中可調節300多個差異表達的蛋白質,以參與細胞增殖和周期調控,表皮生長因子受體(EGFR)是miR-7的靶向目標,CDR1as可靶向調控miR-7,也可以間接靶向調控EGFR,揭示了CDR1as在肝癌中發揮作用的新的功能機制。本研究檢測了肝癌細胞中CDR1as的表達發現,其在肝癌細胞中表達異常上調,并且敲減CDR1as明顯抑制肝癌細胞的增殖、遷移和侵襲。本研究通過生物信息學預測、雙熒光素酶報告基因檢測實驗驗證了CDR1as可靶向負調控miR-876-5p,于是猜測CDR1as在肝癌中的功能也許可能與miR-876-5p具有一定的聯系。
miRNA在人類腫瘤中的重要調控功能已得到認可,但是其調控網絡十分復雜,至今仍處在不斷地探索階段〔12〕。Xu等〔13〕報道miR-875-5p在肝癌的臨床樣本分析中的表達下調,并且過表達miR-875-5p可通過抑制上皮間質轉化而抑制肝癌細胞的遷移和侵襲,抑制miR-875-5p則具有相反的作用,并通過雙熒光素酶報告基因檢測實驗和回補實驗驗證miR-875-5p可靶向調控BCL6共抑制因子樣蛋白(BCORL)1的表達,揭示了miR-875-5p抑制肝癌細胞遷移侵襲的機制與靶向BCORL1相關。我們推測miR-875-5p在肝癌中的功能也許與CDR1as在肝癌中的功能具有一定的聯系。本研究驗證了miR-875-5p在肝癌中發揮抑制癌癥進一步惡化的作用;重要的是抑制miR-875-5p逆轉了敲減CDR1as對肝癌細胞的增殖、遷移和侵襲的抑制作用,這揭示了miR-875-5p也可以反向負調控CDR1as在肝癌中的表達和功能,為CDR1as、miR-875-5p在肝癌的診斷、治療中的潛在價值的開發奠定理論基礎。
綜上,環狀RNA CDR1as在肝癌細胞中調控癌細胞的增殖、遷移和侵襲,其機制與靶向miR-875-5p具有相關性,為肝癌的治療提供新的候選靶標。

