質量守恒定律在初中化學解題中的應用分析

摘 要:化學是初中階段學生最后接觸到的一門學科,對于初中階段的化學教學來說,最大的重點就是質量守恒定律.在化學教學的過程中,不免會出現一些研究物質變化的問題,這就會涉及到質量守恒定律的相關內容,因此在初中階段的化學學習過程中,學生不僅要掌握一定的理論知識,還需要掌握守恒定律.這樣在實際的解題過程中,學生就能夠做到定性和定量的統一分析,從而能夠快速、準確的解決化學問題.立足于質量守恒定律在化學結題當中的應用,進行了解題分析,從而為教師和學生在解題的過程中提供一定的思路.
關鍵詞:質量守恒定律;解題分析初中化學;
中圖分類號:G632文獻標識碼:A文章編號:1008-0333(2021)11-0098-02
作者簡介:張優維(1978.11-),女,浙江省寧波人,中學一級教師,從事初中化學教學研究.
質量守恒定律從的概念十分簡單,具體是指,在發生化學反應的過程中,參與反應的物質當中,物質的總質量在化學反應前后使保持一致的.但是對于初中生而言,質量守恒定律的學習是有一定困難的,主要是因為學生不能結合實際的化學問題,對質量守恒定律進行合理的分析,因此,學生不能把清楚的了解到在真實的化學反應過程中,質量守恒定律存在的意義.
一、借助質量守恒,促進學生知識理解
初中階段的化學知識的學習,最離不開的就是化學反應式.化學方程式是化學知識學習的最基礎內容,也是打開學生質量守恒定律大門的最佳路徑.因此教師在日常的教學過程中可以通過一些習題,來讓學生借助質量守恒定律與化學基礎知識相結合,從而在幫助學生深入了解化學知識的同時,學習質量守恒定律.
例如下面這兩道題:
在化學方程式A+B=C+D,其中的agA與agB進行完全的化學反應之后,就會產生Ccg,經過化學反應之后能夠生成D的質量為d=ag+bg-cg.
在化學方程式A+B=C+3D,其中的agA與agB進行完全的化學反應之后,就會產生Ccg,經過化學反應之后能夠生成D的質量為d=ag+bg-cg.
在這兩道化學題當中,能夠看到第一道題A+B=C+D,其中生成物D的系數為“1”,在第二道題當中A+B=C+3D,所以D的系數為“3”.通過兩道題之間的對比分析,其實很清楚的知道D的質量是相同的.在這里就利用了質量守恒定律,在化學反應式中,等號前的質量與等號后的質量使相等的,與化學方程式當中的系數并沒有必然的關系.
二、根據質量守恒,解答反應物生成質量
在初中階段的化學考試過程當中,有這樣一種題型深深的影響著學生的考試分數,那就是解答題.這一類問題在解題的過程中十分繁雜,會用到很多細小的知識點.自然,解答題也不會放過這兩守恒定律這個知識點.并且初中階段的學生更加注重自己的中考成績,所以解答題使學生得分的重要題型.因此在教學的過程中教師需要抓住解答題這一重要形式,借助質量守恒定律,來幫助學生解答題型中的反應物生成質量問題.
對于反應物生成質量這一類的解答題,本身就是有質量守恒定律轉化而來,因此在解答反應物生成質量相關問題時,不能忽略質量守恒定律,例如下面這道題:
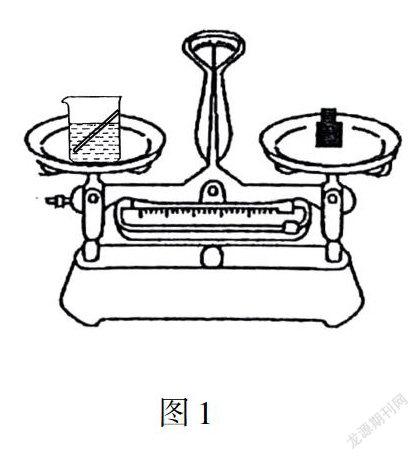
生鐵一般同時含有Fe元素和C元素,某興趣小組做了如下實驗(實驗儀器如圖1所示):將6g生鐵置入燒杯中,并圖1向燒杯中添加了65g的稀硫酸,生鐵與稀硫酸剛好進行完全反應. 反應前燒杯和其中物質的總重量為97g,反應后燒杯和其中物質的總重量為96.8g.試求:(1)實驗所產生的H2的質量;(2)該生鐵中鐵的質量分數;(3)所得溶液溶質的質量分數.
在這道題當中,通過質量守恒定律,可以分析出氫氣使在反應過程中生成的,因此在發生化學反應之后,燒杯中的物質不存在氫氣,因此實驗所產生的氫氣質量計算方式應該為:m(H2)=97g-96.8g=0.2g.通過質量守恒定律,學生就可以十分簡單的回答出第一個問題,拿到一定的分數.
在解答問題(2)的過程中,也需要借助在問題(1)解答過程中求出的氫氣質量0.2g,來進行計算.根據化學方程式:Fe+H2SO4FeSO4+H2↑以及原題當中給出的“將6g生鐵置入燒杯中”了解到生鐵的質量為6g,因此雜質質量為0.4g.所以鐵的質量分數計算為:5.6g÷6g×100%最終結果為93.3%.因此如果未能借助質量守恒定律進行第一問的計算,那么第二問學生也就無法做到準確回答.
在解答問題(3)的過程中,根據問題(2)了解到貼到質量分數為93.3%,因此生成的FeSO4就是15.2g.質量守恒定律在化學反應當中強調的是質量不便,因此就能夠分析出溶液的質量為70.4g,溶液當中的硫酸亞鐵質量以及溶液的質量都能夠解出,因此溶質的質量分數就可以通過算式15.2g÷70.4g×100%來計算,最終的結果為21.6%.
通過質量守恒定律,教師就能夠幫助學生在解答題中,不斷樹立學生的思路,使學生能夠根據題意以及質量守恒定律,發現解答題當中的一些隱性條件,從而將一道十分繁雜難解的題目變得更加簡單,使學生能夠輕松的掌握解答題的解題思路與方案,從而高效的對各種試題進行解答,提高學生的邏輯思維能力.
三、巧用質量守恒,分析反應組成元素
在質量守恒定律的教學過程中,教師需要讓學生從化學反應的本質入手去進行質量守恒定律的分析.化學反應的本質就是參與反應的各種物質的分子,通過反應分解成了原子,原子在化學反應當中又再次進行組合,從而形成新的分子.因此質量守恒定律從微觀點角度來看,就是在化學反應前后原子的數目、種類并未發生變化.在化學學習的過程當中,學生會遇到一些具有逆向思維的習題,就是通過化學反應的生成物對組成的元素進行反推的元素組成題.在這一類題的解答過程中教師就需要巧妙的將質量守恒定律融合進去,幫助學生形成良好的逆向思維.
例如,把某種物質放在氧氣中燃燒,已經知道這種物質的質量是1.8g,而且確定得到了充分燃燒,這時生成了新的物質:二氧化碳和水,兩種物質的質量分別是
4.4g和3.6g,現在需要推斷這種可燃物中必然會有什么元素.
在這道題的結題過程中,首先要根據原題來進行分析,在化學反應的過程中,新的生成物使二氧化碳和水.根據質量守恒定律進行反推,化學反應前后,物質的質量總和是不發生變化的,元素的種類也不會發生變化.通過質量守恒定律可知,可燃物當中必然存在氫元素和碳元素.再次回到原題,原題當中給出了二氧化碳質量為4.4g,水的質量為3.6g,那么學生就可以根據這兩個條件推算出碳元素和氫元素的質量綜合,在質量綜合計算出來后,學生就能夠輕易地發現可燃物品中所包含的元素:加入兩種元素的質量和為1.8g,那么可燃物中就只包含碳、氫兩種元素;假如質量綜合地域1.8g,那么,相差出來的質量就是氧元素,由此可知,可燃物中必然包含的三種元素:碳、氫、氧.根據相關的化學方程式,可以計算4.4g的二氧化碳當中,包含了碳元素的質量為1.2g,3.6g水當中含有的氫元素為0.4g,兩者相加1.2g+0.4g=1.6g結果是小于可燃物的1.8g,因此可以說明可燃物中包含碳氫氧三種元素.
例如選擇題蔗糖在隔絕空氣加熱時,會生成碳和水,則可以推斷蔗糖的組成元素是().
A.只有碳 B.只有碳氫 C.只有氫氧 D.碳氫氧
根據質量守恒定律,反應前后元素的種類保持不變.生成物是碳和水,含碳、氫、氧三種元素,故反應物一定也含碳,氫、氧三種元素,因為是隔絕空氣加熱,所以蔗糖中一定含有碳、氫、氧三種元素,所以答案應選D.
在解題過程中,發現學會使用質量守恒定律是這一題的重要條件.
綜上所述,能夠看到在初中階段的學習過程中,無論是填空、選擇、解答各種題型都與質量守恒定律息息相關.因此在教學的過程中,教師需要把握住質量守恒定律這個重點,引導學生根據質量守恒定律解決相關問題.
參考文獻:
[1]辛雪.質量守恒定律在初中化學解題中的應用分析[J].數理化學習(初中版),2020(02):57-58+61.
[2]孫麗清.質量守恒定律在初中化學解題中的應用分析[J].名師在線,2019(11):63-64.
[3]劉維維.質量守恒定律在初中化學中的應用分析[J].中國校外教育,2018(13):123-124.
[4]曹劍.質量守恒定律在初中化學解題中的應用分析[J].數理化學習(初中版),2015(04):38-39.
[責任編輯:季春陽]

