四維斑點追蹤顯像技術評價維持性血液透析尿毒癥患者左心室心肌功能的研究
高繼康 梅旭峰 陳曉冰 惠姍姍 張雨濛
有研究認為,慢性腎病患者的死亡原因中心血管并發癥大約占50%,其中尿毒癥心肌病是透析患者的首位死因[1]。由于左心室心肌功能不全的出現要早于整體心功能不全,因此,早期診斷左心室心肌功能不全越來越被重視。以往評價左心室心肌功能的手段有組織多普勒[2]和二維斑點追蹤顯像技術[3],這兩種技術準確性和重復性較差,四維斑點追蹤顯像技術被認為是目前較先進的心肌運動定量工具[4],但用于維持性血液透析尿毒癥患者左心室心肌功能評價的研究較少。筆者采用該技術評價維持性血液透析尿毒癥患者的左心室心肌縱向、環向、徑向收縮運動,旨在了解患者左心室心肌收縮功能,為臨床進行合理的血液透析治療、預防整體心功能不全等提供幫助,現報道如下。
1 對象和方法
1.1 對象 選取2020年1至12月杭州市余杭區第一人民醫院進行血液透析治療的尿毒癥患者74例(血液透析組),其中男46例,女28例,年齡39~84(63.95±12.43)歲;普通低通量透析45例,高通量透析15例,血液透析濾過14例;采用的血管通路為上肢動-靜脈瘺59例,頸內靜脈長期置管15例;血液透析時間(67.04±55.74)個月;實驗室檢查結果:血紅蛋白(110.43±17.56)g/L,血甲狀旁腺素(366.30±182.05)pg/ml,β2微球蛋白(21.44±7.09)ng/L,同型半胱氨酸(41.70±28.01)μmol/L,肌酐(800.90±293.72)μmol/L,尿素氮(20.44±8.49)mmol/L。所有患者均無慢性阻塞性肺疾病、肝硬化和血液系統疾病等,常規心電圖檢查均排除心肌梗死及心律失常表現。同時選取本院健康體檢者45例作為正常對照組,其中男27例,女18例,年齡29~81(62.44±13.78)歲;均無高血壓、冠心病、肺心病、慢性腎病、糖尿病等病史,常規心電圖檢查未見明顯心肌缺血及心律失常。兩組對象除收縮壓之外,年齡、性別、身高、體重、舒張壓、心率等比較差異均無統計學意義(均P>0.05),見表1。本研究經本院醫學倫理委員會審批,所有受試患者均知情同意。
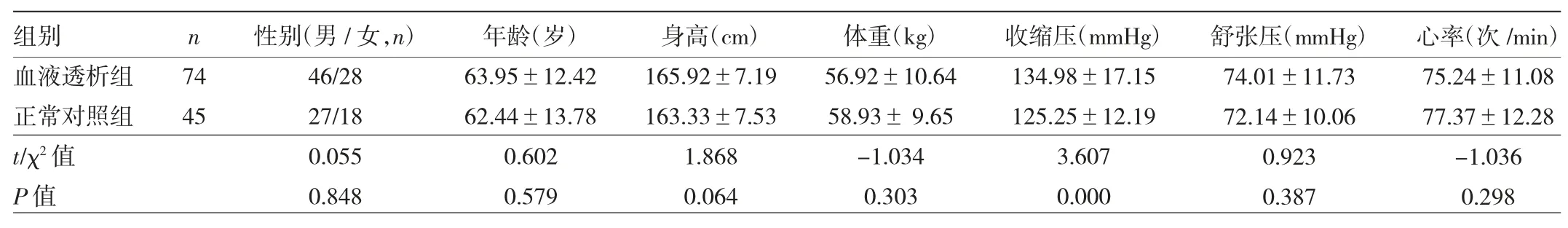
表1 兩組對象一般資料的比較
1.2 方法
1.2.1 超聲心動圖檢查 采用美國GE Vivid E9型彩色多普勒超聲診斷儀,探頭采用4V型心臟四維容積探頭,脫機分析采用EchoPac V203型軟件。所有受檢者取左側臥位,平靜呼吸,同步連接心電圖,先取胸骨旁左心室長軸切面,利用M型超聲測量左心室舒張末期內徑(LVDd)、室間隔舒張末期厚度(IVSd)、左心室舒張末期后壁厚度(LVPWd),自動計算左心室質量(LVM);手工計算相對室壁厚度[RWT,RWT=(IVSd+LVPWd)/LVDd)]。隨后顯示心尖四腔切面,切換進入四維模式,選擇6個心動周期,幀頻范圍大于心率的30%,動態存儲左心室四維全容積圖像。
1.2.2 脫機分析 將存儲資料導入EchoPac工作站,進行脫機分析。打開左心室四維全容積動態圖像,進入測量菜單,選擇容積模式,軟件自動同時顯示心尖部左心室二腔、三腔、四腔切面的二維動態圖像,于舒張期及收縮期分別在二尖瓣環水平中點及左心室心尖部心內膜面標記2點,軟件自動勾畫左心室心內膜線,手動校正心內膜位置后,系統自動計算顯示左心室舒張末期容積(LVEDV)、左心室收縮末期容積(LVSDV)、左心室射血分數(LVEF)、左心室每搏輸出量(LVSV)、心輸出量(CO);繼續選擇四維應變模式后,系統新添收縮期左心室心外膜線,手動修正心外膜線后,軟件自動進行四維應變分析,顯示左心室縱向應變(LS)、圓周應變(CS)、面積應變(AS)、徑向應變(RS)曲線。測量左心室心肌LS包括前壁中段縱向應變(ALSm)、下壁中段縱向應變(ILSm)、前間隔中段縱向應變(ASLSm)、后間隔中段縱向應變(PSLSm)、前側壁中段縱向應變(ALLSm);后側壁中段縱向應變(PLLSm)、心尖部縱向應變(APLS)、整體心肌縱向應變(GLS);測量心肌CS包括前壁中段圓周應變(ACSm)、下壁中段圓周應變(ICSm)、前間隔中段圓周應變(ASCSm)、后間隔中段圓周應變(PSCSm)、前側壁中段圓周應變(ALCSm);后側壁中段圓周應變(PLCSm)、心尖部圓周應變(APCS)、整體心肌圓周應變(GCS);測量心肌AS包括前壁中段面積應變(AASm)、下壁中段面積應變(IASm)、前間隔中段面積應變(ASASm)、后間隔中段面積應變(PSASm)、前側壁中段面積應變(ALASm);后側壁中段面積應變(PLASm)、心尖部面積應變(APAS)、整體心肌面積應變(GAS);測量心肌RS包括前壁中段徑向應變(ARSm)、下壁中段徑向應變(IRSm)、前間隔中段徑向應變(ASRSm)、后間隔中段徑向應變(PSRSm)、前側壁中段徑向應變(ALRSm);后側壁中段徑向應變(PLRSm)、心尖部徑向應變(APRS)、整體心肌徑向應變(GRS)。
2 結果
2.1 兩組對象左心室結構和四維心功能參數測值的比較 與正常對照組比較,血液透析組LVEDV、LVESV、LVEF和LVM、LVDd、IVSd、LVPWd、RWT的差異均有統計學意義(均P<0.05),而LVSV、CO的差異均無統計學意義(均P>0.05),見表2。
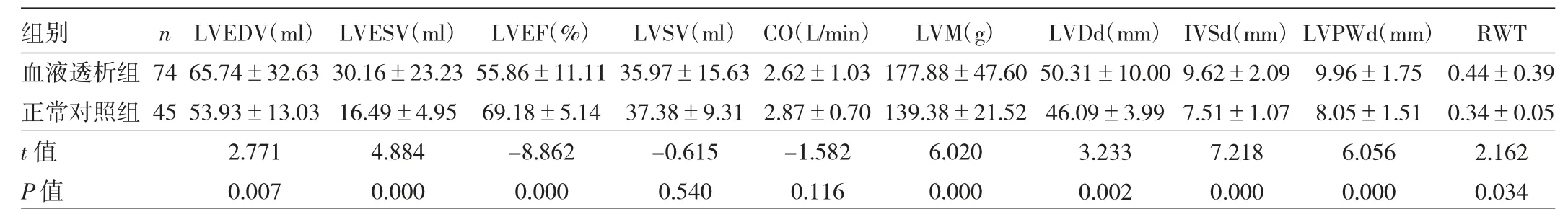
表2 兩組對象左心室結構和四維心功能參數測值的比較
2.2 兩組對象左心室心肌四維應變測值比較 血液透析組GLS、GCS、GAS、GRS均小于正常對照組(P<0.01);血液透析組除PSCSm外,ALSm、ILSm、ALLSm、ASLSm、PLLSm、PSLSm、ACSm、ICSm、ALCSm、ASCSm、PLCSm、AASm、IASm、ALASm、ASASm、PLASm、PSASm、ARSm、IRSm、ALRSm、ASRSm、PLRSm、PSRSm均小于正常對照組(均P<0.01);血液透析組APCS、APRS均大于正常對照組(均P<0.01),兩組間APLS、APAS的差異均無統計學意義(均P>0.05)。見表3、圖1-2。
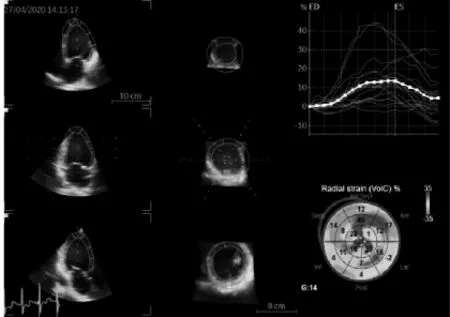
圖1 血液透析組整體心肌徑向應變(G RS)曲線圖(G RS為14%)
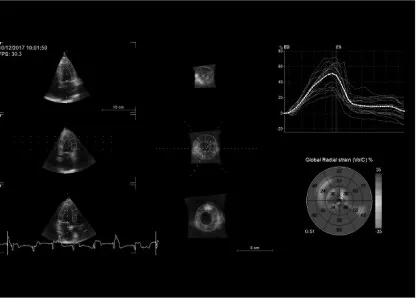
圖2 正常對照組整體心肌徑向應變(G RS)曲線圖(G RS為51%)
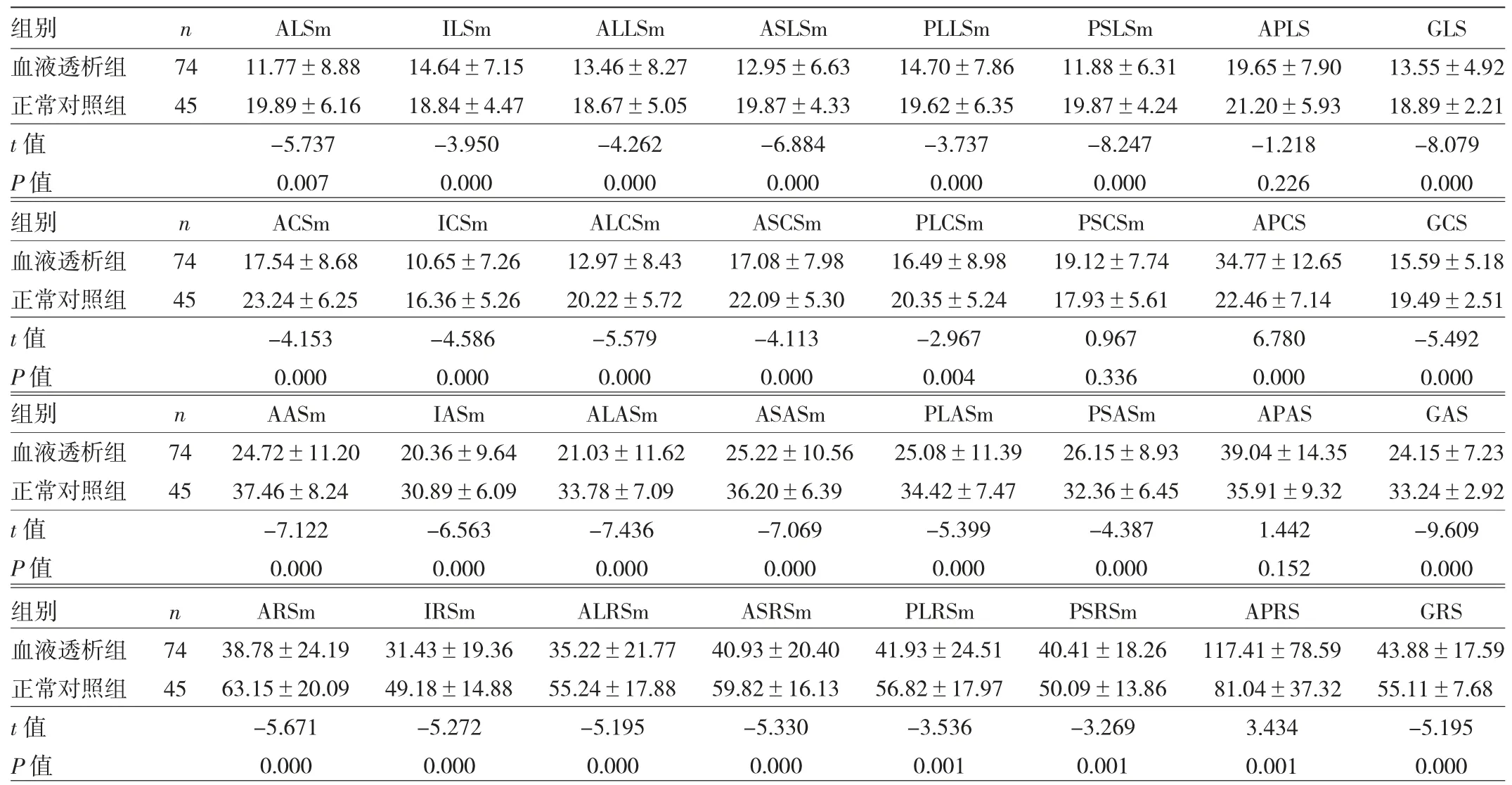
表3 兩組對象左心室心肌四維應變測值比較(%)
2.3 相關性分析 LS參數中ALSm、ASLSm、PLLSm、PSLSm、APLS、GLS與LVEF均呈正相關(r=0.20、0.29、0.40、0.36、0.44、0.48,均P<0.05),其中GLS與LVEF相關性較高,其直線回歸方程為Y=0.212X+1.718,見圖3。CS參數ICSm、ALCSm、ASCSm、GCS與LVEF均呈負相關(r=-0.22、-0.23、-0.26、-0.24,均P<0.05),其中ASCSm與LVEF相關性較高,其直線回歸方程為Y=-0.187X+27.502,見圖4。AS參數中AASm、IASm、ALASm、ASASm、PLASm、PSASm、APAS、GAS與LVEF均呈正相關(r=0.35、0.20、0.44、0.44、0.55、0.59、0.44、0.70,均P<0.05),其中GAS與LVEF相關性較高,其直線回歸方程為Y=0.457X-1.355,見圖5。RS參數中APRS、GRS與LVEF均呈負相關(r=-0.42、-0.34,均P<0.05),APRS與LVEF相關性較高,其直線回歸方程為Y=-2.989X+284.386,見圖6。
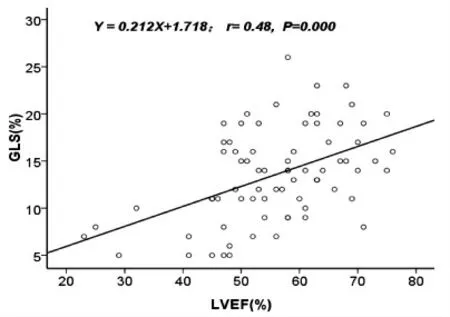
圖3 血液透析組整體心肌縱向應變(GLS)與左心室射血分數(LVEF)的散點圖
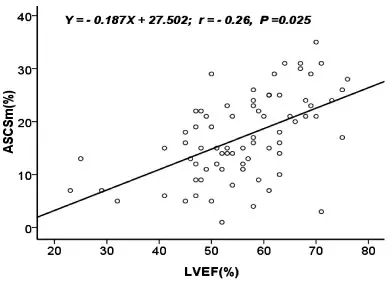
圖4 血液透析組前間隔中段圓周應變(ASCSm)與左心室射血分數(LVEF)的散點圖

圖5 血液透析組整體心肌面積應變(GAS)與左心室射血分數(LVEF)的散點圖
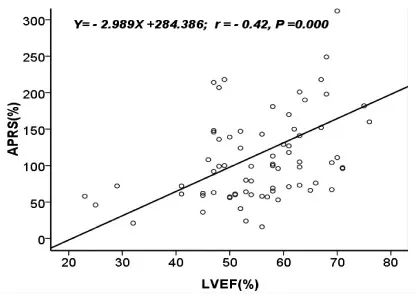
圖6 血液透析組心尖部徑向應變(APRS)與左心室射血分數(LVEF)的散點圖
2.4 ROC曲線分析 參照正常對照組,根據ROC曲線分析,不同左心室心肌四維應變參數預測血液透析組存在左心室心肌收縮功能不全,見表4。LS參數中PSLSm診斷效能較高,當界值為-17.50%時(負號代表心肌運動方向),AUC為0.850,靈敏度和特異度分別為0.824、0.756,見圖7;AS參數中GAS診斷效能較高,當界值為-29.50%時,AUC為0.876,靈敏度和特異度分別為0.743、0.911,見圖8;CS參數中ICSm診斷效能較高,當界值為-13.50%時,AUC為0.755,靈敏度和特異度分別為0.716、0.711,見圖9;RS參數中ARSm診斷效能較高,當界值為50.50%時,AUC為0.801,靈敏度和特異度分別為0.743、0.822,見圖10。
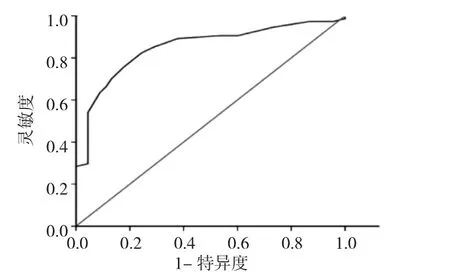
圖7 后間隔中段縱向應變預測維持性血液透析尿毒癥患者左心室心肌功能不全的ROC曲線
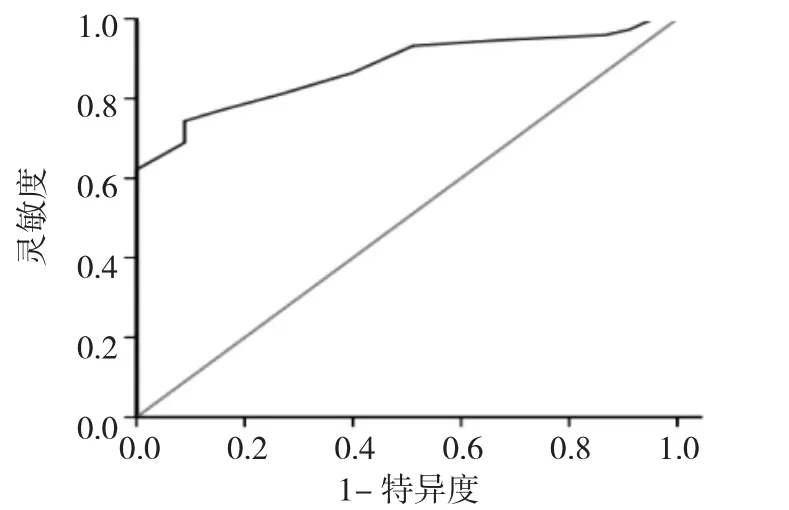
圖8 整體心肌面積應變預測維持性血液透析尿毒癥左心室心肌功能不全的ROC曲線
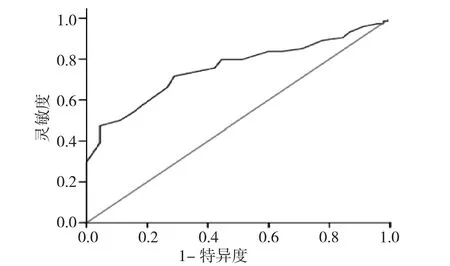
圖9 下壁中段圓周應變預測維持性血液透析尿毒癥患者左心室心肌功能不全的ROC曲線
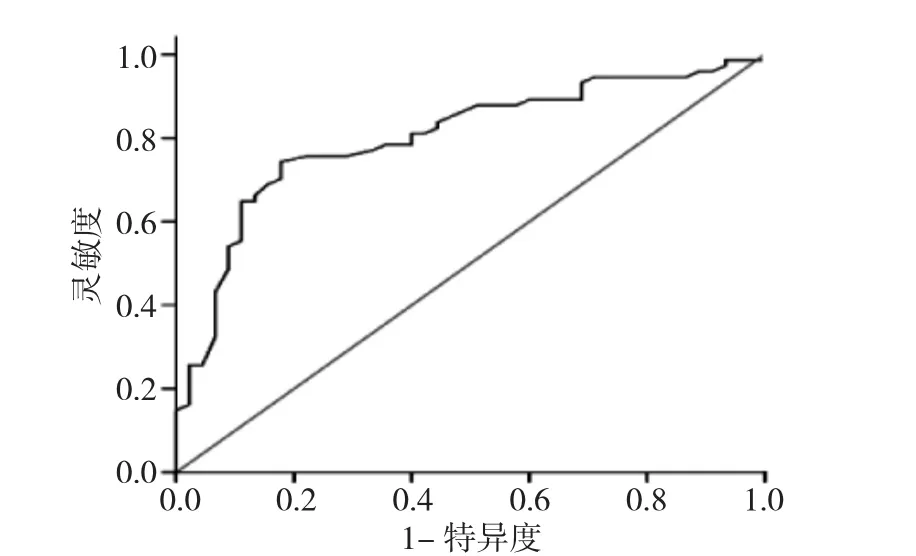
圖10 前壁中段徑向應變預測維持性血液透析尿毒癥左心室心肌功能不全的ROC曲線
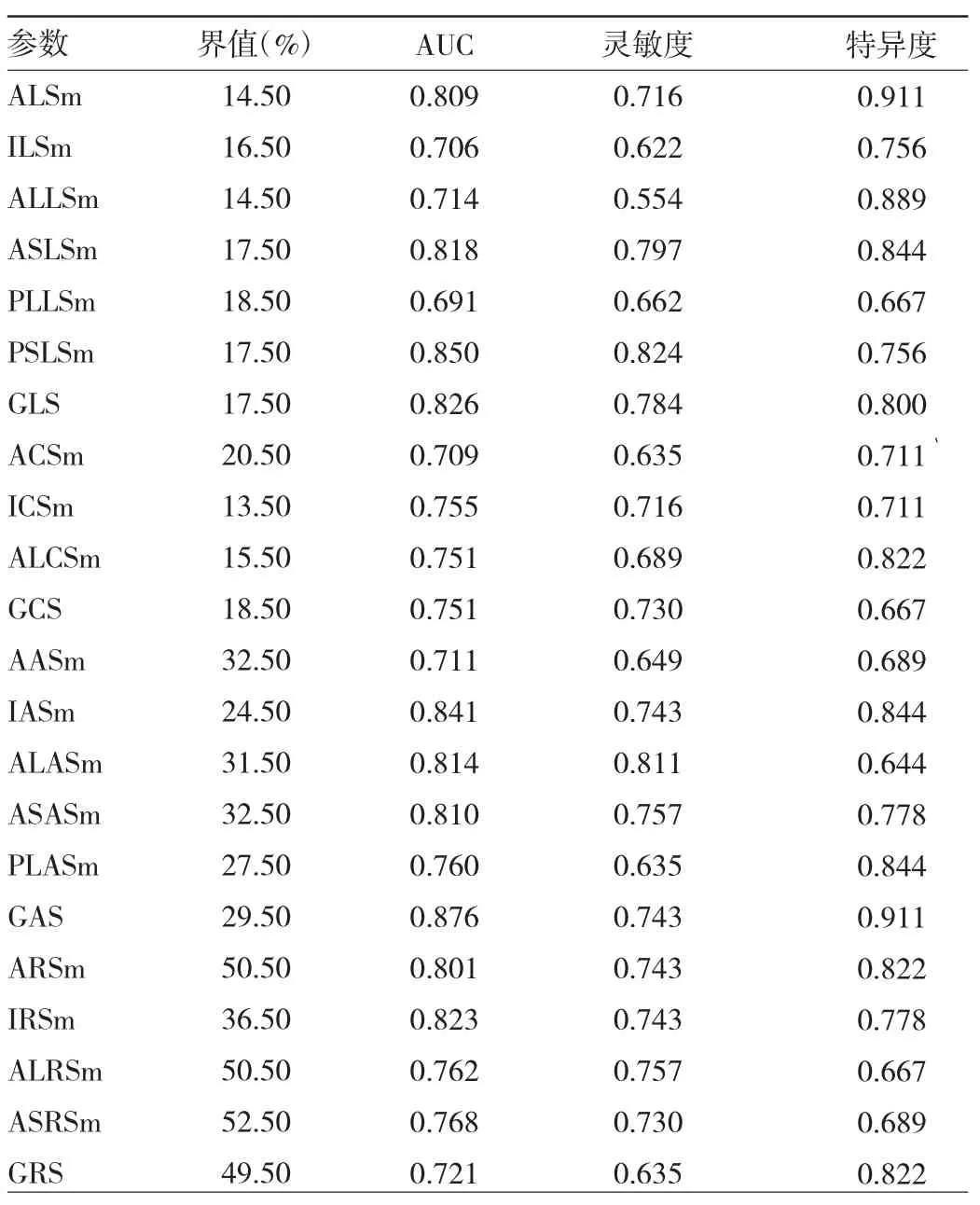
表4 血析透析組不同左心室心肌四維應變參數診斷界值
2.5 一致性分析 左心室心肌LS、AS、CS、RS參數的觀察者內ICC:觀察者內LS、CS、AS、RS分別為0.75±0.13、0.75±0.11、0.83±0.06、0.78±0.08(均P<0.01);觀察者間LS、CS、AS、RS分別為0.79±0.09、0.80±0.10、0.81±0.11、0.77±0.12(均P<0.01),在所有參數中,GLS的ICC最高,觀察者內為0.938,觀察者間為0.960,均P<0.01。
3 討論
3.1 四維應變參數評價維持性血液透析尿毒癥患者左心室心肌收縮功能的臨床意義 心肌由縱行纖維(70%)和環行纖維(30%)構成,縱行纖維與心肌縱向運動有關,環行纖維與心肌徑向、環向運動有關,LS、CS、RS分別反映縱向、環向、徑向心肌收縮功能[5]。對于縱向、圓周、徑向運動的測量,本研究采用四維斑點追蹤顯像技術,該技術是實時三維超聲心動圖與斑點追蹤技術結合發展起來的一項新技術,能夠快速地在三維空間上追蹤回聲斑點的運動軌跡,相比二維斑點追蹤顯像局限于二維平面的回聲斑點跟蹤技術,能夠更真實、準確地定量評價心臟整體、局部功能及心肌各節段的力學狀態[6]。
血液透析治療雖然可以直接清除部分尿毒癥毒素(如尿素氮、肌酐等),糾正電解質紊亂、酸堿平衡失調、減輕心臟前負荷,從而改善心功能[1]。但是未清除完的毒素(如本研究中的肌酐、尿素氮、β2微球蛋白、同型半胱氨酸、血甲狀腺素等測值遠高于參考值)等仍會對心臟進行持續影響。本研究發現,左心室心肌GLS、GCS、GAS、GRS以 及ALSm、ILSm、ALLSm、ASLS、PLLSm、PSLSm、ACSm、ICSm、ALCSm、ASCSm、PLCSm、AASm、IASm、ALASm、ASASm、PLASm、PSASm、ARSm、IRSm、ALRSm、ASRSm、PLRSm、PSRSm均小于正常對照組(均P<0.01),這說明維持性血液透析狀態下,左心室無論是縱向還是環向的整體心肌和絕大多數節段心肌收縮功能是減退的,其原因推測如下:首先,β2微球蛋白、同型半胱氨酸等分子毒素在體內的聚集可使患者出現微炎癥狀態,血管鈣化,動脈彈性消失,順應性降低,脈率加快,收縮壓增高[7],造成后負荷增大,心肌收縮射血受阻,從而使心肌形變減低。其次,過多的肌酐、尿素氮可使心肌膽堿脂酶活動度受抑制,心肌收縮力下降;甲狀旁腺素通過甲狀旁腺素相關蛋白受體作用于心肌細胞,導致細胞內鈣離子濃度升高,激活蛋白激酶c,引起代謝異常及心肌肥大,同時繼發性腎性高血壓也會引起左心室肥厚,而心肌細胞的肥大和肌纖維增粗,可使左心室心肌間質灶性纖維化,毛細血管相對密度減低,進而引起心肌缺血、缺氧,心肌的僵硬度增加[7],心肌收縮力減弱;另外,慢性貧血可引起心肌長期缺氧,退行性變性,心臟貯備功能減退[7],這些因素均可使心肌自身收縮性能減低,心肌應變測值降低。
對于維持性血液透析狀態下尿毒癥患者的左心室心肌功能不全的具體程度,結合本文ROC曲線分析,筆者初步擬定了以下診斷標準,僅供參考。當GLS<-17.50%時,可診斷左心室整體心肌出現縱向收縮功能不全;當GCS<-18.50%時,可診斷左心室整體心肌出現環向收縮功能不全;當GRS<49.50%時,可診斷左心室整體心肌出現徑向收縮功能不全;對于局部心肌的收縮功能評價,當PSLSm<-17.50%,可診斷左心室節段心肌存在縱向收縮功能不全;當ICSm<-13.50%可診斷左心室節段心肌存在環向收縮功能不全;當ARSm<50.50%時,可診斷左心室節段心肌出現徑向收縮功能不全。
3.2 維持性血液透析尿毒癥患者左心室心尖部心肌環向、徑向收縮功能增強 本研究發現,血液透析組APLS與正常對照組的差異無統計學意義(P>0.05),APCS、APRS均大于正常對照組(均P<0.05),這說明左心室心尖部心肌縱向收縮功能受損不明顯,而其環向、徑向收縮功能增強。其原因可能如下:首先,由于β2微球蛋白增高,可造成淀粉樣變物質沉積于心肌,該物質會首先沉積于心內膜下心肌,該物質對心肌LS的影響,文獻顯示其規律為早期心尖區LS在正常值范圍內,而心基底部及心中間部受累,心肌功能受損情況呈心尖區-心基底部階梯狀加重,即典型的“心尖部應變保留征象”[8],故本文的LS與正常對照組差異無統計學意義;其次,血液透析患者,動靜脈內瘺和貧血可造成回心血量增多,前負荷增加[7],本研究顯示,血液透析組LVEDV略高于正常對照組(P<0.01),根據長度-張力曲線,在最適初長度范圍內,心肌纖維隨初長度增加可增強心肌收縮[6],因此,前負荷增加對維持性血液透析患者心肌收縮還是具有正性作用。雖然在絕大多數節段心肌,此正性作用無法抵消后負荷增加和心肌自身收縮性能下降這兩者負性因素,而在心尖部可能由于是冠狀動脈末稍供血,心肌纖維可能受尿毒癥毒素侵襲較輕以及心尖離主動脈較遠,需主動收縮克服增大的后負荷來維持泵血所發揮的角色較弱,故心尖部各應變測值未低于正常對照組。由于縱行肌成份多于環行肌纖維,毒性物質侵襲縱行肌可能較重,環行肌相對較輕,故環行肌正性作用大于負性作用,故CS和RS測值增高,其收縮功能環向和徑向收縮功能顯示增強。
3.3 維持性血液透析尿毒癥患者的AS能較早反映左心室整體心功能減退 AS測量的是左心室內膜面面積縮小的百分率,該參數反映所分析節段或整體心內膜面積隨心肌運動而改變的程度,反映的是心肌在縱向、環向、徑向上的綜合運動[9]。相比于LS、CS、RS,AS參數更能全面反映左心室收縮功能[10]。本研究顯示GAS和左心室壁中間段所有心肌面積應變參數均與左心室整體收縮功能指標-LVEF呈正相關(GAS與LVEF相關性最高,達0.702;節段性心肌中,PSASm相關性最高達0.589,均P<0.05),相關性較LS、CS、RS參數要高,相關節段數也較其它參數多。這說明心肌面積應變能更好地反映左心室整體功能,隨著左心室心肌收縮功能不全的出現,心肌面積應變值降低,傳統心功能評價指標LVEF較其初始狀態也開始下降,然而本研究血液透析組的LVEF平均值達(55.86±11.11)%,絕大多數患者LVEF超過50%,左心室收縮功能在正常范圍,未達到整體心功能不全的程度,因此心肌面積應變參數能更早地反映左心室整體心功能開始減退。根據ROC曲線分析,當GAS<-29.50%、PSASm<-27.50%時可說明維持性血液透析尿毒癥患者左心室整體和局部心肌功能出現不全,其整體心功能也開始出現了相應地衰退。綜上所述,四維斑點追蹤技術能夠定性和定量評價維持
性血液透析尿毒癥患者左心室整體心肌和不同節段心肌的收縮功能,且通過心肌面積應變參數能反映整體心功能變化。但本研究仍存在局限性:肥胖、胸廓畸形、肺部疾病等患者所采集的四維全容積圖像清晰度較差,一定程度會影響四維斑點追蹤顯像技術分析結果;另外,本研究選擇樣本略顯不足,希望今后開展針對更多病例、更深層次的研究。

