肝癌與肺腺癌中FEN1的表達和預后分析
趙恒宇,鄭浩青,黃河儒,李維嘉,吳振興
(杭州醫學院,浙江 杭州 310053)
0 引言
肝癌已成為人類第四大死因,目前我國肝癌發患者數約占世界肝癌發患者數的50%[1,2]。肝癌病例中有75%-85%為肝細胞肝癌(hepatocellular carcinoma,LIHC)[3]。乙肝病毒、丙肝病毒、酗酒和馬兜鈴酸是LIHC的危險因素,這些因素將導致肝細胞損傷、炎癥反應激活、細胞死亡以及腫瘤進展[4,5]。目前,LIHC缺乏早期診斷標志物和特異性治療藥物[6]。
肺癌死亡率最高的癌癥,約85%的肺癌病例為非小細胞肺癌(non-small-cell lung cancer,NSCLC),而肺腺癌(lung adenocarcinoma,LUAD)是NSCLC中最常見的類型[7,8]。吸煙是肺癌的主要危險因素[9,10]。由于目前醫療技術的局限,大量肺癌患者確診時已為晚期[11]。
結構特異性核酸內切酶I(flap endonuclease 1,FEN1)基因定位于染色體11q12,在DNA復制、損傷修復、重組中起到重要作用[12,13]。有研究報道,FEN1過表達存在于多種腫瘤,提示FEN1過表達與腫瘤預后不良相關[14]。已有META分析證明FEN1與LIHC及LUAD相關[15-17]。
本研究使用ONCOMINE、DriverDBv3、人類蛋白質圖譜(The Human Protein Atlas,HPA)、GEPIA、Kaplan-Meier Plotter和UALCAN等數據庫和挖掘工具,探究FEN1表達在LIHC與LUAD中的預后價值。本研究也使用了STRING、Metascape、cBioPortal數據庫等網絡工具對FEN1進行蛋白互作分析、富集分析、突變分析。研究結果表明,FEN1是LIHC和LUAD的潛在診療與預后的生物標志物。
1 方法
1.1 FEN1表達差異分析
ONCOMINE(https://www.oncomine.org)是一個癌基因和癌基因組數據庫[18]。為獲取FEN1在肝癌和肺癌中及正常組織中的表達數據,我們設定數據將篩選條件如下:①Gene:FEN1;② Analysis Type:Cancer vs.Normal Analysis;③ Data Type: mRNA;④臨界值設定條件:P<0.01,Fold Change>1.5,Gene Rank:10%。
DriverDBv3(http://driverdb.tms.cmu.edu.tw)是一個癌癥組學數據庫[19]。本研究使用DriverDBv3分析FEN1基因在原發性LIHC和LUAD中表達與在正常樣本中表達的差異。
UALCA(http://ualcan.path.uab.edu)是一個交互式的癌癥組學數據庫,收錄了癌癥基因組圖譜(The Cancer Genome Atlas,TCGA)等多數據庫資源[20]。本研究使用UALCAN分析FEN1在正常樣品與腫瘤樣品中差異表達。
HPA數據庫(http://www.proteinatlas.org)是一個旨在構建細胞、組織、器官中蛋白質圖譜的數據庫[21-23]。本研究從HPA中下載肝癌、肺癌組織,以及正常肝組織、肺組織中免疫組化圖片并對其進行分析。
1.2 FEN1表達差異的生存分析
GEPIA(http://gepia.cancer-pku.cn/index.htmL)是一個聚合了腫瘤樣本和正常樣本的RNA測序表達的數據庫[24]。本研究利用GEPIA分析FEN1高表達與低表達對LIHC、LUAD患者生存的影響。
The Kaplan-Meier Plotter(https://kmplot.com/analysis)是一個評估基因表達或突變對患者生存的影響的在線工具[25-27]。本研究使用該數據庫驗證了FEN1表達水平高低對肝癌和肺癌患者生存的影響。
1.3 FEN1的蛋白互作分析、富集分析、突變分析
STRING(https://string-db.org)是一個分析蛋白質-蛋白質相互作用(protein-protein interactions,PPI)的數據庫[28,29]。本研究使用STRING分析FEN1的20個相關蛋白的相互作用。
Metascape(https://metascape.org)是一個提供富集分析、PPI分析、基因注釋等功能的在線工具[30]。本研究將STRNG中獲取的20個FEN1相關蛋白進行功能富集分析。
癌癥基因組學的生物門戶(cBioPortal for Cancer Genomics,cBioPortal)是一個多組學數據庫[31]。本研究使用cBioPortal評估FEN1突變對于患者生存時間的影響。研究中將篩選數據的條件設定如下:①Genomic Profiles:Mutation,copynumber alterations from GISTIC,mRNA Expression z-Scores(RNASeq V2 RSEM);② z-score threshold:±1.8。
2 結果
2.1 FEN1在正常與腫瘤組織中的表達差異
對ONCOMINE數據庫中肝癌和肺癌的芯片進行分析。與正常組織相比,FEN1在肝癌與肺癌組織中呈現高表達(圖1A)。通過DriverDBv3分析,FEN1在原發性LIHC和LUAD中表達顯著高于正常組織(圖1B)。通過UALCAN數據庫對TCGA中樣本進行定量分析(圖1C),FEN1在LIHC樣品中表達顯著高于正常組織(P<0.05),FEN1在LUAD樣品中表達也顯著高于正常組織(P<0.05)。通過分析HPA數據庫中免疫組化圖片,FEN1在肝癌與肺癌組織中均為高表達,在正常肝組織與肺組織中均為中表達(圖1D)[21-23]。因此,FEN1在LIHC與LUAD中均存在高表達情況。
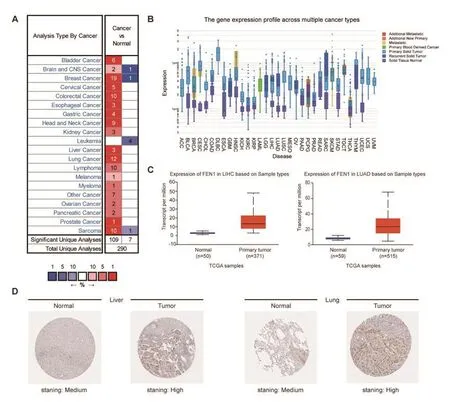
圖1 FEN1在肝癌、肺癌、正常組織中表達差異分析
2.2 FEN1表達差異的生存分析
GEPIA數據庫結果顯示,FEN1表達水平與LIHC和LUAD患者預后相關(圖2)。LIHC中FEN1高表達與患者總生存期(Overall Survival,OS)和無病生存期(Disease-Free Survival,DFS) 相 關(OS log-rankP=0.022,HR=1.5;DFS log-rankP=0.0075,HR=1.5)(圖2A、B)。LUAD 患者FEN1高表達與OS相關,但FEN1表達高低對DFS造成的差異無統 計 學 意 義(OS log-rankP=0.027,HR=1.4;DFS log-rankP=0.63,HR=1.1)(圖2C、D)。
我們使用Kaplan-Meier Plotter驗證GEPIA結果,LIHC中FEN1高表達與OS和DFS相關(OS log-rankP=3.4e?06,HR=2.28;DFS log-rankP=0.0095,HR=1.54)(圖2E、F);LUAD患者FEN1高表達與OS和DFS也相關(OS log-rankP=0.00093,HR=1.66;DFS log-rankP=0.041,HR=1.75)(圖2G、H)。
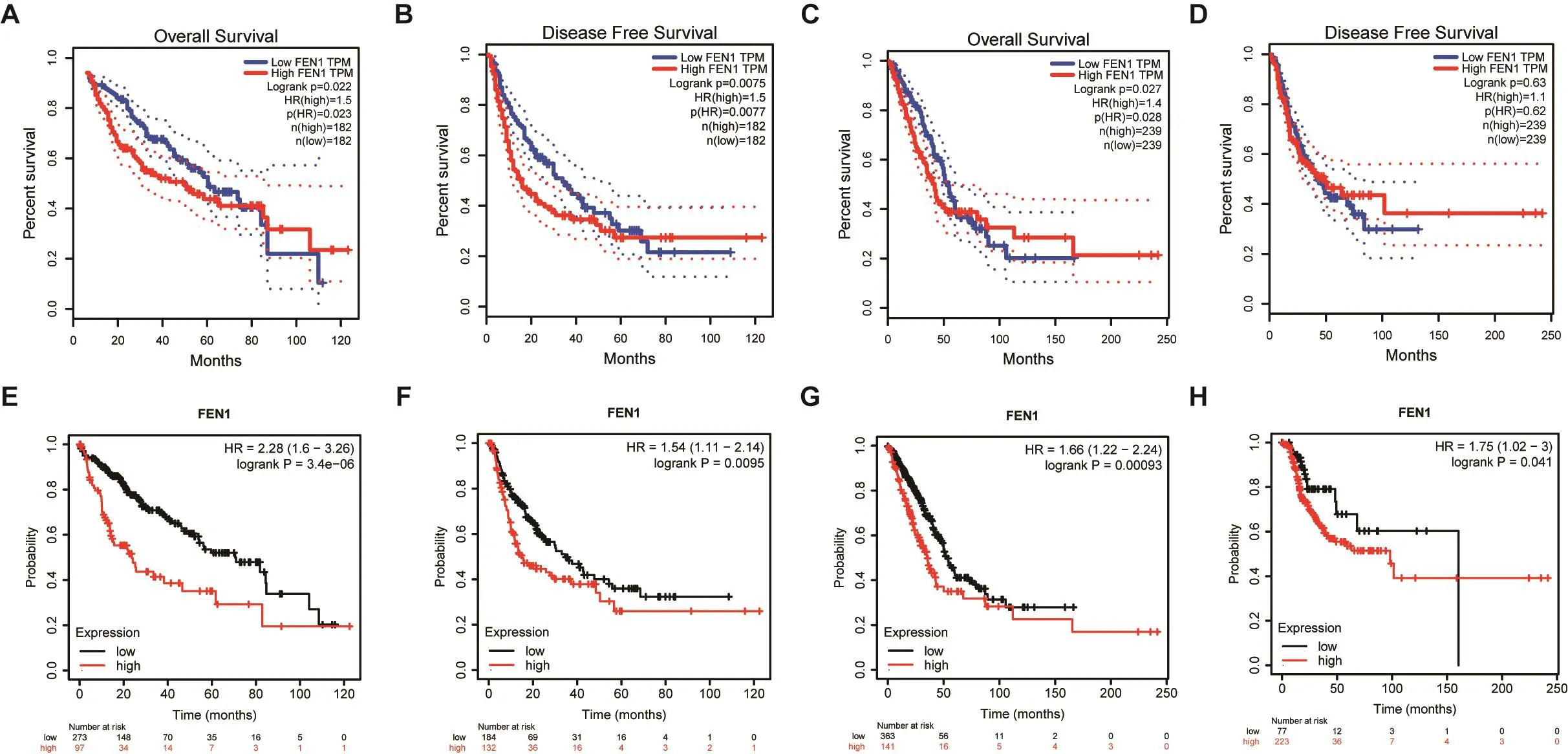
圖2 FEN1表達差異的生存分析
綜合兩個數據庫的分析結果,FEN1表達水平可作為預測LIHC和LUAD患者生存狀況的標志物。
2.3 FEN1的PPI、富集、突變分析
通過STRING構建了FEN1及20個相關蛋白的PPI網絡(圖3A),在Metascape中進行了基因本體(Gene Ontology,GO)和京都基因與基因組百科全書(Kyoto Encyclopedia of Genes and Genomes pathways,KEGG)分 析(圖3B、C、D),FEN1及相關蛋白主要功能為DNA修復(GO:0006281)、DNA 鏈延伸(R-HSA-69190)、DNA 重組(GO:0006310)等功能。通過cBioPortal分析發現,FEN1突變情況對LIHC患者的DFS長短造成的差異有統計學意義(P<0.05)。
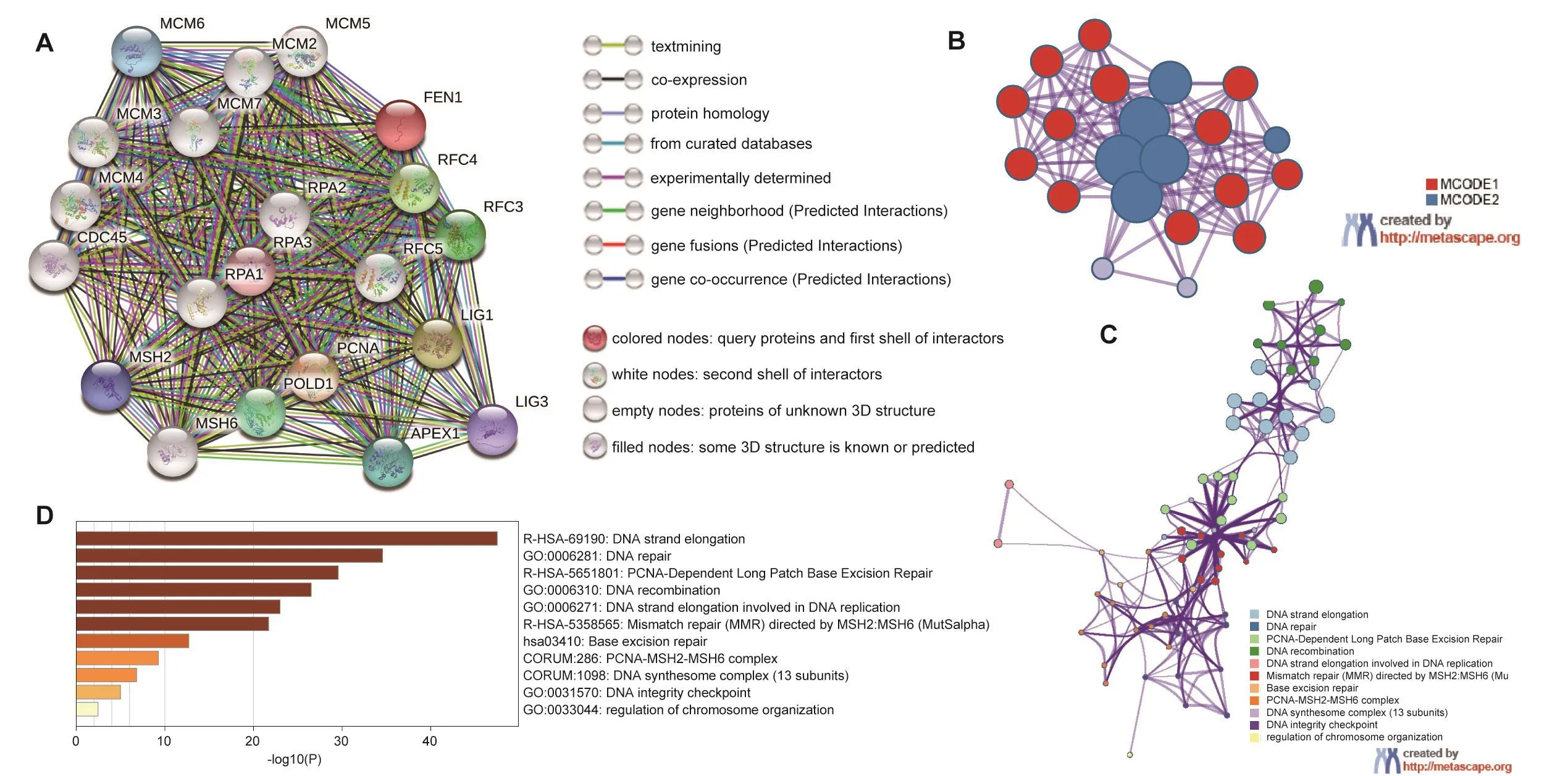
圖3 FEN1的PPI分析和富集分析
3 討論
目前,肝癌和肺癌分別已成為中國人位居第三大、第五大的死因[32]。由于缺乏早期診斷標志物、預后標志物和靶向藥物,肝癌和肺癌患者生存期較短[6,11]。因而尋找肝癌和肺癌的標志物及靶向藥物,是腫瘤研究領域亟待解決的問題。
FEN1是5’核酸酶超家族成員,它參與了岡崎片段成熟、長堿基切除修復RNA引物在后隨鏈復制中的移動、維持端粒長度等功能[33]。因此,FEN1為細胞正常運行提供必要的支持。
本研究分析了FEN1在LIHC和LUAD中的功能、表達及預后價值。其中運用了多組學對FEN1表達進行分析,發現FEN1在LUAD與LIHC中確實存在高表達。本研究還分析了FEN1表達高低對于患者生存期的影響。GEPIA數據庫表明,FEN1高表達與LIHC預后不良相關;Kaplan-Meier Plotter數據庫表明,FEN1高表達與上述兩種癌癥預后不良都有相關性。綜上所述,FEN1表達水平也可作診斷與治療的潛在標志物,可為醫生制定治療策略提供參考。研究也發現FEN1突變與LIHC患者無病生存期相關,提示FEN1突變情況可作為預測LIHC的潛在標志物。
盡管本研究通過多個數據庫進行多組學分析,但仍存在著局限性。一是,FEN1的mRNA 表達差異樣本量較小;二是沒有使用META分析對FEN1在LIHC和LUAD中診斷價值進行評估。我們在近期聚焦于體外實驗,以完善數據庫分析所存在的不足,期待更好地說明FEN1表達與兩種類型惡性腫瘤的相關性。但總的來說,FEN1可成為肝細胞肝癌和肺腺癌潛在的預后和診療生物標志物。

