杜仲預處理對腦缺血再灌注損傷保護作用的最佳劑量探討
杜芬,裴園利,薛瑤瑤,柏魯寧
(1.陜西中醫藥大學,陜西 咸陽 712000;2.陜西中醫藥大學附屬醫院,陜西 咸陽 712000)
缺血性卒中是一種臨床常見的神經系統疾病,具有高發病率、死亡率、致殘率等特點,且以老年人居多[1]。此病目前臨床最有效的治療手段是使缺血區重新獲得血氧供應,但血液恢復灌注這一舉措會相應出現更加嚴重的腦功能障礙,即腦缺血再灌注損傷(cerebral ischemia reperfusion injury,CIRI)[2]。CIRI是一種不可逆損傷,發生后會導致神經細胞損傷,造成神經功能缺損,其病理機制復雜,目前臨床沒有特效藥物,許多研究者將目光投向中醫藥。杜仲(EucommiaulmoidesOliv)是我國傳統名貴滋補中藥材之一,現代藥理學研究發現,杜仲的莖、根中富含苯丙素類化學成分[3],具有顯著的降血脂、降血壓及提高免疫力等活性,而其中化學成分咖啡酸和阿魏酸對體外微血管內皮細胞損傷具有明顯保護作用[4],對改善缺血區的神經元,修復神經損傷具有一定的作用。本研究通過探討杜仲不同劑量預處理對大鼠腦缺血再灌注保護作用的影響,旨在探討杜仲對腦組織起保護作用的最佳劑量。
1 材料與方法
1.1 實驗藥物
實驗所用中藥生杜仲由陜西中醫藥大學附屬醫院中藥房提供,經陜西中醫藥大學生藥教研室鑒定,符合國家標準。生杜仲煎煮之前先用涼水浸泡30 min,水面沒過藥物大拇指一橫指即可,煎藥濃縮成生藥濃度為 1 g/mL,趁熱過濾方可,置于4 ℃冰箱保存。尼莫地平片(山西亞寶藥業集團股份有限公司,生產批號:180813)同購自陜西中醫藥大學附屬醫院。
1.2 實驗動物及分組
SD清潔級雄性大鼠,體質量260~280 g,由成都達碩實驗動物有限公司提供,合格證號:SCXK(川)2015-030,統一飼養于陜西中醫藥大學中藥藥理實驗室,飼養環境符合規定,分籠飼養,飲食和飲水自由,室內溫度23~26 ℃。大鼠按隨機數字表共分為6組:假手術組、模型組、陽性藥物組、杜仲低劑量組、杜仲中劑量組及杜仲高劑量組,每組10只。
1.3 主要實驗試劑、耗材與儀器
蘇木素伊紅染色試劑盒(HE)、4%多聚甲醛、10%水合氯醛均購自武漢博士德生物工程有限公司; MCAO線栓購自平頂山豫順生物科技有限公司;電子天平,梅特勒-托利多儀器(上海)有限公司;Morris水迷宮系統,上海欣軟信息科技有限公司;4 ℃冰箱,中國海爾(Haier)公司。
1.4 動物預處理與模型制備
動物適應性飼養5 d后,按照陽性藥物組(10 mg/kg)、杜仲低劑量組(2 g/kg)、杜仲中劑量(4 g/kg)及高劑量組(8 g/kg)灌胃給藥,每日1次,連續14 d,保證藥物適宜的溫度與統一的濃度,在灌胃過程中避免操作不當藥物流失,如若發生補足流失劑量。大鼠術前均禁食12 h,自由飲水,采用新進改良Zea-Longa 線栓法[5]制備腦缺血再灌注損傷模型,統一采用腹腔注射10%水合氯醛0.35 mL/100 g麻醉大鼠,麻醉后將大鼠仰面四肢固定于木板上,按照個人操作習慣選擇頭尾固定方向,常規備皮消毒后找到頸總、頸內和頸外動脈,插入線栓使其由頸總經過頸內到達大腦中動脈,控制線栓插入時間,不宜進入時可用利多卡因浸潤頸總動脈達到擴血管作用,固定線栓,縫合消毒, 2 h后拔出線栓,實現再灌注。假手術組不插入線栓,其余步驟與手術組相同。大鼠蘇醒后觀察大鼠是否具備造模成功標志,對沒有癥狀及意外死亡的大鼠取同批次SD大鼠按相應的組別要求造模以補足實驗大鼠只數。
1.5 觀察指標及檢測方法
1.5.1 神經功能評分
再灌注24 h后采用Zea-Longa評分法評估大鼠神經功能缺損評分,對于可自由活動、直線行走及行為正常等無神經功能缺損癥狀者計0分;對于無法伸展對側前爪或不能完全伸展,伴有輕度神經功能缺損者計1分;對于行走時身體向偏癱一側轉圈,達到中度神經功能缺損癥狀者計2分;對于行走時向偏癱一側傾斜或傾倒,達到重度神經功能缺損者計3分;對于意識喪失、無法自發行走者計4分。
1.5.2 大腦含水量
大鼠再灌注24 h后,開顱取腦,去除小腦和嗅球部分,用生理鹽水將表面血漬沖洗干凈,用濾紙吸干表面水分,精準稱量后所得數據計為濕重,后將腦組織置于110 ℃恒溫干燥箱干烤24 h,并準確稱取腦組織所得數據計為干重,腦含水量(%)=(濕重-干重)/濕重×100%。
1.5.3 Morris水迷宮實驗
Morris水迷宮實驗裝置為一圓柱形水池,池內平臺可移動,實驗時固定到某一象限不動,水位高于平臺 1.5 cm,水溫需維持在(25 ±1) ℃。造模前5 天對所有大鼠進行第一階段水迷宮實驗訓練(定位航行試驗),每天分別從第1、4象限將大鼠放入水中訓練2次,間隔時間為15 min,規定設置時間90 s/次,若在90 s內順利找到平臺者,終止實驗,未找到平臺者,引導其上臺后停留10~15 s,以此加深大鼠記憶。第6天連接電腦詳細記錄定位航行實驗相關數據,并進行第二階段測試(空間探索實驗),我們將平臺撤離并選取原平臺所在鄰象限或者對象限作為入水點,記錄90 s內大鼠通過平臺所在象限的次數以及記錄停留平臺所在象限的時間。造模后24 h重復定位航行及空間探索實驗,完成后通過數據整理對比造模前后大鼠空間學習探索記憶功能的差異。實驗結束后的大鼠需要立即采取保暖措施,實驗過程中,必須保持環境的絕對固定性和安靜隱蔽性,實驗人員不能隨意走動,防止給大鼠形成空間記憶標志物。
1.5.4 腦組織病理學觀察(HE染色)
先取各組自額極起第4片腦片,用甲醛溶液固定24 h以上。修整組織塊,標記。然后依次進行脫水、透明、浸蠟、包埋、切片、染色、后再脫水、透明,中性樹膠封固。
1.6 統計學方法
2 結果
2.1 不同劑量杜仲預處理對CIRI大鼠神經功能及腦含水量的影響
模型制備成功后,大鼠會出現不同程度運動障礙,主要表現為對側前爪不能伸展、行走時身體向偏癱一側轉圈、傾斜或傾倒。模型組大鼠神經功能評分最高,為(2.70±0.48)分,與模型組比較,杜仲低劑量組大鼠神經功能評分降低,但差異無統計學意義;杜仲中、高劑量組和陽性藥物組大鼠神經功能評分明顯下降,且差異有統計學意義(P<0.05)。各組大鼠腦含水量存在差異,模型組大鼠腦含水量最高,為(88.05±0.87)%,與假手術組相比較,差異有統計學意義(P<0.05)。與模型組比較,杜仲低劑量組大鼠腦含水量降低,但差異無統計學意義(P>0.05);杜仲中、高劑量組和陽性藥物組大鼠腦含水量明顯下降,且差異有統計學意義(P<0.05),詳見表1。
表1 杜仲對CIRI大鼠神經學評分及腦含水量的影響
2.2 不同劑量杜仲預處理對CIRI后大鼠空間學習記憶功能的影響
2.2.1 定位航行實驗
在訓練5 d后進行數據記錄,術前與假手術組比較,模型組、陽性藥物組和杜仲低、中、高劑量組大鼠的逃避潛伏期與活動總路程無顯著差異(P>0.05)。再灌注24 h后,模型組大鼠逃避潛伏期與活動總路程最長,分別為(69.82±30.24)s,(1 156.03±642.78)mm。與模型組比較,杜仲低劑量組大鼠逃避潛伏期與活動總路程縮短,但差異無統計學意義(P>0.05);杜仲中、高劑量組與陽性藥物組大鼠逃避潛伏期與活動總路程明顯縮短,且差異有統計學意義(P<0.05),詳見表2,圖1。
表2 杜仲對大鼠術后定位航行實驗活動總路徑和潛伏期的影響
2.2.2 空間探索實驗
就游泳軌跡而言,經過5 d的訓練,各組在術前的游泳軌跡差別不明顯;術后與模型組相比較,杜仲中、高劑量及陽性藥物組目標明確,向著平臺游泳,且活動范圍大,空間探索趨勢明顯,見圖1;再灌注24 h后,各組間大鼠穿越平臺次數和所在平臺停留時間存在差異。模型組大鼠穿越平臺次數最少為(0.90±0.74)次,所在平臺停留時間最短為(17.32±8.24)s,與模型組比較,杜仲低劑量組大鼠穿越平臺次數增加,所在平臺停留時間延長,但差異無統計學意義(P>0.05);杜仲中、高劑量組和陽性藥物組大鼠穿越平臺次數明顯增加,所在平臺停留時間明顯延長,且差異有統計學意義(P<0.05),詳見表3。
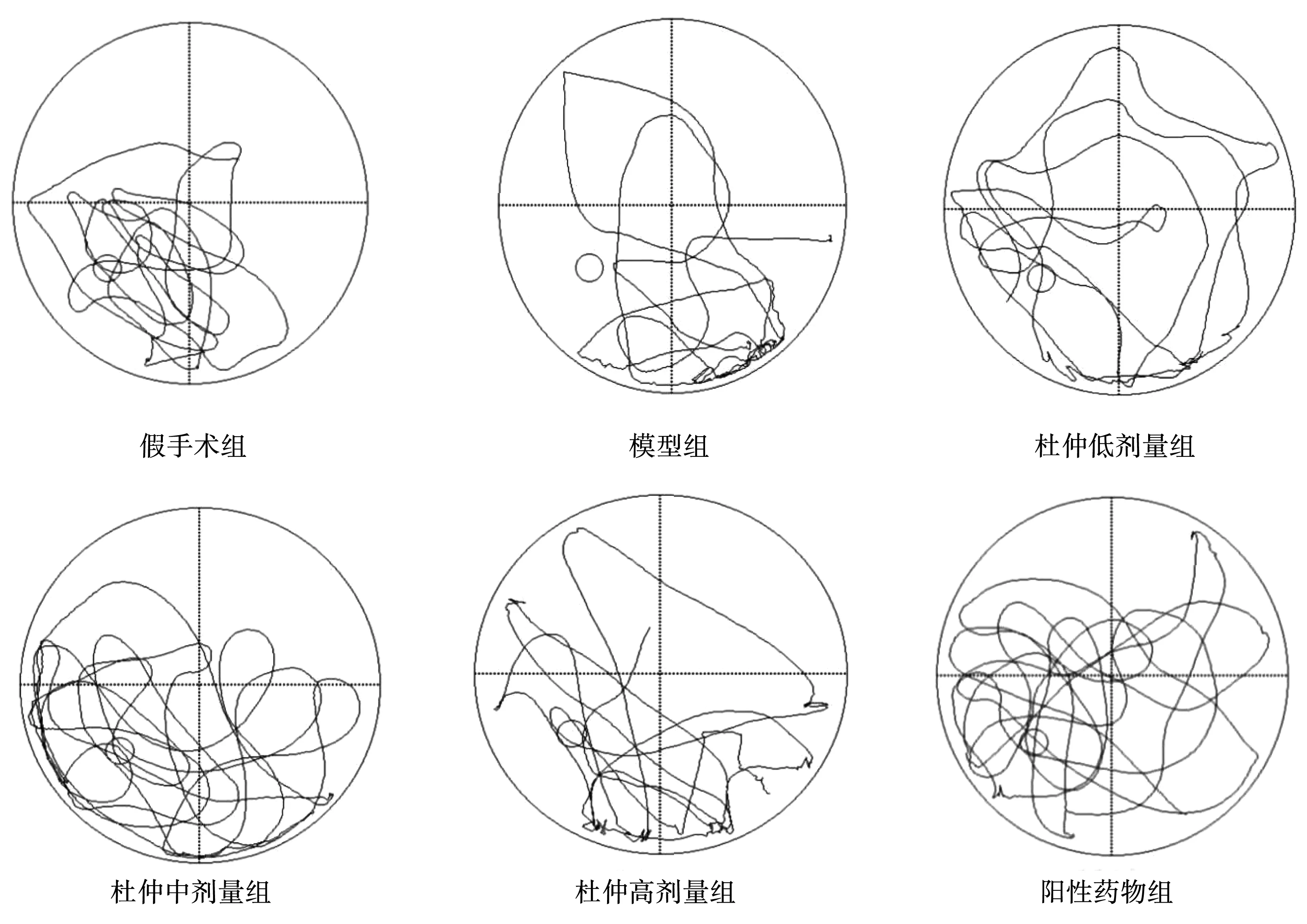
圖1 術后各組大鼠空間探索軌跡圖
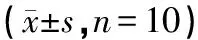
表3 杜仲對大鼠術后空間探索實驗中穿越平臺次數和所在平臺停留時間的影響
2.3 各組對腦組織病理學改變的影響 (HE染色)
如圖2顯示,假手術組皮層結構緊密,神經元分布均勻;模型組皮層軟化,結構疏松,呈碎片狀,神經元數量減少,多無完整的細胞結構,呈不同程度的壞死,胞核固縮深染,胞質胞核界限不清,腦膜斷裂,腦膜處及血管周圍可見少量炎性細胞浸潤;杜仲低劑量組組織多見毛細血管周圍間隙變大,腦膜多見水腫,結構疏松,腦膜血管擴張神經元數量輕度減少且排列不規則;杜仲中劑量組組織可見血管擴張,毛細血管周圍間隙變大,水腫,結構疏松。杜仲高劑量組及陽性藥物組皮層結構緊密,神經元分布均勻,出現少量神經元緊縮深染,未見神經元明顯腫脹或壞死。
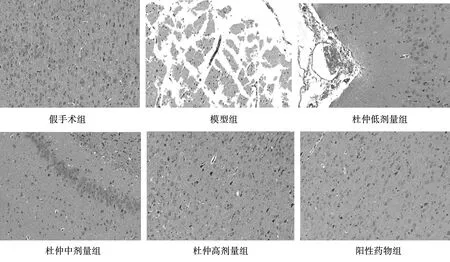
圖2 CIRI后各組大鼠皮層腦組織病理改變(HE,×20)
3 討論
CIRI是一種繼發性損傷,常常會導致不可逆的腦組織損傷,其發病機制目前尚未完全闡明,可能與氧化應激、內質網應激、自噬、細胞凋亡等密切相關[6]。現代藥理學研究表明杜仲具有擴張血管、抗菌、抗炎、鎮痛等多種藥理作用[7],更有研究表明杜仲在保護神經元方面具有較好的效果,證實其成分綠原酸能夠抑制LPS誘導的小膠質細胞活化、NO的產生、IL-1β及TNF-α的釋放,充分發揮對神經的保護作用[8]。本研究結果也表明,杜仲能減輕腦缺血大鼠的神經功能障礙,且隨著劑量增加,效果更加顯著。
腦水腫是腦缺血性疾病功能障礙的主要原因,惡性腦水腫也是腦缺血患者死亡的主要原因,是其最嚴重的并發癥之一[9]。本研究發現模型組大鼠腦含水量明顯升高,給予杜仲預處理后,可降低腦缺血大鼠的腦含水量,且具有一定的量效關系。臨床研究表明缺血性腦卒中患者常存在包括記憶紊亂在內的認識障礙、精神運動速度和執行功能下降[10-11],有研究指出腦缺血后神經認知功能的障礙與海馬受損神經元的數目有密切關聯[12-13]。本實驗發現模型組大鼠逃避潛伏期及活動總路程明顯延長,穿越平臺次數明顯減少,平臺所在停留時間明顯縮短,給予杜仲預處理后,大鼠逃避潛伏期及活動總路程降低,穿越平臺次數增加,平臺所在停留時間延長,且高劑量效果明顯,具有一定的量效關系,說明杜仲可明顯改善CIRI大鼠的認知能力。
針對劑量的選擇,我們通過藥理實驗中動物與人體間的等效劑量的換算,再聯合藥物及動物本身特性并參考相應文獻在發揮藥效的基礎上逐漸規律性加大劑量范圍,以此探討并提出一個“最佳”劑量[14],本實驗結果顯示8 g/kg杜仲預處理可明顯改善腦缺血大鼠的神經功能評分、降低大腦含水量及改善學習記憶能力。
杜仲對CIRI大鼠具有一定的保護作用,能降低腦缺血大鼠神經功能障礙、降低大腦含水量、改善學習記憶能力,且存在一定的量效關系,8 g/kg杜仲預處理效果最佳。但杜仲藥理成分復雜,到底何種有效成分發揮作用,其具體的機制是什么,都需進一步深入研究。

