中華蛸寄生叢集球蟲(頂復亞門: 叢集球蟲科)新種的形態學與分子生物學研究*
任 靜 何衛彤 王麗華 唐 艷 鄭小東①
(1. 中國海洋大學海洋生物多樣性與進化研究所 青島 266003;2. 中國海洋大學海水養殖教育部重點實驗室 青島 266003)
中華蛸(Octopus sinensisd’Orbigny, 1841)隸屬于軟體動物門(Mollusca)、頭足綱(Cephalopoda)、八腕目(Octopoda)、蛸科(Octopodidae)、蛸屬(Octopus), 主要分布在太平洋西北部(Guerraet al, 2010; Gleadall,2016), 曾被認為是真蛸(O. vulgarisCuvier, 1797)的同物異名(Warnkeet al, 2004; Okumuraet al, 2005;Iglesiaset al, 2007)。近年來, 基于形態特征和分子生物學分析, 從物種水平上將中華蛸與真蛸分開(Guerraet al, 2010; Amoret al, 2014; Gleadall, 2016)。中華蛸生長快, 具有重要的商業價值和開發潛力(Garridoet al, 2018; Danet al, 2019)。近幾年, 有關中華蛸養殖和餌料選擇(Danet al, 2018, 2019)、分類研究(Amoret al, 2017)等方面的研究相繼開展, 但有關中華蛸寄生蟲和疾病診斷等方面鮮有報道。
叢集球蟲隸屬于粘孢子總門(Myzozoa)、頂復亞門(Apicomplexa)、類錐體綱(Conoidasida)、真球蟲目(Eucoccidiorida)、叢集球蟲科(Aggregatidae)、叢集球蟲屬(Aggregata), 是頭足類消化道中一類常見的寄生蟲(Castellanos-Martínezet al, 2019)。叢集球蟲的生命周期包括無性生殖階段和有性生殖階段, 無性生殖又稱為裂體生殖, 有性生殖階段包括配子生殖和孢子生殖, 在孢子生殖階段, 叢集球蟲的成熟卵囊內包含大量的孢子囊, 孢子囊中有子孢子。叢集球蟲營異主寄生(Dobell, 1925; Hochberg, 1990), 在其生活史中,無性生殖階段寄生在中間宿主-甲殼類動物中, 有性生殖階段寄生在終宿主-頭足類動物中(Dobell, 1925;Gestalet al, 2002), 具有感染性的子孢子包含在孢子囊中, 這些孢子囊可通過頭足類動物的糞便釋放到海洋中進而感染甲殼類中間宿主(Castellanos-Martínezet al, 2019)。
目前, 有關叢集球蟲的記錄有限, Poynton 等(1992)通過石蠟切片對Aggregata dobelli和A.millerorum的表型特征進行描述。Gestal 等(1999)通過掃描和透射電子顯微鏡及原子力顯微鏡技術研究了A. octopiana孢子發育階段的不同形態和細胞學結構。隨著分子生物學的發展, 分子標記技術為頭足類寄生蟲形態學鑒定與診斷提供了新手段, 成為分類學的重要補充。Kope?ná 等(2006)分析了寄生于頭足類中的叢集球蟲屬的系統發育關系, 首次分析了叢集球蟲的系統發生地位。隨后, 相關研究結合表型特征及18S rRNA 核苷酸序列成功鑒定出叢集球蟲屬Aggregata eberthi及A. octopiana兩新種, 并對發生在歐洲水域的這兩種叢集球蟲的系統發育狀況進行了評估(Castellanos-Martínezet al, 2013; Tedescoet al,2017)。近年來, 在東北太平洋、東北大西洋、西北印度洋、西南大西洋、西地中海等海域均有叢集球蟲的報道(Labbé, 1895; Narasimhamurti, 1979; Poyntonet al, 1992; Gestalet al, 2000, 2005, 2010; Sardellaet al,2000), 然而國內對于叢集球蟲的研究較少, Ren 等(2019)在大規模死亡的短蛸中發現了叢集球蟲, 截至目前, 于長蛸和短蛸中鑒定出一個叢集球蟲新種(任靜, 2021)。本研究在中華蛸體內鑒定出的叢集球蟲為一新種, 是對叢集球蟲屬生物學資料的補充, 同時也為中華蛸疾病診斷和組織病理學研究提供參考。
1 材料與方法
1.1 樣品采集
野生中華蛸采自福建連江(26°16′N, 119°47′E)以及浙江南麂島(27°29′N, 121°01′E), 經解剖觀察, 被叢集球蟲感染的中華蛸個體共31 只, 主要感染位置為中華蛸消化系統中的盲囊和腸。被感染中華蛸的胴背長、體重、采集地等信息均被詳細記錄(表1)。
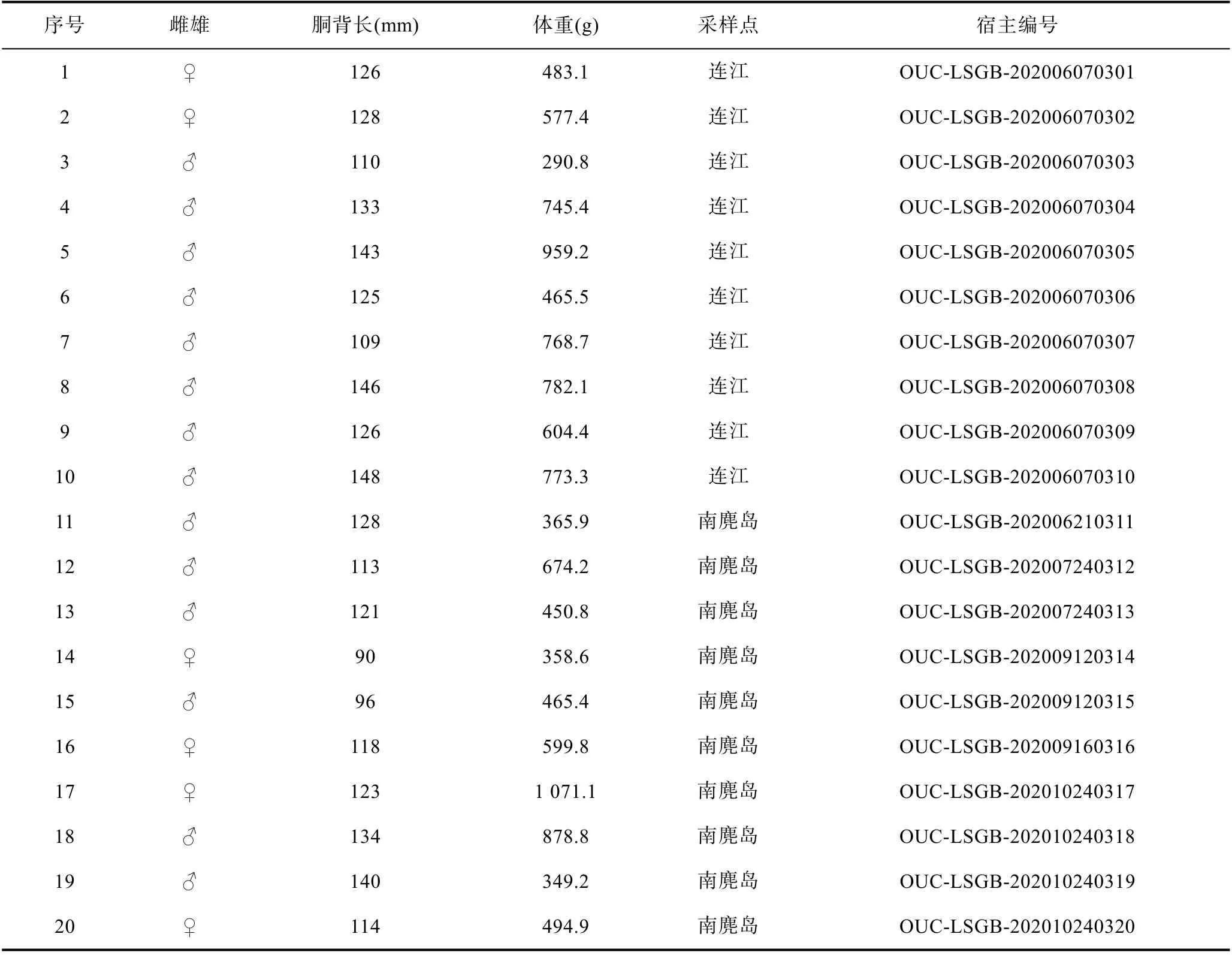
表1 被叢集球蟲感染的中華蛸樣品信息Tab.1 Sampling information of O. sinensis infected by Aggregata

續表
1.2 形態學鑒定
從鮮活中華蛸盲囊中分離出卵囊, 制成臨時玻片標本, 采用光學顯微鏡(Olympus BX53)下觀察其形態特征并拍照, 測定叢集球蟲孢子生殖階段的卵囊、孢子囊和子孢子各項形態特征數據。對卵囊、孢子囊和子孢子進行測量, 用微米(μm)表示, 并計算其平均值和標準偏差。將嚴重感染的盲囊和腸組織固定于波恩試劑中, 乙醇梯度脫水, 石蠟包埋, 使用切片機(Leica RM2016)切片。切片厚度為5 μm, 用蘇木精和伊紅染色(Cullinget al, 1985), 制成永久玻片標本,然后觀察孢子囊內的子孢子, 拍照并統計數目。
掃描電鏡(SEM)樣品取自宿主盲囊, 將叢集球蟲的白點狀卵囊置于2.5%戊二醛固定液中固定4 h, 用勻漿法制備分離的孢子囊。乙醇梯度脫水, 分離的孢子囊用液態CO2進行臨界點干燥, 噴金鍍膜處理后(Gestalet al, 1999)用掃描電子顯微鏡(VEGA3)觀察并拍照。透射電鏡(TEM)樣品為分離的叢集球蟲卵囊,置于2.5%戊二醛中固定4 h, 清洗后置于鋨酸固定液中, 乙醇梯度脫水, 包埋, 通過鉆石刀切片并進行染色, 用透射電子顯微鏡(JEM1200)電鏡下觀察。
1.3 分子生物學鑒定
叢集球蟲卵囊中提取總DNA。取大約50 mg 卵囊懸浮于600 μL 提取緩沖液中, 使用超聲波細胞破碎儀破碎, 加入蛋白酶K 消化過夜, 參照苯酚-氯仿法提取DNA (Sambrooket al, 1989), 質量檢測合格后的DNA 置于–20 °C 保存備用。
對基因組DNA 中18S rRNA 小亞基進行擴增, 所用引物為Primer1-F: 5′-GGGGGTATTTGTATTTAAC AAGCA-3′, Primer1-R: 5′-CCTACGGAAACCTTGTT ACGA-3′ (Castellanos-Martínezet al, 2013)。目的片段長度約為800 bp, PCR 擴增采用50 μL PCR 體系, 包含5 μL 10×PCR buffer, dNTPs 0.2 mmol/L, MgCl22 mmol/L, Primer1-F 0.25 μmol/L, Primer1-R 0.25 μmol/L, 模板DNA 100 ng,TaqDNA 聚合酶2 U。反應程序為: 94 °C 預變性10 min, 隨后循環35 次包括94 °C 變性1 min, 51 °C 退火1 min, 72 °C 延伸1 min, 最后72 °C 延伸10 min。擴增產物在1.5%瓊脂糖凝膠電泳下檢測, 生工生物有限公司雙向測序。18S rRNA 基因序列已上傳至 GenBank (Nos:MW577122、MW577123、MW577124、MW577125、MW577126、MW577127、MW577128、MW577129、MW577130 和MW577131)。
用DNASTAR 軟件包中的Seqman 軟件對測序結果進行排列校對, 將本研究獲得的18S rRNA 基因序列在GenBank 數據庫中進行Blast 比對, 下載近緣物種的 18S rRNA 基因序列, 選用Eimeria bovis(U77084)和E. arnyi(AY613853)作為外群, 使用MEGA 6.0 中的Clustal W 將全部序列進行多重比對分析(Tamuraet al, 2013), 去掉前后不整齊的較長序列, 保留中間的gap 區域。在構建系統發育樹之前,用jModelTest 2.1 軟件(Darribaet al, 2012)計算似然值的核苷酸進化模型, 在AIC 標準下采用默認設置, 篩選出最優模型為GTR+G。系統發育分析采用最大似然法(Maximum Likelihood, ML)和貝葉斯法(Bayesian Inference, BI), 分別使用軟件MEGA 6.0 和MrBayes 3.2 (Ronquistet al, 2012)構建系統發育樹。在最大似然法(ML)分析中, 進化樹的節點可靠性通過1 000 次重復抽樣分析進行評估。在貝葉斯法(BI)的分析中,在馬爾科夫鏈蒙特卡洛分析(Markov chain Monte Carlo, MCMC)命令指導運行了100 萬代, 每1 000 代采樣一次, 每1 000 世代保存一次取樣樹。待分裂頻率標準誤差小于0.01 后, 去除25%的老化樣本。最終獲得的系統發育樹使用軟件 FigTree 1.4.2 編輯(Rambautet al, 2008)。
2 結果
2.1 多刺叢集球蟲, 新種, Aggregata octaculeata sp.nov.
終宿主: 中華蛸(Octopus sinensis)
寄生部位: 盲囊和腸組織及內部
發現地點: 福建連江(26°16′N, 119°47′E)以及浙江南麂島(27°29′N, 121°01′E)
詞源, 拉丁語, oct=八, 亦為蛸屬的前三個字母,aculeata=多刺的, 是以終宿主蛸屬的前三個字母加該種叢集球蟲孢子囊有刺的結構特征命名。
模式標本存放處: 中國海洋大學水產學院標本室, OUC-LSGB-HE0045
2.2 形態描述
被感染的中華蛸樣本有31 個(18 個雄性個體和13個雌性個體), 體重(total weight, TW)為130.8—2140.0 g,胴背長(mantle length, ML)為70—199 mm, 叢集球蟲主要分布于盲囊和腸組織內部(圖1)。
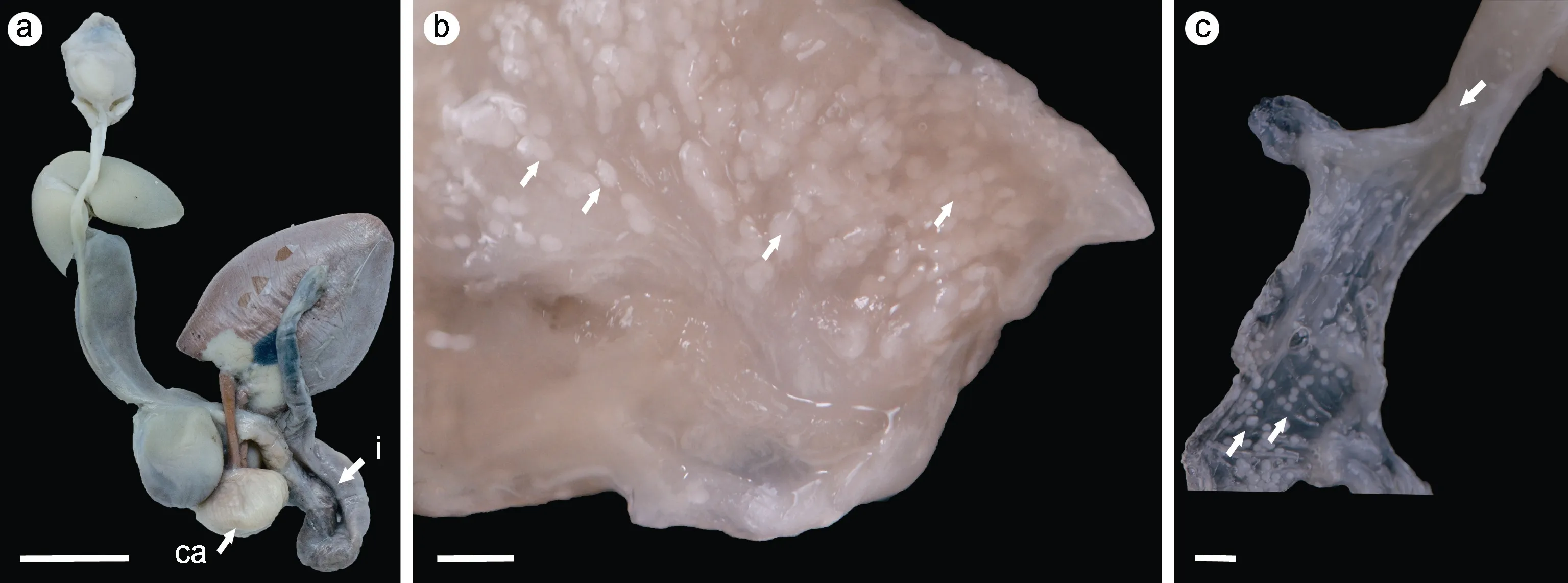
圖1 叢集球蟲分布Fig.1 Distribution of Aggregata
新鮮叢集球蟲壓片, 結果顯示, 成孢子化的卵囊(n=10)白色, 呈近球形或橢球形, 長徑為653.6—806.5 μm [(717.3±55.9) μm], 寬 徑 為 588.1—787.1 μm[(663.3±58.2) μm] (圖2a)。孢子囊(n=30)為卵球形或橢球形, 孢子囊長徑為22.4—26.1 μm [(24.3±0.8) μm], 寬徑為20.5—24.6 μm [(22.4±1.0) μm] (圖2b, 2c)。
掃描電鏡結果同樣顯示孢子囊(n=30)為卵球形或橢球形, 孢子囊(圖3d, 3e, 3f)長徑為16.5—20.8 μm[(17.9±1.0) μm], 寬徑為 14.9—19.6 μm [(16.8±0.9)μm]。孢子囊壁(圖3e, 3h)為雙層, 外層膜狀且光滑, 內層較厚且有刺, 它們緊密地連接在一起, 并有明顯的裂縫線(ds) (圖3f)。我們從新鮮壓片中分離出子孢子(n=10), 呈卷曲狀, 其長度為22.2—28.6 μm [(25.6±1.9)μm], 寬度為3.0—5.0 μm [(4.0±0.7) μm] (圖2d)。

圖2 叢集球蟲形態Fig.2 Morphology of Aggregata
經組織學觀察, 嚴重感染的中華蛸盲囊組織會被大量的叢集球蟲卵囊替代(圖3a), 在被感染的中華蛸盲囊中可以觀察到叢集球蟲的孢子生殖階段(圖3b,3d—3j)和配子生殖階段(圖3c)。在叢集球蟲的生活史中, 配子生殖階段的一個小配子和一個大配子(圖3c)結合能夠產生合子, 從而進入孢子生殖階段, 合子會長成一個具有眾多細胞核的孢向蟲(圖3b), 其特征是細胞質表面有眾多細胞核排列。單個核及細胞質出芽,形成單核球形孢子母細胞。孢子母細胞會進一步發育,成為孢子囊(圖3d—3j), 孢子囊內部的細胞核和細胞質分裂形成子孢子。組織學切片結果顯示孢子囊內子孢子的數目在8—13 個之間(圖3i, 3j)。

圖3 組織學切片下的叢集球蟲形態和電鏡下的孢子囊形態Fig.3 Histological section of Aggregata and morphology of sporocysts under SEM and TEM
2.3 基于18S rRNA 基因序列的叢集球蟲系統發育分析
兩種方法構建的系統發育樹均具有很高的支持度, 拓撲結果強烈支持了叢集球蟲科Aggregatidae 為單系發生, 中華叢集球蟲A. sinensis和A. octopiana的親緣關系最近, 與A. eberthi形成姐妹群, 最后與本研究中的多刺叢集球蟲A. octaculeata聚在一起。此外, 研究結果強烈支持了[(Aggregatidae+Cryptosporidiidae) + Haemogregarinidae] + Adeleidae的系統發生關系(圖4)。
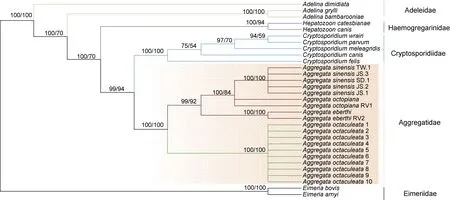
圖4 最大似然法和貝葉斯法構建的類錐體綱18S 的系統進化樹Fig.4 Phylogenetic relationships of Conoidasida by maximum likelihood and Bayesian methods
3 討論
傳統上叢集球蟲的形態學鑒定依賴于孢子生殖階段的形態特征, 依據光學顯微鏡下觀察到成熟孢子囊的大小、孢子囊壁的結構、每個孢子囊內子孢子的數目以及子孢子大小等形態學特征(Gestalet al,2002, 2005, 2010)。本研究通過在光學顯微鏡下觀察新鮮叢集球蟲壓片, 發現叢集球蟲的孢子囊大小為24.3×22.4 μm, 與其他叢集球蟲相比, 孢子囊僅小于A. bathytherma的孢子囊(28.7×27.9 μm) (Gestalet al,2010) (表2)。掃描電鏡結果顯示,A. octaculeata孢子囊大小為17.9×16.8 μm, 這與真蛸體內A. octopiana的孢子囊(11—15 μm)大小存在較大差異(Gestalet al,1999)。叢集球蟲具有宿主特異性,A. octaculeata和A. octopiana分別寄生于不同宿主, 支持了中華蛸作為不同譜系從真蛸中分開的研究結果(Guerraet al,2010; Amoret al, 2014; Gleadall, 2016)。而本研究中孢子囊在掃描電鏡和新鮮壓片中的測量結果差異較大,推測因掃描電鏡前期經過固定、脫水等處理方式所致。中華蛸中的A. octaculeata孢子囊壁有刺(圖3d,3f), 除此之外,A. octopiana的孢子囊壁也有凸起(Gestalet al, 1999; Castellanos-Martínezet al, 2013),其他叢集球蟲孢子囊壁均光滑(Poyntonet al, 1992;Gestalet al, 2000, 2005, 2010; Sardellaet al, 2000) (表2)。多刺叢集球蟲A. octaculeata子孢子包含在孢子囊內, 長度為25.6 μm, 僅小于A. bathytherma的子孢子長度(49 μm) (Gestalet al, 2010)。

表2 叢集球蟲屬內各物種孢子生殖階段主要特征的比較Tab.2 Comparison in morphology of the sporogonic stages for species of Aggregata from cephalopod hosts
在頭足類體內, 叢集球蟲能夠引發宿主感染,導致盲囊上皮細胞脫落和結締組織破裂, 造成黏膜萎縮和潰瘍(Castellanos-Martínezet al, 2019)。目前已在真蛸體內發現A. octopiana分布于鰓、腕等組織處, 導致血細胞浸潤, 甚至造成組織壞死(Mladineoet al, 2007), 叢集球蟲遷移到消化道外被稱為腸外球蟲病(Mladineoet al, 2007; Castellanos-Martínezet al, 2019), 但在本研究中未發現中華蛸的腸外球蟲病。多刺叢集球蟲主要感染中華蛸的盲囊和腸組織,在其他組織部位中并未發現。而嚴重感染的中華蛸盲囊及腸組織會被大量的叢集球蟲卵囊替代(圖3a),從而造成組織損傷。有關研究表明叢集球蟲感染不是章魚的致死因素(Hochberg, 1990), 可能是高密度的叢集球蟲感染使章魚更容易受到其他問題的影響, 如運輸和溫度的劇烈變化造成的應激(Poyntonet al, 1992)。
研究表明, 寄生蟲之間與宿主之間的系統發育關系不一致。雖然真蛸與中華蛸的親緣關系非常近(Gleadall, 2016), 但本研究中的系統發育結果顯示,寄生于中華蛸中的A. octaculeata與寄生于真蛸中的A. octopiana并沒有聚在一起, 與其他叢集球蟲相比,親緣關系相對較遠。
4 結論
在本研究中, 我們從中華蛸體內發現了一種叢集球蟲新種, 命名為多刺叢集球蟲Aggregata octaculeatasp. nov., 形態學結果顯示, 該物種孢子生殖階段包括成熟孢子囊和子孢子, 孢子囊為卵球形或橢球形, 孢子囊壁為雙層, 外層膜狀且光滑, 內層較厚且有刺。基于18S rRNA 分子序列的系統發生結果進一步證實物種隸屬于叢集球蟲屬, 并高度支持了屬內[(中華叢集球蟲A. sinensis+A. octopiana) +A.eberthi] + 多刺叢集球蟲A. octaculeata的系統發生關系。本研究的形態學和分子學數據為進一步研究頭足類寄生蟲分類學及系統發育進化提供基礎資料, 對蛸類分類提供輔助依據, 同時也為中華蛸疾病診斷和組織病理學研究提供理論依據。
致謝 澳大利亞維多利亞博物館盧重成教授對文章撰寫提供了寶貴意見; 南麂列島國家海洋自然保護區管理局陳萬東和倪孝品提供樣品, 中國海洋大學貝類遺傳育種研究室碩士研究生李嘉華協助實驗,謹致謝忱。

