鋰合金電極材料的研究進展分析
牟 粵,邱景義,楊曉飛,張婷婷,張松通,明 海
(1.軍事科學院防化研究院 先進化學蓄電技術與材料北京市重點實驗室,北京 100191)(2.北京化工大學化學工程學院,北京 100029)
1 前 言
在21世紀,人類生活和生產的各方面發展都和能源的獲取與供應密切相關。移動電子設備的飛速發展和電力儲能及輸送時域/空域調配的客觀使役條件,對化學電源的性能提出了更高的要求[1-3]。眾所周知,負極材料對電池的輸出比能量和比功率有重要的影響,是決定電池電化學性能的關鍵因素。經過幾代發展,負極材料經歷了從金屬到碳材料、氧化物、錫合金、碳硅復合物等,再回歸到鋰金屬的演變過程[2]。為了進一步提高鋰金屬電極的循環穩定性和安全性,滿足固態電池、鋰空氣電池和鋰硫電池等的發展需要,鋰合金的研究受到了廣泛的關注。鋰合金材料具有理論儲鋰容量大、儲鋰電位低和環境友好等特性[3],近幾年來,隨著人們對鋰合金材料的研究不斷深入,其在液態/固態鋰電池、新型鋰-非金屬(CFx、SFx、S、O2、CO2、FeSx,金屬氧化物、金屬氮化物、金屬氟化物等)電池體系中的性能取得了較大突破,也使相應電池的比能量和循環穩定性等得到了大幅度提升[4]。圖1列舉了一些在儲能領域常見的鋰合金材料[5-25]。
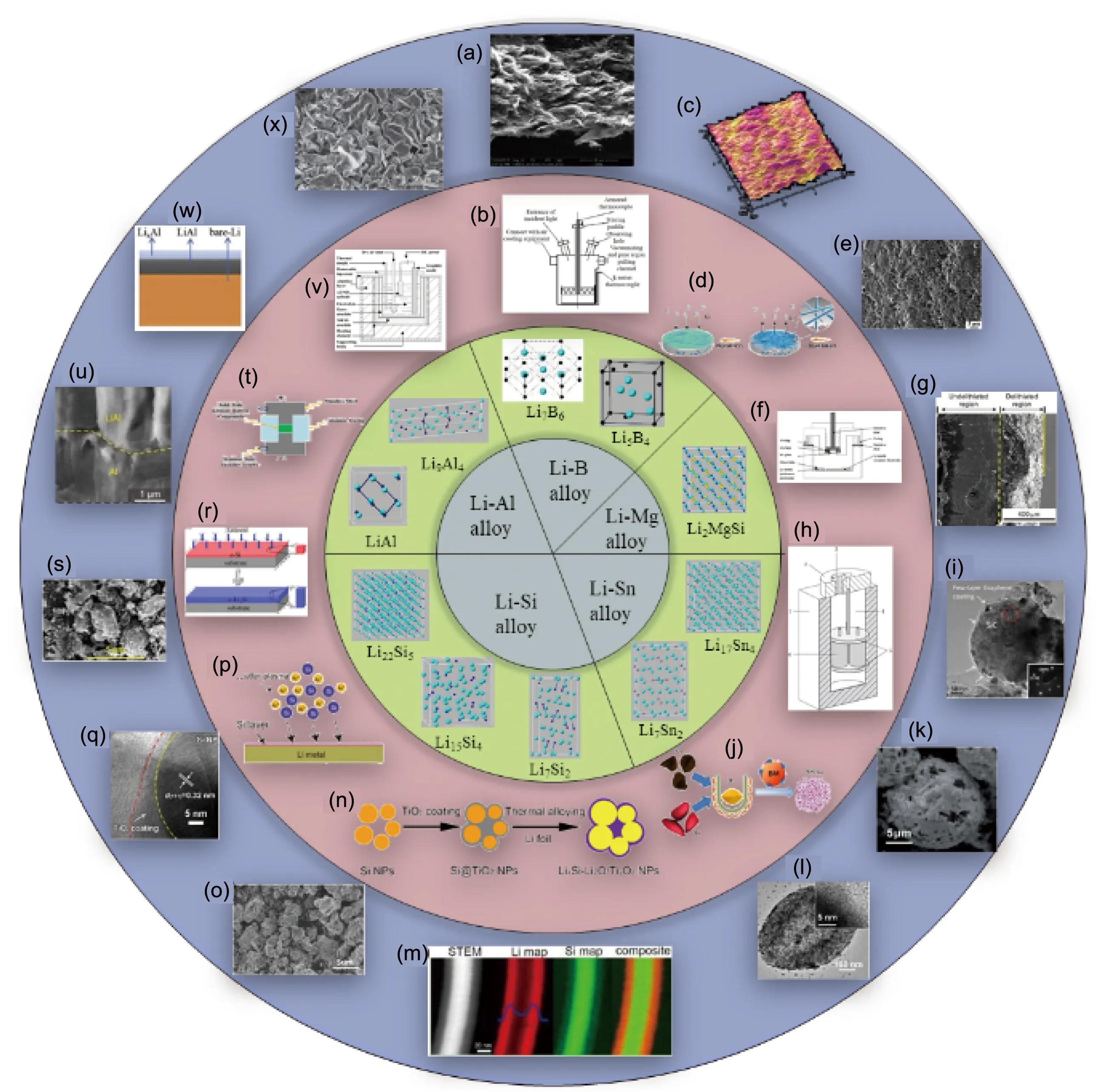
圖1 不同鋰合金電極材料的晶體結構、制備裝置或方法示意圖以及SEM照片Fig.1 Schematics of crystal structure,production device/method and SEM images of different lithium alloys materials:(a~d)Li-B alloy[5-7],(e~g)Li-Mg alloy[8-10],(h~j)Li-Sn alloy[11,12],(k)Li-Sb alloy[13],(l)Li-Ge alloy[14],(m~s)Li-Si alloy[15-20],(t~x)Li-Al alloy[21-25]
鋰合金往往作為安全性更高的電極材料取代純鋰金屬的使用。比如,熱電池采用熔融鹽作為電解質,工作溫度在400~450 ℃,遠高于鋰熔點,導致鋰金屬無法正常使用。可通過使用合金負極材料解決此問題,常用合金材料主要有Li-Al、Li-Mg、Li-Si以及Li-B合金。鋰合金作為負極材料可減少鋰枝晶的生成和粉化膨脹,但同時也帶來了3個不可避免的缺點。首先,鋰合金相比純鋰金屬活性更低,這會降低電池的工作電壓平臺;其次,其它非活性物質的引入往往會造成一些不可預期的副反應,加速電解液的分解;最后,非活性物質的加入使得活性物質——鋰的占比下降,導致電池的總體比能量不可避免地會有所降低。
相比于以純鋰為負極材料的電極,以鋰合金為負極材料的電極的最高理論比容量和電池能量密度均有所降低。此外,鋰合金還會增加電極活性物質之間的界面接觸,導致活性物質與集流體之間、以及活性物質與活性物質彼此之間的電子緊密接觸弱化,由此造成電池內阻升高(工作電壓降低)而影響電池的放電容量,高內阻的熱效應也會影響電池的宏觀結構,如脹氣等。有別于傳統的Li-MnO2、Li-CFx、Li-FeS2、Li-SO2和Li-SOCl2等鋰一次電池,鋰二次電池中與鋰金屬組合形成合金的材料通常包括硅(Si)、錫(Sn)、鍺(Ge)、鋁(Al)和硼(B)等,并且隨著納米材料結構設計和電化學原位表征技術的發展,鋰合金負極材料的電化學反應機理也已基本明確。實際生產中,為補償高比容量負極材料的首次不可逆容量或者與無鋰源正極材料如MnO2、S、V2O5等相匹配,一般會向負極材料中摻入Li。鋰合金作負極一方面可以解決電池體系中因為固體電解質相界面(solid electrolyte interface,SEI)膜的形成或者電極材料結構改變而造成的鋰缺失問題,另一方面也可對一些需要鋰參與的新型電化學體系,如鋰離子電容器等進行載流子補償[26]。已報道的鋰合金有Li-Si、Li-Mg、Li-Al、Li-In、Li-Cd、Li-B、Li-Pb、Li-Sn、Li-Ga、Li-Sb、Li-Bi等[27]。已知鋰合金負極的體積比容量可以達到3200 Ah·L-1,是常規碳基負極體積比容量的4倍;質量比容量可以達到800 mAh·g-1,是常規碳基負極體積比容量的2倍。結合近幾年國內外對鋰合金負極材料的研究,本文將重點介紹鋰-金屬與鋰-非金屬兩大類合金負極材料的發展現狀和最新研究進展,比較各種鋰合金負極材料在各電池體系中的應用及其電化學性能,分析其物理化學特性,梳理目前其面臨的主要問題及現有的解決方案,展望其未來的發展趨勢。
2 鋰-非金屬合金電極材料
2.1 鋰-硼(Li-B)合金
1978年,美國海軍武器中心實驗室最早以Li-B合金作為熱電池電極材料,之后Li-B合金得到持續關注。受限于技術條件,Li-B合金的合成機制和材料性質之前未得到深入研究,且因其穩定性不太理想,導致Li-B合金未得到廣泛推廣。隨著技術的進步,學界對Li-B合金的結構特性、物化性質以及合成方法等有了深入了解,比如鋰含量的影響[28,29]、電化學性能[30-32]、力學性能[33]、結構形貌[7,34]、合成方法[6,35]等。
常見的Li-B合金是鋰硼化合物(Li7B6)與填充在其孔隙之中的金屬鋰構成的復合材料,眾多研究人員[34-40]表征了Li-B合金的各種性質,發現該材料鋰含量高(~70%,質量分數,下同),色澤銀白,柔韌性良好,易軋制成薄帶,熔點大于600 ℃,導電性能以及電化學性能與純鋰接近,且在熱電池工作溫度下不會因液態鋰流動而發生短路或產生電噪聲。如圖2a所示,當填充在孔隙間的金屬鋰溶出后,Li-B合金表面展露出骨架化合物Li7B6的形貌,呈現為團簇的絲狀物,與圖2b的鋰金屬電極形貌形成對比。Sanchez等[41]以含萘的四氫呋喃清除Li-B合金中的自由鋰,測出該合金骨架孔洞的平均直徑為1.5 μm。相比于金屬鋰,Li-B合金具有更好的熱穩定性,稍大的傳荷電阻,稍低的反應活性。放電時,Li-B合金中的自由鋰可完全脫出,合金骨架中的結構鋰也有約30%參與放電,如圖2c和2d所示,自由Li溶出后,Li-B合金骨架依舊保持著初始形貌,因此該合金電化學性能優良。鑒于B和Li擁有相近原子尺度,并且合金化后的骨架結構能明顯降低有效電流密度[7],因此,Li-B合金可以有效抑制鋰枝晶的產生和生長,提升電池穩定性。電池對電極材料的均勻性和一致性要求較高,而Li-B合金熔煉后難以避免缺陷的存在,Huang等[42]使用電子計算機斷層掃描(computed tomography,CT)技術對商用Li-B合金進行了無損檢測,研究了Li-B合金中鋰元素的含量和空間分布。并根據朗伯-比爾(Lambert-Beer)定律,在CT值、鋰含量和密度之間建立了定量關系,使鋰含量測定誤差小于0.5%,優于通過電感耦合原子發射光譜(inductively coupled plasma-atomic emission spectrometry,ICP-AES)測定的鋰含量的準確度,實現了區域分析。
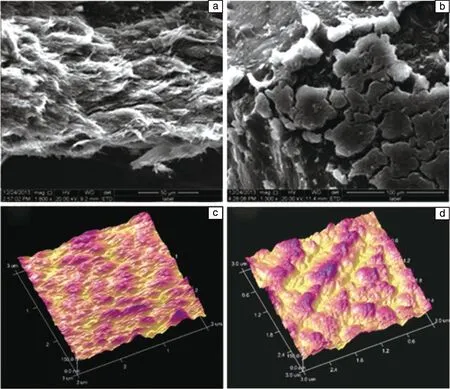
圖2 B質量分數為30%的Li-B合金(a)和金屬鋰(b)在Li溶解后的SEM照片;原始的(c)和經過Li溶解后的(d)B質量分數為30%的Li-B合金的AFM照片[7]Fig.2 SEM images of Li dissolved Li-B alloy with 30wt% B (a)and metal Li (b);AFM images of pristine Li-B alloy (c)and Li dissolved Li-B alloy with 30wt% B (d)[7]
Li-B合金作熱電池負極材料,可顯著簡化材料制備步驟,提高熱電池綜合性能,使相同容量的熱電池體積和重量減小10%~30%,最大放電電流提升3倍,比容量提高近2倍,相比于傳統的Li-Si合金,Li-B合金容量衰減更低[31]。以Li-B合金負極組裝Li/亞硫酰氯(SOCl2)電池,可拓寬Li/SOCl2電池的工作溫度范圍(150~250 ℃),以0.1C電流工作時,其電壓平臺大于3.6 V[43]。此外,該電池工作溫度超過Li熔點時,液態的自由Li吸附在骨架化合物中,提高了電池的安全性[29]。
Li-B合金可通過不同方法制備得到,北京有色金屬研究總院的張浩等[44]將Li金屬和無定型B粉按比例混合,在受控氣氛(氦氣、氫氣混合氣)下熔煉制備出Li含量為70%的Li-B合金,方法相對簡單。Ding等[45]在鍍釩玻璃基板上以脈沖激光沉積法(pulsed laser deposition,PLD)制備出正方結構的硼(B50)薄膜,并在之后的電化學過程中轉變成Li-B合金。該材料組裝的電池室溫下工作電壓為0.01~3.0 V,采用非水電解質時其放電容量僅為44 mAh·g-1,而在85 ℃溫度下工作時,其Li放電容量提高至268 mAh·g-1。近年來,Li-B合金在鋰離子電池以及鋰金屬電池中有了更多的應用[46]。當B形成Li5B并作為電極材料時,該電池的理論容量可達12 395 mAh·g-1,因此Li5B理論上是非常理想的負極材料。但是Li5B只存在于原子隔離/分散形式的B中。Dong等[47]嘗試將惰性B分散到Fe基體中激活,對前驅體Fe2B/Fe和B2O3/Fe進行電化學活化,使B與Li結合為Li5B。以其為電極材料組裝的電池初始比容量為800 mAh·g-1,250次充放電后比容量增長至1500 mAh·g-1,其中有一個較長的活化過程。這種方法對研發新的鋰電池負極有重要的借鑒意義。中南大學陳立寶課題組分別將三維的Li-B合金[48]以及Mg摻雜Li-B合金[5]作為負極與LiCoO2正極組成電池,該電池均表現出了非常優秀的電化學性能。且研究結果表明B含量對Li-B合金的電化學性能有顯著影響,B含量為15%時該電池表現出最佳的循環性能;當B含量低于15%時,該電池負極材料骨架趨于松散而無法有效抑制循環過程中的體積變化;當B含量高于15%時,該電池過電位增大且電極材料界面阻抗上升。
普通Li-B合金在鋰離子電池中應用也有許多優點,其重量輕、易制取、成本低、無毒,是理想的負極材料。圖3a比較了Li/LiFePO4電池和LiB/LiFePO4電池的充放電曲線[46],可見Li-B合金和Li電化學性能非常接近。相比于鋰金屬負極,Li-B合金負極在抑制鋰枝晶、降低界面阻抗和改善電池循環性能上有明顯優勢。Duan等[49]以Li-B合金作鋰硫電池負極,電池中SEI形成快且穩定,容量衰減明顯小于以純鋰金屬作負極組裝的鋰硫電池。同時在合適的Li-B比例下,以Li-B合金為負極的電池的放電容量與以金屬鋰為負極的電池接近,說明Li-B合金在容量上沒有劣勢。此外,B含量高的合金,其纖維網絡結構更發達,游離鋰有更大的比表面積,因此其性能更好,目前已發表的以Li-B合金為負極的文章中B含量最高為30%。Zhang等[7]將Li-B合金應用于鋰硫電池中,并對50周充放電后的LiB-S和Li-S全電池進行對比,發現鋰金屬表面出現鋰枝晶,而Li-B合金表面未出現,可見Li-B合金可以使電流分布更均勻,且抑制枝晶鋰和改善循環性能的效果顯著。圖3b對比了Li金屬和Li-B合金作為鋰硫電池負極的充放電性能,可以明顯看到Li-B合金作負極時電池的庫倫效率更高,并且放電時平臺電壓高,極化趨勢小。
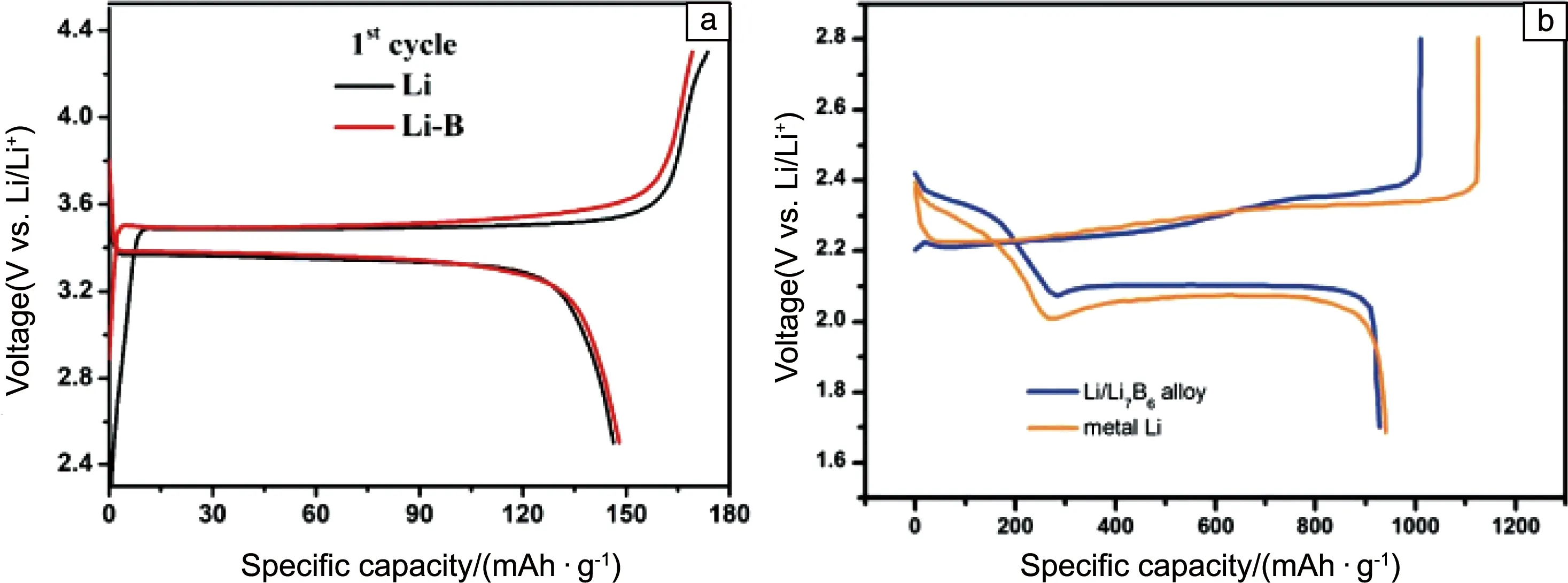
圖3 Li/LiFePO4電池和LiB/LiFePO4電池首次充放電曲線(a)[46],Li/S電池和LiB/S電池首次充放電曲線(b)[7]Fig.3 First charge/discharge profiles of Li/LiFePO4 cell and LiB/LiFePO4 cell (a)[46],first charge/discharge profiles of Li/S cell and LiB/S cell (b)[7]
總體來說,Li-B合金目前主要作為熱電池負極使用,放電時,其電化學性能優秀,容量可媲美金屬鋰且更加穩定。而在可充電電池中,Li-B合金可以有效抑制鋰枝晶的產生和生長,降低電極/電解質的界面電阻。同時B有助于形成穩定的SEI,在鋰離子、鋰金屬、鋰氧氣和鋰硫電池上均有良好的應用前景。關于Li-B合金電極材料的發展,通過改性等手段穩定電池工作過程中電極的體積,并采用規模化方法制備致密均勻的合金材料,將大大提升Li-B合金材料的循環性能,這也會是未來Li-B合金材料研究和發展的重點。
2.2 鋰-硅(Li-Si)合金
Si在地殼中的含量豐富,是典型的鋰離子電池負極材料,且放電電位低,理論比容量可達到4200 mAh·g-1。Si與Li化合可生成Li12Si7、Li7Si3、Li13Si4和Li22Si5等,其中Li22Si5對應的貯鋰容量為4200 mAh·g-1。然而,Si基材料充放電時體積變化大、電導率低、循環性能差,設計開發結構穩定的Si基材料或對Si基材料進行改性是當前Si基負極研究的重點。
為得到循環穩定、性能優異的Si基材料,可將Si預嵌Li變為Li-Si合金,從而緩解體積效應,彌補形成SEI膜的Li損失。目前,已有很多研究工作致力于合成性能更優異的Li-Si合金,主要包括Li-Si合金的元素組成調節[50-53]、物化性質優化[54-58]以及合成策略設計[21,59,60]。如果合金中Li含量夠高,Li-Si合金化的混合焓就為負值,表明了該合金的穩定性[61]。為了分析Li-Si間的合金化行為,Wang等[18]結合原位鋰化實驗和分子動力學模型探索電化學驅動的固態非晶化機制。通過原位掃描透射電子顯微鏡(scanning transmission electron microscopy,STEM)觀察Si納米線的鋰化過程,發現其存在晶態Si核和非晶態LixSi殼(如圖4a所示)。界面處的Li分布曲線表明,Li-Si合金反應的前沿區域處于富電子狀態。為適應富電子環境,Si—Si鍵斷裂,形成孤立Si。當x達到臨界值3.75時,非晶態Li3.75Si轉變為晶體。Wang等[62]采用第一性原理計算研究了應變方式對LiSi、Li2Si和Li7Si2合金中鋰離子擴散的影響,3種Li-Si相分別對應鋰化過程中鋰離子濃度由低到高的變化。在上述3種Li-Si合金中,拉伸應變可導致鋰離子遷移能壘減小,而壓縮應變則可導致鋰離子遷移能壘增大。
Li-Si合金作為高比能電池負極材料時,可以顯著提升電池容量。然而,Li-Si合金負極在電池運行中的循環穩定性很差,因此必須針對其缺陷進行改性[63]。Wang等[15]制備了預鋰化TiO2保護的LixSi納米顆粒(如圖4b所示)。高穩定性的鋰化TiO2提供電子快速傳輸通道,提高了LixSi/Si間的電導率,使SEI難以在LixSi/Si上形成,同時包覆層能抑制Si的膨脹與粉碎,并保護LixSi核心免受腐蝕,提高該電極材料在干燥空氣中的穩定性。
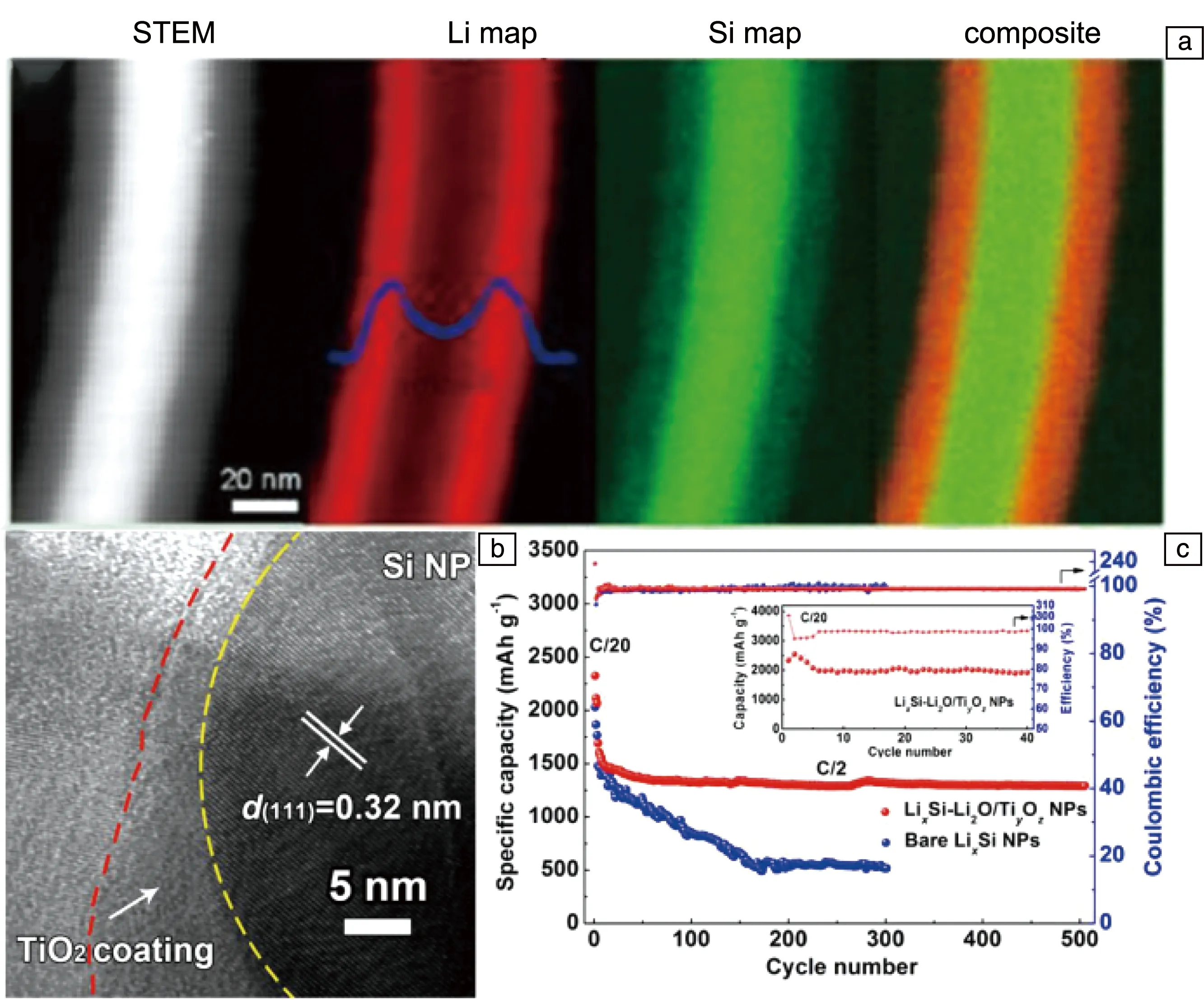
圖4 鋰化的Si納米線的STEM和元素分布照片(a)[18];LixSi-Li2O/TiyOz核殼納米顆粒的HRTEM照片(b),TiO2包覆的納米LixSi顆粒為電極的半電池的循環性能(c)[15]Fig.4 STEM image and element mappings of lithiated Si nanowires (a)[18];HRTEM image of core-shell NPs of LixSi-Li2O/TiyOz (b),cycling performance of LixSi nanoparticle coated by TiO2 in half cell (c)[15]
如圖4c所示,電池在0.5 C電流下經500次循環后,容量保持在1300 mAh·g-1左右,保持率為77%[15]。Kwon等[64]將非晶Si薄膜與Li金屬短接進行電化學鋰化,將Li-Si合金成分的變化作為溫度的函數進行考察,在100~120 ℃、0.0 V下生成了Li21Si5(容量4008 mAh·g-1)。脫鋰時,Li21Si5轉化為非晶態Si,只有在100~120 ℃、0.0 V下通過長期鋰化才能恢復,并且恢復能力很差,同時會粉碎形成不連通的Si顆粒。
對Li-Si合金的力學性能研究也極為關鍵。第一性原理計算表明,結晶和非晶態Li-Si合金的彈性模量與Li濃度緊密相關[65]。此外,考慮合金的電子結構,彈性軟化可能是因為Li—Si鍵的增加,而Li—Si鍵比共價Si—Si鍵弱,所以預計Li-S合金斷裂能會隨Li濃度的增加而降低。
鋰空氣/鋰硫電池中常使用金屬鋰作為負極,因為Li擁有超高的能量密度。但Li過于活潑,直接作負極往往帶來安全隱患,因此使用化學活性相對安全穩定的鋰合金作為負極是不錯的選擇,Li-Si合金可提升電池安全性而不太影響電池容量。Deng等[19]通過高能球磨制備了Li21Si5顆粒,顆粒尺寸分布在1~5 μm(如圖5a)。其在大電流(~400 A·g-1)下充放電50次(圖5b),保持了571 mAh·g-1的可逆容量,庫倫效率在98.5%左右[19]。Zhang等[20]將預負載的Li3N在負極上分解,原位形成Li-Si合金負極,該負極經歷100多次充放電后依舊穩定,且沒有明顯的鋰枝晶生長,穩定性遠勝于鋰負極。其開發的LixSi-O2電池在200 mA·g-1的電流密度下,比能量達到500 mAh·g-1,庫倫效率接近100%。
Li-Si合金的常用的制備方法有預鋰化方法、電化學方法以及熱熔法等,但Li和Si的熔點相差巨大,結合方式多樣,原子半徑相差也較大,因此如何通過有效手段獲得穩定的Li-Si合金材料,將是未來研究的一個重點。同時,Li-Si合金穩定性較Li-B合金差,后續通過預氧化處理或者壓實熟化促進Li-Si合金穩定性提升的設計也是該材料推廣使用的關鍵。
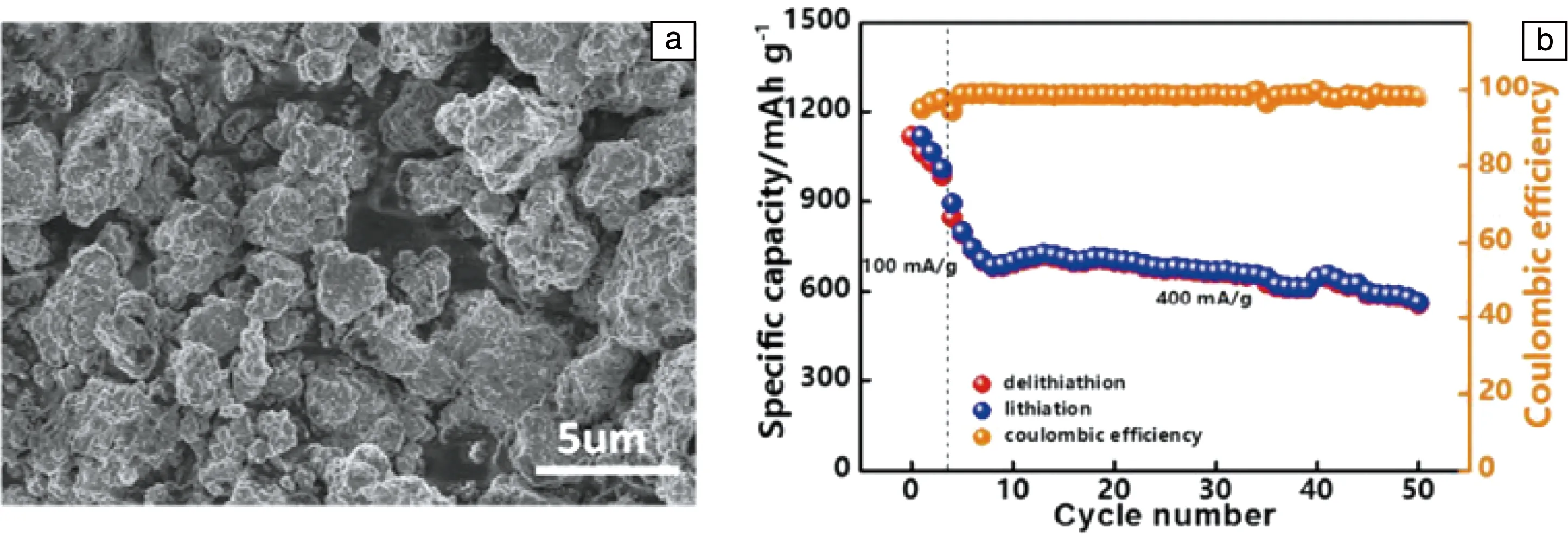
圖5 球磨法獲得的Li21Si5的SEM照片(a),Li21Si5為電極的半電池的循環性能(b)[19]Fig.5 SEM image of Li21Si5 obtained by milling (a),cycling performance of Li21Si5 electrode in half cell (b)[19]
3 鋰-金屬合金電極材料
3.1 鋰-錫(Li-Sn)合金
Sn與Li合金化時表現出優異的儲鋰性能,理論容量達994 mAh·g-1,體積比容量達7200 mAh·cm-3,且Sn價格低廉、無毒環保、資源豐富。但Sn基材料在充放電過程中體積膨脹嚴重、易粉化、循環性能很差,尤其是Sn與Li形成的Li22Sn5在充放電過程中體積膨脹率高達676%(圖6a)[67]。為抑制其體積膨脹,目前對Sn基材料的研究集中在合金化方面,以期獲得穩定的Sn基負極材料[68]。Li-Sn合金工作電壓遠高于Li的析出電位,因此不必擔心Li的沉積問題;在充放電過程中不存在溶劑的共嵌入問題,因此對溶劑的選擇性友好,應用前景可觀。目前,對Li-Sn合金的研究涵蓋多方面,包括相平衡[11,69,70]、離子擴散[71]、電化學性能[72]、機械性能[73-76]、嵌脫鋰機制[77]等。

圖6 Li22Sn5粉末的SEM照片(a)[67],SnLi4.4@C復合材料的TEM照片(b)[12]Fig.6 SEM image of Li22Sn5 powders (a)[67],TEM image of SnLi4.4@C composite material (b)[12]
Li-Sn合金的主要合成方法有感應熱熔法、電化學鋰化法和鋰金屬顆粒摻雜法[78]。感應熱熔法最常用,是將Li和Sn于真空或惰性氣體(通常是氬氣)保護下感應加熱,充分合金化后粉碎得合金粉末。感應熱熔法對原材料和環境要求較高,但制備快捷,原子比可控,因此多用于合成比例確定的合金的制備,如SnLi4.4、Li8Sn3等[11,12]。電化學鋰化法是將電極與鋰金屬短接,或組成半電池得到Li-Sn合金。電化學鋰化法鋰化過程長、難以控制合金的原子比,但反應較溫和,條件簡單。鋰金屬顆粒摻雜法制備過程簡單快捷,但鋰粉難以保存,摻雜后也需要輥壓并經合金化反應才能獲得合金,且合金中鋰分布也不太均勻。
Li-Sn合金化時會產生巨大的體積膨脹,所以Sn基負極往往通過加入惰性相來緩沖其體積變化,以提高其循環穩定性,再配合一定的結構設計和優化處理更好地發揮合金材料的優勢[12,72,79,80]。碳是常用的添加元素,Fan等[12]合成了層狀復合的核殼結構材料SnLi4.4@C(如圖6b所示)。該材料在200次充放電后的容量為680 mAh·g-1,在5 A·g-1電流下擁有310 mAh·g-1的比容量。SnLi4.4@C復合材料電化學性能改善是由于:① 碳基體中分布納米級SnLi4.4顆粒,可以得到高效的電子和離子傳輸通道,并抑制Sn納米顆粒在長時間循環中被粉碎或聚集;② SnLi4.4已預處理,因此其體積膨脹所引起的粉化會得到緩解,增強復合材料的穩定性。Elia等[81]以LixSn-C合金作負極制備鋰空氣全電池,使用聚偏二氟乙烯(polyvinylidene fluoride,PVDF)基凝膠聚合物作隔膜。通過分析鋰離子導電率及其電化學性能,可知該凝膠聚合物薄膜可抑制正極到負極的氧交叉,增強電池的循環性能,顯著提高鋰空氣全電池的性能與安全性。此外,其團隊[82]以Li-Sn-C鋰化合金為負極,采用三氟甲磺酰亞胺鋰(lithium bis(trifluoromethanesulfonyl)imide,LiTFSI)/甘醇二甲醚為電解液,獲得了性能良好的鋰空氣全電池。這說明使用安全性高的鋰合金負極,并引入特殊定制的電解質,是提高鋰空氣電池安全性和電化學穩定性的有效策略。
除碳外,研究人員也會添加一些金屬元素改進Sn電極的性能。Fürtauer等[83]熔煉合成CuLi2Sn和Cu2LiSn,在CuSn和Cu2Sn中基于有序晶格形成通道,Cu和Li原子部分混合占據的位置上有大量空位。CuLi2Sn空間群為F-43m,理論容量為273 mAh·g-1;Cu2LiSn空間群為P63/mmc,理論容量為106 mAh·g-1。之后,其團隊[84]還發現了2種新的合金相——Li3CuSn和Li6Cu2Sn3,其中Li3CuSn和CuLi2Sn在結構與性能上有一些相似之處,其差異主要是在原子堆疊順序上;Li6Cu2Sn3和Li13Ag5Si6擁有相近的結構,Li13Ag5Si6作為鋰離子電池負極,其容量可達到800 mAh·g-1,因此Li6Cu2Sn3也有望作為一種優秀的負極材料。總之,Li-Cu-Sn三相合金的空間群結構對離子傳導很有幫助,并且其結構和Cu骨架的支撐作用可使材料體積膨脹得到有效的控制。
Sn的氧化物也可作負極,在充放電過程中可還原生成Li-Sn合金。Zhang等[72]以溶膠-凝膠反應制備Li2SnO3,并將其作負極裝入電池,Li2SnO3在電化學反應過程中被還原為Sn金屬和Li2O,隨后在Li2O基體中形成Li-Sn合金,Li2O基體的緩沖保證了Li-Sn合金電極的可逆性,因此通過該方法制備的材料的穩定性優于常規固相反應得到的材料。Wang等[85]以石墨作為分散劑,以SnO/SiO和Li的混合物作為反應物,制備出在石墨中均勻分散的納米Sn/Si復合材料,200次充放電后,以該材料為電極的電池可逆容量保持在574.1 mAh·g-1,單次循環的容量衰減小于0.2%,性能優于純SnO或SiO等負極材料。
Sn金屬價格低廉、比容量高、導電性好,自身及其氧化物均是具有潛在應用價值的負極材料。Sn和Li的合金化與Si和Li合金化類似,可緩解體積效應、提高電池的首次庫倫效率和電極表面SEI的穩定性。為緩解體積膨脹,也可將Li-Sn合金與C材料復合,獲得和Si-C材料類似的效果。Li-Sn合金在儲能領域的發展,最重要的還是需進一步抑制其體積膨脹,探索適配的惰性電解液體系,以及穩定材料的表面性能。此外,Li-Sn合金材料的大規模合成,兼顧其一致性、均勻性和高振實密度,是其現階段邁向實用化的一個關鍵問題。
3.2 鋰-鋁(Li-Al)合金
Li與Al可化合生成LiAl、Li3Al2和Li9Al4等。Li9Al4的理論容量可達到2234 mAh·g-1,是石墨負極理論容量的7倍左右。采用LiAl作為負極,其理論容量可達993 mAh·g-1,且充放電時體積膨脹率只有97%,高容量和低體積膨脹率的優點使得Li-Al合金成為當前負極材料的研究熱點。但是Li-Al合金作負極材料時,其表面SEI難以穩定,會導致活性材料失活,并且在10次充放電循環后仍可以觀察到腐蝕現象,存在容量衰減非常明顯等問題[86-88]。
目前,合成Li-Al合金電極材料的方法主要有感應熱熔法、電化學法、反應法。感應熱熔法在真空或氣氛保護下進行,條件苛刻但重現性好,原子比例易控制。電化學法通過將Li向Al電極沉積,獲得合金電極。反應法將Li和Al直接輥壓,可通過控制固化溫度和時間獲得不同原子比的Li-Al合金(圖7a)[25]。此外,將原料混合反應也可制取合金,如將LiH和Al,Si在氬氣環境中混合,并進行球磨,加熱去氫后即可獲得LiAlSi合金[89,90]。
研究表明,將Li-Al合金應用于鋰硫電池時,電池性能較穩定,恒電流充放電500次后,仍可保持500 mAh·g-1以上的比容量[23]。而且將薄Li-Al合金保護的鋰金屬應用在鋰硫電池體系中可減輕多硫化物穿梭的不利影響[25],Li-Al合金改性后的鋰電池具有良好的倍率性能、更低的電荷轉移電阻、更好的循環穩定性和更高的庫侖效率。Ding等[91]在凝膠電池中采用Al含量為0.1%的Li-Al合金作為負極,該電池表現出優異的表-界面穩定性,且相比于以純金屬鋰為電極的電池,該電池阻抗更低,室溫靜置5 d后,純鋰電極的界面阻抗為150~650 Ω,該鋰合金電極的界面阻抗為100~250 Ω。Zhong等[24]以Li-Al合金修飾Li-B電極的表面,并將其應用于全固態電池中,發現該方法可改善電極/電解質間的界面性能,防止Li的局部偏析,抑制鋰枝晶生長(如圖7b)。

圖7 Li負極上包覆Li-Al合金的SEM照片(a)[25],Li-Al合金原位修飾后Li-B負極的SEM照片(b)[24]Fig.7 SEM image of Li anode coated by Li-Al alloy (a)[25],SEM image of Li-B anode in-situ modified by Li-Al alloy (b)[24]
在Li-Al合金體系中加入其他元素,可以提升材料的性能[92]。Zn是常用摻雜元素,Chumak等[87,93]組裝并研究了以Li(Al0.8Zn0.2)為負極和以V2O5為正極的電池。Al和Zn在室溫下幾乎不混溶,因此Li脫出時Li(Al0.8Zn0.2)在局部發生分解生成Al和Zn,且通過XRD證實了連續LiAl-LiZn固溶體的存在。研究認為,用Zn取代Al對提高電性能有裨益,其在提高電極對體積膨脹適應性的同時,還能保護電極免受裂紋和接觸損失。除此之外Li-Al-Si合金也常被用作鋰電池的負極材料[89,94]。
此外,Mg-Li-Al-Zn[22,95]、Mg-Li-Al-Ce-Y-Zn[96]以及Mg-14Li-1Al-0.1Ce[97]等合金也可作為Mg電池的負極。
上述研究表明,Li-Al合金容量較大,但不能形成穩定的SEI,往往需要加入相對惰性的元素提升其循環性能,或尋找和電極體系相適應的電解液,改善SEI穩定性。除去將Al作為活性物質外,還可以利用Li-Al合金對鋰金屬的親和性以及Al元素在電極體系中的穩定性進行改善,將Li-Al合金作為負極表面改性材料,引導金屬鋰沉積,甚至減輕多硫化物穿梭[25]。
3.3 鋰-鎂(Li-Mg)合金
Li-Mg二元合金顯示出較大的固溶度比例,并且不發生相變,這表明Mg可以和大量Li合金化。在Li-Mg合金化過程中,首先形成貧鋰α相,然后轉變為富鋰BCC-β相。合金中Mg主要起骨架作用,保持材料結構完整性,同時降低電極對電解質的催化活性,提高鋰離子擴散速度(擴散系數:5×10-7cm2·s-1),從而快速調節Li分布,抑制鋰枝晶形成[98]。Li-Mg合金孔隙率高[99]、比表面積較大,且其開路電壓接近純鋰的負電位(~20 mVvs.Li/Li+),為形成高能量密度電池提供了基本條件。
Li-Mg合金的制備主要通過熱熔法、電化學鋰化法和化學合成法實現。熱熔法一般將金屬鋰熔化,后逐漸加入Mg金屬條或顆粒至合適的比例。電化學鋰化法是通過電化學方法向Mg中沉積Li,得到相應的Li-Mg合金。該方法合成條件簡單,但反應深度較淺,化學計量比也難以控制。化學方法合成Li-Mg合金的途徑主要是通過機械球磨粉末原材料后燒結,或通過氫驅動化學反應[100],該方法制得的Li-Mg合金原子比例可控,并且反應程度比熱熔法更徹底、成分更均勻。
Li-Mg合金在熱電池中已有應用,為抑制Li-B合金氧化,會向其中加入Mg,形成Li-Mg-B三元合金。Li-Mg-B合金在為石油/天然氣和地熱鉆孔設備供電方面顯示出巨大的應用潛力。Niu等[101-104]以Li-Mg-B合金為負極制成熱電池,該熱電池工作溫度為150~300 ℃,開路電壓為3.1~3.4 V,電流密度為10 mA·cm-2時,初始工作電壓超過2.90 V,容量達到1356.7 mAh·g-1。Wang等[105]制備了Li-Mg-B三元合金箔,并研究其相結構和放電行為,在共晶電解質的輔助下,該Li-Mg-B三元合金負極與MnO2正極匹配組裝電池,電池表現出極高的性能:200 ℃下,Li-Mg-B合金電極的Li容量為1507.5 mAh·g-1,高于Li-B合金電極(70%Li)。很顯然,在LiB合金中加入Mg可以降低制造成本且不會造成容量損失。
Li-Mg合金在鋰電池中有廣闊的應用前景,眾多工作聚焦于優化Li-Mg合金、改善電池性能[106]。Jagannathan等[107]發現Li-Mg合金電極在脫鋰時,Li從富鋰的β相遷移到貧鋰α相,且放電后電極結構完好,說明Mg可以作為Li合金化和脫出的本體骨架,但與平穩的脫Li過程相比,Li的合金化程度有限。Liu等[9]研究了Li2.6BMg0.05合金負極的電化學性能。該電極循環壽命長,與電解液的副反應少,可形成穩定的SEI。該合金主要由Li5B4、Li和Li3Mg7組成,鋰溶解后顯示出多孔骨架結構,比容量達到1181.6 mAh·g-1,電極表面鋰枝晶的形成也被顯著抑制(如圖8a和8b)。Yoon等[8]研究了Mg(ClO4)2和HF作為電解液添加劑在1 mol·L-1六氟磷酸鋰/碳酸乙烯酯+碳酸二乙酯+乙二醇二甲醚(LiPF6/EC+DEC+DME,EC∶DEC∶DME=10∶9∶1)電解液中對鋰金屬電極的影響。SEM照片顯示,電化學反應后電極表面沉積了密集的半球形Li-Mg合金顆粒。研究結果表明,電極表面在Li-Mg共沉積作用下形成Li-Mg合金,并在HF作用下形成LiF,二者的協同效應抑制了鋰枝晶生成。Zhang等[10]通過層析中子成像技術分析了電化學脫鋰過程中Li-Mg合金中的Li的空間分布,具體說是確定了Li濃度沿厚度方向的分布。如圖8c所示,脫鋰區域與未脫鋰區域的合金形貌差異巨大。圖8d展示了脫鋰過程中鋰合金的層析中子成像解析圖,表達了鋰在脫出時的分布情況(綠色表示Li濃度低,紅色表示Li濃度高),并以此建立分析模型,科學表達、量化擴散控制的脫鋰過程。Liu等[100]通過氫驅動化學反應制備了六方晶系的Li2MgSi,與Mg2Si相比,其穩定性顯著提高。球磨后,Li2MgSi從六方結構轉變為立方結構,最大比容量為807.8 mAh·g-1,遠高于原始材料,且100次循環后容量保留率達到50%。
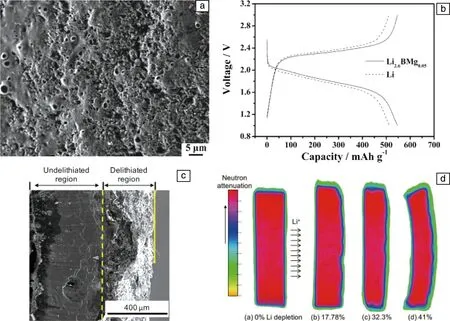
圖8 循環70次后的Li2.6BMg0.05表面SEM照片(a),Li2.6BMg0.05/S與Li/S的充放電曲線對比(b)[9];Li脫嵌與未脫嵌的Li-Mg合金形貌對比照片(c),鋰損耗不同水平下的中子衰減示意圖(d)[10]Fig.8 SEM image of surface morphology of Li2.6BMg0.05 after 70 cycles (a),charge-discharge curves of Li2.6BMg0.05/S and Li/S (b)[9];SEM cross-sectional view of undelithiated and delithiated region (c),pseudo-color images of different Li depletion level for neutron attenuation (d)[10]
Li-Mg合金在工業上已有成熟應用,主要作為輕質結構合金應用在航空航天領域。Li-Mg合金主要以固溶體方式存在,混合比例范圍相當大。在Li脫出以后,Mg作為骨架能維持材料結構穩定。類似Li與B合金化可得到高孔隙率合金的效果,Li-Mg合金也可作為熱電池的負極,將Mg摻入Li-B合金體系,使電池擁有優良的性能。用于二次電池時,Li-Mg合金憑借高鋰離子擴散系數和親鋰性,可抑制鋰枝晶的生長。由于其固溶度高,因此尋找合適的Li-Mg元素比例非常重要,而Mg作為高電化學活性的物質,也需要注意Mg在電極體系中的溶解。此外,考慮到Mg對Li的親和性和對材料骨架的維持能力,其作為摻雜元素添加到其它Li金屬體系中也有一定的前景。
3.4 其他鋰-金屬合金
鋰具有較小的原子半徑和極高的化學活性,能與眾多金屬形成合金材料,除了以上列舉的常見合金材料外,還可形成Li-Cu、Li-Sb、Li-Ge、Li-Zn和Li-Ti等合金,但由于原子半徑差異過大或外層電子軌道結構匹配性差等問題,這些合金的制備較此前介紹的合金更有難度,尤其是在獲得結構穩定、組分均勻的合金電極上。
Ge具有高電導率(Si電導率的100倍)和優良的鋰離子擴散系數(Si離子擴散系數的400倍),理論比容量為1600 mAh·g-1,體積容量為7366 Ah·L-1,在所有負極材料中僅次于Si(Si體積容量為8334 Ah·L-1)[108]。然而,Ge與Li的原子半徑相差較大,在脫出的過程中不可避免地有巨大的體積膨脹,膨脹率可達到272%,嚴重阻礙了Li-Ge合金的實際應用。目前主要以特殊結構的單質Ge緩解體積膨脹。Chiang等[109]計算了不同配比的液態Li-Si和Li-Ge合金的結構和電子性質,證明了將Si和Ge分別與Li混合,其產物呈現出截然不同的局部鍵合特性。Sinho等[14]通過還原金屬置換反應,制取了介孔Ge顆粒,該介孔顆粒容量達到1550 mAh·g-1,且在0.5 C下非常穩定(如圖9a)。
Cu具有良好的導電能力和穩定性,以Li-Cu合金作為鋰電池的負極,放電過程中鋰溶解后得到的Cu框架可以抑制鋰離子枝晶的形成。中科院長春應用化學研究所明軍團隊[110]制作了一種Cu-Cu2O三維納米棒陣列,Cu2O在鋰化過程中會生成Li2O覆蓋在Cu上。當Li+-溶劑分子-陰離子絡合物從Cu上接受一個電子時,特別是當Cu電極的供電子能力較高時,很容易使溶劑分子或雙三氟甲磺酰亞胺基(TFSI-)受誘導發生分解(即還原),而生成的Li2O在Cu表面就能很好地防止這一現象發生,同時Li2O的親鋰性也能減緩鋰枝晶生成,延長電池壽命。以Li-Cu合金作為負極,不僅可以兼顧高的Li存儲容量,也能依托Cu骨架實現高的結構穩定性[111],這對提升鋰電池的性能和穩定性等非常有幫助。Matsuno等[112]研究Cu2Sb電化學嵌鋰的反應動力學問題,指出其首次充放電存在較大的不可逆容量,在0.7 V左右出現平緩的電壓平臺,之后的循環則表現出良好的可逆性。因此可得出結論,Cu2Sb首次充放電和之后充放電的鋰沉積機制不同,伴隨明顯的電化學極化,并繪出了Li-Cu-Sb的三元相圖[113]。Henriques等[114]通過Knudsen隙透質譜法(Knudsen effusion mass spectrometry,KEMS)研究了Cu-Li-Sn合金的固相、固液相和液相區域的熱力學數據,計算了其在350~660 ℃溫度范圍內各組分的熱力學活度、混合焓和熵值,并用XRD獲得了該材料相應的晶體學參數。
Zn具有良好的鋰親和性,其合金可作為三維骨架引導金屬鋰均勻沉積,并抑制電極體積膨脹和鋰枝晶的產生[115,116]。三維骨架構筑了負極離子通道,使鋰可以更好地均勻沉積[117]。Ye等[118]在泡沫Cu上沉積Zn后進行鋰化,得到三維的Li-Zn合金和泡沫Cu的復合材料Li-Zn合金@泡沫Cu,該復合材料作負極時,在1 mA·cm-2電流密度下循環260次,庫倫效率為97.8%,在10 mA·cm-2電流密度下,無明顯枝晶產生,在對稱電池中的壽命2倍于普通的鋰沉積泡沫Cu電極。此外,Li-Zn合金@泡沫Cu材料作負極與LiFePO4或硫正極匹配,獲得的全電池具有非常優異的電化學性能。Li-Zn合金在全固態電池中也有相當不錯的表現,可明顯改善鋰負極和固態電解質之間的接觸界面性能,改善鋰負極與固體電解質間的界面潤濕性,并引導金屬鋰的均勻、有序沉積[119]。Alexander等[120]通過熔融方法制備Li-Zn合金,基于Li6.28Al0.24La3Zr2O12(LLZA)固態電解質組成對稱電池,Li-Zn合金和LLZA接觸緊密且界面電阻較低,僅為7.5 Ω·cm-2,其組成的電池在不同電流下均表現出良好的循環性能。軍事科學院防化研究院張浩團隊[121]通過燒結法實現在Cu-Zn合金網上均勻包覆ZnO材料,依靠Cu-Zn合金的低層錯能,實現由化學能驅動表層原子擴散,而表面的ZnO使該材料擁有更好的親鋰性,實現調控鋰沉積、抑制鋰枝晶生成,在2 mA·cm-2電流密度下穩定循環500次以上。該方法的有效性和易操作性在1 m2的黃銅網和其他Cu合金(錫青銅)網上均得到了驗證。
Sb由于其獨特的褶皺層狀結構,對鋰離子表現出較高的導電性和反應活性,形成Li3Sb時,能提供660 mAh·g-1的理論容量。相比于Si,Ge和Sn,Sb在Li合金化/脫出時的體積膨脹較小,但也有147%。類似于Sn基合金,Sb基合金也可通過添加非活性物質抑制其體積膨脹。Hassoun等[122]在碳基體中將Li與Sb合金化,反應后合金的容量為250 mAh·g-1,充放電100次后仍保持穩定結構。研究人員針對Li-Sb合金的電子結構和相圖也開展了系統的研究[123],Zhuang等[124]采用XPS研究Li-Sb合金的形成及電子結構,價帶結構表現出明顯的非剛性能帶特征,表明合金中Li與Sb間有很強的共價鍵傾向,并且Li-Sb電極的合金化反應存在相變滯后現象[125]。Hou等[13]以Zn微球為模板,置換生成Sb后去除Zn,可得到多孔空心Sb微球(如圖9b),該材料做電極的電池在100次循環后容量穩定在660 mAh·g-1。

圖9 介孔Ge顆粒的TEM照片(a)[14],多孔空心Sb微球的SEM照片(b)[13]Fig.9 TEM image of Ge mesopores particles (a)[14],SEM image of Sb porous hollow microspheres (b)[13]
對鋰-金屬類合金來說,一個重要的問題是鋰合金化/脫出時巨大的體積膨脹,因此必須持續提升電極循環過程中的穩定性。與Si同族的Ge,Sn等在性質上有許多相似之處,比如比容量高、體積膨脹大、首次循環效率低等。此外,其與Li合金化的難易度有差別,根據混合焓計算,Li-Sn最易合金化,之后是Li-Ge和Li-Si[109]。而容量則按照Li-Si、Li-Ge、Li-Sn排序,體積膨脹率排序也如此。Si和Sn作為負極材料時常摻入碳等其他元素,而Ge在研究時常使用純Ge,通常通過改變Ge的微觀結構來改善其電化學性能,目前研究的重點方向仍然聚焦在純Ge負極。Cu在合金電極中則主要起骨架和引導鋰離子的作用,Li-Cu合金在鋰金屬電池中的研究較多。Zn在做合金骨架的同時,還能表現出良好的鋰親和性,引導控制鋰沉積,同時改善界面性能。
4 結 語
目前,文獻報道的鋰合金負極材料種類較少,已被報道的典型鋰合金材料及其所應用的電池體系和性能比較如表1所示,且絕大部分合金負極都存在著首次不可逆容量大、循環性能不理想等問題。造成鋰合金負極首次不可逆容量大的原因主要是:電解液在電極表面分解形成固體電解質相界面(SEI)膜,特別是納米合金的尺寸效應造成電極催化活性較高,易形成過厚SEI膜導致鋰損失,選擇合適的電解液可以減少這一部分損失。明軍團隊[126]對電解液與合金電極的親和性以及其在電池中的溶劑化作用進行了研究,重點闡述了電解液調控溶劑化結構對電池的重要性;合金化材料體積膨脹產生的機械應力使部分活性物質與集流體的電子緊密接觸弱化,甚至活性物質從集流體上脫落,這部分的Li在脫鋰反應中無法脫出,形成“死鋰”,使電池內阻升高并加劇枝晶的生長。此外,鋰合金負極不同原子間存在較大的尺寸差異,導致電極材料在Li脫出時產生劇烈的體積形變,使結構不穩定,由此誘發循環性能退化[127,128]。
針對上述問題,為了更好地將鋰合金類負極材料推向實用化,可以考慮采用以下4類典型改性方法:
第一,多元鋰合金的優化設計。向鋰合金中加入半徑合適的原子,以梯度半徑排列的形式增加堆積密度,提高材料的微觀空間利用率。該方法可有效改善電極在循環過程中的穩定性,減小電池的容量損失[89,103,129]。比如Lu等[130]以Li-Cu-Ni合金為基礎結合核殼結構的納米線設計獲得電池負極材料,極好地提升了材料的循環穩定性和倍率性能。此外,一些元素有助于構建穩定的骨架或者形成介于電子云重疊與共價鍵結合之間的緊密耦合(如B和Mg)[5],在合金化/脫出的時候保護材料結構不受破壞,引導Li有序沉積并提供空位。
第二,電解液的優化控制。電解液及其添加劑的調控對電池性能的影響尤其顯著,特別是表界面性能。鋰合金電極往往存在體積膨脹問題,因此穩定的、不易脫落的SEI就非常重要,向電解液中添加SEI穩定劑對電極性能的改善非常明顯[82],找到和電極體系匹配的電解液也可大幅改善合金化/脫出時的表界面性能。而針對鋰合金化學性質活潑、易燃的特性,可向電解液中添加阻燃劑或者使用凝膠態或固態電解質等提升電池的安全性[81,131]。而鋰合金電極因為親鋰性好、沉積電位低以及潤濕性好等優勢,在全固態電池中有著比金屬鋰更好的應用效果[119,120,132]。
第三,鋰合金表面的穩定化處理。電極表面對電池體系的重要性不言而喻。而鋰合金電極的體積效應顯著,因此可考慮在鋰合金表面涂覆一層剛性或彈性的材料,避免電極/電解液或電極/電極的直接接觸[15,20,133]。同時,還可通過涂覆支持離子選擇性快速通過的高分子膜來改善電極的浸潤性,以提高電池電化學性能。
第四,復合材料的構建。復合材料能為鋰合金在電化學循環中提供穩定存在的骨架[134],也能帶來一些其他的結構設計,比如核殼結構以及蛋黃殼結構等[135],這些結構能引導Li沉積在勢壘較低的空位,為電極膨脹提供緩沖空間,同時也可抑制鋰枝晶的形成、增加離子遷移通道等。在Si和Sn的使用中,與碳復合的材料已非常常見。
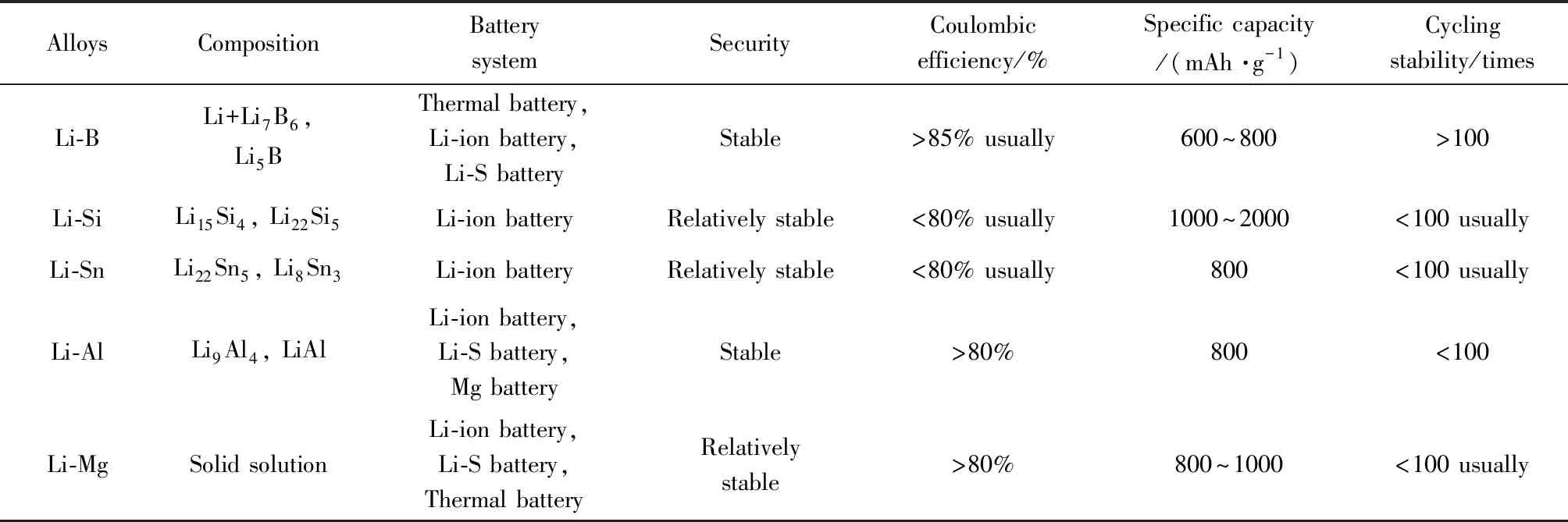
表1 各合金電極材料性能匯總Table 1 Properties of various alloy electrodes
綜上所述,鋰合金負極材料具有高比容量、低成本等優點,通過納米結構設計和制備均勻組分的材料緩解合金電極材料的體積效應和鋰枝晶生長,將會是下一代鋰離子電池電極材料最具潛力的研發思路之一。在未來的應用研究中,尚有一些問題需要克服:① 調控鋰合金負極表面SEI的形成以提高其庫倫效率;② 研究高效的鋰合金負極材料工業化制備工藝以加速其商業化進程。鋰合金負極材料有望為下一代高比能固態鋰離子電池以及鋰-氧氣、鋰-硫、鋰-二氧化碳、鋰-氟化硫等新電池體系提供穩定的負極材料,對未來的新能源產業有著重要的意義。

