局部枸櫞酸抗凝在危重癥患者持續腎臟替代療法中的臨床應用
焦清海,鄭麗環,張雪梅,王 征,杜 菲,陳 亮
(河北省邯鄲市第一醫院重癥醫學科,河北 邯鄲 056000)
在重癥監護病房(intensive care unit,ICU)血液動力學不穩定的危重癥患者行血液凈化治療時首選持續腎臟替代療法(continuous renal replacement therapy,CRRT),因ICU患者有出血及肝素導致的血小板減少的風險,使肝素抗凝的使用受到一定的限制。2012年KIDIGO指南推薦對于急性腎損傷的患者行CRRT時的抗凝首選局部枸櫞酸抗凝(regional citrate anticoagulation,RCA)[1]。以往的研究RCA顯著延長了濾過器的使用壽命[2],減少了出血并發癥,對尿毒癥和酸堿狀態提供了良好的控制,且在兒科患者中也有廣泛應用[3]。RCA對于大多數肝功能受損的患者也是安全的,而對于那些有嚴重的多器官功能障礙和高乳酸血癥的患者必須謹慎[4],但以往的研究都為小樣本的非隨機對照研究,對于危重患者CRRT的抗凝問題,RCA仍是目前研究的熱點。為進一步探討RCA在ICU危重患者持續靜脈靜脈血液濾過中的應用價值,筆者回顧性分析需行CRRT治療的668例危重患者的臨床資料,觀察兩組不同抗凝方式的有效性及安全性,旨在為ICU廣泛應用提供臨床依據。
1 資料與方法
1.1一般資料 回顧性分析2013年10月—2019 年10月在邯鄲市第一醫院重癥科就診需行CRRT治療且模式為連續靜脈靜脈血液濾過(continuous venous hemofiltration,CVVH)的危重患者668例的臨床資料,依據抗凝方式不同分為RCA組370例和肝素抗凝組298例。納入標準:①于我科住院需行CRRT治療,且模式為CVVH的危重患者;②年齡>18歲。排除標準:①枸櫞酸及普通肝素過敏;②觀察前12 h應用抗凝劑及各種影響患者凝血的藥物;③CRRT前凝血功能異常。本研究經醫院倫理委員會審批通過。
1.2方法 記錄患者的一般臨床資料,包括性別、年齡、急性生理和慢性健康(acute physiology and chronic health,APACHEⅡ)評分、CRRT治療原因、濾器壽命,濾器中止應用的原因、兩種抗凝方式相關的并發癥。
1.3CRRT及抗凝方案
1.3.1CRRT血管通路及置換液配方 通路為股靜脈留置12 F雙腔血液透析導管(廣東百合醫療科技股份有限公司),血液凈化機為日本旭化成可樂麗醫療株式會社生產的ACH-10,濾器均為費森尤斯人工合成膜血液濾過器AV600S。參照南京軍區總醫院port配方自行配制置換液,RCA時置換液中不含鈣,且結合泵入枸櫞酸的量,相應減少5%碳酸氫鈉用量。
1.3.2枸櫞酸抗凝方案 輸血用枸櫞酸鈉注射液(上海輸血技術有限公司)的初始泵速為血流速的1.2~1.5倍,開始抗凝后30~60 min監測濾器后鈣離子濃度,根據濾器后游離鈣濃度調整枸櫞酸抗凝液泵速,維持濾器后游離鈣濃度在0.2~0.4 mmol/L,抗凝達標后每隔4 h監測濾器后鈣離子濃度。在鎖骨下靜脈導管處泵入10%葡萄糖酸鈣注射液,監測動脈血氣分析中游離鈣濃度,調整10%葡萄糖酸鈣注射液的用量,保持動血游離鈣濃度為1.0~1.2 mmol/L。
1.3.3肝素抗凝方案 首次負荷量1 000~3 000 U靜脈滴注,在上機前5~10 min給予,然后以5~15 U·kg-1·h-1持續泵入,每間隔4~6 h檢測一次活化部分凝血活酶時間(activated partial thromboplastin time,APTT),根據結果,調整肝素鈉輸注速度,保持APTT于正常值的1.2~1.5倍。
1.4統計學方法 應用SPSS 22.0軟件統計分析數據。計量資料比較采用t檢驗;計數資料比較采用χ2檢驗;Kaplan-Meier生存曲線應用Log-Rank檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1一般資料 兩組性別、年齡、APACHE Ⅱ評分、CRRT治療原因等一般資料比較差異均無統計學意義(P>0.05)。見表1。

表1 兩組一般資料的比較
2.2濾器壽命的比較 RCA組濾器平均壽命(50.7±20.7)h長于普通肝素組(33.5±20.1)h,差異有統計學意義(t=11.100,P<0.001),見圖1。濾器壽命<24 h者所占比例,肝素抗凝組高于枸櫞酸抗凝組,濾器壽命≥48 h者所占比例,肝素抗凝組低于枸櫞酸抗凝組,差異有統計學意義(P<0.05);濾器壽命在24~48 h者,兩組比較差異無統計學意義(P>0.05)。見表2。

表2 兩組濾器壽命的比較

圖1 兩組濾器壽命的生存曲線
2.3血液濾過治療中斷原因的比較 分析兩組血濾中斷的原因,枸櫞酸抗凝組過濾器凝血比例低于肝素抗凝組,達到治療目的結束治療下機比例高于肝素組,櫞酸抗凝組治療超過72 h需要更換濾器比例高于肝素抗凝組,差異有統計學意義(P<0.05)。見表3。

表3 兩組患者血液濾過治療中斷原因的比較
2.4兩組出血事件的比較 兩組抗凝均無嚴重出血事件。枸櫞酸抗凝組枸櫞酸蓄積比例為3%,調整枸櫞酸用量或血泵速度均可改善蓄積。
2.5兩組治療結束后代謝性指標的標較 治療后,兩組血清總Ca2+、動脈血pH、游離Ca2+、Na+、HCO3-比較差異無統計學意義(P>0.05)。見表4。
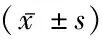
表4 兩組CVVH治療結束后代謝指標比較
3 討 論
目前,20%的ICU患者需要腎替代治療,而CRRT是首選的血液凈化技術,因其可對容量精確控制,穩定酸堿平衡和電解質紊亂,穩定患者血流動力學在ICU的AKI、膿毒癥和多器官功能衰竭患者中廣泛應用[5]。CRRT中斷最常見的原因是體外循環凝血,這會降低治療效果,而失血及體外循環的更換會增加治療成本[6],導致患者血流動力學不穩定,有研究顯示采用雙機換管法對連續性腎臟替代治療患者上機以降低更換濾器對血流動力學的影響[7],但科室血液凈化設備需配備充足,因此有效的抗凝尤其重要。據調查肝素是被廣泛應用且能熟練掌握的抗凝藥物,多數急診科在無禁忌情況下行CRRT時首選肝素抗凝49.68%,其次為RCA25.80%,和低分子肝素23.56%[8],故國內急診CRRT治療時應用RCA情況仍不理想,對RCA的認識有待提高。在CRRT中全身給予肝素,會增加出血的風險。國內外研究提示,RCA對CRRT抗凝效果顯著,可有效延長濾器使用壽命,改善患者腎功能,且不會影響患者凝血功能[2,9]。肝功能異常的患者,應用RCA也是相對安全的,但需密切監測患者的酸堿狀態及電解質[10]。越來越多的研究證明,RCA是一種安全有效的抗凝方式,但都為小樣本的非隨機對照研究研究。
研究顯示RCA在CVVHD模式較肝素抗凝有更長的濾器壽命,但可能出現代謝性酸中毒、代謝性堿中毒、低鈣血癥等代謝并發癥[11],為進一步探討RCA在危重患者CRRT中的有效性及安全性,本研究比較了RCA及肝素抗凝濾器壽命,血濾停止的原因以及與兩種抗凝方式相關的代謝異常和出血并發癥。
本研究結果顯示,RCA組的濾器壽命明顯長于肝素組,枸櫞酸抗凝組36.2%的濾器因超過72 h而計劃更換過濾器,肝素抗凝組只有14.1%,肝素治療組44.6%因過濾器凝血而中止治療,而局部枸櫞酸組僅有10.8%,更進一步說明RCA方法較肝素治療的透析器及管路的凝血事件發生率低,能保證置換液劑量,減少患者因頻繁的上下機的血壓波動,減少患者失血及耗材費用,減輕護士工作量,同時也減少了對于深靜脈導管的操作次數,可能降低了導管感染的概率。RAC在ICU高出血風險患者血液凈化治療中的應用也效果顯著[12],其可有效改善ICU血液凈化伴高出血風險的凝血指標,降低出血風險,為患者節約醫療費用,值得推廣。目前臨床工作中,直接監測枸櫞酸濃度是不可行的,故以監測濾器后的鈣離子濃度間接反映抗凝的有效性,枸櫞酸起始劑量為4 mmol/L,濾器后鈣離子范圍為0.25~0.35 mmol/L,有研究報道,69.7%的患者在RCA-CVVHD啟動時濾器后鈣離子的濃度在靶范圍內[13],在12 h內,濾器后鈣離子的濃度高于目標范圍的患者比例從13.1%顯著下降到7.8%,在最初低于、在目標范圍或高于目標范圍的濾器后鈣離子患者之間,濾器的生存率沒有顯著差異,提示可以減少濾器后鈣離子的監測頻率。
本研究選擇通過鎖骨下靜脈導管補充鈣離子,密切監測濾器后離子鈣的濃度、血清總鈣、游離鈣的濃度,調整鈣離子的補充,治療結束時枸櫞酸抗凝組總鈣、游離鈣、鈉離子、pH值與肝素組差異無統計學意義(P>0.05)。也有研究通過監測廢液中鈣離子的濃度,提出了數學模型來量化鈣補充劑的需要,使RCA處方個性化,并簡化CVVH模式下RCA的管理建立數學模型,補充體內丟失的鈣,減少了鈣的監測頻率,減少了醫療費用[14-15]。因進入體內的枸櫞酸可代謝為碳酸氫鹽,代謝性堿中毒是RCA的并發癥之一。在枸櫞酸抗凝過程中,調整抗凝劑的用量后,也要相應調整置換液中碳酸氫鈉的用量,以達到維持酸堿平衡的目的。
本研究顯示枸櫞酸蓄積發生率為3%,主要集中于血流動力學不穩定、多器官功能障礙患者,總鈣/游離鈣>2.5為枸櫞酸蓄積的閾值,也有研究顯示血乳酸增高也是早期發現枸櫞酸蓄積的有效指標[16],當枸櫞酸蓄積時,相應調整下調枸櫞酸鈉用量、增加置換液速度、下調血流速度,均可達到抗凝效果。枸櫞酸主要在肝臟、腎臟、骨骼肌的線粒體內[17],經三羧酸循環代謝,嚴重低血壓、低氧血癥及肝功能障礙為RCA的相對禁忌證。
本研究為回顧性研究,危重癥患者行CVVH時應用RCA,濾器壽命明顯延長,減少了耗材的應用,無明顯代謝并發癥及出血風險,治療過程中需監測濾器后鈣離子濃度及人體鈣離子濃度來保證抗凝的有效性及安全性,有望成為ICU患者CVVH治療時的一線抗凝方式。

