鼻咽癌調強放療計劃質量量化評價方法研究
顧慧寬,陳利,胡江,鄧小武,周凌宏
1.南方醫科大學生物醫學工程學院,廣東廣州510515;2.中山大學腫瘤防治中心放療科/華南腫瘤學國家實驗室/腫瘤醫學協同創新中心,廣東廣州510060
前言
放射治療是腫瘤治療的三大手段之一[1],是鼻咽癌(Nasopharyngeal Carcinoma, NPC)首選治療手段。隨著放療技術的發展,精準治療的概念被提出[2-3],如何提升和控制治療計劃的質量一直是放射物理的研究熱點之一。臨床上放療計劃質量的評估方法為觀察各平面劑量分布情況及使用劑量體積直方圖(Dose-Volume Histogram,DVH)進行評價和分析[4-5],判斷若干臨床要求是否滿足或評價項目是否可行,然后給出通過或不通過計劃的結論。這種方法一般基于物理師和臨床醫生的經驗,容易被肉眼觀察的結果或心理偏差等主觀因素影響最終選擇;也缺乏有效的定量分析方法量化計劃質量差異,無法識別次優計劃或質量異常計劃。
本研究以臨床醫生計劃評價及選擇為最終評價標準,根據RTOG0615 臨床試驗[6]及臨床處方劑量要求,設計針對NPC 調強放療(Intensity-Modulated Radiation Therapy,IMRT)計劃質量的量化評價方法,由醫生與物理師協同合作評價項目,確定每個項目的計算節點與權重,建立鼻咽癌計劃質量評估模型,把計劃質量量化為計劃質量指數(Plan Quality Index,PQI)。對153 例既往病例進行回顧性分析,通過調節計劃的處方劑量驗證計算模型的敏感性,同時用模型計算的結果與臨床醫生的選擇結果相比較,驗證該模型在臨床應用的有效性。
1 材料與方法
1.1 患者臨床資料
回顧性選取2014年8月~2019年12月在中山大學腫瘤防治中心進行放射治療的153例NPC病例,其中T1 期4 例、T2 期12 例、T3 期87 例、T4 期50 例;男114 例,女39 例。中位年齡45 歲。本文是回顧性分析,實驗對象是已經結束治療的病例,并不涉及到患者的臨床治療,患者相關信息均做了匿名處理以保護其隱私權。
根據國際指南及中心相關規定,由醫師勾畫原發腫瘤靶區(Nasopharynx Gross Tumor Volume,GTVnx)、轉移淋巴結(Lymph Node Gross Tumor Volume, GTVnd),并外擴形成計劃靶區(Planning Target Volume,PTV):原發灶計劃靶區為PGTVnx,頸部轉移淋巴結計劃靶區為PTVnd,臨床高危預防區域為PTV1,臨床低危預防區域為PTV2。對部分危及器官(Organ at Risk,OAR)外擴后形成計劃危及體積(Planning Organ-at-Risk Volumes,PRV)結構。
1.2 病例選取要求
所有病例均采用統一的處方劑量:PGTVnx,70 Gy;PTVnd(L/R),66 Gy;PTV1,60 Gy;PTV2,54 Gy/33 F,計劃的目標劑量要求見表1,使用Eclipse(v10.0,Varian,USA)計劃系統為每例患者設計了9 野IMRT計劃,使用6 MV 光子射線和各向異性(Anisotropic Analytical Algorithm, AAA)算法,劑量計算網格為2.5 mm×2.5 mm×2.5 mm。

表1 鼻咽癌IMRT計劃設計劑量目標Tab.1 Clinical goal and constraint of intensity-modulated radiotherapy plan for nasopharyngeal carcinoma(NPC)
1.3 計劃質量量化評價算法
本研究采用多指征項的計劃質量量化評估機制,對靶區和危及器官分別設計計劃質量評價函數,并由醫生提供函數的權重。共54 個評價指征項目,每個項目量化計算函數由線性函數及多個評價節點連接不同斜率的分段函數組成,圖1中是其中兩項計劃質量計算函數示意圖。
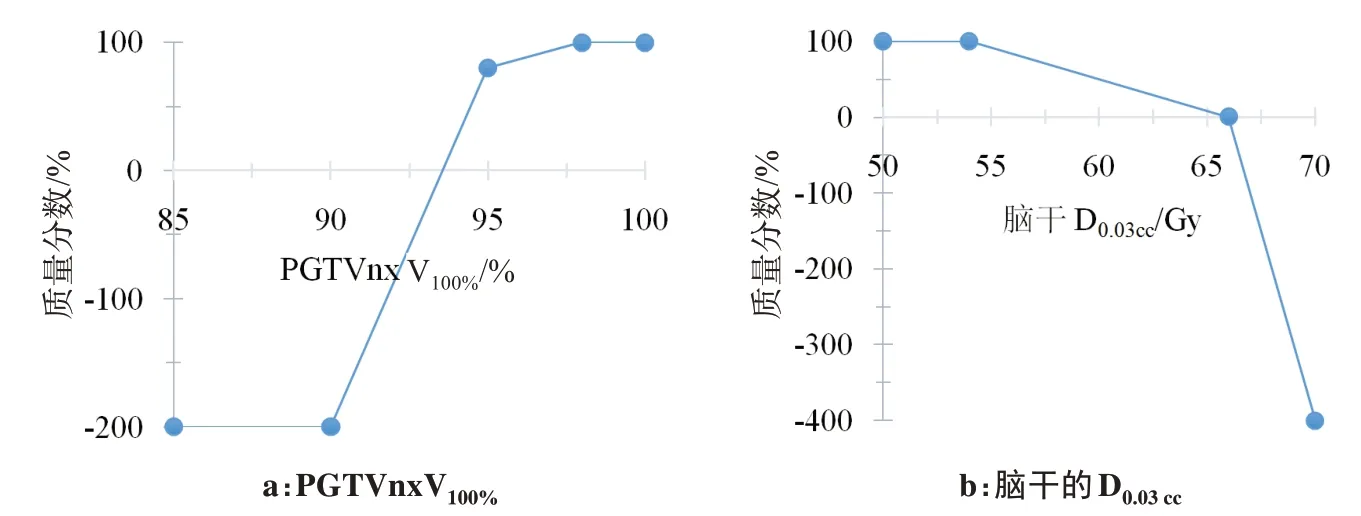
圖1 計劃質量評價函數示意圖Fig.1 Schematic diagrams of calculation formulas for plan quality evaluation
根據放射治療原則,靶區處方劑量覆蓋越高,OAR 劑量越低,則得分越高。部分節點設有負值,例如,PGTVnx 靶區劑量覆蓋率和腦干的最大劑量D0.03cc(最小體積0.03 cc對應的絕對劑量)的質量計算如公式(1)和(2)所示:

適形度指數CI、均勻性指數HI根據公式(3)、(4)進行計算[7-8]:
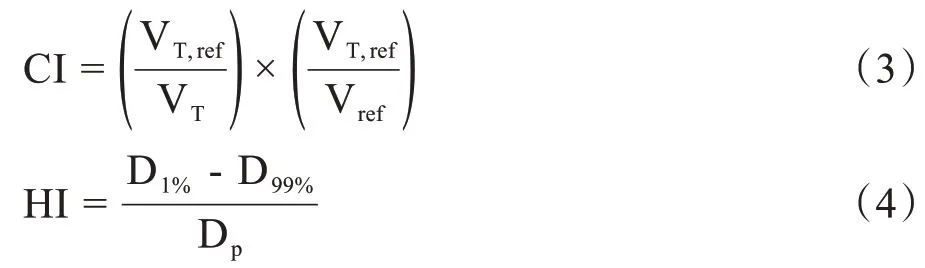
其中,VT,ref為接受劑量≥參考劑量的靶區體積(cm3),VT為靶區體積(cm3),Vref為接受劑量≥參考劑量的體積(cm3)。CI 的范圍為0~1,CI=1 時適形性最佳;CI=0 時無適形性。D1%、D99%為受照射劑量最高的1%、99%的PTV 中的最小劑量(cGy),Dp為處方劑量(cGy)。HI理想值為0,隨劑量不均勻性增大而增大。
PQI為所有評價項目的質量分數的總和,即:

其中,xi為是第i個計劃質量評價項目,wi是該評價項目的權重因子,n是評價項目數量,本研究中PQI總分設置為364 分,即∑wi= 364,總分做歸一處理,詳細數據見表2。
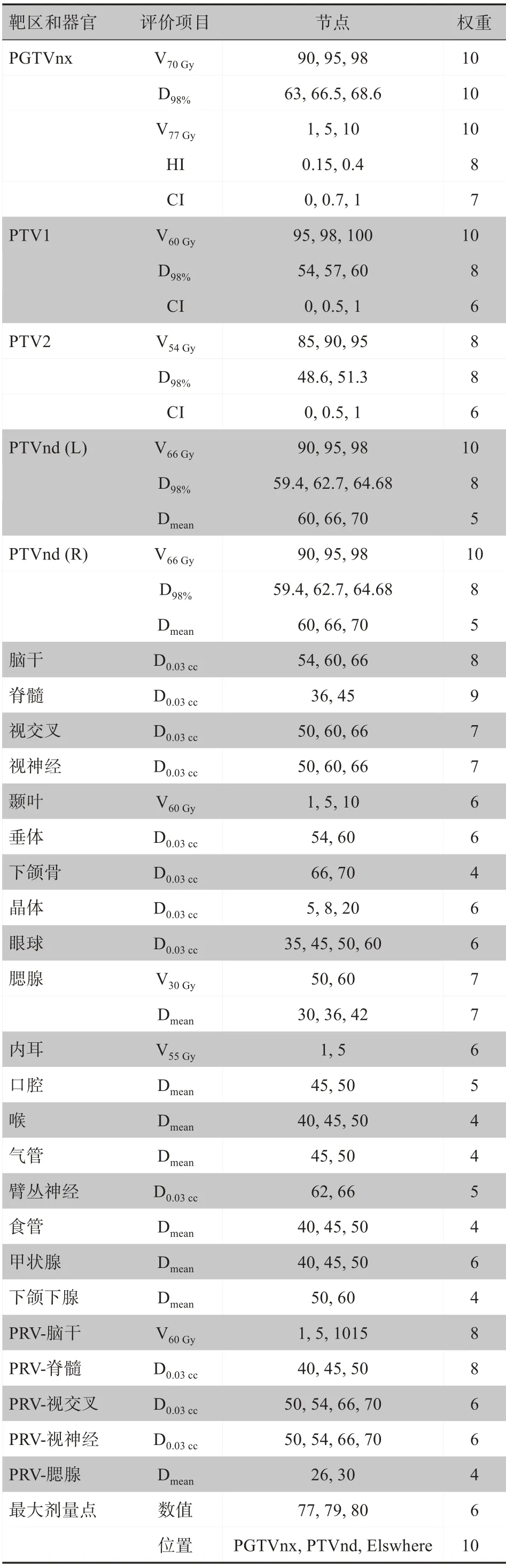
表2 計劃質量計算評價內容和權重Tab.2 Evaluation items and weights for plan quality calculation
通過DICOM協議將所有患者的計劃(包括CT圖像、結構、計劃和劑量文件)傳至PlanIQ(SNC Corp.,USA)軟件[9-11],根據上述設計的評價項目和計算節點設計PQI計算模型,進行計劃質量的量化評估計算。
1.4 量化評價方法的驗證
設計PQI算法對處方劑量改變的敏感性實驗,選取123 例病例,每例包含A、B、C 3 個試驗計劃,計劃A為已經確認并治療的臨床計劃;根據臨床上劑量控制不確定度在5%內的要求[12],本研究使用3%劑量偏差生成試驗計劃B(將計劃A 的處方劑量歸一到97%劑量曲線)和試驗計劃C(將A 歸一到103%劑量曲線),A、B、C 均為臨床可接受計劃。用上述量化評估模型對3 組計劃進行PQI 計算并統計分析,認為每例中計劃A 應得分最高,且計劃B 和C 的分數應與A有明顯差異,驗證模型的敏感性。
設計PQI 算法與臨床醫師決策計劃的一致性試驗,根據已有的30 例病例,每例包含臨床計劃Clinical 和未被選擇的計劃Unselected 兩組計劃。用上述評價算法對兩組計劃計算PQI并進行統計分析,得分高者為評價算法選擇的計劃,將評價算法與醫生選擇的結果進行一致性的比較,認為每組中Clinical 應得分最高,驗證模型的有效性與臨床實用性。
1.5 統計學分析
采用SPSS 20.0 軟件進行分析,對試驗組3 組計劃的全部評價項目進行正態性分析及方差齊性檢驗,因試驗組樣本大于50,使用Kolmogorov-Smirnov統計量,P>0.05 代表服從正態分布;取Levene 方差齊性檢驗結果,P>0.05 代表方差齊;對符合正態分布并方差齊的項目進行多組配對資料的方差分析(F-test);若有一項不符合則進行多組配對資料的秩和檢驗(Friedman test),P<0.05 為差異有統計學意義。對驗證組2 組計劃進行配對t檢驗的統計分析,P<0.05 為差異有統計學意義。
2 結果
2.1 計劃質量計算結果
圖2顯示123 例NPC 病例臨床計劃A 的PGTVnxV70Gy和左腮腺V30Gy,左顳葉V60Gy體積百分數的結果,不同臨床計劃的各項目之間數據存在明顯差異,PGTVnxV70Gy、左腮腺V30Gy、左顳葉V60Gy波動范圍分別為91.44%~99.92%、36.95%~100%、0%~23.56%。圖3顯示臨床計劃A的PQI直方圖,由圖可知PQI數值近似服從正態分布,均值79.33,標準差12.404,A、B、C 3組計劃各評估項目PQI值計算結果如表3所示。
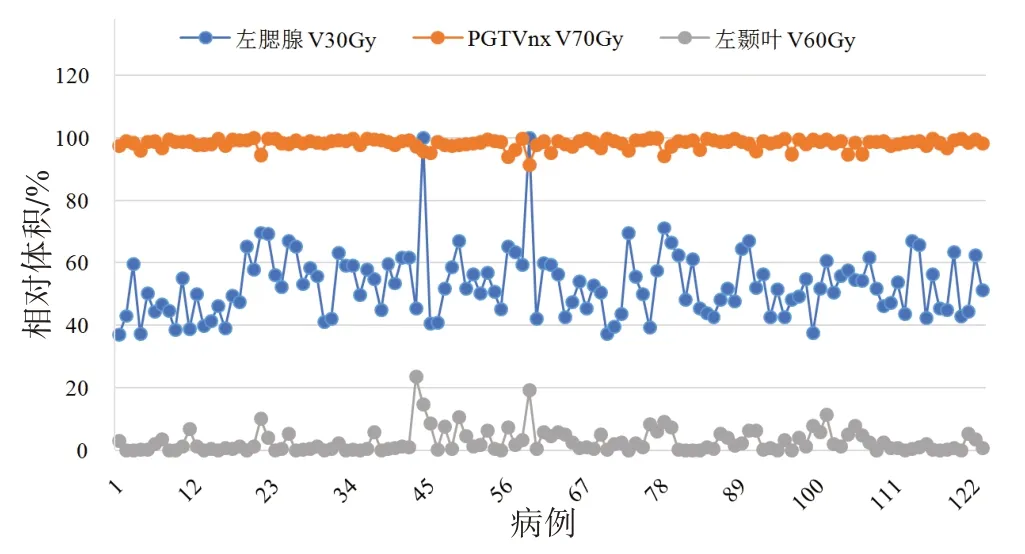
圖2 123例NPC病例臨床計劃的PGTVnx V70 Gy和左腮腺V30 Gy,左顳葉V60 Gy體積變化曲線Fig.2 Relative volume change curves of the V70 Gy of PGTVnx,the V30 Gy of the left parotid gland and the V60 Gy of the left temporal lobe in clinical plans for 123 NPC cases
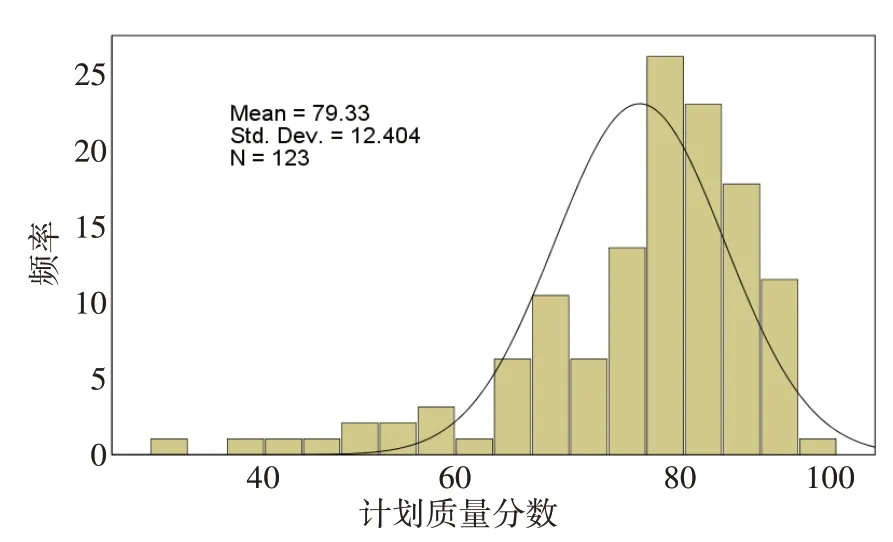
圖3 123例NPC病例臨床計劃PQI直方圖Fig.3 Histogram of plan quality index(PQI)of clinical plans for 123 NPC cases
2.2 PQI隨處方變化的結果及比較
圖4顯示了123例病例A、B、C 3組計劃PQI的莖葉圖,3組計劃PQI均值分別為79.33±12.40,63.93±12.78,68.27±9.84,表3顯示123例病例3組計劃各個項目的評分結果有明顯差異及變化趨勢,靶區PGTVnx的V70Gy及D98%的覆蓋(B>A>C)及PGTVnx 高劑量區V77Gy(A>C>B)等趨勢均可表明PQI隨處方變化有明顯改變,組間差異均有統計學意義(P<0.01)。
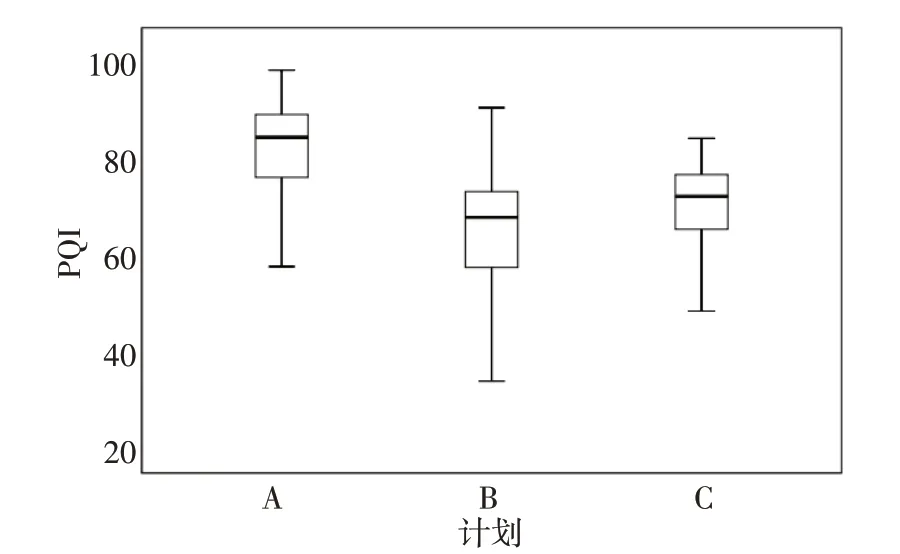
圖4 123例NPC病例的3組IMRT計劃PQI莖葉圖Fig.4 Stem-and-leaf map of PQI of 3 groups of IMRT plans for 123 NPC cases
表3 3組計劃靶區和危及器官劑量參數PQI比較(±s)Tab.3 Comparisons of the PQI dosimetric parameters of target areas and organs-at-risk among 3 groups of plans(Mean±SD)
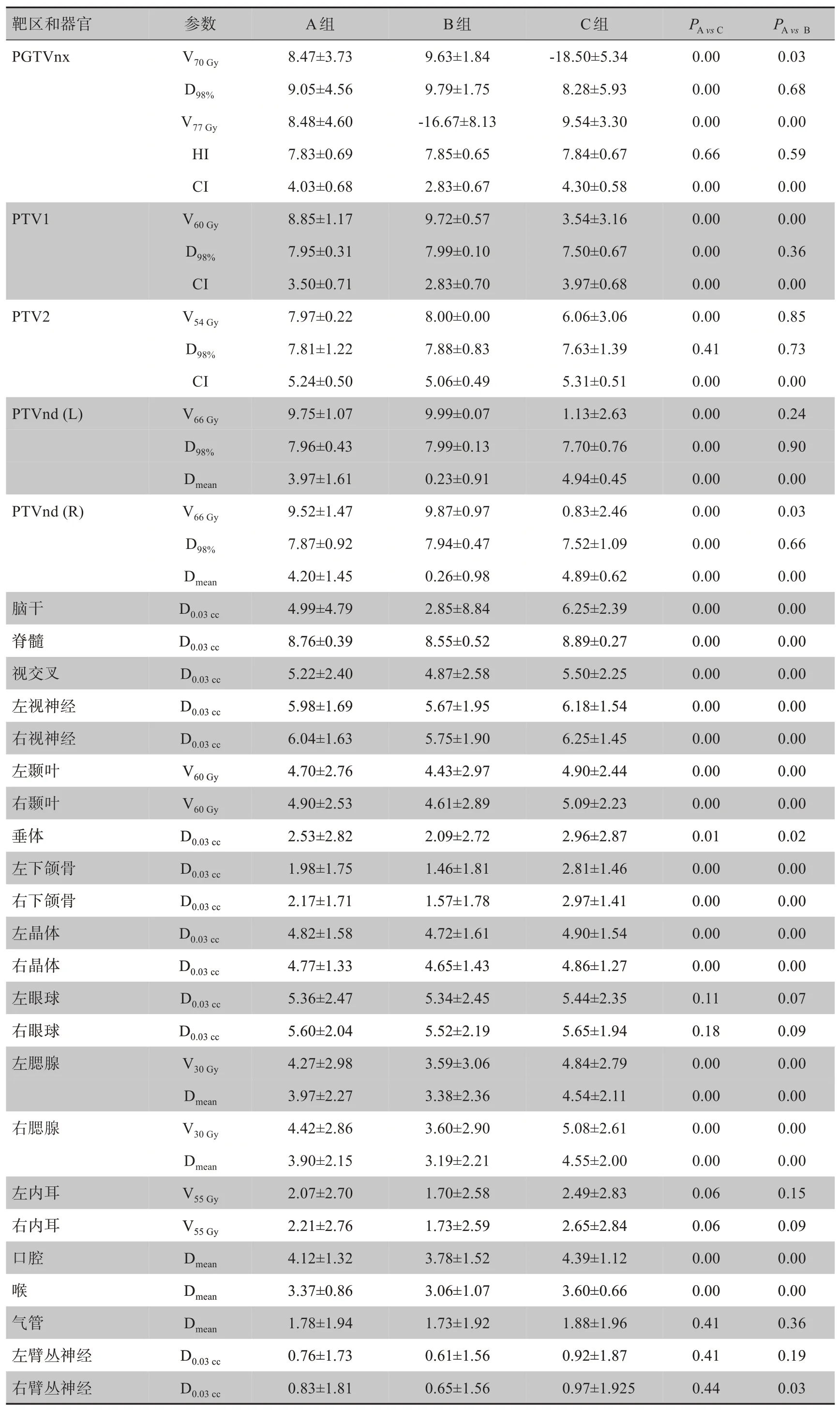
表3 3組計劃靶區和危及器官劑量參數PQI比較(±s)Tab.3 Comparisons of the PQI dosimetric parameters of target areas and organs-at-risk among 3 groups of plans(Mean±SD)
靶區和器官PGTVnx參數V70 Gy PA vs C PA vs B PTV1 D98%V77 Gy HI CI V60 Gy CI V54 Gy D98%PTV2 D98%PTVnd(L)CI V66 Gy D98%Dmean PTVnd(R)V66 Gy D98%Dmean腦干D0.03 cc A組8.47±3.73 9.05±4.56 8.48±4.60 7.83±0.69 4.03±0.68 8.85±1.17 7.95±0.31 3.50±0.71 7.97±0.22 7.81±1.22 5.24±0.50 9.75±1.07 7.96±0.43 3.97±1.61 9.52±1.47 7.87±0.92 4.20±1.45 4.99±4.79 B組9.63±1.84 9.79±1.75-16.67±8.13 7.85±0.65 2.83±0.67 9.72±0.57 7.99±0.10 2.83±0.70 8.00±0.00 7.88±0.83 5.06±0.49 9.99±0.07 7.99±0.13 0.23±0.91 9.87±0.97 7.94±0.47 0.26±0.98 2.85±8.84 C組-18.50±5.34 8.28±5.93 9.54±3.30 7.84±0.67 4.30±0.58 3.54±3.16 7.50±0.67 3.97±0.68 6.06±3.06 7.63±1.39 5.31±0.51 1.13±2.63 7.70±0.76 4.94±0.45 0.83±2.46 7.52±1.09 4.89±0.62 6.25±2.39 0.00 0.00 0.00 0.66 0.00 0.00 0.00 0.00 0.00 0.41 0.00 0.00 0.00 0.00 0.00 0.00 0.00 0.00 0.03 0.68 0.00 0.59 0.00 0.00 0.36 0.00 0.85 0.73 0.00 0.24 0.90 0.00 0.03 0.66 0.00 0.00脊髓視交叉左視神經右視神經左顳葉右顳葉垂體左下頜骨右下頜骨左晶體右晶體左眼球右眼球左腮腺V30 Gy Dmean右腮腺V30 Gy Dmean左內耳V55 Gy 4.27±2.98 3.97±2.27 4.42±2.86 3.90±2.15 2.07±2.70 3.59±3.06 3.38±2.36 3.60±2.90 3.19±2.21 1.70±2.58 4.84±2.79 4.54±2.11 5.08±2.61 4.55±2.00 2.49±2.83 0.00 0.00 0.00 0.00 0.06 0.00 0.00 0.00 0.00 0.15 D0.03 cc D0.03 cc D0.03 cc D0.03 cc V60 Gy V60 Gy D0.03 cc D0.03 cc D0.03 cc D0.03 cc D0.03 cc D0.03 cc D0.03 cc右內耳口腔喉氣管左臂叢神經右臂叢神經V55 Gy Dmean Dmean Dmean D0.03 cc D0.03 cc 8.76±0.39 5.22±2.40 5.98±1.69 6.04±1.63 4.70±2.76 4.90±2.53 2.53±2.82 1.98±1.75 2.17±1.71 4.82±1.58 4.77±1.33 5.36±2.47 5.60±2.04 2.21±2.76 4.12±1.32 3.37±0.86 1.78±1.94 0.76±1.73 0.83±1.81 8.55±0.52 4.87±2.58 5.67±1.95 5.75±1.90 4.43±2.97 4.61±2.89 2.09±2.72 1.46±1.81 1.57±1.78 4.72±1.61 4.65±1.43 5.34±2.45 5.52±2.19 1.73±2.59 3.78±1.52 3.06±1.07 1.73±1.92 0.61±1.56 0.65±1.56 8.89±0.27 5.50±2.25 6.18±1.54 6.25±1.45 4.90±2.44 5.09±2.23 2.96±2.87 2.81±1.46 2.97±1.41 4.90±1.54 4.86±1.27 5.44±2.35 5.65±1.94 2.65±2.84 4.39±1.12 3.60±0.66 1.88±1.96 0.92±1.87 0.97±1.925 0.00 0.00 0.00 0.00 0.00 0.00 0.01 0.00 0.00 0.00 0.00 0.11 0.18 0.06 0.00 0.00 0.41 0.41 0.44 0.00 0.00 0.00 0.00 0.00 0.00 0.02 0.00 0.00 0.00 0.00 0.07 0.09 0.09 0.00 0.00 0.36 0.19 0.03
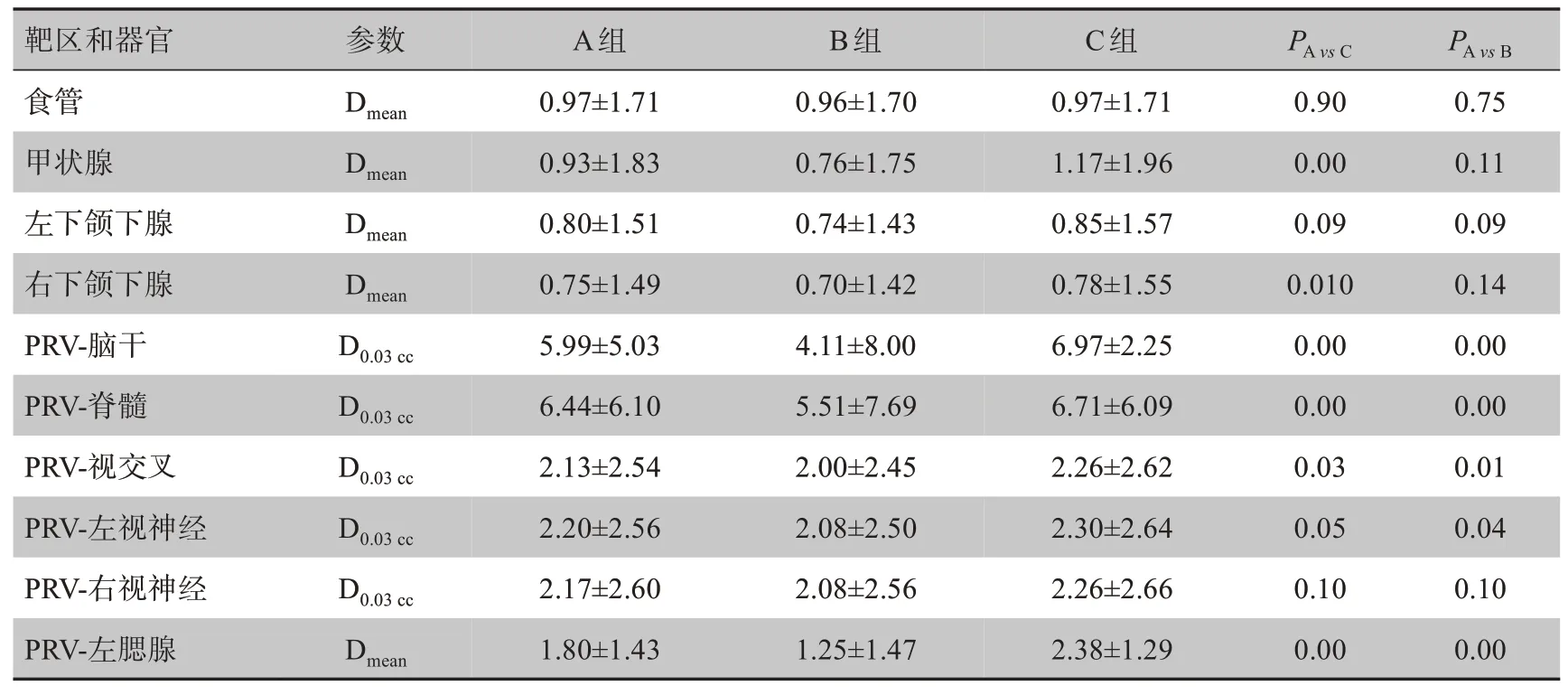
續表3
2.3 PQI與醫生選擇結果的一致性比較
圖5顯示30 例NPC 病例的兩組IMRT 計劃的PQI 柱形圖,兩組計劃PQI 均值分別為80.15±10.96,74.78±9.41,差異具有統計學差異(P<0.01)。其中有25例病例的PQI選擇結果與醫生選擇結果一致,一致性比例為83.3%。
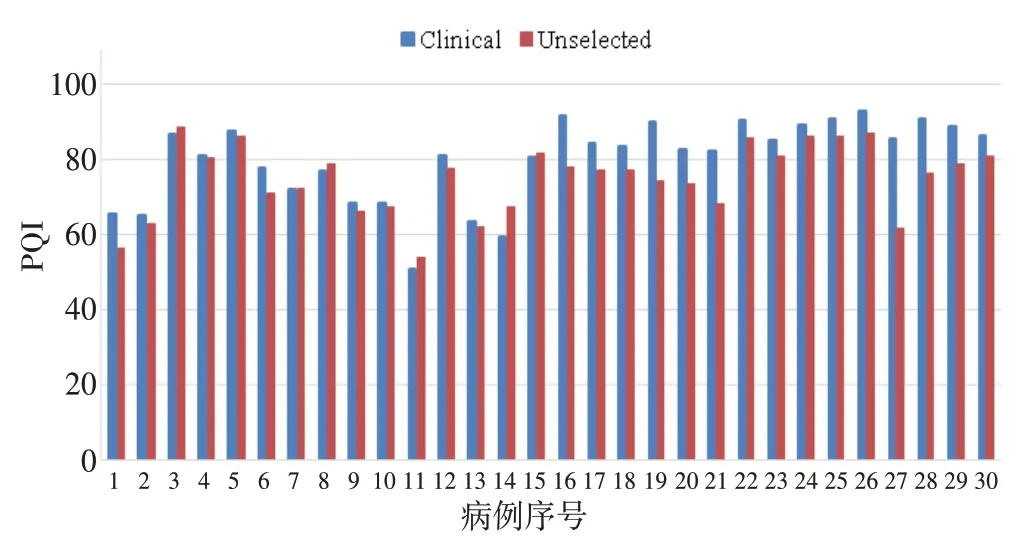
圖5 30例NPC病例兩組IMRT計劃PQI的柱形圖Fig.5 Histogram of the PQI of 2 groups of IMRT plans for 30 NPC cases
圖6顯示30 例病例兩組計劃之間的PQI 分數差異(Clinical-Unselected)的頻率分布直方圖,由圖可知兩組計劃分數差異均在20%以內,PQI 差異為2%分布頻率最高。在選擇結果不一致的5 例計劃中,PQI差異在1%以內的病例數為1,在2%以內的病例數為3。考慮臨床計劃質量本身容許的劑量分布差異,如果取容差2%,則本計劃質量計算模型計算的PQI 結果與臨床醫師選擇一致性為93.3%。
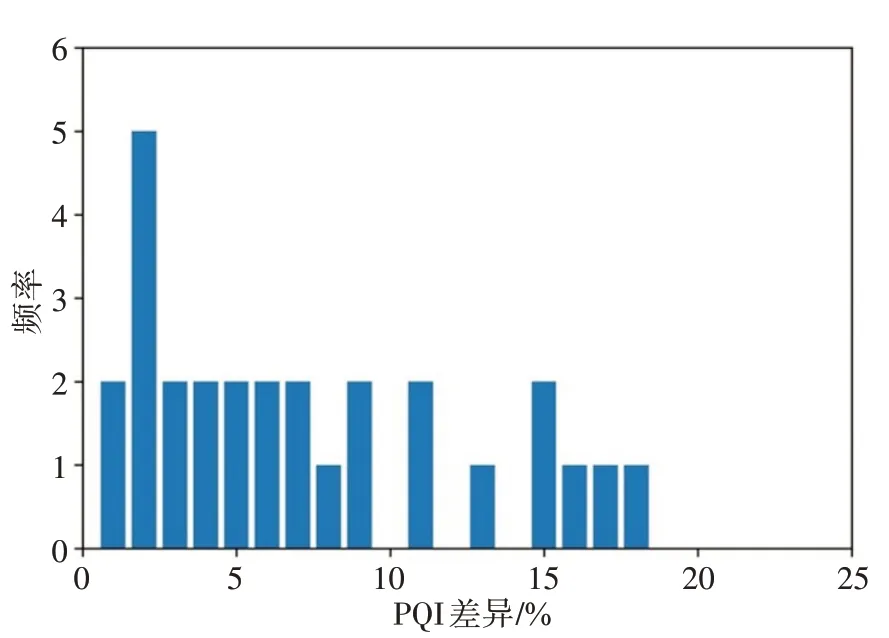
圖6 臨床計劃與未被選中計劃差異分布直方圖Fig.6 Histogram of the differences between the clinical plans and the unselected plans
3 討論
在鼻咽癌放療的臨床工作中,放療計劃傳統方法主要依照主觀經驗進行質量評估,目前還沒有通用的定量標準[13],傳統方法使用若干DVH 評價參數[14-15]進行二維劑量層面的定性分析,評價結果只有接受或不接受兩種形式。但計劃優化過程中可能產生多個臨床可接受計劃,定性分析方法無法精準描述不同計劃之間的差異,也無法選擇和分辨臨床醫生對個體放療的需求。本研究設計了綜合的計劃質量量化評價方法,通過設置NPC 調強放療計劃的質量評價項目,根據臨床醫生預設的評價項目權重因子,對每個項目設計量化的質量計算方法,可以量化質量的差異。現有研究中評分函數多為單一斜率的線性函數,僅定義評分上限和下限值[16-17]。本研究由不同評價節點連接建立線性組合函數,并對臨床優先級較高的評價項目設置負的質量計算方法,如圖1b 可以看到具有圖形直觀性的評價函數及計算方法,在腦干的最大劑量大于70 Gy時,該評價項目扣4倍分數。計算結果表明PQI 可以量化計劃優化過程中產生的計劃差異的確切數值,本研究設計的敏感性實驗證實該模型可以準確量化計劃處方劑量變化所帶來的計劃質量差異如圖4所示。
PQI量化評價方法有很多優點。首先,模型可以定量計算劑量分布與預設優化條件之間的差異,如圖2所示,即使是臨床接受的不同計劃,其各個評價項目之間均具有明顯差異,提示了計劃質量的一致性較差,需要有量化的指標,本研究的計算結果表明123例NPC計劃的PQI呈正態分布(圖3),與3%處方偏差的計劃相比,臨床計劃的PQI最高;其次,可以通過更換不同組的權重因子和量化計算節點,快速生成具有選擇傾向性的評估模型,幫助臨床醫生在多個評估計劃中,選擇出更符合自身習慣和要求的計劃,如圖5和圖6所示,模型與醫生選擇結果一致性比例為93.3%,認為該模型與醫生選擇結果具有較高一致性;最后,評估模型得到的PQI 數值可以支持不同放療中心之間的計劃數據交流和比較,減少中心內和不同中心之間同類計劃的差異,提升現階段放療計劃的整體質量,也有助于臨床計劃數據的快速收集和積累,對未來的療效評價和治療響應提供數據支撐。
綜上所述,本研究所設計的鼻咽癌放療計劃質量的量化評估算法可以計算出量化的計劃質量數值PQI,具有較高的劑量處方敏感性和臨床醫師選擇一致性,具有臨床實用性。