八種評分系統對肝硬化失代償期患者短期預后的預測價值
祝 強 楊繼敏 劉中亮
首都醫科大學密云教學醫院消化內科,北京 101500
肝硬化每年以5%~7%的速度從代償期發展到失代償期[1],代償期中位生存期為10~12年,失代償期中位生存期為2~4年,終末階段常出現慢加急性肝衰竭(ACLF)和肝硬化急性失代償(AD),表現為多器官功能衰竭和短期高死亡率[2]。在過去的三十年中已經提出了許多評分來預測肝硬化的預后,但在進行臨床現場決策時適用性通常令人不滿意。因為單個患者與評分所基于的平均患者群體不同,所處疾病階段差異、不同地區流行病學差異等。本研究擬對 MELD、MELD-Na、AIMS65、GBS、CTP、mDF、ABIC、CLIF-C ADs[3-8]八種評分系統進行比較,辨別適合本地區預測短期預后的評分系統。
1 資料與方法
1.1 一般資料
選取2015年1月至2020年7月首都醫科大學密云教學醫院收治的227例肝硬化失代償期患者資料。根據入院后28 d隨訪結果分組。A組(未輸血好轉組,n=145),男83例,女62例,年齡52~78歲;B組(輸血好轉組,n=50),男33例,女17例,年齡52~82歲;C組(臨床死亡組,n=32),男18例,女14例,年齡54~82歲。納入標準:符合《肝硬化診治指南(2019更新)》[9]中的診斷標準。排除標準:肝癌或其他惡性腫瘤;肝臟或其他器官移植史;HIV感染者;合并其他嚴重疾病;臨床資料嚴重缺失者。
1.2 方法
1.2.1 觀察指標 患者入院24 h內的實驗室指標以及年齡、肝性腦病等。肝性腦病的診斷及分級以《肝硬化肝性腦病診療指南》為標準[10]。以臨床死亡及輸血事件為主要研究終點。
1.2.2 八種評分系統介紹 MELD[5]公式=3.78 ln[bilirubin(mg/dl)]+11.20 ln(INR)+9.57 ln[creatinine(mg/dl)]+6.431× 病 因。 病 因 為 膽汁性或酒精性為0,其他為1;低危:≤14分,中危:15~18分,高危:>18分。MELD-Na[8]公式 =MELD+1.32×(137-Na)-[0.033×MELD×(137-Na)]。血清鈉≤125 mmol/L者按125 mmol/L計算,≥137 mmol/L者按137 mmol/L計算。AIMS65[4]根據Alb、INR、神志改變、收縮壓、年齡計算,總分為5分。GBS根據收縮壓、血尿素氮、Hb、脈搏、黑便、暈厥、肝臟疾病、心力衰竭計算,<6分為低危,≥6分為中高危。CTP[5]根據肝性腦病(級)、腹水、TBil、INR、Alb計算,A級:5~6分,B級:7~9分,C級:≥10分。mDF[5]公式=4.6(patient's PT-reference PT)+total bilirubin(mg/dl)。≥32分,短期死亡率高。ABIC[5]公式=(age×0.1)+[serumbilirubin(mg/dl)×0.08]+[serumcreatinine(mg/dl)×0.3]+(INR×0.8)。A 級:< 6.71,B級:6.71~ 8.99,C級:≥ 9.0。CLIF-CADs[7]公式 =10×[0.03×Age{years}+0.66×ln(Creatinine{mg/dl})+1.71×ln(INR)+0.88×ln(WBC{109cells/L})-0.05×Sodium{mmol/L}+8]。分數越高,預后越差。
1.3 統計學處理
采用SPSS 25.0及MedCalc 19.4統計學軟件進行統計分析。正態分布計量資料以()表示,依方差不同采用ANOVA檢驗和Kruskal-Wallis H檢驗;組間比較采用χ2檢驗。測算ROC來比較八種評分的預測價值,使用delong法比較AUC值間的差異。P<0.05為差異有統計學意義。
2 結果
2.1 三組各觀察指標比較
三組年齡、性別、脈搏比較差異無統計學意義,見表1。病因(酒精性肝硬化、乙型肝炎/丙型肝炎、混合性、隱源性肝硬化、其他)構成比較差異無統計學意義(P>0.05),見表2。C組的WBC、TBil、血尿素氮、血肌酐、INR、PT、腹水和肝性腦病評分水平高于A組,收縮壓、Hb、Na、Alb水平低于A組(P<0.05),結果顯示在肝硬化不同階段,觀察指標具有不同的權重。
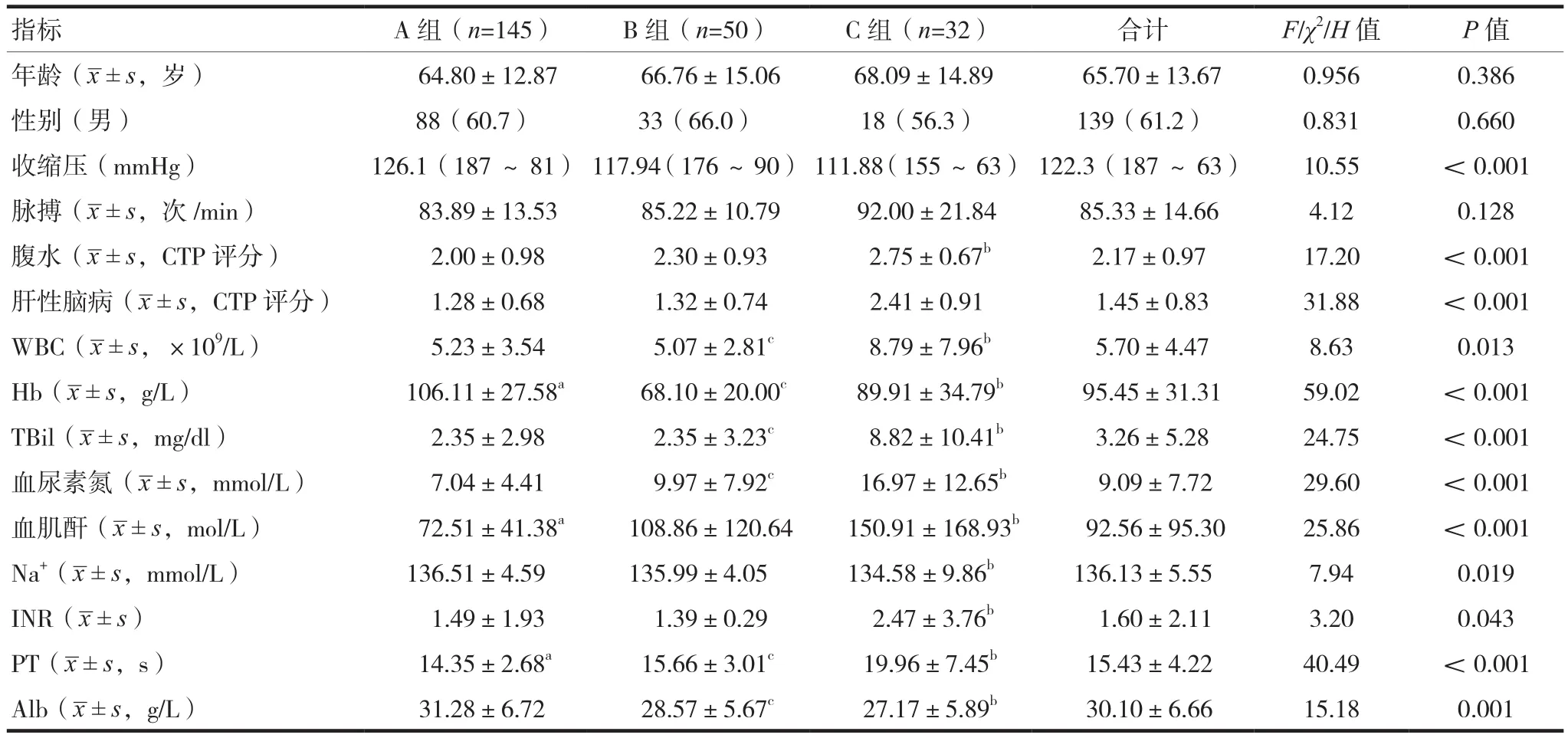
表1 三組各觀察指標比較
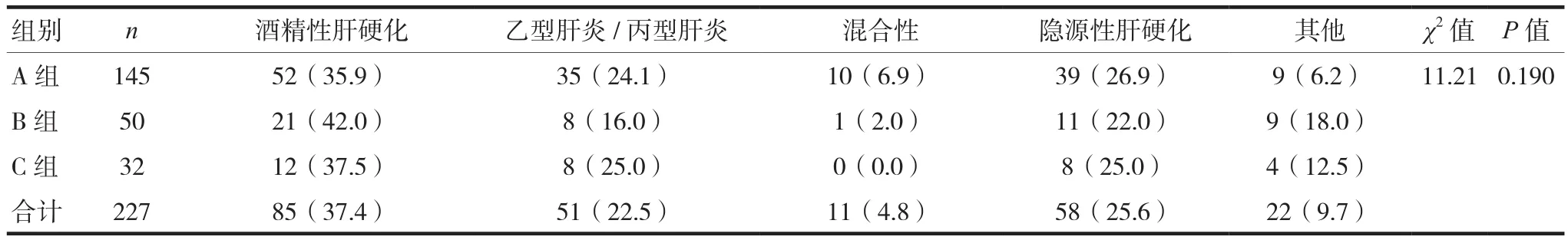
表2 三組患者病因構成比較[n(%)]
2.2 三組風險分級比較
三組對八種評分產生的風險分級比較,差異有統計學意義(P<0.05),顯示八種評分在不同階段預測存在偏差,見表3~4。
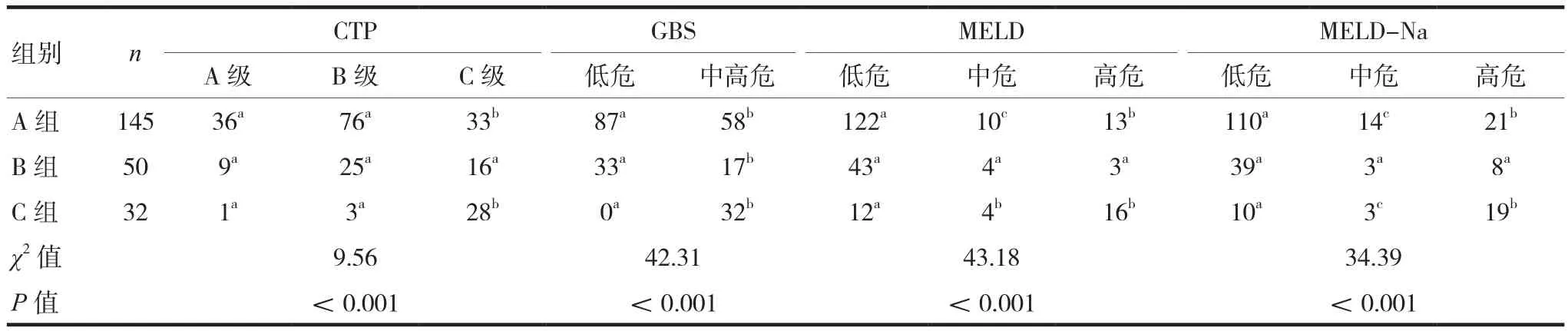
表3 三組CTP、GBS、MELD、MELD-Na風險分級比較
2.3 三組八種評分比較
C組八種評分高于A組和B組(P<0.001);B組 GBS、AIMS65、CTP高于A 組(P< 0.05),見表 5。
表5 三組八種評分比較(,分)
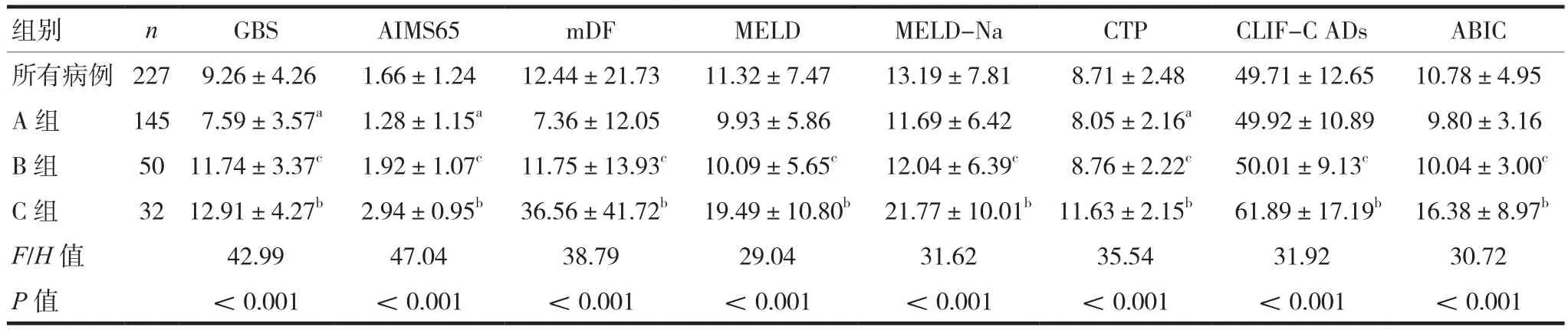
表5 三組八種評分比較(,分)
注:與B組比較,aP<0.05;與A組比較,bP<0.05;與C組比較,cP<0.05
組別 n GBS AIMS65 mDF MELD MELD-Na CTP CLIF-C ADs ABIC所有病例 227 9.26±4.26 1.66±1.24 12.44±21.73 11.32±7.47 13.19±7.81 8.71±2.48 49.71±12.65 10.78±4.95 A 組 145 7.59±3.57a 1.28±1.15a 7.36±12.05 9.93±5.86 11.69±6.42 8.05±2.16a 49.92±10.89 9.80±3.16 B 組 50 11.74±3.37c 1.92±1.07c 11.75±13.93c 10.09±5.65c 12.04±6.39c 8.76±2.22c 50.01±9.13c 10.04±3.00c C 組 32 12.91±4.27b 2.94±0.95b 36.56±41.72b 19.49±10.80b 21.77±10.01b 11.63±2.15b 61.89±17.19b 16.38±8.97b F/H值 42.99 47.04 38.79 29.04 31.62 35.54 31.92 30.72 P值 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001
2.4 八種評分對短期臨床預后的預測價值
在本研究中CTP評分預測臨床死亡價值最高(AUC=0.864);其余評分的AUC在0.824~0.758間,見圖1。八種評分預測輸血事件的價值有限,GBS的AUC值為0.727,其余評分的AUC值在0.585~0.464間,見圖2。
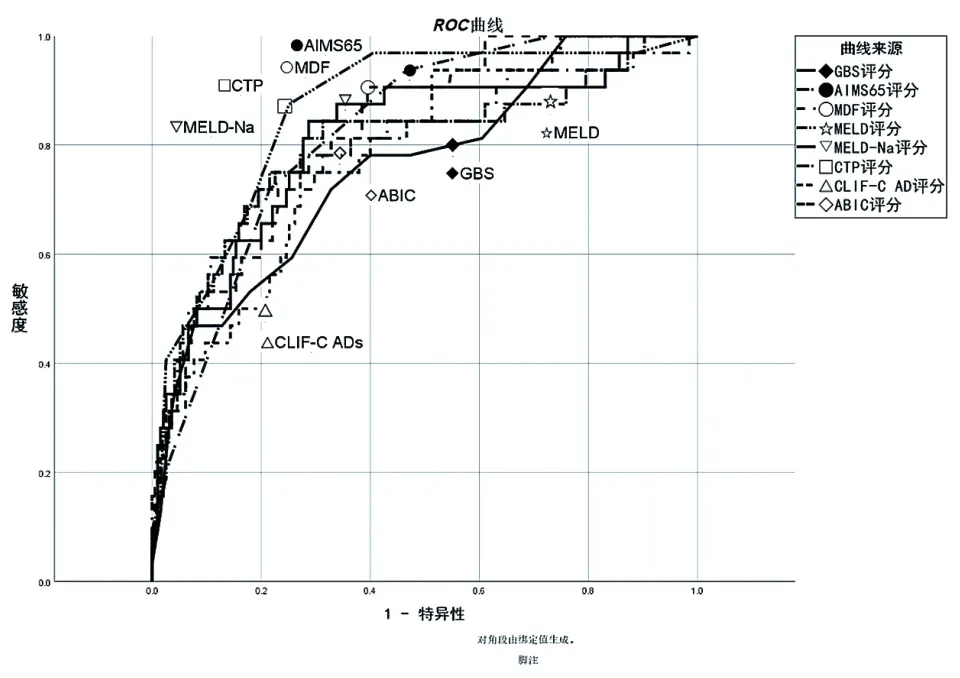
圖1 八種評分預測臨床死亡的ROC曲線(C組)
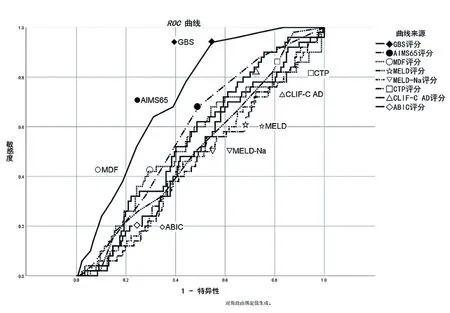
圖2 八種評分預測輸血的ROC曲線(B組)
2.5 八種評分系統的AUC值差異比較
C組中CTP的預測價值優于CLIF-C ADs、GBS(Z=2.045、2.073,P< 0.05),見圖 3。B 組 中GBS的預測價值優于ABIC、AIMS65、CLIF-C ADs、mDF、CTP、MELD(Z=4.297、3.016、3.716、3.026、3.810、3.830,P< 0.05),見圖 4。
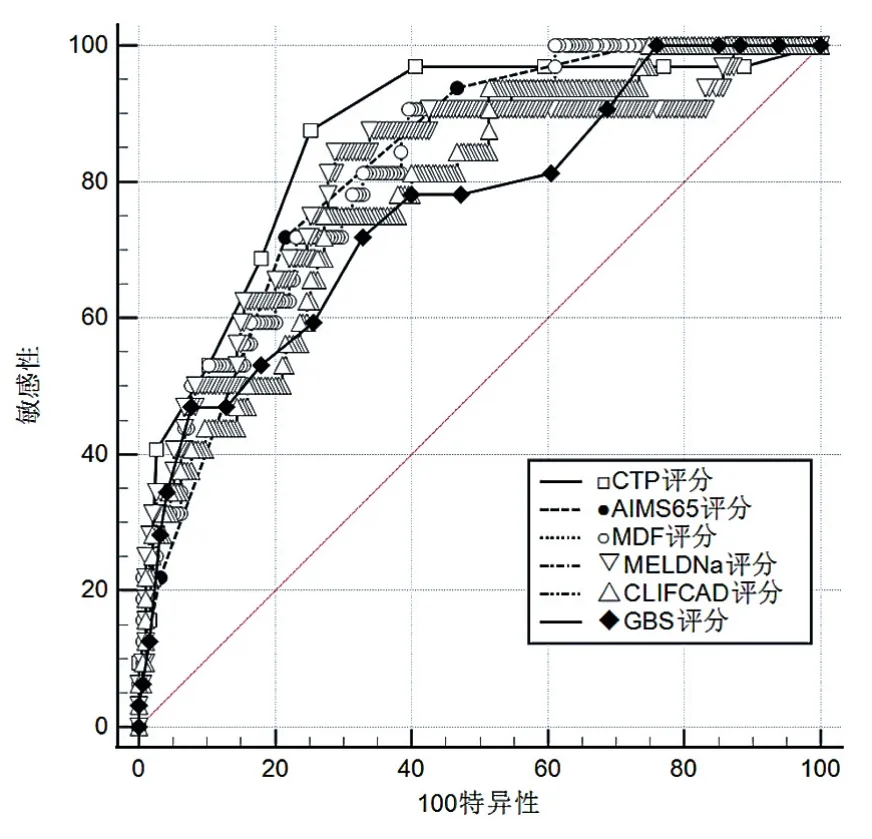
圖3 預測臨床死亡的AUC值比較(C組)
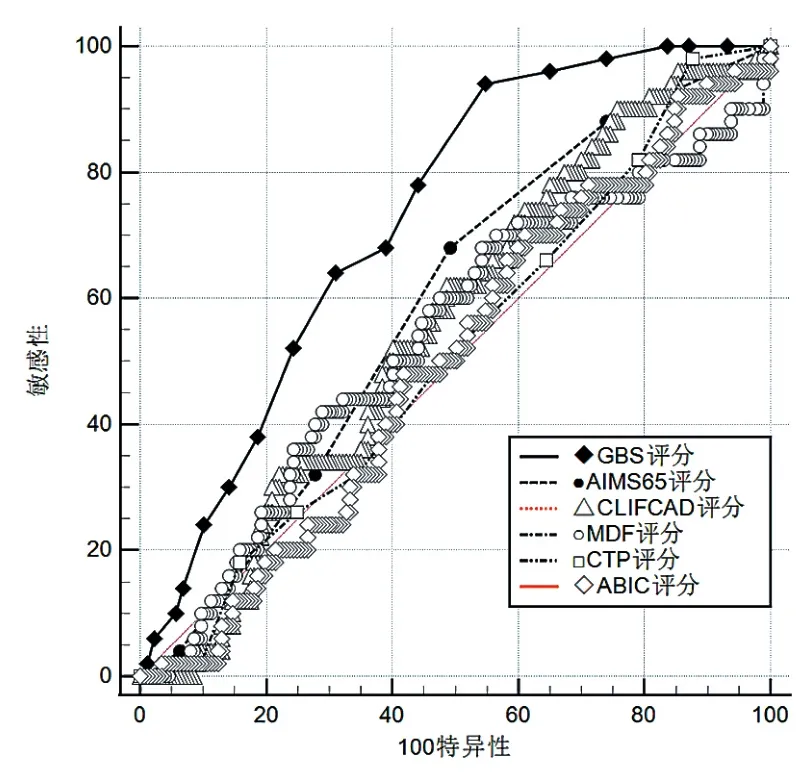
圖4 預測輸血的AUC值比較(B組)
3 討論
肝硬化進入失代償階段將演變為伴有多器官、多系統功能障礙的全身性疾病,患者往往發展為肝移植或死亡[11]。臨床醫師需要識別出患者的臨床特征并進行預后分析,有利于改善失代償期管理。
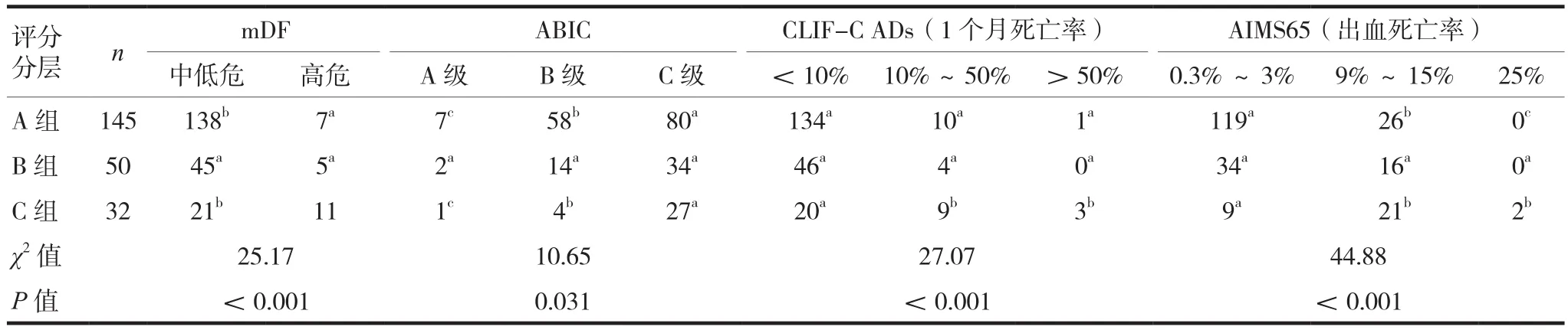
表4 三組mDF、ABIC、CLIF-C ADs、AIMS65風險分級比較
年齡是可預測生存的變量,本研究中年齡在三組間比較差異無統計學意義,考慮可能與本地區醫療干預不足及流行病學特征等有關。種族、性別和病因不是導致死亡的獨立危險因素。血清Na+是死亡的獨立預測因子[12],與本研究結果一致。
八種評分在肝硬化不同階段的預測存在偏差。因觀察指標不同或權重變化、個體生物學變異性和流行病學、檢測方法等因素影響,各地區對于評分系統認可度不一。本研究通過比較八種評分在三組間的預測差異,顯示在預測28 d死亡率時,CTP評分診斷價值最高(AUC=0.864);其余評分的AUC為0.824~0.758;對各評分AUC差異進行比較時顯示CTP的預測價值優于CLIF-C ADs、GBS(Z=2.045、2.073,P< 0.05),與凡小麗等[3]研究結果相符。有研究顯示[13]在預測3個月的死亡率時MELD評分優于CTP評分。可能的原因是在短期預測中反映循環系統惡化的指標所占權重更大。CTP包含2項循環狀態指標(腹水和肝性腦病)、MELD包含1項循環狀態指標(血肌酐)、MELD-Na包含2項循環狀態指標(血肌酐和Na),但考慮Na不足以替代腹水和肝性腦病對循環狀態的評估作用。在本研究中觀察到MELD-Na能識別出MELD評分低的患者中隱藏的高危人群。如果將CTP的肝性腦病替換為AIMS65中的精神狀態,則兩者在5項指標中重疊3項。如果將mDF的PT時間延長替換為CTP中的INR,則CTP是在mDF基礎上的拓展評分。在本研究中,CLIF-C ADs評分的預測表現中等,考慮其對沒有慢加急性肝衰竭背景的肝硬化急性失代償患者預測更準確[7]。ABIC和MELD之間有3項指標重疊。ABIC沒有包含病因,但納入年齡,在本研究中的預測效果介于MELDNa和MELD之間。
在本研究中八種評分對輸血事件預測價值均有限,與馬佳麗等[14]研究結果相符,其中GBS優于其他評分;AIMS65預測臨床死亡時優于GBS,預測輸血時劣于GBS,與Koichiro等[4]的研究結果相符。
各評分系統有不同優缺點,如MELD及MELDNa重復性好,已取代CTP用于分配肝臟供體的優先順序[15];但其結果需要復雜計算,實用性差,且低估合并腹水患者的死亡風險[16]。臨床醫師希望識別出患者的臨床特征,并進行充分的風險分級以制訂最佳治療策略,希望未來有新技術可以提供更好的支持。

