黃茅海浮游生物及其粒徑結構的潮汐變化特征研究*
劉子嘉 李 芊, 3 陳寅超 帥義萍 馬夢真
黃茅海浮游生物及其粒徑結構的潮汐變化特征研究*
劉子嘉1, 2李 芊1, 2, 3①陳寅超1, 2帥義萍1, 2馬夢真1, 2
(1. 熱帶海洋環(huán)境國家重點實驗室 中國科學院南海海洋研究所 廣州 510301; 2. 中國科學院大學 北京 100049; 3. 南方海洋科學與工程廣東省實驗室(廣州) 廣州 511458)
河口區(qū)浮游生物作為食物鏈的重要組成部分, 在海洋生物地球化學循環(huán)中起到重要作用。為了解黃茅海河口浮游生物及其粒徑結構的時空分布特征, 于2017年8月17日至21日對黃茅海河口區(qū)域微微型浮游生物(pico-, <2 μm), 微型浮游生物(nano-, 2—20 μm)及小型浮游生物(micro-, 20—200 μm)及其粒徑結構進行觀測。結果顯示, 河口外側總葉綠素濃度最高, 為19.34 μg/L, 且大粒徑浮游生物占比最高。底層水體受上溯海水影響較為明顯, 表現(xiàn)出鹽度及營養(yǎng)鹽濃度隨潮汐呈現(xiàn)顯著的周期性變化。潮汐過程對不同粒徑的浮游生物影響不同, 對微微型浮游生物影響較小, 對大粒徑浮游生物影響較大。漲潮時, 表層標準化浮游生物粒徑譜(NBSS)斜率增大, 大粒徑浮游生物占比增多。落潮時, NBSS斜率減小, 小粒徑浮游生物占比增多。潮汐過程及由其引起的營養(yǎng)鹽、溫度和可利用光強的改變是影響黃茅海河口浮游生物分布的主要因素。研究可為河口區(qū)浮游生態(tài)系統(tǒng)以及海洋生物地球化學循環(huán)過程等的研究提供重要依據(jù)。
浮游生物; 浮游生物粒徑; 潮汐; 黃茅海
浮游生物作為海洋食物鏈的基本組成部分, 在海洋生物泵和碳循環(huán)過程中起到重要作用(Chisholm, 2000)。浮游生物的生長、攝食以及營養(yǎng)鹽吸收等新陳代謝過程與其粒徑結構息息相關(Dong, 2018)。小粒徑的浮游植物由于比表面積較小而在資源貧乏的環(huán)境中更具優(yōu)勢, 而在資源豐富的環(huán)境中大粒徑的浮游植物由于有更高的光合作用效率而更為豐富(Chisholm, 1992; Mara?ón, 2007)。也有研究指出, 營養(yǎng)鹽與溫度會共同影響浮游生物的粒徑結構(Mara?ón, 2012), 溫度升高或會導致浮游生物粒徑減小(Yvon-Durocher, 2011)。除溫度、鹽度以及營養(yǎng)鹽等環(huán)境因子外, 海洋物理過程(如: 潮汐、鋒面等)也會影響浮游生物的粒徑結構分布(Rodríguez, 2001; Sin, 2015; 施玉珍等, 2017)。
河口作為陸地與海洋間的紐帶, 是研究海洋碳循環(huán)過程的關鍵場所(Li, 2018)。河口區(qū)浮游生物作為食物鏈的關鍵環(huán)節(jié), 在河口生態(tài)系統(tǒng)以及生物地球化學循環(huán)過程中起著重要作用, 對其進行研究有著重要的理論與實踐意義(郭沛涌等, 2003)。由于受到潮汐以及徑流等過程影響, 河口區(qū)域水動力環(huán)境復雜。其中, 潮汐是影響河口區(qū)浮游生物分布的重要因子之一(Sin, 2015)。黃茅海河口是位于珠江口西側的喇叭形河口灣, 上有虎跳門水道與崖門水道匯入, 下與南海相連, 為潮流優(yōu)勢型河口(高原等, 2010), 其環(huán)境主要受到河流徑流和潮流所影響(Jia, 2019)。目前, 針對黃茅海河口的研究大多集中于對其潮汐動力特征、泥沙輸運以及環(huán)境因子的變化等方面進行研究(楊名名等, 2016; 周爭橋, 2019; Cui, 2019), 而對浮游生物及其粒徑的分布和其隨潮汐的變化特征研究仍然較少。
標準化浮游生物粒徑譜(normalized biovolume size spectrum, NBSS)常被用來表征浮游生物粒徑結構, 其斜率可以用來描述浮游生物的粒徑分布情況(San Martin, 2006)。較小的斜率值表示浮游生物群落中小粒徑生物占比較高, 且生態(tài)系統(tǒng)的能量傳遞效率較低(Zhang, 2019; Liu, 2021)。在標準化粒徑譜斜率相近時, 粒徑譜截距可以用來表征浮游生物群落總生物量的大小(Quinones, 2003), 較高的截距值表示浮游生物群落總生物量相對較高。通過對不同環(huán)境下浮游生物及其粒徑結構的變化情況進行分析, 對其在黃茅海河口區(qū)域分布以及隨潮汐變化特征進行探究, 有助于進一步了解該區(qū)域的生物地球化學循環(huán)過程, 也可以為生態(tài)建模以及模擬等提供科學依據(jù)。
1 材料與方法
1.1 樣品采集與分析
調查于2017年8月在黃茅海水域進行, 共計包括3個采樣站位。S1、S2及S3站位水深分別為7.8、3.1及7.8 m。其中, S1、S3站位水樣采集于低低潮位時, S2號站位為時間序列站位(圖1), 具體采樣時間如表1所示。水體溫度及鹽度利用船載CTD進行測量, 通過CTD所攜帶的采水器對表層(距海表0.5 m)和底層(距海底0.5 m)水體樣品進行采集。所采集水樣預先經200 μm篩絹過濾, 用于測量營養(yǎng)鹽以及葉綠素等, 各樣品均取2個平行樣。
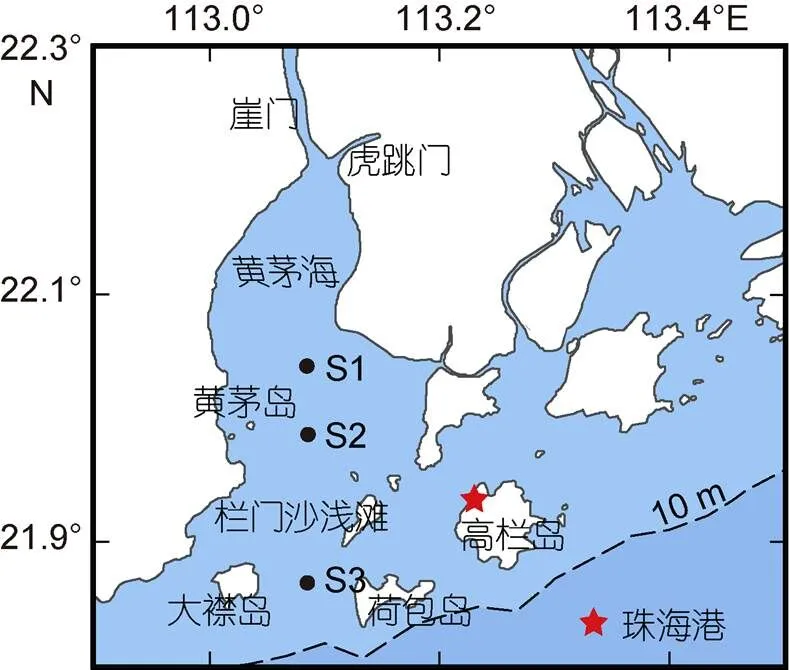
圖1 黃茅海采樣站位圖
表1 各站位采樣日期及采樣時間
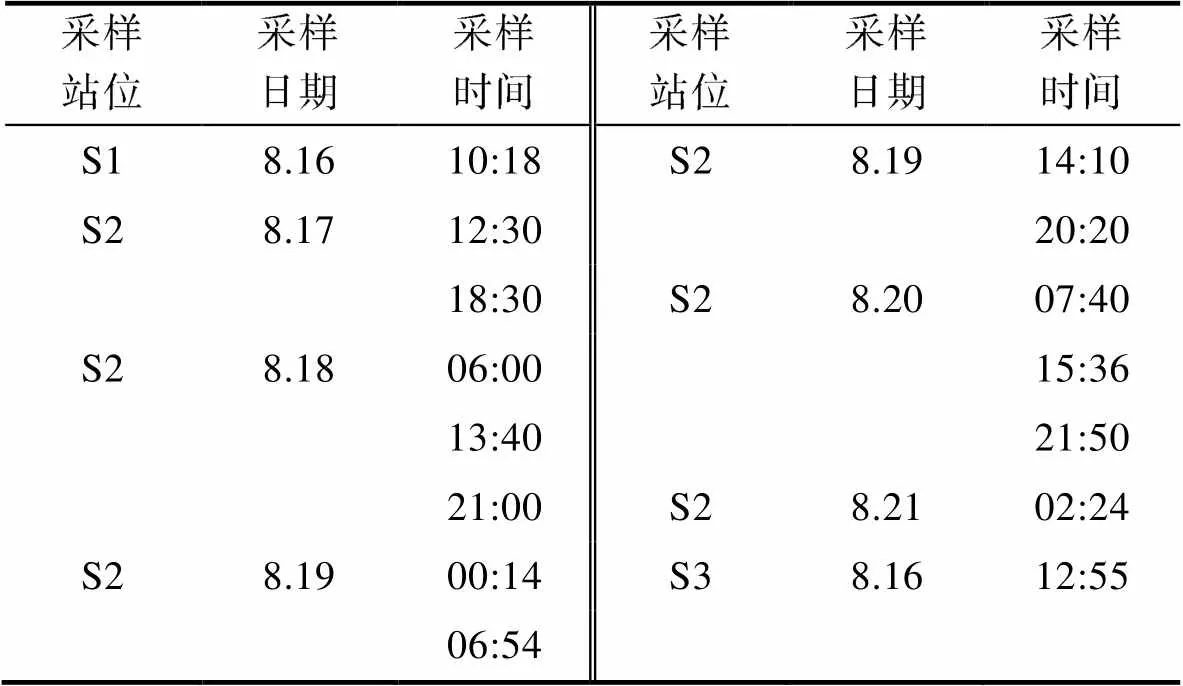
Tab.1 Date and time of sampling at each station
在50 kPa壓強下, 選取500 mL預過濾水樣在現(xiàn)場經0.7 μm玻璃纖維濾膜(GF/F)過濾。所得濾膜避光保存于-20 °C冰箱中, 用于總葉綠素濃度測量。同時, 保留100 mL經GF/F濾膜過濾后海水于聚乙烯瓶中冷凍保存于-20 °C, 用于營養(yǎng)鹽濃度測量。實驗室內, 在避光條件下將濾膜在90%的丙酮中萃取24 h, 4 000 r/min, 離心10 min后采用熒光法測定總葉綠素(Tchl) 濃度(Dong, 2018)。硅酸鹽(Si)濃度、硝酸鹽和亞硝酸鹽(N+N)及可溶活性磷酸鹽(SRP)利用SEAL AA3型流動注射分析儀在實驗室內測定, 其檢出限分別為0.02、0.02、0.03 μmol/L(Li, 2021)。
對于微微型浮游生物(pico-, <2 μm), 現(xiàn)場取50 mL預過濾水樣經20 μm篩絹再過濾后, 保存2 mL濾液于凍存管中, 用終濃度為0.5%的多聚甲醛固定, 避光放置15 min后, 保存于液氮中。原綠球藻(, Pro)、聚球藻(, Syn)和微微型真核生物(picoeukaryotes, Euk) 的豐度在實驗室內利用流式細胞儀(Beckman Coulter’s cytoflex S) 進行測量(周衛(wèi)文等, 2020)。
在此次調查中僅采集表層微型浮游生物(nano-, 5—20 μm) 及小型浮游生物(micro-, 20—200 μm) 樣品。其采集與測量過程參照San Martin等(2006)的方法, 將表層海水在現(xiàn)場經終濃度為1%的酸性魯哥試劑固定后, 在實驗室內由流式細胞攝像系統(tǒng)(FlowCAM)測量, 以獲取其粒徑數(shù)據(jù)。測量采用4倍物鏡, 在自動觸發(fā)模式下進行。每次測量結束后, 將無效圖像從數(shù)據(jù)庫中刪除(氣泡、重復圖像等)(García-Mu?oz, 2014)。
本文中所使用潮汐數(shù)據(jù)選取距離采樣站位最近的珠海站于調查期間內的潮汐預報數(shù)據(jù), 潮高基準面在平均海平面下148 cm (國家海洋信息中心, 2016)。
1.2 數(shù)據(jù)處理與標準化粒徑譜構建
以由等效球直徑(ESD, μm)計算得出的顆粒體積為尺度劃分粒徑級, 其值經由FlowCAM計算并導出, 并校正了由魯哥試劑固定而導致的細胞收縮(Montagnes, 1994)。
粒徑間隔的劃分和標準化粒徑譜的構建依據(jù)以下公式進行:
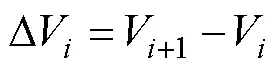

其中,V表示不同粒徑級(μm3),A表示對應粒徑級間隔(?V)內顆粒的總體積(μm3/mL)(Blanco, 1994)。斜率(a)和截距(b)為標準化粒徑譜線經線性回歸后得到的常數(shù)。
1.3 統(tǒng)計及分析方法
本文中采樣站位圖使用軟件Ocean Data View (ODV) v.4繪制, 其余用圖使用軟件Origin Pro 2018繪制。利用軟件SPSS v.22.0 (SPSS) 進行相關數(shù)據(jù)統(tǒng)計分析。由于S1、S3站位樣品采集于低低潮位時, 所以本文選取S2站位低低潮位時各變量均值與其余站位進行對比分析。
2 結果
2.1 調查水域環(huán)境特征
由潮汐曲線(圖3)可知, 2017年8月17日至21日期間黃茅海水域的潮汐變化較為規(guī)律。在一個太陰日中呈現(xiàn)兩次高潮和兩次低潮, 且相鄰兩次高潮位潮高相差較大, 屬于不正規(guī)半日潮混合潮特征。在觀測期間內其潮高最大值為288 cm, 出現(xiàn)在21日8時13分。潮高最小值為20 cm, 出現(xiàn)在21日16時23分。
調查期間, 由S1至S3站位, 黃茅海水域表層溫度略有上升(由30.80 °C上升至31.11 °C), 底層溫度在S3站位最低, 為24.42 °C (圖2a)。表層鹽度由河口至外海逐漸升高(0.98—10.96), 底層鹽度在S3站位最高, 為33.63 ‰ (圖2b)。其中, S2站位水體表層溫度與底層溫度無顯著性差異(=1.39,=26,>0.05) 。表層溫度平均值為30.91 °C, 無顯著周期性變化規(guī)律, 隨時間呈現(xiàn)升溫趨勢(圖3a)。底層溫度平均值為30.45 °C, 在高高潮位時溫度降低, 在其余潮位時溫度較高, 隨時間呈現(xiàn)升溫趨勢(圖3a)。S2站位水體表層鹽度顯著低于底層鹽度 (=-3.73,=26,<0.01) 。S2站位表層鹽度平均值為5.82, 在低低潮位及高低潮位鹽度值較低, 且與潮高呈顯著正相關關系 (=0.76,=13,<0.01, 表2), 表明潮高較高時表層鹽度較高。底層鹽度平均值為13.55, 有明顯的周期性變化規(guī)律, 與潮高有顯著的正相關關系(=0.77,=13,<0.01, 表2) 。在一個太陰日內, 底層鹽度在低低潮位時有極小值, 隨后逐漸增大, 在高低潮位時無顯著減小(圖3b)。
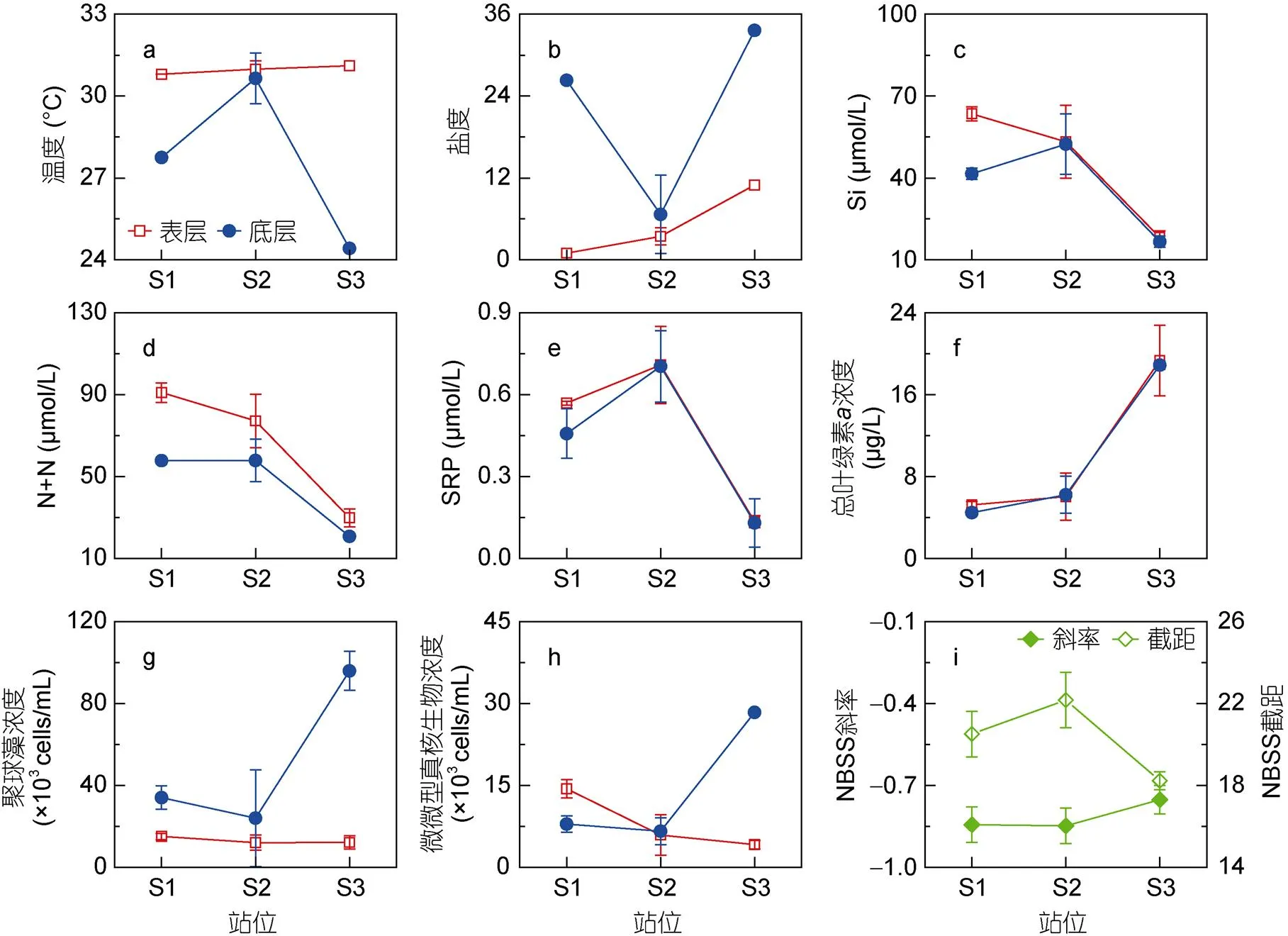
圖2 溫度 (a)、鹽度 (b)、硅酸鹽 (Si, c)、硝酸鹽和亞硝酸鹽 (N+N, d)、可溶活性磷酸鹽 (SRP, e)、總葉綠素a (Tchl a, f)、聚球藻 (Syn, g)、微微型真核生物 (Euk, h) 濃度、標準化粒徑譜 (NBSS) 斜率以及截距 (i) 的水平分布曲線
注: S2站的數(shù)據(jù)為最低潮位時各變量的平均值
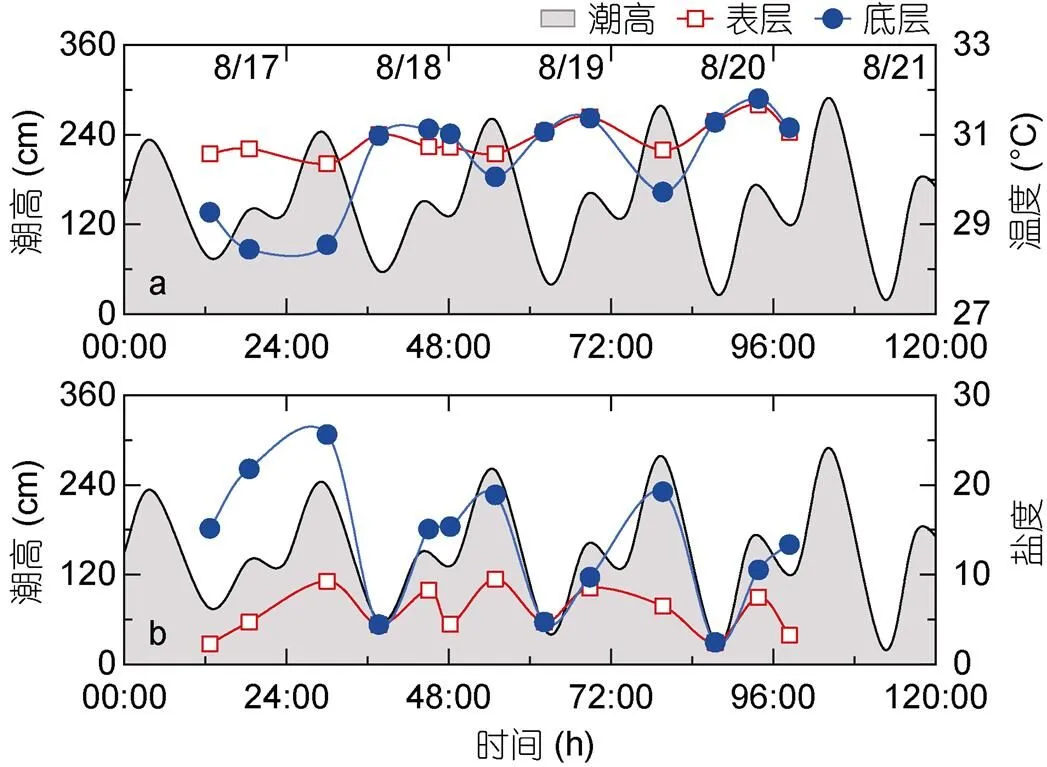
圖3 溫度(a)、鹽度(b)及潮高隨時間變化曲線
注: 采樣日期(月/日)標注在圖片頂部
調查期間, 硅酸鹽(Si)濃度范圍為18.22— 68.63 μmol/L, 硝酸鹽及亞硝酸鹽(N+N)濃度范圍為20.74—94.61 μmol/L, 可溶活性磷酸鹽(SRP)濃度范圍為0.12—0.90 μmol/L, 這與前人的研究結果一致(黃向青等, 2012; 張偉等, 2015)。由S1至S3站位, Si、N+N以及SRP在表層和底層均呈現(xiàn)下降趨勢, 在S3站位時濃度最低(圖2c—e)。如圖4所示, S2站位表層Si濃度平均值為51.49 μmol/L, 與底層濃度(43.38 μmol/L)無顯著性差異(=1.91,=26,>0.05)。其中, 底層Si與潮高呈顯著負相關(=-0.70,=13,<0.01, 表2), 在潮高較高時其濃度較低(圖4a)。表層N+N濃度平均值為70.12 μmol/L, 顯著高于底層N+N濃度 (51.15 μmol/L,=3.64,=26,<0.01), 底層N+N濃度與潮高呈顯著負相關 (=-0.62,=13,<0.01, 表2), 在潮高較高時, N+N濃度較低 (圖4b)。此外, 表層SRP濃度平均值為0.59 μmol/L, 與底層濃度(0.43 μmol/L)無顯著性差異(=1.71,=26,>0.05), 底層SRP隨潮高增加而顯著線性減小(=-0.62,=13,<0.01, 表2), 在低低潮位時有極大值, 而在其余潮位時濃度減小(圖4c)。
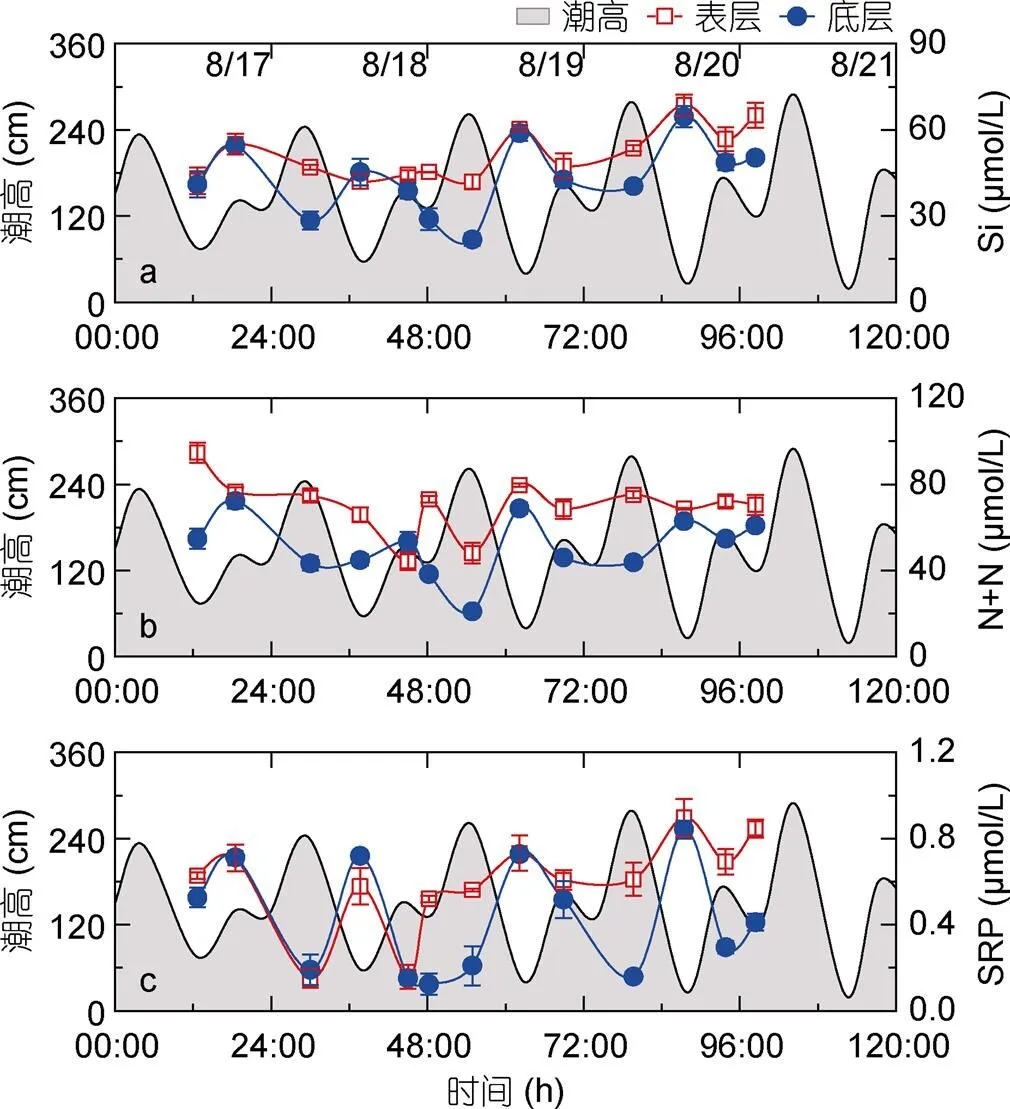
圖4 硅酸鹽 (Si)、硝酸鹽和亞硝酸鹽 (N+N)、可溶活性磷酸鹽 (SRP) 濃度及潮高隨時間變化曲線
2.2 葉綠素及微微型浮游生物群落結構的時空分布
由S1至S3站位, 表層與底層總葉綠素均逐漸增大(圖2f), 在S3站位時濃度最高, 分別為19.34 μmol/L (表層)和18.88 μmol/L(底層)。其中, S2站位表層總葉綠素濃度在觀測期內變化范圍為2.16—8.31 μg/L, 平均濃度為4.87 μg/L, 隨時間呈現(xiàn)較為明顯的下降趨勢, 無顯著的周期性變化規(guī)律(圖5a)。底層總葉綠素濃度顯著高于表層總葉綠素濃度(=-2.73,=26,>0.05), 其變化范圍為4.02—8.04 μg/L,平均濃度為4.87 μg/L, 與潮高呈顯著的正相關關系(=0.57,=13,<0.05, 表2), 即潮高較高時, 底層葉綠素濃度較高(圖5a)。
原綠球藻(Pro)在此次調查所采集的各個樣品中均未被檢出。表層聚球藻(Syn)濃度在S1站位最高, 為15.09×103cells/mL, 底層Syn濃度在S3站位最高, 為95.94×103cells/mL(圖2g)。在S2站位(圖5b), 聚球藻(Syn)濃度表層顯著低于底層(=-2.73,=26,<0.05), 表層Syn濃度除極大值173.2×103cells/mL(8月18日, 06:00)外, 在低低潮位時濃度較低, 其余時間濃度小幅上升,平均濃度為28.62×103cells/mL。底層Syn濃度變化較為劇烈, 呈周期性變化, 平均濃度為99.11×103cells/mL, 在低低潮位時濃度較低, 在其他時間則濃度上升。表層微微型真核生物(Euk)由S1 (14.42×103cells/mL) 至S3 (4.2×103cells/mL) 站位逐漸降低, 底層Euk在S3站位濃度最高, 為28.41×103cells/mL(圖2h)。在S2站位(圖5c), 表層Euk平均濃度為5.97×103cells/mL, 與底層濃度無顯著差異(=-1.43,=26,>0.05)。
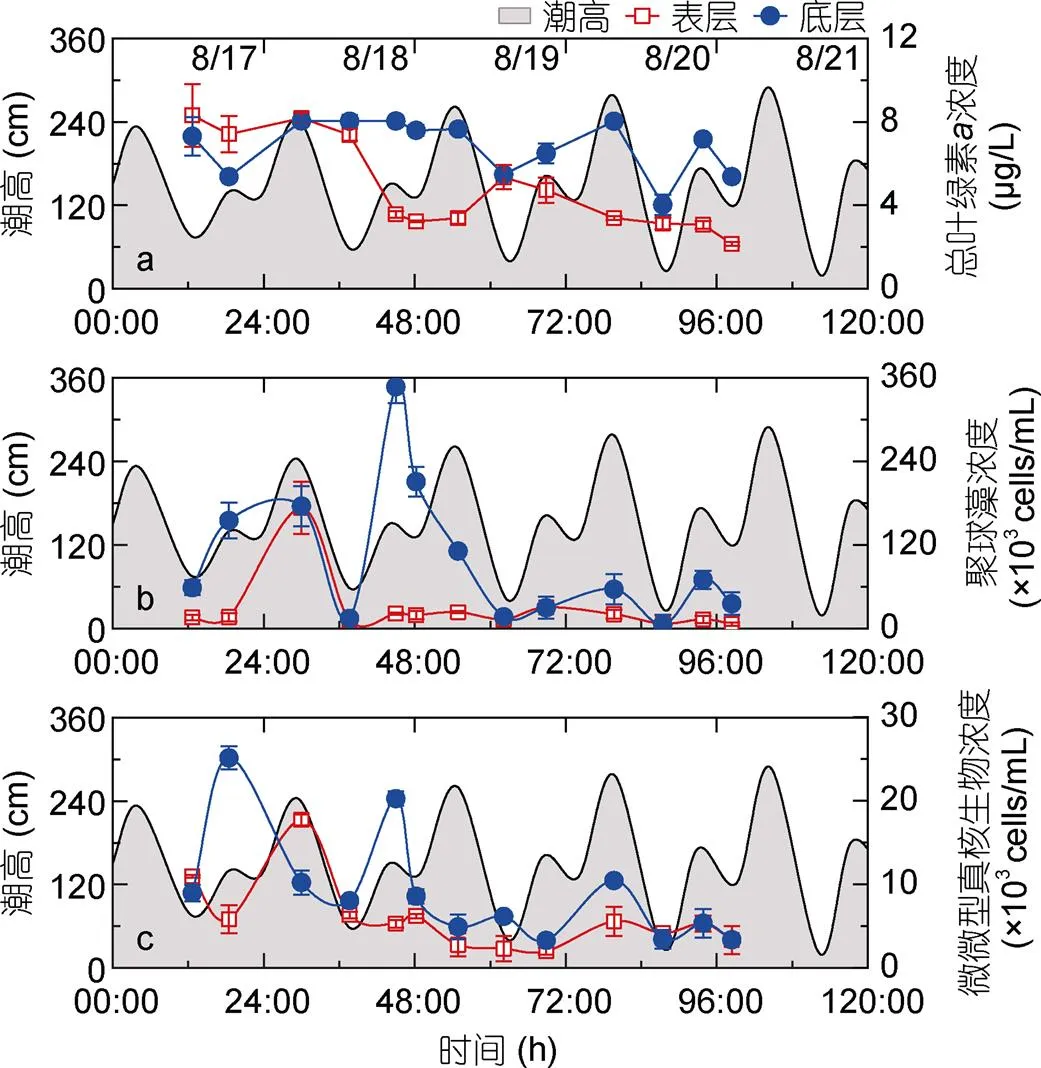
圖5 總葉綠素(Tchl a)、聚球藻(Syn)、微微型真核生物(Euk)濃度及潮高隨時間變化曲線
2.3 標準化粒徑譜參數(shù)的時空分布
由S1至S3站位, S1與S2站位標準化粒徑譜斜率無明顯差異, S3站位斜率值最高(-0.75, 圖2i), 表明S3站位大粒徑生物相對占比最高。標準化粒徑譜截距在S2站位最大(22.18, 圖2i), 在S3站位截距值最小(18.24, 圖2i), 表明相比較于其他站位, S2站位浮游生物總生物量相對較高。
此外, 根據(jù)標準化粒徑譜參數(shù)分布折線圖可知(圖6), S2站位粒徑譜斜率及截距隨著時間的推移呈現(xiàn)周期性變化。一個太陰日內, 低低潮位時粒徑譜斜率較小, 而后隨著潮位的增高而逐漸增大, 且與潮高呈顯著的正相關關系(圖6a,=0.62,=13,<0.05), 表明在低低潮位時浮游生物群落中小粒徑生物占比較高, 潮高較高時, 大粒徑生物占比逐漸增大。此外, 標準化粒徑譜截距也隨時間呈現(xiàn)周期性變化(圖6b)。在低低潮位時粒徑譜截距有極大值, 而隨著潮高的降低減小, 且與潮高呈顯著負相關關系(=-0.69,=13,<0.01)。這表明在低低潮位時, 浮游生物總生物量較高, 而隨著潮位的增加浮游生物總生物量逐漸降低。
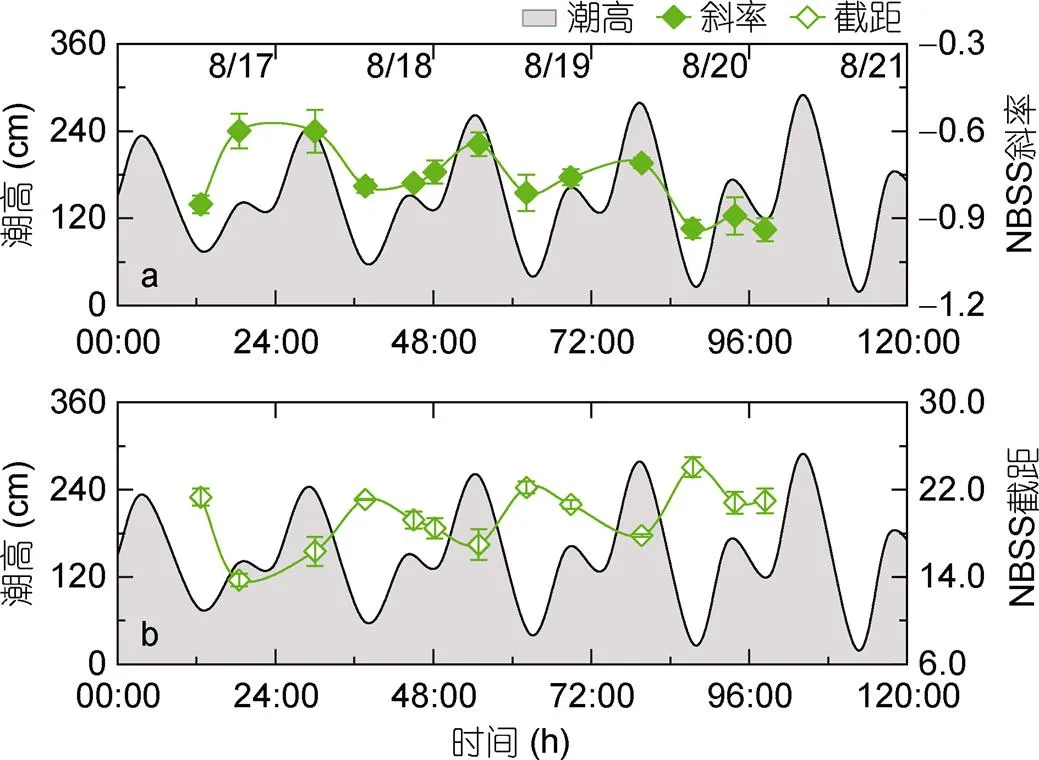
圖6 標準化粒徑譜(NBSS) 斜率、截距及潮高隨時間變化曲線
2.4 浮游生物與環(huán)境因子的關系
由表2可知, S2站位表層水體總葉綠素與溫度、鹽度及營養(yǎng)鹽等無顯著相關性。底層總葉綠素濃度與表層Si (=-0.81,=13,<0.01)、N+N (=-0.70,=13,<0.01)以及SRP (=-0.69,=13,<0.72)呈現(xiàn)顯著的負相關關系, 表明營養(yǎng)鹽濃度越高, 總葉綠素濃度越低。表層Syn與SRP有顯著的負相關關系(=-0.66,=13,<0.05), 表明隨SRP濃度升高, Syn濃度降低。底層Syn也與底層SRP有顯著負相關關系(=-0.62,=13,<0.05)。表層Euk與溫度有顯著的負相關關系(=-0.58,=13,<0.05), 表明溫度越高則其濃度越小。其與表層SRP也有顯著負相關關系(=-0.58,=13,<0.05), 表明表層SRP的增加并未促進表層Euk的生長。底層Euk與溫度、鹽度及營養(yǎng)鹽等無顯著相關性。
標準化粒徑譜斜率與表層溫度有顯著的負相關關系(=-0.67,=13,<0.05), 表明隨著溫度的增加, 粒徑譜斜率降低, 小粒徑生物占比增加。其也與表層鹽度呈顯著的正相關關系(=0.57,=13,<0.05), 表明隨著鹽度的增加, 粒徑譜斜率逐漸增大, 大粒徑生物占比逐漸增大。此外, 表層斜率還和表層SRP濃度呈現(xiàn)顯著的負相關關系(=-0.56,=13,<0.05), 表明隨著SRP的增加, 粒徑譜斜率逐漸減小, 小粒徑生物占比增加。標準化粒徑譜截距與表層溫度呈顯著的正相關關系(=0.63,=13,<0.05), 表明隨著溫度的增大, 浮游生物總生物量增高。
表2 S2站位各變量的Pearson相關分析結果
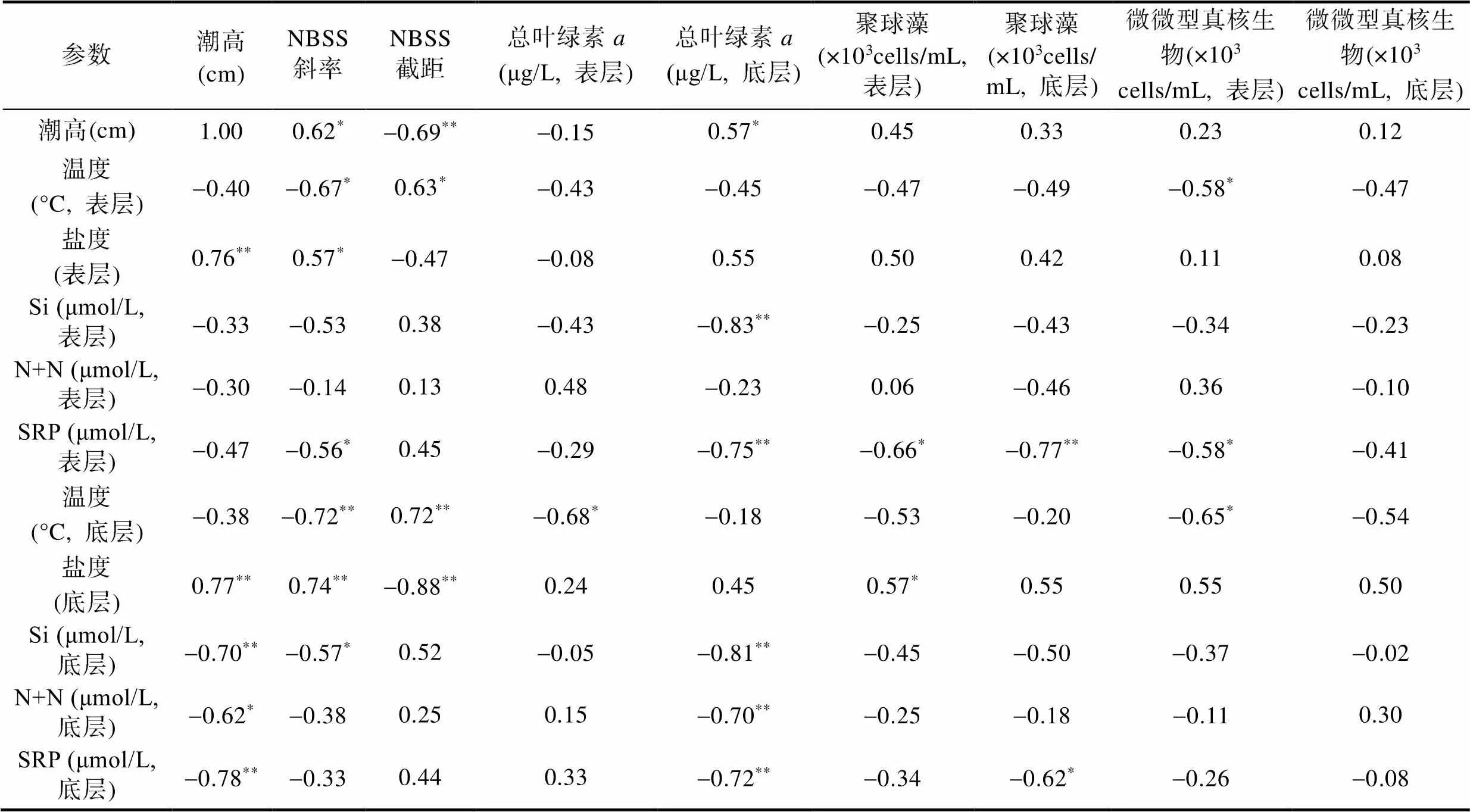
Tab.2 Results of Pearson correlation analysis between different variables at Station S2
注: *表示相關系數(shù)在0.05水平上顯著, **表示相關系數(shù)在0.01水平上顯著。
3 討論
3.1 黃茅海潮汐特征及其對環(huán)境因子的影響
黃茅海河口位于珠江口西側, 頂端有來自崖門和虎跳門的水體匯入其中(黃毅等, 2020)。調查期間, 黃茅海潮高隨時間呈周期性漲落, 在一個太陰日內, 經歷兩次高潮和兩次低潮, 且相鄰兩次高潮潮差較大(圖3a), 屬于不正規(guī)半日潮混合潮(楊名名等, 2016; 黃毅等, 2020)。
有研究指出, 黃茅海夏季的海水呈現(xiàn)高度成層或者似層狀, 鹽水楔隨潮水漲落進退于欄門淺灘與赤鼻島之間(黃方等, 1994)。本文中, S1與S2站位處于黃茅海夏季鹽水楔漲落范圍內(圖1)。調查期間, 黃茅海水域的表層溫度和鹽度與底層差異較大, 呈現(xiàn)出較為明顯的分層特征(圖2a, 2b)。由河口內側至外側, 溫度略有降低, 而鹽度逐漸增大。這與Jia等(2019)在2011年夏季對黃茅海的調查結果是一致的, 主要是受到河口徑流輸入的影響。黃毅等(2020)的研究中曾指出, 欄門沙淺灘海域屬于潮流上溯流與徑流下泄流的交匯區(qū)域, 水動力條件相對較弱, 其以北海域受到徑流作用的影響要強于潮汐作用。S2站位鄰近于黃茅島, 屬于攔門沙淺灘以北海域。在調查期間, S2站位表層鹽度與底層鹽度則隨潮水漲落有顯著的周期性變化。在低低潮位時, 表底層鹽度基本相同。相比較于表層鹽度, 底層鹽度隨潮水上漲的增幅更為劇烈(圖3b), 這表明S2站位底層受到外海高鹽度海水上溯的影響更為強烈。
黃茅海水域營養(yǎng)鹽的空間分布較為規(guī)律, 即其濃度由河口至外海呈現(xiàn)下降趨勢(圖2), 這也與夏季長江口營養(yǎng)鹽的分布趨勢是一致的(方濤等, 2008)。黃茅海海域的營養(yǎng)鹽主要來自于陸源口門的排放, 外海水稀釋作用的加強是導致營養(yǎng)鹽濃度逐漸降低的原因(張偉等, 2015)。同時, 由河口至外海, 徑流作用的影響逐漸降低也會導致營養(yǎng)鹽濃度逐漸降低(Jia, 2019)。在S2站位, 表層的營養(yǎng)鹽濃度普遍高于底層營養(yǎng)鹽濃度(圖4)。這是由于在雨季河口徑流輸入的水體與隨潮汐漲落的鹽楔間會形成強烈的溫度及鹽度躍層, 其存在會阻礙河流徑流輸入水體與上溯鹽楔間物質的垂直交換(Cui, 2019)。盡管S2站位表層營養(yǎng)鹽濃度隨時間有波動, 但與潮高無顯著相關性。表明表層營養(yǎng)鹽濃度變化可能受到潮汐作用較弱。而根據(jù)潮高與底層營養(yǎng)鹽的線性相關結果可知, 在漲潮時底層營養(yǎng)鹽濃度顯著降低(圖4)。漲潮時, 來自外海的低營養(yǎng)鹽海水隨潮汐上溯使得底層營養(yǎng)鹽濃度降低, 即海水上溯是影響底層營養(yǎng)鹽濃度的主要原因(方濤等, 2008)。
3.2 黃茅海浮游生物的空間分布
調查結果顯示, 黃茅海河口葉綠素表層與底層無明顯差異, 且濃度整體較高(>2.16 μg/L)。其在S3站位最高, 達到19.34 μg/L (圖2), 這可能由于受到外海赤潮的影響所致。如孫越峰等(2020)的研究所示, 遼河口夏季葉綠素在近河口處濃度較低, 在河口外側濃度較高是由于受到河口外側赤潮的影響。此外, 在高營養(yǎng)鹽條件下, 較為渾濁的水體和較低的光照條件也會限制浮游植物的生長(Cloern, 1999)。黃茅海河口內側盡管營養(yǎng)鹽濃度較高, 其總葉綠素濃度卻較低。這可能是由于黃茅海河口夏季受到徑流較強的影響, 其上游懸浮顆粒較多, 較高的濁度影響了光照而限制了浮游植物的生長所導致(Jia, 2019)。當總葉綠素濃度較高時, 微微型浮游植物的占比較小, 而小型浮游植物的比例會隨著總葉綠素濃度的增高而增大(Sin, 2000; Goericke, 2011)。小型浮游植物在河口外側占比的增加可能是導致在S3站位標準化粒徑譜斜率最高的原因。這也與前人的調查結果相一致, 即夏季在珠江口, 小型浮游植物在河口下游占據(jù)優(yōu)勢, 而在河口上游則為微微型浮游植物占比較高(黃邦欽等, 2005)。
鹽度是影響微微型浮游生物分布的重要因素(Mitbavkar, 2012)。有研究表明, 水體鹽度大于32.6的環(huán)境更利于原綠球藻(Pro)的生長, 且Pro在低營養(yǎng)鹽水體中更為豐富, 夏季長江口Pro由于受到高營養(yǎng)鹽環(huán)境的限制而未被觀測到(Li, 2012)。黃茅海河口各站位均未觀測到Pro的原因可能是由于較低的鹽度以及較高的營養(yǎng)鹽條件下, Pro的生長受到限制所導致。此外, 光照也是影響河口羽流區(qū)微微型浮游生物分布格局的重要條件(Jiao, 2002)。根據(jù)結果顯示, 黃茅海各站位聚球藻(Syn)的垂向豐度差異較大, 在底層豐度較高(圖2g)。這可能是由于夏季水體表層較強的光照抑制了Syn的生長, 而導致表層豐度較低(楊琳等, 2012)。對于微微型真核生物, 其群落組成復雜, 空間分布格局無法簡單歸因于物理或化學因素帶來的影響(Jiao, 2002)。而結果中, 微微型真核生物(Euk)并未觀測到明顯的垂向分布差異(圖2h), 這可能是由于所調查站位水深較淺所導致(楊琳等, 2012)。
3.3 潮汐對浮游生物及其粒徑結構的影響
浮游生物的生長和粒徑結構會受到營養(yǎng)鹽、溫度以及光照等因素的影響(Cloern, 1999; Dong, 2018)。調查期間, 底層葉綠素濃度與潮高呈顯著的正相關關系。在漲潮時, 底層葉綠素濃度的上升可能是由于潮汐漲落的物理過程及所帶來的化學變化共同所導致。S2站位營養(yǎng)鹽濃度整體較高, 氮磷比顯著高于Redfield比值(16:1)。S2站位底層總葉綠素濃度與營養(yǎng)鹽呈顯著的負相關關系, 高濃度的營養(yǎng)鹽并未促進浮游植物的生長。孫越峰等(2020)在對遼河口海域的調查研究中也發(fā)現(xiàn), 葉綠素濃度在夏季時與硝酸鹽、磷酸鹽、硅酸鹽濃度呈顯著負相關。在河口區(qū)域的高營養(yǎng)鹽環(huán)境下, 可利用光強是影響浮游植物生長的重要因素(Pennock, 1985; 孫越峰等, 2020)。潮流作用引起的沉積物和底棲生物等的再懸浮, 以及由河口徑流輸入的懸浮顆粒物會導致水體濁度增大(Cloern, 1987, 1996), 可利用光強的降低可能是導致S2站位底層浮游植物的生長受到限制的原因。此外, 在潮汐作用下上溯的高葉綠素濃度的外海水的直接輸入也可能是造成S2站位底層葉綠素濃度在漲潮時增大的原因之一。同時, 在河口區(qū)底棲微藻受到潮汐作用再懸浮進入底層水體(De Jorge, 1995), 也會造成浮游植物生物量變化。
有研究顯示, 潮汐對浮游生物的影響與粒徑相關(Sin, 2015)。從微微型浮游生物(Pico-, <2 μm) 至小型浮游生物 (Micro-, >20 μm), 其與潮高的關系隨粒徑增大而增強。在本文中, S2站位除Syn與SRP有顯著負相關性以及Euk在表層與溫度和SRP呈顯著負相關外, Syn和Euk豐度在表層與底層與其與環(huán)境因子間并無顯著相關性。這表明潮汐過程對Pico-生物的影響較小(Sin, 2015)。根據(jù)結果顯示, S2站位標準化粒徑譜斜率與潮高以及海水鹽度呈現(xiàn)顯著的正相關關系(表2)。黃茅海河口外側鹽度以及總葉綠素濃度較高, 且大粒徑生物占比最高(圖2)。在漲潮過程中, 河口外側高鹽度海水上溯, 大粒徑生物隨上溯海水的輸入可能是影響S2站位表層浮游生物的粒徑結構的原因之一。同時, 溫度也是影響浮游生物粒徑結構的重要因素(Morán, 2010)。溫度較高時, 微微型浮游植物生長率以及微型浮游動物對浮游植物的攝食率較高(Dong, 2018)。由S2站位標準化粒徑譜斜率與溫度的顯著負相關關系可知(表2), 小粒徑生物所占比例隨水體溫度的增高而增大, 表明溫度可能也是影響該位置浮游生物粒徑結構的原因之一。此外, 有研究表明, 在光限制或者營養(yǎng)鹽限制的條件下, 浮游生物群落通常以小粒徑生物為主(Chisholm, 1992), 而在光照和營養(yǎng)鹽充足的條件下, 大粒徑浮游植物擁有更高的光合作用效率(Cerme?o, 2005)。如: 硅藻不容易受到光抑制的作用, 能夠更好地適應近岸海域光照強度的快速變化(Key, 2010)。夏季黃茅海河口表層光照充足, 且營養(yǎng)鹽豐富。漲潮時, 高鹽度海水上溯流與河口徑流下泄流交匯而形成鹽楔, 導致S2站位水體分層較為明顯, 水體底部懸浮物質向表層的輸送受到阻礙(黃方等, 1994; Cui, 2019)。S2站位表層高營養(yǎng)鹽和光限制的環(huán)境下, 大粒徑浮游生物生長占優(yōu)勢也可能是導致該站位大粒徑浮游生物在漲潮時占比增多的原因。而落潮時, 鹽楔向河口外側退去, S2站位表層與底層的層化現(xiàn)象減弱, 底部懸浮顆粒物的輸入會導致水體濁度增加(De Jorge, 1995; Cloern, 1996)。且較小粒徑的物質由于密度較低, 更容易被懸浮(Wang, 2013)。因此, 低低潮位時可利用光的減弱以及水體底部小粒徑底棲微藻等的輸入可能是造成S2站位在落潮時小粒徑生物占比增高的原因。
4 結論
夏季, 黃茅海河口區(qū)為不正規(guī)半日潮混合潮, 浮游生物及其粒徑結構的分布受到潮汐影響顯著。河口內側受徑流影響較強, 營養(yǎng)鹽濃度較高。由河口至外海, 總葉綠素濃度逐漸增大, 且大粒徑生物占比在河口外側最大。潮汐過程對底層水體影響較為明顯, 并造成鹽度及營養(yǎng)鹽的改變。其引起的底層再懸浮過程, 以及由海水上溯所引起的底層營養(yǎng)鹽濃度和光照強度的變化影響了浮游生物的粒徑結構和分布情況。潮汐對不同粒徑的浮游生物影響不同, 對微微型浮游生物影響較小, 對較大粒徑浮游生物的影響較為明顯, 漲潮時表層標準化粒徑譜斜率增大, 較大粒徑浮游生物占比增加。
致謝 感謝中山大學海洋科學學院吳加學老師及其課題組成員為本研究中的樣品采集工作提供的大力支持和幫助。
方 濤, 李道季, 孔定江等, 2008. 夏秋季長江口及毗鄰海域N、P營養(yǎng)鹽分布及其潮汐變化. 海洋環(huán)境科學, 27(5): 437—442
孫越峰, 秦艷杰, 李洪波等, 2020. 遼河口海域葉綠素的時空分布特征及其影響因素. 環(huán)境保護科學, 46(2): 44—48
張 偉, 孫 健, 聶紅濤等, 2015. 珠江口及毗鄰海域營養(yǎng)鹽對浮游植物生長的影響. 生態(tài)學報, 35(12): 4034—4044
楊 琳, 汪 岷, 劉冠群等, 2012. 膠州灣微微型浮游植物豐度及其與環(huán)境因子的相關性分析. 海洋與湖沼, 43(5): 967—975
楊名名, 吳加學, 張乾江等, 2016. 珠江黃茅海河口洪季側向余環(huán)流與泥沙輸移. 海洋學報, 38(1): 31—45
周衛(wèi)文, 李 芊, 葛在名等, 2020. 珠江口羽流鋒浮游植物群落對大氣沉降的生態(tài)響應. 熱帶海洋學報, 39(4): 50—60
周爭橋, 2019. 基于實測資料的珠江口海域風和潮汐特征分析. 海洋湖沼通報, (1): 47—53
國家海洋信息中心, 2016. 潮汐表(2017第3冊臺灣海峽至北部灣). 北京: 海洋出版社, 251
施玉珍, 張才學, 張際標等, 2017. 水東灣海域浮游植物潮汐分布特征及其與環(huán)境因子的關系. 生態(tài)學報, 37(18): 5981—5992
郭沛涌, 沈煥庭, 劉阿成等, 2003. 長江河口浮游動物的種類組成、群落結構及多樣性. 生態(tài)學報, 23(5): 892—900
高 原, 賴子尼, 龐世勛等, 2010. 黃茅海河口虎跳門和崖門浮游動物群落的比較. 生態(tài)科學, 29(2): 121—126
黃 方, 葉春池, 溫學良等, 1994. 黃茅海鹽度特征及其鹽水楔活動范圍. 海洋通報, 13(2): 33—39
黃 毅, 吳 潔, 殷征欣等, 2020. 珠江口黃茅海底質沉積中介形類的生態(tài)類型及其分布特征. 海洋開發(fā)與管理, 37(6): 89—94
黃向青, 林進清, 張順枝等, 2012. 珠江口海水化學要素分布和水質特征. 海洋湖沼通報, (3): 162—174
黃邦欽, 洪華生, 柯 林等, 2005. 珠江口分粒級葉綠素和初級生產力研究. 海洋學報, 27(6): 180—186
Blanco J M, Echevarría F, García C M, 1994. Dealing with size-spectra: some conceptual and mathematical problems. Scientia Marina, 58(1—2): 17—29
Cerme?o P, Estévez-Blanco P, Mara?ón E, 2005. Maximum photosynthetic efficiency of size-fractionated phytoplankton assessed by14C uptake and fast repetition rate fluorometry. Limnology and Oceanography, 50(5): 1438—1446
Chisholm S W, 1992. Phytoplankton size. In: Falkowski P G, Woodhead A D, Vivirito K eds. Primary Productivity and Biogeochemical Cycles in the Sea. Environmental Science Research. Boston: Springer, 213—237
Chisholm S W, 2000. Stirring times in the Southern Ocean. Nature, 407(6805): 685—686
Cloern J E, 1987. Turbidity as a control on phytoplankton biomass and productivity in estuaries. Continental Shelf Research, 7(11—12): 1367—1381
Cloern J E, 1996. Phytoplankton bloom dynamics in coastal ecosystems: a review with some general lessons from sustained investigation of San Francisco Bay, California. Reviews of Geophysics, 34(2): 127—168
Cloern J E, 1999. The relative importance of light and nutrient limitation of phytoplankton growth: a simple index of coastal ecosystem sensitivity to nutrient enrichment. Aquatic Ecology, 33(1): 3—15
Cui Y S, Wu J X, Ren J, 2019. Physical dynamics structures and oxygen budget of summer hypoxia in the Pearl River Estuary. Limnology and Oceanography, 64(1): 131—148
De Jorge V N, Van Beusekom J E E, 1995. Wind-and tide-induced resuspension of sediment and microphytobenthos from tidal flats in the Ems estuary. Limnology and Oceanography, 40(4): 776—778
Dong Y, Li Q P, Liu Z J, 2018. Size-dependent phytoplankton growth and grazing in the northern South China Sea. Marine Ecology Progress Series, 599: 35—47
García-Mu?oz C, García C M, Lubián L M, 2014. Metabolic state along a summer north-south transect near the Antarctic Peninsula: a size spectra approach. Journal of Plankton Research, 36(4): 1074—1091
Goericke R, 2011. The size structure of marine phytoplankton- What are the rules? California Cooperative Oceanic Fisheries Investigations Reports, 52: 198—204
Jia H L, Chen M R, Su W, 2019. Structural characteristics and associated factors influencing phytoplankton abundance and species composition in Huangmaohai Bay, Pearl River Estuary. Journal of Coastal Research, 35(1): 72—81
Jiao N Z, Yang Y H, Koshikawa H, 2002. Influence of hydrographic conditions on picoplankton distribution in the East China Sea. Aquatic Microbial Ecology, 30(1): 37—48
Key T, McCarthy A, Campbell D A, 2010. Cell size trade-offs govern light exploitation strategies in marine phytoplankton. Environmental Microbiology, 12(1): 95—104
Li Q P, Ge Z M, Liu Z J, 2021. Transparent exopolymer particles in a coastal frontal zone of the Northern South China Sea and the associated biogeochemical implications. Journal of Geophysical Research: Biogeosciences, 126(2): e2020JG005893
Li Q P, Zhou W W, Chen Y C, 2018. Phytoplankton response to a plume front in the northern South China Sea. Biogeosciences, 15(8): 2551—2563
Li Y, Li D J, 2012. Spatial distributions of picoplankton and viruses in the Changjiang estuary and its Adjacent Sea area during Summer. Journal of Marine Sciences, 2012: 465168
Liu Z J, Li Q P, Ge Z M,, 2021. Variability of plankton size distribution and controlling factors across a coastal frontal zone. Progress in Oceanography, 197: 102665
Mara?ón E, Cerme?o P, Latasa M, 2012. Temperature, resources, and phytoplankton size structure in the ocean. Limnology and Oceanography, 57(5): 1266—1278
Mara?ón E, Cerme?o P, Rodríguez J, 2007. Scaling of phytoplankton photosynthesis and cell size in the ocean. Limnology and Oceanography, 52(5): 2190—2198
Mitbavkar S, Rajaneesh K M, Anil A C, 2012. Picophytoplankton community in a tropical estuary: detection of-like populations. Estuarine, Coastal and Shelf Science, 107: 159—164
Montagnes D J S, Berges J A, Harrison P J, 1994. Estimating carbon, nitrogen, protein, and chlorophyllfrom volume in marine phytoplankton. Limnology and Oceanography, 39(5): 1044—1060
Morán X A G, López-Urrutia á, Calvo-Díaz A, 2010. Increasing importance of small phytoplankton in a warmer ocean. Global Change Biology, 16(3): 1137—1144, doi: 10. 1111/j.1365-2486.2009.01960.x
Pennock J R, 1985. Chlorophyll distributions in the Delaware estuary: regulation by light-limitation. Estuarine, Coastal and Shelf Science, 21(5): 711—725
Quinones R A, Platt T, Rodríguez J, 2003. Patterns of biomass-size spectra from oligotrophic waters of the northwest Atlantic. Progress in Oceanography, 57(3—4): 405—427
Rodríguez J, Tintoré J, Allen J T, 2001. Mesoscale vertical motion and the size structure of phytoplankton in the ocean. Nature, 410(6826): 360—363
San Martin E, Harris R P, Irigoien X, 2006. Latitudinal variation in plankton size spectra in the Atlantic Ocean. Deep Sea Research Part II: Topical Studies in Oceanography, 53(14—16): 1560—1572
Sin Y, Jeong B, Park C, 2015. Semidiurnal dynamics of phytoplankton size structure and taxonomic composition in a macrotidal temperate estuary. Estuaries and Coasts, 38(2): 546—557
Sin Y, Wetzel R L, Anderson I C, 2000. Seasonal variations of size-fractionated phytoplankton along the salinity gradient in the York River estuary, Virginia (USA). Journal of Plankton Research, 22(10): 1945—1960
Wang Y P, Voulgaris G, Li Y, 2013. Sediment resuspension, flocculation, and settling in a macrotidal estuary. Journal of Geophysical Research: Oceans, 118(10): 5591—5608
Yvon-Durocher G, Montoya J M, Trimmer, M, 2011. Warming alters the size spectrum and shifts the distribution of biomass in freshwater ecosystems. Global Change Biology, 17(4): 1681—1694
Zhang W J, Sun X X, Zheng S, 2019. Plankton abundance, biovolume, and normalized biovolume size spectra in the northern slope of the South China Sea in autumn 2014 and summer 2015. Deep Sea Research Part II: Topical Studies in Oceanography, 167: 79—92
TIDAL EFFECTS ON PLANKTON COMMUNITY AND SIZE-STRUCTURE IN THE HUANGMAO BAY OF THE SOUTH CHINA SEA
LIU Zi-Jia1, 2, LI Qian1, 2, 3, CHEN Yin-Chao1, 2, SHUAI Yi-Ping1, 2, MA Meng-Zhen1, 2
(1. State Key Laboratory of Tropical Oceanography, South China Sea Institute of Oceanology, Chinese Academy of Sciences, Guangzhou 510301, China; 2. University of Chinese Academy of Sciences, Beijing 100049, China; 3. Guangdong Laboratory of Southern Ocean Science and Engineering (Guangzhou), Guangzhou 511458, China)
As a key component of the aquatic food chain, plankton plays an important role in the marine biogeochemical cycle. To explore the temporal and spatial patterns of the plankton community, a field survey was carried out in the Huangmao Bay of the South China Sea (SCS) from August 17thto 20th, 2017. We estimated the plankton size structure based on the normalized biovolume size spectrum (NBSS) by FlowCAM and the composition of the picoplankton community by flow cytometry. Our results suggest that the highest concentration of total chlorophyll-was located outside the bay where large-sized plankton was relatively dominant. The onshore intrusion of seawater had a great impact on the bottom layer, leading to periodical salinity and temperature fluctuations during each tidal cycle. The tidal variation showed distinct effects on the plankton of different sizes. Picoplankton was merely affected by tidal forcing, but large-sized plankton was greatly influenced. In addition, a substantial increase in the NBSS slope (a higher fraction of large-sized plankton) was observed during high tides, while the NBSS slope decreased substantially (a higher fraction of small-sized plankton) during low tides. Therefore, the tidal forcing along with the changes in nutrients, temperature, and light were the main drivers affecting the distribution of plankton in the Huangmao Bay. This study may provide valuable data and insights for a better understanding of planktonic ecosystem dynamics and the biogeochemical cycle in the coastal area of the SCS.Key words plankton; plankton size; tide; Huangmao Sea
* 廣東省特支計劃領軍人才項目, 2019TX05H216號; 南方海洋科學與工程廣東省實驗室 (廣州) 重大專項, GML2019ZD0305號。劉子嘉, 博士研究生, E-mail: zijialiu@outlook.com
李 芊, 博士生導師, 研究員, E-mail: qianli@scsio.ac.cn
2021-04-27,
2021-06-16
Q178
10.11693/hyhz20210400107