小麥TaGeBPL基因的克隆及表達分析
王蒙蒙,張香宇,張 露,徐曉敏,王 琦,王長有,吉萬全,2,張 宏,2
(1.西北農林科技大學農學院,陜西楊陵 712100;2.農業部作物基因資源與種質創制陜西科學觀測實驗站,陜西楊凌 712100)
表皮毛是由表皮細胞發育而來,是植物表皮組織的一種特化結構,可增加表皮層厚度,減少水分、熱量的散失,也會分泌某些化學物質來防御病蟲、微生物的侵害,對植物生長發育具有重要保護作用[1-2]。表皮毛被認為是研究植物細胞分化調控的理想模型[3],同時也具有抗蟲、抗病、抗逆等功能[4]。因此,研究與植物表皮毛相關的基因不僅為細胞分化和植物發育提供參考,對小麥遺傳改良及育種工作也具有借鑒意義[5]。
近年來,隨著擬南芥表皮毛發育調控機制研究的不斷深入,多個參與調控植物表皮毛發育的相關基因已被報道,如GL1[6]、TTG1[7]、GL3[8]、TTG2[9]和GL2[10]。其中,GL1是第一個被克隆到的與表皮毛發育相關的關鍵基因,其增強子序列對基因發揮功能具有重要作用[11]。研究表明,表皮毛細胞發育與其他形態建成類似,是一個嚴格受時空調控的過程,需要不同的轉錄因子相互作用完成[12-13]。GeBP(GLABROUS1-enhancer binding protein)型轉錄因子作為其中轉錄因子之一,通過識別并結合GL1基因增強子來調控GL1基因的表達,進而控制表皮毛的生成[14]。GeBP是植物中特有的一類轉錄因子[15],截至目前,除了擬南芥、水稻等模式植物外,番茄中亦有GeBP轉錄因子的報道[14,16],但在小麥中還未見到GeBP轉錄因子的相關報道。
擬南芥中GeBP轉錄因子是一種具有DNA結合活性的核蛋白,主要在葉原基、分生組織以及維管組織中表達[15],GPL1、GPL2、GPL3在內的GeBP/GPLs家族成員都含有保守中央區域和亮氨酸拉鏈C端區域,并且在體內可形成二聚體[17],但目前其功能未知。前人研究發現,GeBP蛋白與CPR5(Pathogenis-related gene 5)蛋白存在一定的聯系,暗示GeBP基因發揮其功能可能與CPR5基因有關[18]。CPR5是一個多效性基因,在細胞壁代謝[19]、細胞增殖[20]、細胞衰老[21]、細胞死亡[22]、植物抗病性[23-24]方面中發揮重要功能,而GeBP可通過調節CPR5基因來發揮作用[18]。此外,遺傳學分析也表明,GeBP發揮自身功能在一定程度上依賴于CPR5[18]。在病菌脅迫過程中,CPR5是調控植物細胞防御的重要因子之一[25]。Perazza等[18]對gebp gpl1,2,3缺失突變體轉錄組結果數據分析中發現,GeBP/GPLs和CPR5轉錄組數據存在部分重疊,CPR5通路中發現了大量的GeBP/GPLs依賴基因,GeBP/GPLs基因控制著CPR5調控的部分基因,作用于CPR5通路下游,GeBP/GPLs的功能雖是CPR5功能的一個子集,但GeBP/GPLs和CPR5之間的轉錄組分析數據、表型和遺傳關系均表明,兩者參與了類似的過程。例如,gebp gpl1,2,3缺失突變體、VP16:GPL2過表達突變體、cpr5缺失突變體這三個株系接種丁香假單胞菌(Pseudomonassyringaepvtomato)DC3000后,三個株系中病原體的生長量較對照組野生型均明顯下降,說明有關基因激活了病原體的應答通路,抑制病原體的入侵,并且gebp gpl1,gebp gpl2,gebp gpl3缺失突變體和VP16:GPL2過表達突變體株系中病原菌應答標記基因PR1和PR5的轉錄水平也高于對照組野生型,表明GeBP/GPLs是PR基因的抑制因子,由此也證明GeBP轉錄因子在病原菌防御途徑中發揮著一定作用[18]。
本課題組前期對小麥自發斑點細胞壞死RILs(N13039H/N)轉錄組學數據分析時發現,GeBP同源基因在兩個不同材料中的表達水平差異顯著[26]。鑒于小麥GeBP家族轉錄因子參與生物、非生物脅迫以及對病原菌的抵抗防御反應尚不清楚,因此,本研究克隆了小麥中一個GeBP類基因,并對其進行生物信息學分析、亞細胞定位、表達特性分析以及酵母轉錄激活活性驗證,以期為研究小麥GeBP家族基因功能提供參考和依據。
1 材料與方法
1.1 試驗材料
供試材料西農N13039H、抗白粉病近等基因系N9134R、感白粉病近等基因系N9134S、本氏煙草(Nicotianabenthamiana)以及小麥白粉菌(Blumeriagraminisf.sp.tritici,Bgt)E09菌株均由西北農林科技大學農學院提供。
1.2 材料處理
將均勻一致、成熟飽滿的N9134R和N9134S籽粒種于盆中,置于20 ℃/12 ℃(光照16 h/黑暗8 h)人工培養箱中培養,待小麥長至兩葉一心期時,接種E09菌株。在接種0、12、24、36、48和72 h后分別取適量葉片提取RNA,置-80 ℃保存。
1.3 基因組DNA、總RNA的提取及cDNA第一鏈的合成
利用Trizol法[27]提取西農N13039H、抗白粉病近等基因系N9134R、感白粉病近等基因系N9134S各樣品的總RNA。用PrimeScriptTMⅡ 1st strand cDNA Synthesis Kit試劑盒(TaKaRa,大連)合成cDNA第一鏈。
1.4 目的基因的克隆
根據自發斑點細胞壞死RILs(N13039H/N)的轉錄組測序數據,利用Ensembl Plants數據庫(http://plants.enseml.org/index.html)將搜索到的候選基因(TraesCS3D02G037800)序列為參考序列,利用Primer Premier 5.0設計3D染色體上目標基因特異引物TaGeBPL-F/R(表1),并以西農N13039H cDNA為模板進行PCR擴增。擴增程序:94 ℃ 3 min;94 ℃ 30 s,60 ℃ 50 s,72 ℃ 2 min,38個循環;72 ℃ 10 min。利用1.5%瓊脂糖凝膠電泳檢測PCR擴增產物,將與預期片段長度一致的目的條帶回收、純化,使用DNA連接酶將目標片段插入pMD19-T載體(TaKaRa,大連),并轉化至大腸桿菌感受態細胞DH5α。平板過夜后,利用菌落PCR檢測陽性單克隆并測序驗證。測序由奧科鼎盛生物科技有限公司完成。

表1 本研究用到的引物信息Table 1 Primers used in the study
1.5 生物信息學分析
通過NCBI(https://www.ncbi.nlm.nih.gov)和Ensembl Plants中BLAST程序對TaGeBPL基因的核酸序列及氨基酸序列進行比對;用ExPASy(http://web.Expasy.org/protparam/)對TaGeBPL蛋白進行理化性質分析;用SOPMA(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl?page=npsa_sopma.html)和SWISS-MODEL(https://swissmodel.expasy.org/interactive/CKkukm/models/)對蛋白質的二級和三級結構進行預測;用TMpred(http://www.cbs.dtu.dk/services/TMHMM/)和SignalP(http://www.cbs.dtu.dk/services/SignalP-3.0/)進行跨膜區和信號肽預測;用ProtScale(https://web.expasy.org/protscale)和NetPhos(http://www.cbs.dtu.dk/services/NetPhos)對蛋白的親疏水性和磷酸化位點進行預測;用Plant CARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)分析基因啟動子區域的順式作用元件;用cNLS Mapper(http://nls-mapper.iab.keio.ac.jp/cgi-bin/NLS_Mapper_form.cgi)和Cell-PLoc 2.0(http://www.csbio.sjtu.edu.cn/bioinf/Cell-PLoc-2)預測編碼蛋白的核定位信號和亞細胞定位;用MEME Suite(http://meme-suite.org/index.html)分析氨基酸保守motif;用NCBICD-Search(https://www.ncbi.nlm.nih.gov/Structure/bwrpsb/bwrpsb.cgi)分析蛋白的保守結構域;用MEGA 7.0軟件,采取最大似然法構建系統進化樹,Bootstrap值為1 000。
1.6 TaGeBPL基因的表達分析
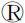
1.7 亞細胞定位
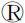
1.8 酵母轉錄自激活活性驗證
與GFP同源重組引物設計原理相同,用Premier 5.0設計引物pGBKT7-TaGeBPL-F/R(表1),以pMD19-T::TaGeBPL質粒為模板進行PCR擴增。使用限制性內切酶EcoRⅠ和BamHⅠ對pGBKT7載體進行雙酶切,瓊脂糖凝膠電泳檢測后對PCR擴增產物和酶切產物進行回收、純化和同源同組,并轉化大腸桿菌感受態細胞DH5α,挑取陽性單克隆。根據奧科鼎盛生物科技有限公司測序結果,提取質粒后獲得pGBKT7::TaGeBPL重組載體。
獲取重組載體后,以重組載體pGBKT7::TaGEBPL為試驗組、共轉載體pGBKT7-53+pGADT7-T為陽性對照、空載體pGBKT7為陰性對照,分別轉化至酵母菌株Y2HGold中,取適量菌液涂布在SD/-Trp培養基上,封口倒置,置于30 ℃黑暗培養箱中培養48~96 h,觀察菌落生長情況。待菌長至2~3 mm,挑取單克隆于 1 mL的SD/-Trp液體培養基中震蕩培養(220 r·min-1,30 ℃)至OD600約為0.1,以100、10-1、10-2和10-3倍數稀釋菌液,各取2 μL分別點涂在SD/-Trp、SD/-Trp/X-α-Gal、SD/-Trp/-His/-Ade培養基上,置于30 ℃黑暗培養箱中培養 48~96 h,觀察菌生長情況,進行轉錄因子自激活檢測。
2 結果與分析
2.1 目的基因的擴增
以小麥西農N13039H的cDNA為模板,以TaGeBPL-F/R為特異性引物進行PCR擴增,得到一條與預期目標相一致的條帶(圖1),將擴增產物回收純化后連接至pMD19-T載體,轉化至大腸桿菌DH5α,并進行籃白斑篩選、PCR檢測和測序,最終獲得一條長度為1 527 bp的片段。利用Ensembl Plants基因組數據庫將所得序列進行Blast比對分析,結果顯示與中國春TraceCS3D02G037800最接近,相似度高達 99.1%,位于小麥3D染色體上,而與小麥3A和3B染色體組上的TraceCS3A02G042900、TraceCS3B02G040600基因的相似度僅為 84.1%和91.6%。目的基因初步分析得出,該基因共編碼508個氨基酸(圖2),推測其分子式為C2342H3835N695O811S10,理論分子量為55 025.98 Da,理論等電點為6.33。
2.2 TaGeBPL蛋白理化性質和結構域分析
利用ExPASy對目的基因編碼蛋白質的理化性質進行分析,發現該蛋白氨基酸序列中賴氨酸和谷氨酸含量較高,脂肪指數為50.12,平均親水性為-1.153,屬于親水性蛋白,其不穩定系數為49.31,同屬于不穩定蛋白。利用SOPMA和SWISS-MODEL預測該蛋白的二級、三級結構,發現該蛋白是由四種構象組成。SignalP和TMpred預測結果顯示,該蛋白不含有信號肽和跨膜結構域。NetPhos預測結果表明,該蛋白氨基酸序列含有較多的磷酸化位點。cNLS Mapper預測結果顯示,該蛋白含有兩個單一型NLS和一個雙分型NLS(圖2)。Cell-PLoc預測結果顯示,該蛋白定位于細胞核內,與NIL預測結果一致。NCBI CD-Search保守結構域分析表明,該蛋白含有DUF573結構域,位于氨基酸第164至247位點之間,屬于GeBP轉錄因子家族,因此將該基因命名為TaGeBPL。
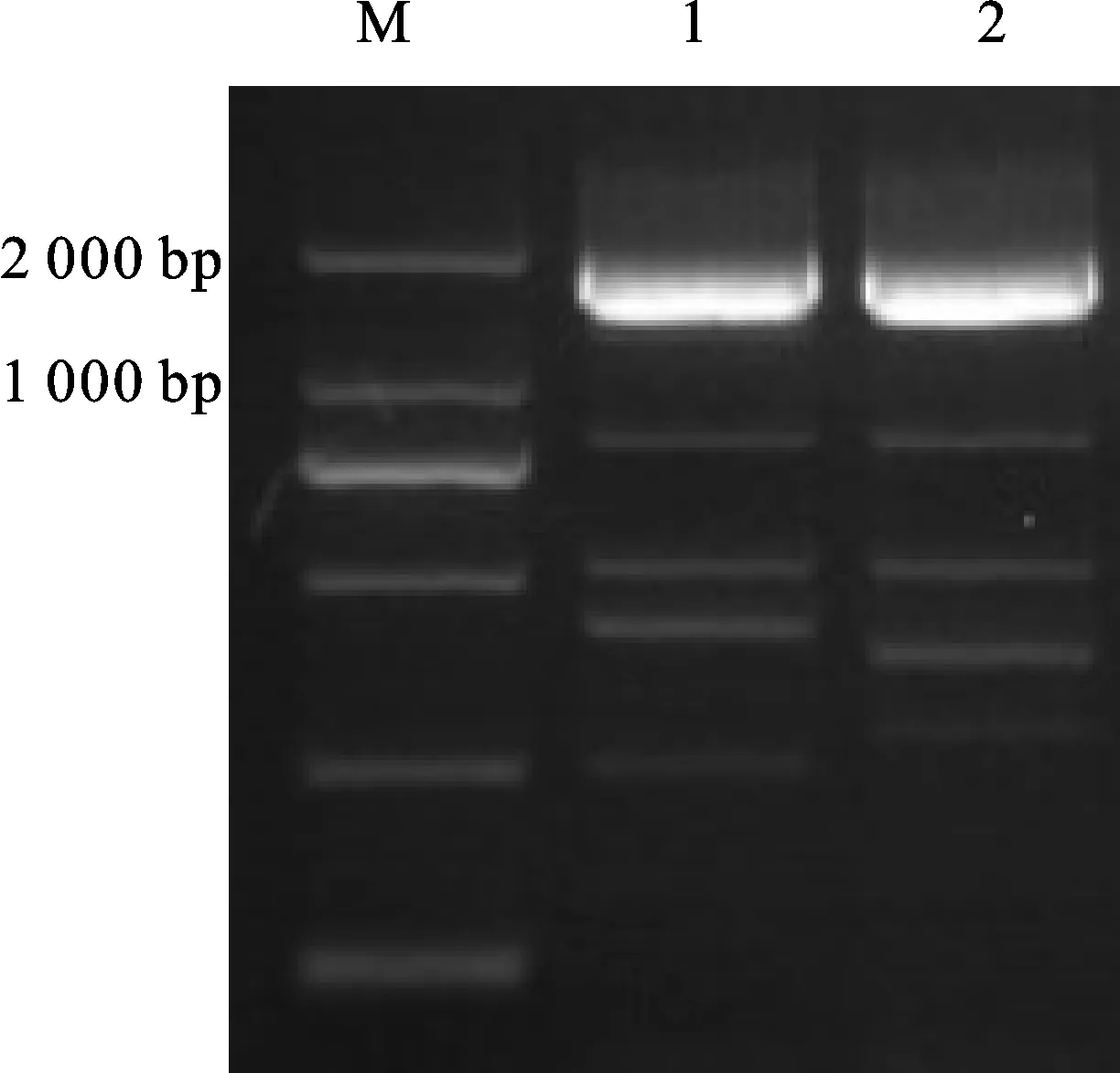
M:DL2000;1~2:PCR擴增產物。M:DL2000;1-2:PCR amplification products.圖1 PCR擴增結果Fig.1 PCR amplification results

黑色下劃線表示DUF573結構域;方框部分表示核定位信號區。Black underline represent DUF573 domain;Boxes indicate the region of nuclear localization signal.圖2 TaGeBPL蛋白的氨基酸序列Fig.2 Amino acid sequence of TaGeBPL protein
2.3 蛋白同源性及系統發育分析
利用PlantTFDB、RGAP、TAIR等數據庫檢索GeBP家族轉錄因子,發現在已被鑒定的擬南芥和水稻中,絕大多數GeBP家族成員氨基酸序列的中央區域均含有DUF573結構域。將小麥西農N13039H的TaGeBPL轉錄因子與擬南芥和水稻中的GeBP轉錄因子保守結構域進行多序列比對分析,結果(圖3)顯示,TaGeBPL與AT2G20613.1、AT4G00130.1、AT5G41765.1、LOC_Os01g14720.1的保守域氨基酸序列長度有較大差異性,而與其他氨基酸的序列長度相近,結構域相似性也較高。

圖3 TaGeBPL與擬南芥、水稻GeBP蛋白的氨基酸序列比對Fig.3 Sequence alignment of TaGeBPL and GeBP of Arabidopsis thaliana and Oryza sativa
為進一步了解小麥TaGeBPL的進化關系,從PlantTFDB數據庫下載擬南芥和水稻中的GeBP轉錄因子氨基酸序列,通過MEGA 7.0軟件構建系統發育樹,結果(圖4)表明,TaGeBPL與水稻LOC_Os02g18660.1、LOC_Os02g53150.1處于同一分支,親緣關系較近,相似性較高。
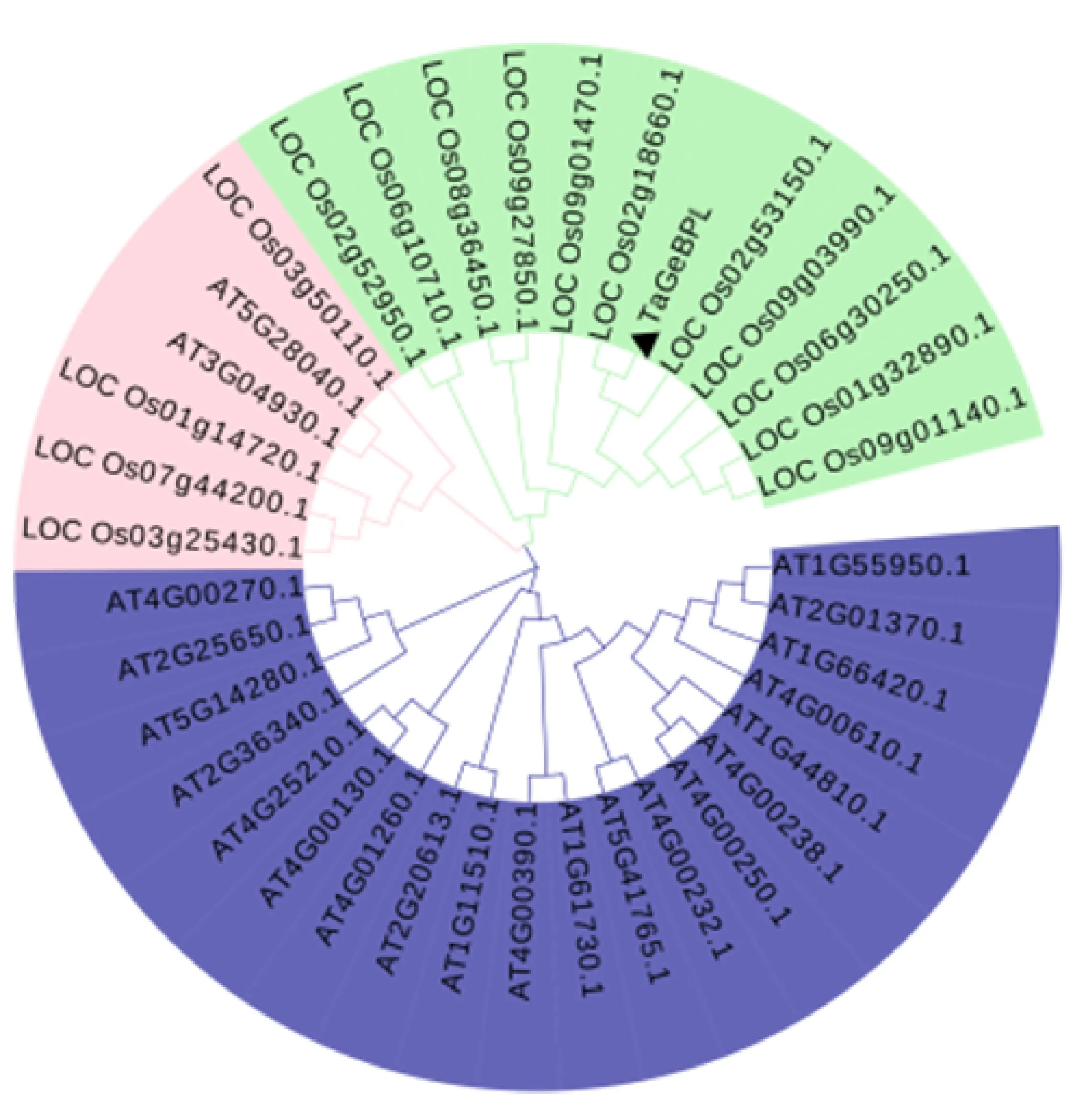
圖4 TaGeBPL與擬南芥、水稻GeBP蛋白系統發育分析Fig.4 Phylogeny analysis of TaGeBPL and GeBP of Arabidopsis thaliana and Oryza sativa
2.4 啟動子區序列結構分析
利用Ensembl Plants數據庫分析TaGeBPL基因起始密碼子上游約2 000 bp的序列,結果(表2)發現,TaGeBPL的啟動子區域含有與逆境、植物激素相關的順式作用元件。如在起始密碼子上游1 163~1 168 bp處含有MBS干旱應答元件,在上游402~407 bp處含有LTR低溫應答元件,在上游1 864~1 868 bp處含有as-1植物激素應答元件,在上游158~162 bp處含有ABRE脫落酸應答元件。此外,啟動子區域還含有多個光應答元件(I-box、G-box、Sp1),其位置和數量均不同。啟動子分析結果表明,該基因可能受多種植物激素信號調控,參與生物和非生物脅迫途徑。

表2 TaGeBPL基因啟動子區順式作用元件Table 2 Cis-acting elements of TaGeBPL gene in the promoter regions
2.5 小麥TaGeBPL基因的表達模式
研究TaGeBPL基因在小麥中的表達模式有利于挖掘其潛在功能,將白粉菌菌株E09接種于抗病近等基因系N9134R和感病近等基因系N9134S中,采用實時熒光定量PCR的方法,對接種白粉菌E09 0、12、24、36、48和72 h后TaGeBPL基因的相對表達量進行測定。結果(表3)表明,接種E09后TaGeBPL基因在N9134R和N9134S兩個材料中的表達模式不同。TaGeBPL基因在N9134R中的表達量呈現“降-升-降”的變化趨勢,接種12、24和72 h時TaGeBPL基因相對表達量顯著下調,分別為0 h時的61%、68%和74%;接種36和48 h時TaGeBPL基因的相對表達量顯著上調,分別為0 h的1.23和 1.19倍。而TaGeBPL基因在N9134S中的表達量呈現“升-降-升-降”的變化趨勢,在12 h時TaGeBPL相對表達量顯著上調,36 h時其表達量達到峰值,約為對照組的2倍,差異顯著,72 h時恢復至未接種對照相同的水平。小麥TaGeBPL基因在N9134S中的表達量始終高于在N9134R中的表達量,推測TaGeBPL基因可能響應白粉菌的侵染,參與了病原菌響應的相關 途徑。
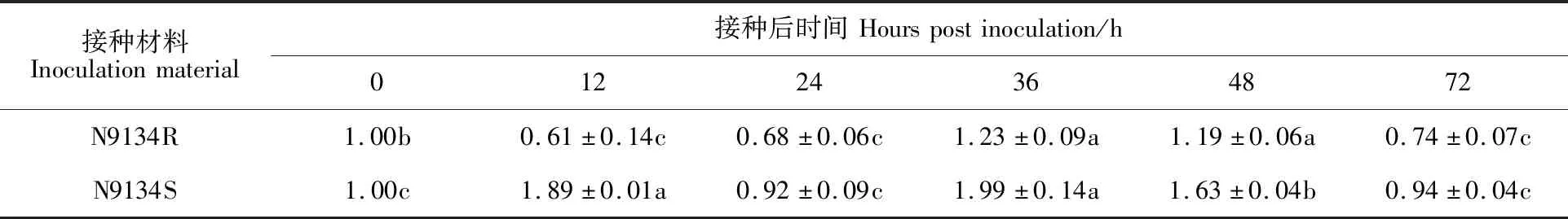
表3 TaGeBPL基因的qRT-PCR分析Table 3 qRT-PCR analysis of TaGeBPL gene
2.6 小麥TaGeBPL的亞細胞定位
NLS Mapper和Cell-PLoc預測結果顯示,該蛋白具有3個核定位信號,定位在細胞核上。為驗證TaGeBPL的亞細胞定位結果,利用本氏煙草瞬時表達系統,以PYJ::GFP空載體為對照組,以PYJ:TaGeBPL:GFP融合載體為試驗組,注射生長良好的煙草植株,結果(圖5)顯示,在綠色熒光通道下,PYJ:TaGeBPL:GFP融合蛋白僅在細胞核內有綠色熒光信號,說明該蛋白定位于細胞核中。
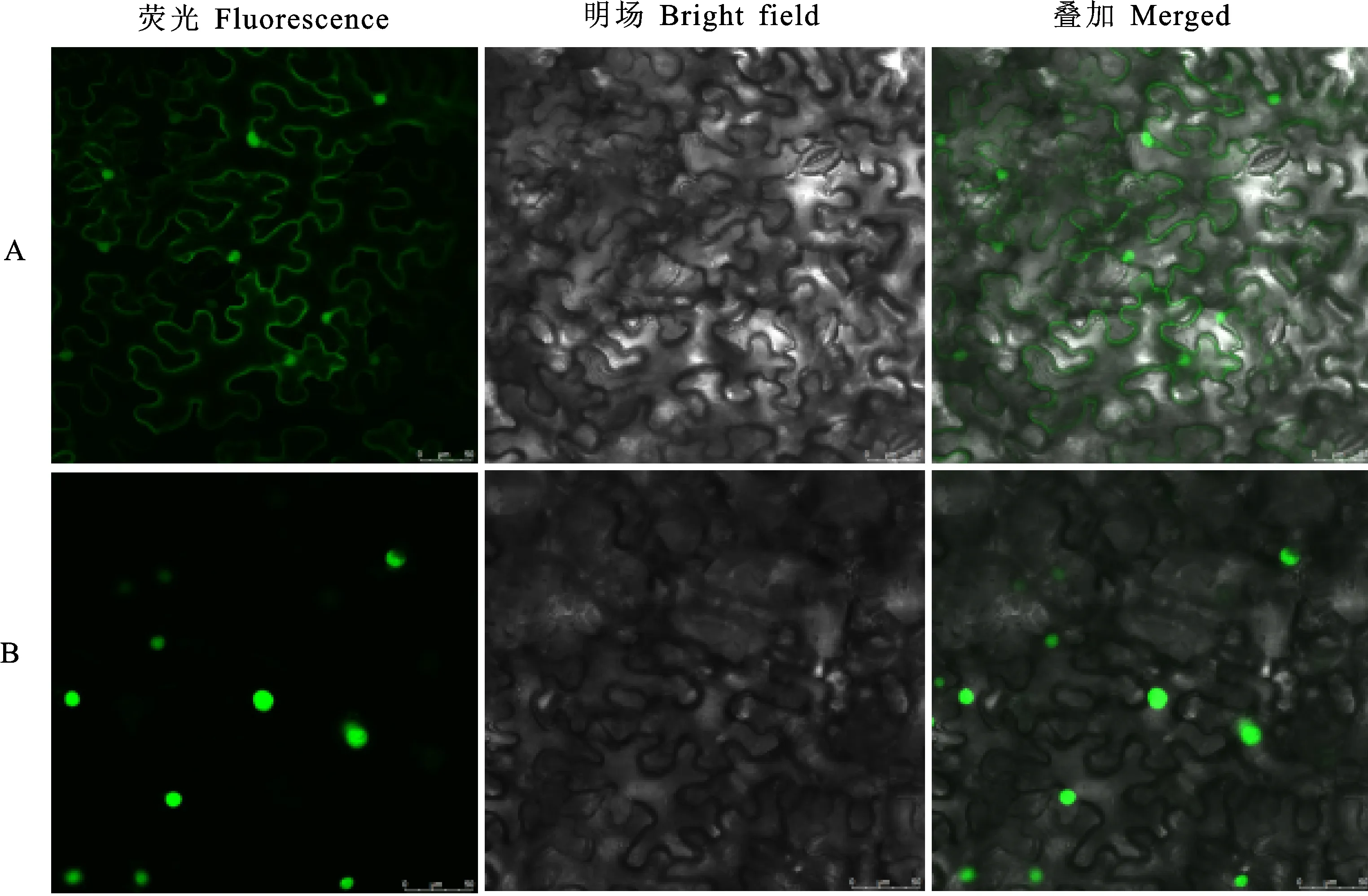
A:對照PYJ::GFP空載體定位;B:PYJ:TaGeBPL:GFP融合載體定位。A:Localization of control PYJ::GFP empty vector;B:Localization of PYJ:TaGeBPL:GFP fusion vector.圖5 小麥TaGeBPL的亞細胞定位Fig.5 Subcellular localization of wheat TaGeBPL protein
2.7 TaGeBPL的轉錄激活活性
轉錄因子的轉錄激活活性對其發揮生物學功能具有重要作用,為檢測TaGeBPL轉錄因子的轉錄激活活性,將試驗組pGBKT7::TaGeBPL、對照組pGBKT7-T+pGBKT7-p53和pGBKT7分別轉至酵母Y2HGold菌株中,發現它們均能在SD/-Trp營養缺陷培養基上正常生長(圖6),說明外源載體pGBKT7::TaGeBPL成功轉入酵母菌中。為檢驗pGBKT7::TaGeBPL融合蛋白對其下游報告基因的激活情況,將含有pGBKT7::TaGeBPL、pGBKT7-T+pGBKT7-p53、pGBKT7的酵母菌株分別涂布于SD/-Trp/X-α-Gal、SD/-Trp/-His/-Ade營養缺陷型固體培養基上,結果(圖6)發現,含pGBKT7::TaGeBPL的Y2HGold菌株不能激活LacZ報告基因表達,使X-α-Gal發生顯色反應,說明誘餌載體pGBKT7::TaGeBPL無法激活Y2HGold酵母菌株中指示基因的表達。在SD/-Trp/-His/-Ade營養缺陷培養基上,pGBKT7::TaGeBPL酵母菌株不能正常生長,證實了TaGeBPL在酵母細胞中無轉錄自激活活性。

100、10-1、10-2、10-3為4種不同稀釋濃度酵母菌液;pGBKT7::TaGeBPL為試驗組;pGBKT7-T+pGBKT7-p53為陽性對照組;pGBKT7為陰性對照組。100,10-1,10-2 and 10-3are four different dilution concentration of yeast solution;pGBKT7::TaGeBPL is experimental group,pGBKT7-T+pGBKT7-p53 is positive control group;pGBKT7 is negative control group.圖6 小麥TaGeBPL轉錄激活活性分析Fig.6 Transactivation activity assay of TaGeBPL in wheat
3 討 論
本研究基于前期轉錄組測序結果,利用RT-PCR技術克隆得到小麥TaGeBPL基因。該基因僅存在于染色體第3同源群,且與現階段已知的小麥唯一GeBP基因(TraesCS1D02G132000)同源性低于30%。擬南芥中,GeBP轉錄因子家族成員的基因結構較簡單,在染色體上隨機分布,含有DUF573結構域[14],與前人研究相同,TaGeBPL蛋白也含有DUF573結構域,但其功能未知。對擬南芥、水稻和小麥GeBP基因編碼蛋白的保守結構域進行比對,發現它們具有較高的相似性,TaGeBPL同水稻LOC_Os02g18660.1、LOC_Os02g53150.1親緣關系較近,而LOC_Os02g18660.1和LOC_Os02g53150.1在植株頂端分生組織和種子中的表達量較高,在生殖生長階段發揮重要功能[16],推測小麥中TaGeBPL蛋白可能具有相似功能。在利用生物信息學分析TaGeBPL的基礎上,本研究進行了基因時空特異性表達檢測,qRT-PCR結果表明,白粉菌接種后各個時間點該基因在抗感材料中的相對表達量不相同,且在各個時間點感病材料中TaGeBPL基因的表達量始終高于抗病材料中的表達量,推測小麥中TaGeBPL基因參與了病原菌響應途徑,與GeBP基因在擬南芥中的研究結果[17]一致,這不僅為后期研究小麥GeBP基因作用與機理奠定基礎,也為探究擬南芥等其他物種GeBP同源基因的功能提供參考。此外,擬南芥GeBP蛋白可在體內形成二聚體[17],可從與之互作的蛋白為出發點,間接地研究目標蛋白在植物體中的更多功能[28]。需要注意的是,擬南芥中二聚體的形成與亮氨酸拉鏈區域的最后四個氨基酸有密切的關系,而小麥TaGeBPL蛋白C端沒有亮氨酸拉鏈特殊區域,可能不同物種或同一家族的不同成員之間有差異,總的來說,研究蛋白二聚體為分析GeBP轉錄因子家族提供了思路,對其功能挖掘也具有重要意義[29]。
功能分析是研究基因的一個方面,探究其作用機理可更加深刻地認識該基因。本研究利用cNLS Mapper發現,TaGeBPL轉錄因子位于細胞核中,具有兩種類型的核定位信號,這一特征表明TaGeBPL轉錄因子不需要依靠其他具有NLS轉錄因子的介導,可以直接被受體蛋白識別進入細胞核內[30]。這與擬南芥GeBP/GPLs不同,擬南芥GPL3蛋白雖然定位于細胞核內,但并未發現其具有核定位信號[17],這表明不同物種GeBP進入細胞核的方式可能不同。亞細胞定位結果表明,TaGeBPL僅在細胞核中有綠色熒光信號,進一步驗證了其在核中發揮作用。在擬南芥中GeBP也位于植物細胞核中,而水稻中GeBP家族成員不僅存在于細胞核中,還存在于細胞質、葉綠體類囊體薄膜上[16],原因可能是在不同物種GeBP參與了不同的生理過程。
植物中眾多轉錄因子參與植物激素調控途徑[31],GeBP轉錄因子也不例外。如在模式植物中,Chevalier等[17]發現,擬南芥GeBP/GPLs基因通過對A型ARR基因的調控,進而參與細胞分裂素反應,且對細胞分裂素的響應具有冗余作用[17];而石 蕾[16]研究表明,水稻LOC_Os06g10710在乙烯處理后表現出敏感響應,說明不同物種的GeBP轉錄因子家族成員可能參與不同的植物激素信號調節途徑。在模式植物中,GeBP/GPLs對細胞分裂素的作用僅發生在特定的組織和器官中,而并非整個植株中都能發揮此作用[17]。此外,此方面的研究對象是具有亮氨酸拉鏈的GeBP家族成員,無亮氨酸拉鏈的其他成員是否參與植物激素調節是未知的。而在小麥中該蛋白不含有明顯特征的亮氨酸拉鏈,所以TaGeBPL能否響應細胞分裂素調控途徑還需要下一步的研究。值得注意的是,轉錄因子調控功能基因的表達通常是由相同或不同轉錄因子協同作用的結果,本研究對TaGeBPL的轉錄激活活性試驗為后續互作蛋白的篩選研究奠定了基礎。

