Letermovir:異基因造血干細胞移植后巨細胞病毒感染的預防藥物
《新英格蘭醫學雜志》2017年12月期刊登了Marty等研究人員題為“letermovir(LET)在造血細胞移植中對巨細胞病毒感染的預防”的臨床研究論文。letermovir是美國FDA 15年來批準的第一個治療巨細胞病毒(CMV)感染的新藥。作為非核苷類CMV抑制劑,letermovir的藥物靶向為病毒終末酶復合物,進而阻止病毒復制。
本研究為Ⅲ期雙盲臨床試驗,共納入了565例來自20個國家的67個研究中心的、年齡≥18歲病例。受試者均符合:①CMV血清陽性;②隨機分組前5天內血漿CMV-DNA拷貝數小于可檢測下限;③移植后28 d內可開始接受臨床試驗研究藥物用藥等入組條件。排除標準為:嚴重肝功能損害、估計肌酐清除率小于10 mL/min,和正在或者近期接受抗CMV活性的抗病毒藥治療的患者。此外,隨機時無須考慮中性粒細胞植入。其中31.0%為CMV病高風險患者,50.1%進行了清髓預處理,35.0%接受了抗胸腺細胞球蛋白治療(ATG)。除了接受親緣供者的異基因造血干細胞移植外,還有13.8%接受了不匹配的非親緣供者的干細胞,14.3%接受了單倍體匹配供者的干細胞,以及4.1%接受了臍帶血干細胞(表1)。565例患者均在隨機前5天內,血漿CMV-DNA陰性;其中70例患者在隨機時被發現CMV-DNA陽性,因此在療效分析中被剔除。letermovir治療組和安慰劑組的基線指標是可比的。
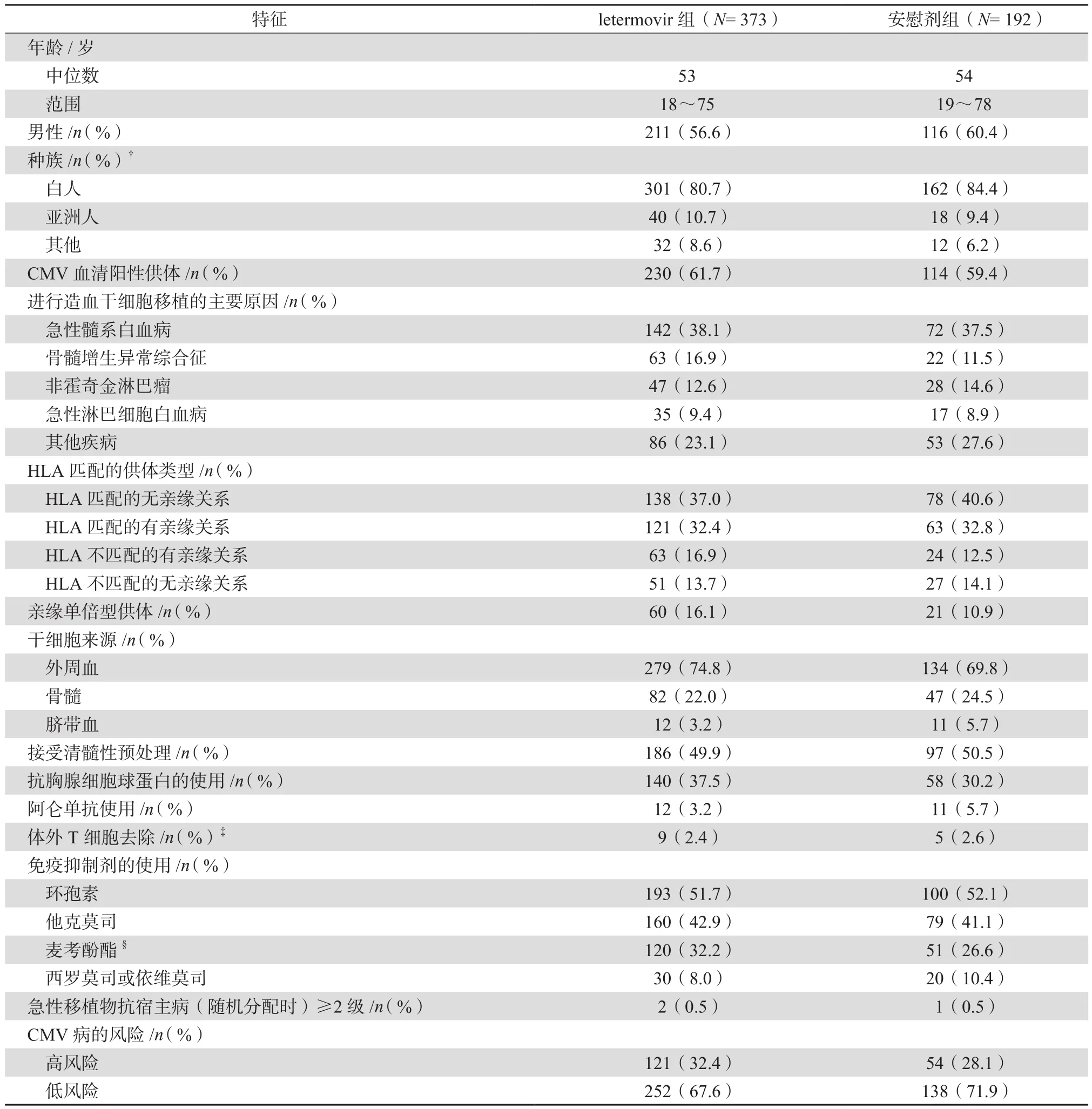
表1 接受隨機化試驗方案患者的基線特征(安全性人群)*
CMV病高風險定義為在隨機化時滿足以下一個或多個標準:①親緣供者在指定的3個人類白細胞抗原(HLA)基因位點(HLA-A、B或DR)中至少有一個不匹配;②非親緣供者在指定的四個HLA基因位點(HLA-A、B、C和DRB1)中至少有一個錯配的;③具有半匹配供者;④使用臍帶血作為干細胞來源;⑤使用體外去除T細胞的移植物;⑥由于發生≥2級移植物抗宿主病(GVHD)而每天應用潑尼松≥1 mg/kg(或其等效藥物)者。所有不符合上述高風險定義的患者均視為低風險。
研究過程中,納入患者按2∶1的比例隨機分配至letermovir治療組與安慰劑組,letermovir治療組最終為325例患者,而安慰劑組為170例(圖1)。患者在移植后當天至移植后第28天中的任何一天開始服用letermovir或者安慰劑。每位患者根據各自組別1次/d口服或靜脈滴注letermovir,或者口服或靜脈滴注相應劑量的安慰劑;口服劑量有兩種選擇,常規劑量為480 mg 1次/d,但如果同時服用環孢素時,考慮到有機陰離子轉運蛋白OATP1B1和OATP1B3介導的藥物相互作用,口服劑量減量為240 mg,而靜脈滴注劑量仍用240 mg。給藥總時長約為100 d或者14周。
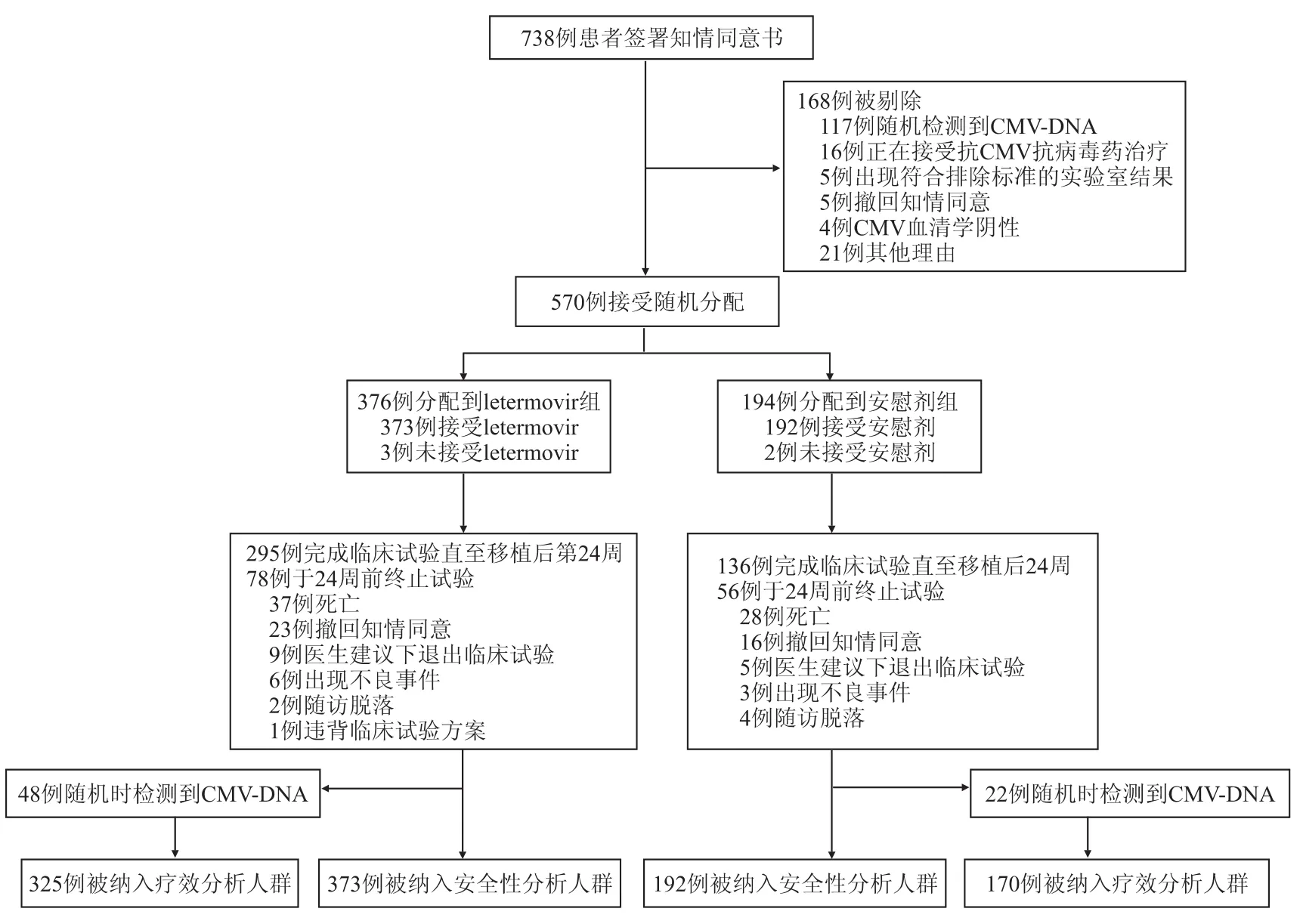
圖1 研究過程流程圖
本研究主要終點為患者在移植后24周內確診有臨床意義的CMV感染;若患者在移植后24周內因任何原因終止letermovir治療,或24周內出現臨床數據遺失,亦計入主要終點事件。研究發現,letermovir治療組與對照組相比,達到治療主要終點者,對照組(103例,60.6%)顯著高于治療組(122例,37.5%),進一步的分層分析確定,治療組中具有臨床意義的CMV感染57例 (17.5%),其中接受抗CMV搶先治療52例(16.0%),確診為CMV腸道感染5例(1.5%);在安慰劑組中,具有臨床意義的CMV感染71例(41.8%),其中接受抗CMV搶先治療68例(40.0%)、確診為CMV腸道感染3例(1.8%)。因此本研究結果表明在高風險患者中,相比于安慰劑,letermovir可以顯著降低具有臨床意義的CMV病風險(P<0.001)。見表2。
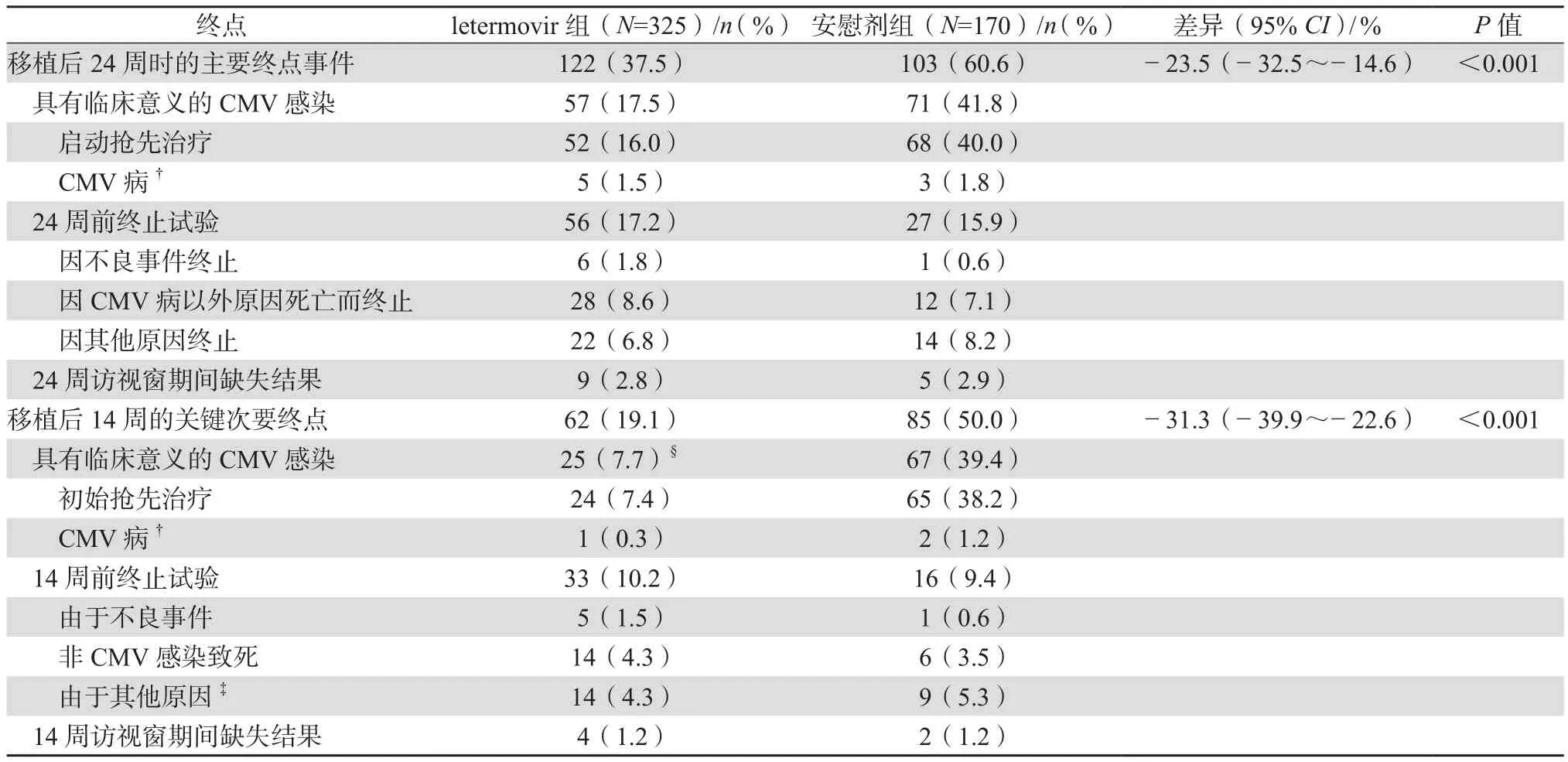
表2 療效終點(主要療效人群)*
letermovir治療組和安慰劑組患者在移植后24周內的藥物相關死亡率為0,而且兩組的藥物相關性不良事件發生率差異沒有統計學意義。治療組和安慰劑組移植后16周內常見不良事件分別為GVHD(39.1%對38.5%)、腹瀉(26.0%對24.5%)、惡心(26.5%對23.4%)、發熱(20.6%對22.4%)、皮疹(20.4%對21.4%)、嘔吐(18.5%對13.5%)、咳嗽(14.2%對10.4%)、外周性水腫(14.5%對9.4%)、乏力、黏膜感染、頭痛、腹痛等(表3),最嚴重的不良事件有感染(17.7%對14.0%)、急性腎臟損傷(9.7%對13.0%)。此外需要特別提及一些不良事件,比如房顫及房撲(4.6%對1.0%),丙氨酸轉氨酶升高5倍(3.5%對1.6%),高鉀血癥(7.2%對2.1%)等在letermovir治療組患者中的發生率比安慰劑組略高,但進一步的分析結果說明上述心房心率失常不良事件的發生與letermovir沒有相關性。
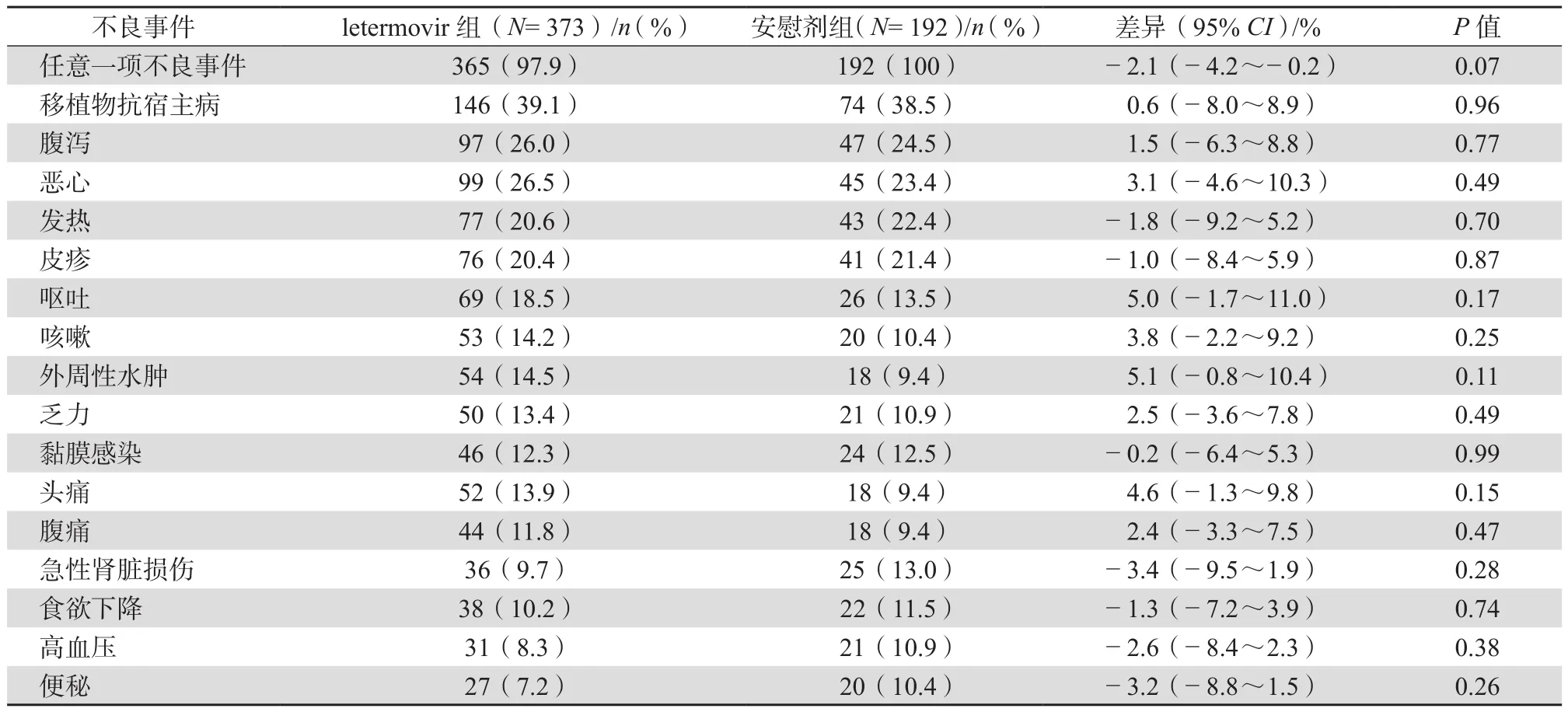
表3 不良事件(安全性人群)*
上述研究為letermovir在接受造血干細胞移植的成年患者CMV感染預防上提供了循證基礎。
專家點評:孫競教授(南方醫科大學南方醫院主任醫師、碩士生導師)
自1979年Balfour教授將CMV稱為“移植患者的巨魔”后,四十多年來CMV感染的診治取得長足進步,特別是CMV-DNA定量檢測技術普及和搶先治療在臨床的應用,使得移植后CMV感染的發病率有了明顯下降。但CMV血癥在異基因干細胞移植患者中仍然保持了較高的發生率,其導致的間接效應,如繼發性植入功能不良、GVHD、全因死亡率等對患者的預后仍產生巨大的影響。而現有抗CMV藥物也存在諸多不足,如劑型單一、靶點相似、可導致粒細胞缺乏/腎損害等。臨床需要一種針對新靶點、兼有靜脈和口服劑型、耐受性好、且能抑制CMV血癥發生的預防用藥。該論文的發表是對這一醫學需求的及時回應,同時預防CMV感染能降低24周全因死亡率的結果,也是第一次通過隨機對照研究證明CMV血癥的間接效應。當然,該論文除了給臨床治療提供了一種新的方法,也帶來了更多的思考,例如如何看待抗CMV預防下CMV-DNA檢測的臨床意義,如何利用CMV特異性免疫指標評估預防的療程,這些都有待未來進一步探索。
致謝:感謝上海北翱醫藥科技有限公司為本文摘譯提供幫助和默沙東(中國)投資有限公司給予的學術支持。
編者說明:本譯文根據首次發表于The New England Journal of Medicine[2017,377(25): 2433-2444]的原著“Letermovir prophylaxis for cytomegalovirus in hematopoietic-cell transplantation”進行的編譯,文中所有圖表已取得首次發表期刊的版權轉讓書,不涉及侵犯版權等問題。

