鼻腔鼻竇腺泡狀橫紋肌肉瘤10例臨床病理分析
姚 瑤,化宏金,潘敏鴻,李 揚(yáng),李紅霞,楊沁怡,丁 穎,范欽和,李 海
橫紋肌肉瘤是一類顯示不同程度骨骼肌分化方向的肉瘤類型,它們是一組異質(zhì)性腫瘤。WHO(2020)軟組織和骨腫瘤分類根據(jù)臨床組織病理學(xué)及分子遺傳學(xué)特征將其劃分四種不同的亞型:胚胎性、腺泡狀、多形性及梭形細(xì)胞/硬化性[1]。1956年Riopelle等[2]首次報(bào)道腺泡狀橫紋肌肉瘤(alveolar rhabdomyosarcoma, ARMS),Enzinger等[3]報(bào)道ARMS發(fā)病率占橫紋肌肉瘤的30%,其屬于小藍(lán)圓細(xì)胞肉瘤,單純組織形態(tài)學(xué)通常僅顯示有限的骨骼肌分化特征,診斷較為困難。多數(shù)ARMS發(fā)生于周圍軟組織,位于鼻腔鼻竇者臨床罕見。眾多不同類型小藍(lán)圓細(xì)胞腫瘤好發(fā)于鼻腔鼻竇,需進(jìn)行鑒別診斷。此外,ARMS有部分免疫組化標(biāo)志物異常表達(dá),易造成誤診,對(duì)治療效果和預(yù)后產(chǎn)生較大影響。本文收集10例鼻腔鼻竇腺泡狀橫紋肌肉瘤(sinonasal tract alveolar rhabdomyosarcoma, SNT-ARMS)進(jìn)行回顧性分析并復(fù)習(xí)文獻(xiàn),探討其診斷及鑒別診斷的要點(diǎn),以期提高對(duì)該腫瘤的認(rèn)識(shí)水平。
1 材料與方法
1.1 臨床資料收集2013年6月~2020年10月南京醫(yī)科大學(xué)第一附屬醫(yī)院病理學(xué)部診斷的10例SNT-ARMS,病例均經(jīng)高年資病理科醫(yī)師復(fù)核、確診。10例患者年齡9~64歲,中位年齡42歲,3例男性,7例女性;其中7例為住院患者,3例為會(huì)診或門診患者。
1.2 免疫組化標(biāo)本均經(jīng)常規(guī)10%中性福爾馬林固定,常規(guī)脫水,石蠟包埋,4 μm厚切片,行HE及免疫組化EnVision法染色,并設(shè)立陰、陽性對(duì)照。抗體包括:desmin、Myogenin、MyoD1、CKpan、CK-L、CD56、CK5/6、Ki-67、Syn、CgA、NSE、NeuN、NF、S-100、ALKp80、CD99、CD34、CD20、CD3、CD5、CD45RO、CD45、Pax-5、HMB-45、CK8/18、SMA、p53、FLI-1、TTF-1、Melan-A、CD138、PLAP、CD117、SOX10、SMMHC、CK7、EMA、Tdt。抗體均購自福州邁新公司,具體操作步驟嚴(yán)格按試劑盒說明書進(jìn)行。
1.3 FISH檢測(cè)FOXO1基因FISH FOXO1(13q14)基因斷裂探針購自廣州安必平醫(yī)藥公司,根據(jù)HE染色切片選擇需要區(qū)域的腫瘤組織進(jìn)行染色,F(xiàn)ISH操作流程進(jìn)行檢測(cè)。判讀標(biāo)準(zhǔn):探針為GSP FOXO1(13q14)基因斷裂探針(雙色),探針雜交區(qū)域?yàn)槿祟?3號(hào)染色體長臂(13q14)FOXO1基因所在區(qū)域,紅色熒光信號(hào)標(biāo)記FOXO1基因5′端,綠色熒光信號(hào)標(biāo)記FOXO1基因3′端。DAPI定位細(xì)胞核,熒光信號(hào)為藍(lán)色。正常細(xì)胞為單個(gè)細(xì)胞核中2個(gè)黃色信號(hào),F(xiàn)OXO1基因斷裂的細(xì)胞為細(xì)胞核中1個(gè)紅色信號(hào)、1個(gè)綠色信號(hào)、1個(gè)黃色信號(hào)。每張切片至少計(jì)數(shù)100個(gè)腫瘤細(xì)胞,如FOXO1基因斷裂細(xì)胞的數(shù)目≥30%,則判定為FOXO1基因斷裂,檢測(cè)結(jié)果為陽性。
2 結(jié)果
2.1 臨床特征6例住院患者均因鼻腔或鼻竇部新生物及相應(yīng)臨床癥狀就診,多表現(xiàn)為鼻塞、涕血、復(fù)視等癥狀;CT示鼻腔鼻竇內(nèi)見軟組織影,病變累及周圍骨質(zhì)呈膨脹性破壞,2例體積較大,累及范圍較廣者顯示鼻中隔及眼眶、顱底骨質(zhì)破壞。3例會(huì)診及門診患者均因頸部淋巴結(jié)腫大就診,淋巴結(jié)穿刺結(jié)果分別診斷為轉(zhuǎn)移性神經(jīng)內(nèi)分泌癌、淋巴瘤及橫紋肌肉瘤,后經(jīng)PET-CT檢查發(fā)現(xiàn)全身多發(fā)淋巴結(jié)腫大及鼻腔內(nèi)軟組織影;其中1例還伴全身多發(fā)骨轉(zhuǎn)移,影像學(xué)診斷提示為淋巴瘤可能性大;另1例女性患者因鼻竇橫紋肌肉瘤放療2年后,發(fā)現(xiàn)乳腺腫塊就診,乳腺腫塊穿刺結(jié)果診斷為ARMS。
2.2 病理檢查眼觀:送檢標(biāo)本均為灰白、灰黃色破碎組織一堆,部分呈息肉樣改變(圖1),大小1.2 cm×1 cm×0.8 cm~4.5 cm×4 cm×3.8 cm。鏡檢:在鼻腔黏膜下方固有層內(nèi)可見幼稚的小藍(lán)圓細(xì)胞彌漫浸潤,未見腫瘤組織侵犯表面鼻竇黏膜上皮(圖2),腫瘤細(xì)胞形態(tài)一致、分化原始,胞質(zhì)稀少,核深染(圖3),核分裂象活躍,部分病例內(nèi)腫瘤組織大片壞死,存活的腫瘤組織圍繞血管周排列。腫瘤細(xì)胞呈彌漫實(shí)性片狀或巢團(tuán)狀排列,瘤巢之間可見纖維血管間隔(圖4),部分瘤巢中央的細(xì)胞因退變失去黏附性而脫落、漂浮于腔內(nèi),形成腺泡狀或囊性結(jié)構(gòu)(圖5),多數(shù)病例內(nèi)腫瘤細(xì)胞的實(shí)性片狀、巢狀及腺泡狀排列方式通常混合存在,比例多少不等;3例腫瘤組織缺乏腺泡狀生長方式,完全以實(shí)性片狀排列為主。4例腫瘤組織可見散在腫瘤性花環(huán)狀多核巨細(xì)胞(圖6),2例腫瘤內(nèi)可見少許圓形上皮樣橫紋肌母細(xì)胞,含有豐富的嗜酸性胞質(zhì);1例腫瘤內(nèi)部分細(xì)胞含有顯著的透明樣胞質(zhì)。淋巴結(jié)內(nèi)轉(zhuǎn)移性腫瘤形態(tài)與原發(fā)灶一致,特征性的腺泡狀結(jié)構(gòu)可見,轉(zhuǎn)移至乳腺內(nèi)的腫瘤組織呈彌漫片狀及單行樣排列,累及乳腺小葉,易誤診為乳腺浸潤性小葉癌。
2.3 免疫表型本組desmin、Myogenin和(或)MyoD1均陽性,其中Myogenin彌漫一致核強(qiáng)陽性(圖7),MyoD1陽性強(qiáng)度和范圍較弱。6例腫瘤細(xì)胞CD56陽性,3例腫瘤細(xì)胞CKpan局灶陽性(圖8),2例腫瘤細(xì)胞CK-L局灶陽性,4例腫瘤細(xì)胞Syn陽性(圖9),1例腫瘤細(xì)胞Syn及CK-L共陽性,1例腫瘤細(xì)胞Syn及CKpan共陽性,1例腫瘤細(xì)胞ALKp80陽性。CK5/6、CgA、NSE、NeuN、NF、S-100、CD99、CD34、CD20、CD3、CD5、CD45RO、CD45、Pax-5、HMB-45、CK8/18、SMA、p53、FLI-1、TTF-1、Melan-A、CD138、PLAP、CD117、SOX10、SMMHC、CK7、EMA、Tdt均陰性。
2.4 FISH檢測(cè)FOXO1基因10例患者均行FISH檢測(cè),結(jié)果顯示:均存在FOXO1基因斷裂重組(圖10)。
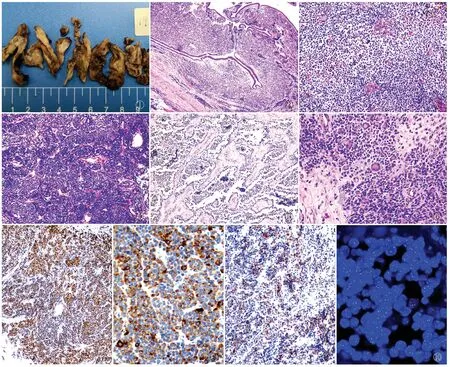
①②③④⑤⑥⑦⑧⑨⑩
2.5 隨訪及預(yù)后本組有8例患者獲得隨訪,其中6例患者死亡,中位生存期13個(gè)月,2例患者術(shù)后11、27個(gè)月生存至今。
3 討論
頭頸部ARMS臨床相對(duì)少見,多發(fā)于鼻腔或鼻旁竇,臨床表現(xiàn)不具有特征性,多數(shù)腫瘤生長迅速,位于鼻腔者可產(chǎn)生鼻塞、鼻衄等癥狀,而鼻旁竇的患者則可能出現(xiàn)眼球突出、面部脹痛、復(fù)視及顱神經(jīng)受損的癥狀[4-5]。SNT-ARMS影像學(xué)檢查缺乏特異性,難以做出準(zhǔn)確的術(shù)前診斷。SNT-ARMS易有淋巴道轉(zhuǎn)移,在疾病的進(jìn)程中可以出現(xiàn)局部或全身多發(fā)的淋巴結(jié)轉(zhuǎn)移,罕見情況下腫瘤以頸部淋巴結(jié)腫大為首發(fā)癥狀,全身檢查后在鼻腔鼻竇處查及原發(fā)灶。本組3例會(huì)診或門診患者,均因頸部淋巴結(jié)腫大就診,后經(jīng)PET-CT檢查后發(fā)現(xiàn)全身多發(fā)淋巴結(jié)腫大及鼻腔內(nèi)軟組織影,其中1例伴全身多發(fā)骨轉(zhuǎn)移。此外,有文獻(xiàn)報(bào)道女性SNT-ARMS患者有轉(zhuǎn)移至乳腺的傾向[6]。本組亦有1例女性患者因鼻竇ARMS放療2年,發(fā)現(xiàn)乳腺腫塊復(fù)發(fā)就診。亦有文獻(xiàn)報(bào)道,SNT-ARMS的腫瘤細(xì)胞廣泛累及骨髓及血液系統(tǒng),類似于白血病的臨床表現(xiàn)[7-8]。
SNT-ARMS與發(fā)生于軟組織的同類腫瘤相似,腫瘤由形態(tài)單一、分化幼稚的小藍(lán)圓細(xì)胞組成,腫瘤排列呈巢狀。瘤巢之間為纖維血管間隔,腫瘤細(xì)胞巢中央的細(xì)胞常因退變失去黏附性而脫落、漂浮于腔內(nèi),形成特征性的腺泡狀結(jié)構(gòu),其特征性的腺泡狀結(jié)構(gòu)在淋巴結(jié)和其他臟器的轉(zhuǎn)移灶中常見。ARMS的腫瘤分化通常較為原始,不見或僅見少許橫紋肌母細(xì)胞分化,約50%病例可見一種獨(dú)特的核位于外周的花環(huán)狀腫瘤性巨細(xì)胞,具有診斷提示意義[3-5]。ARMS有一些少見的形態(tài)學(xué)亞型:實(shí)性亞型者缺乏常見的腺泡狀、巢狀生長結(jié)構(gòu),而表現(xiàn)為彌漫實(shí)性片狀的生長方式,診斷較為困難;透明細(xì)胞亞型則表現(xiàn)為腫瘤細(xì)胞具有豐富的透明狀胞質(zhì)[9],易誤診為其他類型的透明細(xì)胞腫瘤包括轉(zhuǎn)移性腎透明細(xì)胞癌、透明細(xì)胞肌上皮癌等。本組病例幾乎囊括上述經(jīng)典的及罕見的組織形態(tài)學(xué)特征。
鼻腔鼻竇是眾多小圓細(xì)胞腫瘤好發(fā)部位,其多種不同分化方向的腫瘤類型均可呈未分化小藍(lán)圓細(xì)胞形態(tài),包括:上皮性癌(未分化癌、NUT中線癌、小細(xì)胞神經(jīng)內(nèi)分化癌及SMARCB1基因缺陷型癌)、肉瘤(尤因肉瘤、橫紋肌肉瘤、間葉性軟骨肉瘤、差分化滑膜肉瘤)、淋巴瘤、小細(xì)胞性惡性黑色素瘤以及嗅母細(xì)胞瘤等[10]。在病理醫(yī)師的日常臨床診斷實(shí)踐中,不同類型的鼻腔鼻竇小藍(lán)圓細(xì)胞惡性腫瘤鑒別困難;病理醫(yī)師通常需依賴多組免疫組化標(biāo)志物檢測(cè),必要時(shí)尚需借助分子遺傳學(xué)檢測(cè)手段才能確診。
鑒別診斷:(1)小細(xì)胞神經(jīng)內(nèi)分泌癌,部分鼻腔鼻竇的ARMS可以表達(dá)細(xì)胞角蛋白或神經(jīng)內(nèi)分泌標(biāo)志物,且表達(dá)模式與小細(xì)胞神經(jīng)內(nèi)分泌癌相同,細(xì)胞角蛋白呈核旁點(diǎn)狀高爾基體區(qū)陽性,易誤診[4,11]。在鼻腔鼻竇小圓細(xì)胞腫瘤的診斷過程中,病理醫(yī)師通常采用上皮、淋巴、神經(jīng)內(nèi)分泌、惡性黑色素瘤的免疫組化標(biāo)記進(jìn)行診斷,由于多數(shù)SNT-ARMS患者年齡偏大使病理醫(yī)師對(duì)橫紋肌肉瘤的診斷放松警惕,當(dāng)腫瘤細(xì)胞上皮和(或)神經(jīng)內(nèi)分泌標(biāo)志物表達(dá)時(shí)易診斷為癌。因此,筆者建議在鼻腔鼻竇部位查見小藍(lán)圓細(xì)胞腫瘤時(shí),應(yīng)進(jìn)行橫紋肌分化的免疫組化標(biāo)志物進(jìn)行診斷,包括desmin、MyoD1和Myogenin,后兩者均為胞核表達(dá),且更有特異性[12]。(2)SNT-ARMS常會(huì)出現(xiàn)區(qū)域或全身淋巴結(jié)的轉(zhuǎn)移,有時(shí)還會(huì)以淋巴結(jié)腫大為首發(fā)癥狀。部分ARMS還可表達(dá)ALK蛋白[13],易誤診為間變大細(xì)胞淋巴瘤,診斷時(shí)需考慮淋巴結(jié)內(nèi)ARMS存在的可能性,輔以相應(yīng)的橫紋肌標(biāo)志物可以確診。此外,ARMS不表達(dá)CD30,其雖表達(dá)ALK蛋白,但并不具有ALK基因的易位[14],與間變大細(xì)胞淋巴瘤不同。(3)胚胎性橫紋肌肉瘤(embryonal rhabdomyosarcoma, ERMS):鼻腔鼻竇也是ERMS包括其特殊亞型葡萄簇肉瘤的好發(fā)部位[15],實(shí)體亞型的ARMS易與ERMS混淆[16]。ERMS組織學(xué)的異質(zhì)性更為顯著,腫瘤細(xì)胞除表現(xiàn)為圓形外,還可呈梭形、星狀或卵圓形,間質(zhì)常出現(xiàn)黏液變性,橫紋肌母細(xì)胞分化更為顯著。此外,ARMS與ERMS的橫紋肌母細(xì)胞多呈條帶狀、蝌蚪樣不同,其橫紋肌母細(xì)胞多為圓形,胞質(zhì)內(nèi)橫紋少見;出現(xiàn)花環(huán)狀多核巨細(xì)胞高度提示為ARMS。免疫表型:雖然兩種均表達(dá)橫紋肌標(biāo)志物,但ARMS通常表現(xiàn)為Myogenin胞核的彌漫強(qiáng)表達(dá),而ERMS則表現(xiàn)為Myogenin強(qiáng)弱不等的表達(dá)[12]。對(duì)于鑒別較為困難的病例,F(xiàn)OXO1融合基因的檢測(cè)可以明確區(qū)分。對(duì)于部分罕見的病例兼有ERMS和ARMS成分,此類腫瘤的本質(zhì)尚存爭(zhēng)議,但它們通常不具有ARMS特有的分子遺傳學(xué)改變,且生物學(xué)行為更接近于ERMS[17-18]。
分子遺傳學(xué):ARMS具有特征性的染色體易位t(2;13)(q35;q14),產(chǎn)生PAX3-FOXO1融合基因[18-19],少數(shù)病例(約10%)為PAX7-FOXO1融合基因。不同的融合基因類型具有預(yù)后意義,伴PAX7-FOXO1的病例通常比PAX3-FOXO1者預(yù)后好[19]。PAX3-FOXO1融合基因并非為ARMS所特有,最近文獻(xiàn)報(bào)道鼻腔鼻竇雙表型肉瘤(biphenotypic sinonasal sarcoma, BSNS)少數(shù)病例也可以涉及相同的融合基因,有部分BSNS病例甚至可以伴橫紋肌的分化,導(dǎo)致兩者混淆[20-21]。兩者的組織形態(tài)學(xué)差異明顯,BSNS屬于低級(jí)別的單形性梭形細(xì)胞肉瘤,特征性的表達(dá)SMA和S-100蛋白。上述結(jié)果提示分子遺傳學(xué)檢測(cè)可以為軟組織腫瘤的診斷提供幫助,但評(píng)判時(shí)需結(jié)合腫瘤的鏡下形態(tài)學(xué)特征綜合考慮。
預(yù)后與治療:臨床顯示ARMS比ERMS預(yù)后差,成年患者比兒童及年輕人預(yù)后差,而發(fā)生于鼻腔鼻竇者比發(fā)生于四肢軟組織或頭頸部其他部位者預(yù)后差[4-5,15]。本組10例患者中有8例獲得隨訪,其中6例患者死亡,中位生存期13個(gè)月。手術(shù)聯(lián)合化療和(或)放療的綜合性治療是首選的治療方案,早期患者提倡手術(shù)切除后結(jié)合放、化療;局部晚期患者可考慮先誘導(dǎo)化療或放療,待腫塊縮小后再行手術(shù),以提高腫瘤完整切除的機(jī)會(huì)[22]。有遠(yuǎn)處轉(zhuǎn)移的橫紋肌肉瘤者預(yù)后不佳,但最新針對(duì)晚期ARMS治療的研究表明,先通過大劑量的放療合并化療控制原發(fā)灶和轉(zhuǎn)移灶,再給患者行移植同種異體來源的造血干細(xì)胞,可以使部分患者即使是臨床Ⅳ期的患者也能獲益,患者可保持腫瘤無復(fù)發(fā)狀態(tài)達(dá)1年以上[23]。

