3-碘甲狀腺原氨酸的受體、通路及藥理學效應研究進展
莫麗莉 鄒常超 徐啟麗 韋波 李偉 曾安寧 陳章榮 劉興德 周海燕
中圖分類號 R96 文獻標志碼 A 文章編號 1001-0408(2022)02-0244-07
DOI 10.6039/j.issn.1001-0408.2022.02.20
摘 要 3-碘甲狀腺原氨酸是甲狀腺激素的內源性衍生物,也可作為外源性藥物使用,可發揮減少心輸出量、冠脈流量,減慢心率,促進脂肪分解,降低基礎代謝,改善學習及記憶能力等藥理學效應。其對代謝的調節作用與甲狀腺素類似,而對心臟的調節作用及產熱功能則與其相反。3-碘甲狀腺原氨酸作為一種新型化學信使,可通過多種受體及信號通路發揮不同的藥理學效應。本文就外源性3-碘甲狀腺原氨酸發揮的多種藥理學效應及其機制的研究進展作一綜述,以期為心血管、代謝性疾病及神經系統疾病提供新的治療藥物。
關鍵詞 3-碘甲狀腺原氨酸;受體;信號通路;藥理學效應
Research progress of receptor, pathway and pharmacological effect of 3-iodothyronamine
MO Lili1,2,ZOU Changchao3,XU Qili1,2,WEI Bo1,LI Wei1,2,ZENG Anning4,CHEN Zhangrong1,LIU Xingde3, ZHOU Haiyan1,2(1. Dept. of Cardiology, the Affiliated Hospital of Guizhou Medical University, Guiyang 550004, China; 2. School of Clinical Medicine, Guizhou Medical University, Guiyang 550004, China; 3. Dept. of Cardiology, the Second Affiliated Hospital of Guizhou University of Traditional Chinese Medicine, Guiyang 550004, China; 4. Dept. of Cardiology, Qiannan Buyi and Miao Autonomous Prefecture People’s Hospital, Guizhou Duyun 558000, China)
ABSTRACT ? 3-iodothyronamine (T1AM) is an endogenous derivative of thyroid hormone. It can also be used as exogenous drug. It can play pharmacological effects such as reducing cardiac output and coronary flow, slowing heart rate, promoting lipolysis, reducing basic metabolism and improving learning and memory ability. Its regulatory effect on metabolism is similar to that of thyroxine, but regulatory effect on heart and thermogenic function is opposite to that of thyroxine. As a new chemical messenger, T1AM can exert different pharmacological effects through a variety of receptors and signal pathways. This review summarizes the research progress of various pharmacological effects and mechanisms of exogenous T1AM, in order to provide new therapeutic drugs of cardiovascular, metabolic diseases and nervous system diseases.
KEYWORDS ? 3-iodothyronamine; receptor; signal pathway; pharmacological effect
3-碘甲狀腺原氨酸(3-iodothyronamine,T1AM)是甲狀腺激素通過脫羧、脫碘形成的衍生物,其結構與甲狀腺激素相似,但部分功能卻與甲狀腺激素相反。2004年,Scanlan等[1]首次在人和嚙齒動物體內檢出T1AM,并發現該成分能夠在極短時間內降低體溫、減少心輸出量、減慢心率,是G蛋白偶聯痕量胺相關受體1(trace amine associated receptor-1,TAAR1)的有效激動劑。近年來,隨著T1AM相關研究的增多,學者們還發現其可作為一種新型化學信使,在內分泌系統、神經系統等發揮降低代謝、改善記憶等不同藥理學效應,但其具體作用機制不明[2-13]。已有研究表明,外源性T1AM不與甲狀腺激素受體相互作用,而是通過與其他受體[如β-腎上腺素受體(β-adrenergic receptor,ADRB)、5-羥色胺受體1B(5-serotonin receptor 1B,5-HTR1B)等]作用或與質膜中的相關位點[如沉默信息調節因子6(sirtuin 6,SIRT6)、SIRT4等]結合,以非基因學機制來發揮藥理學效應[5,14-20]。目前,T1AM的臨床研究有限,多數研究是在動物和細胞水平上針對外源性T1AM開展的,以探討其藥理學效應及作用機制。基于此,為總結T1AM的研究現狀,本文在介紹T1AM結構、功能、生物合成途徑的基礎上,對其作用受體、通路及藥理學效應進行綜述,以期為心血管、代謝性疾病及神經系統疾病提供新的治療藥物。
1 T1AM的結構、功能及生物合成途徑
在結構上,T1AM與甲狀腺激素有相同的碳骨架,而T1AM不存在含羧酸基團的丙氨酸側鏈,僅在芳環上保留了1個碘原子[21]。在功能上,外源性T1AM的一些藥理學效應(如調節心臟功能、產熱等)與3,5,3′-三碘甲狀腺原氨酸(3,5,3′-triiodothyronine,T3)或甲狀腺功能亢進相反,而其他作用(如代謝調節)則為協同。由于T1AM的結構與甲狀腺激素類似,學者們最初推測T1AM產生于甲狀腺:首先,甲狀腺激素借助碘化鈉同向轉運蛋白和甲狀腺過氧化物酶,經脫羧和脫碘反應合成衍生物;隨后,該衍生物通過芳香族L-氨基酸脫羧酶介導而合成T1AM[22]。但最近一項研究證明,功能性L-氨基酸脫羧酶缺失的患者體內血清T1AM水平正常[23]。上述研究提示,T1AM在合成過程中很有可能不需要借助L-氨基酸脫羧酶。此外,學者們還發現,與甲狀腺素一起孵育的大鼠甲狀腺細胞FRTL-5不能產生T1AM[24];而在與T3一起孵育的大鼠心肌細胞H9c2中檢出了T1AM[25]。學者們在臨床工作中發現,接受甲狀腺切除和放射性碘治療的患者的血清T1AM水平高于健康個體,推測T1AM可能是在甲狀腺外由甲狀腺素代謝物產生的[26]。一項利用甲狀腺切除小鼠的實驗證實,T1AM可在腸道中合成:腸道中的甲狀腺素經鳥氨酸脫羧酶和3種脫碘酶亞型介導、催化,從而合成T1AM[27]。然而,該實驗的給藥方式是腹腔注射,而甲狀腺切除后患者接收替代治療的方式是口服,兩者給藥途徑不同,所以該實驗的結論存在一定爭議,但其仍能在一定程度上證實T1AM是在甲狀腺以外的器官中合成的。
2 外源性T1AM的作用受體、通路及其藥理學效應
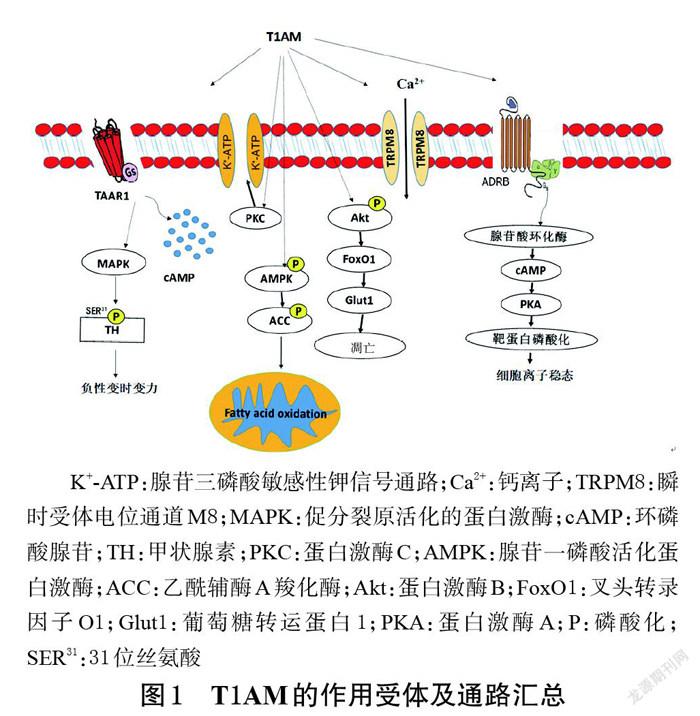
T1AM主要分布于嚙齒動物體內,包括血清、大腦、心、肝、腎、胃、肺及骨骼肌,且其在組織中的分布濃度遠高于在血清中的濃度[25];同時,T1AM也分布于人類的血液、大腦中[25]。為探究其作用機制及成藥性,學者們通過給予外源性T1AM在細胞及動物水平上開展了相關研究。T1AM的作用受體及通路匯總見圖1。
2.1 T1AM作用于G蛋白偶聯受體影響心臟、神經細胞和細胞離子穩態
G蛋白偶聯受體是T1AM的作用靶點之一,也是細胞信號轉導領域一類重要的蛋白質分子,可對生物體的生長發育、生殖、攝食、代謝以及行為等起到調控作用[28-30]。T1AM可直接作用于G蛋白偶聯受體中的TAAR1和ADRB[31-35]。
2.1.1 T1AM作用于TAAR1產生心臟負性變時、變力作用 TAAR有9種不同的亞型,在多種組織中廣泛表達,其中TAAR1是單胺類神經遞質傳遞的重要調節器,因其具有調節單胺類神經遞質傳遞的作用,其激動劑在心血管、神經系統等疾病治療領域中有一定的潛力[35]。由于T1AM與TAAR1的高親和力,學者們初始認為T1AM僅通過作用于TAAR1來介導小鼠體溫下降[5]。但隨后學者們通過TAAR1基因敲除小鼠證實,在給予T1AM后,TAAR1基因敲除小鼠的體溫仍會下降,表明T1AM對小鼠體溫的調節還可通過作用于其他受體來實現[1]。另有利用C57BL/6J小鼠及Wistar大鼠的研究表明,T1AM可通過激活TAAR1或其他TAAR亞型來減少心輸出量、主動脈壓、冠脈流量,并可劑量依賴性地減慢心率[1,36-38]。在成年雄性C57BL/6J小鼠實驗中,給予T1AM后,小鼠心率立即下降,并于持續6~8 h后逐漸恢復正常[1]。在離體大鼠心臟灌流實驗中,20~38 μmol/L的T1AM可使大鼠心輸出量立即降低,其中38 μmol/L的T1AM可使大鼠10 min內的心輸出量較對照組降低63%、心率降低50%,且20 μmol/L及以下劑量的T1AM不會造成大鼠心動過緩[1]。學者們在Wistar大鼠Langendorff離體心臟灌流實驗中發現,T1AM能夠引起大鼠心輸出量、主動脈壓、冠脈流量和心率下降,并且上述作用具有劑量依賴性;該研究結果還提示,T1AM可能是通過激活TAAR1來介導這一心臟效應[37]。有一項針對慢性心力衰竭患者的臨床研究結果顯示,其血清T1AM水平明顯增高,且增高水平與左室射血分數降低相關,提示T1AM對心臟有直接的負向調節作用[39]。
2.1.2 T1AM作用于TAAR1受體產生神經細胞保護作用 有研究顯示,TAAR1受體與多種神經系統疾病有關,如T1AM與TAAR1受體的結合,可有助于改善小鼠的學習記憶能力[2,40]。阿爾茨海默病的發病機制有多種假說,大腦內嗅皮層中β淀粉樣蛋白異常聚集是其中的一種假說,該蛋白的異常聚集可抑制海馬區長時程增強,使學習記憶能力受損[41]。在一項使用野生型小鼠和阿爾茨海默病模型小鼠內嗅皮層切片進行的電生理實驗中,學者們分別或聯合灌注了β淀粉樣蛋白、T1AM、TAAR1激動劑RO5166017、TAAR1拮抗劑EPPTB,結果顯示,T1AM恢復了模型小鼠內嗅皮層的長時程增強,TAAR1拮抗劑EPPTB消除了T1AM的上述作用,而TAAR1激動劑RO5166017則模擬了T1AM的上述效應,表明T1AM可通過激活TAAR1而阻止β淀粉樣蛋白異常聚集所誘導的神經細胞功能障礙[2]。此外,由于T1AM結構與T3相似,T3可以透過血腦和脊髓屏障,提示T1AM也可能會透過血腦和脊髓屏障而進入腦脊液和神經組織。有研究證實,T1AM可作用于TAAR1以減少脊髓神經細胞凋亡,減輕脊髓損傷[40]。由于此前有研究表明,T1AM對甲狀腺激素受體沒有作用[37],但對TAAR1有較高的親和力和激活作用,因此推測線粒體介導的凋亡是TAAR1下游的一種潛在機制。一項以脊髓損傷模型大鼠為對象的研究顯示,T1AM組脊髓損傷模型大鼠的運動功能評分顯著高于對照組和T1AM+TAAR1拮抗劑組(P<0.05),提示T1AM對神經功能具有一定的保護作用,有利于脊髓損傷后大鼠運動功能的恢復;同時,TAAR1拮抗劑組大鼠的運動功能與對照組相似,說明T1AM的上述作用可能是通過TAAR1來介導的。該研究還通過TUNEL實驗證實了T1AM參與并減少了神經細胞的凋亡[40]。綜上所述,T1AM可以通過介導TAAR1而減少神經細胞凋亡,從而保護神經細胞,促進神經功能的恢復。
2.1.3 T1AM作用于ADRB增加細胞內Ca2+內流,調節細胞離子穩態 ADRB是T1AM的另一受體,T1AM可通過ADRB2增加人結膜上皮細胞IOBA-NHC中Ca2+的內流,從而調節細胞離子穩態[42]。Dinter等[42]通過過表達ADRB的人胚胎腎細胞HEK293證實,異丙腎上腺素可通過作用于ADRB而激活興奮性G蛋白的信號轉導,使得cAMP積累增加;在異丙腎上腺素基礎上加用低濃度(10-8~10-7 mol/L)的T1AM,可明顯增強ADRB2介導的興奮性G蛋白信號轉導和cAMP積累效應,而對ADRB1介導的興奮性G蛋白信號轉導無影響;此外,在異丙腎上腺素基礎上加用高濃度(10-5~10-4 mol/L)的T1AM,其cAMP積累效應強于單用異丙腎上腺素,但弱于異丙腎上腺素加用低濃度T1AM,該現象可能與高濃度T1AM激活了抑制性G蛋白信號轉導有關。另有研究發現,T1AM可增加人結膜上皮細胞IOBA-NHC中的Ca2+內流,非選擇性ADRB拮抗劑噻嗎洛爾既可以阻斷去甲腎上腺素引起的Ca2+內流,同時又可以逆轉T1AM引起的Ca2+內流,提示T1AM可能是通過作用于ADRB2使細胞內Ca2+內流增加,從而調節細胞離子穩態[42]。
2.2 T1AM作用于瞬時受體電位通道調節細胞離子穩態,減少炎癥介質釋放
瞬時受體電位通道是一類跨膜非選擇性陽離子通道,包括28個成員。TRPM8和瞬時受體電位香草酸亞型1(transient receptor potential vanilloid 1,TRPV1)均對溫度敏感,其中TRPM8可在低于28 ℃時被激活,TRPV1則可在高于43 ℃時被激活[43-45]。有研究指出,T1AM可通過激活TRPM8來增加人結膜上皮細胞IOBA-NHC中的Ca2+內流;此外,其還可抑制TRPV1激動劑辣椒素引起的Ca2+內流和白細胞介素6釋放,在調節細胞離子穩態的同時減少炎癥介質的釋放[44]。Khajavi等[46]通過IOBA-NHC細胞實驗證實,在適度降溫和給予TRPM8激動劑icilin的條件下,T1AM可增加IOBA-NHC細胞的Ca2+內流,而TRPM8阻滯劑BCTC可阻斷這種作用。T1AM可模擬TRPM8激動劑icilin的作用,引起細胞Ca2+內流的增加;此外,TRPM8阻滯劑BCTC可逆轉T1AM引起的Ca2+內流[45]。該細胞實驗證實,在適度降溫的條件下,T1AM可激活TRPM8,從而增加Ca2+內流,并調節細胞離子穩態;T1AM可逆轉TRPV1激動劑辣椒素引起的Ca2+內流,抑制TRPV1激活所引起的白細胞介素6釋放;T1AM可模擬TRPV1特異性受體拮抗劑辣椒平的阻斷作用,提示T1AM可能是通過抑制TRPV1信號通路導致白細胞介素6釋放減少。
2.3 T1AM作用于5-HTR1B調節體溫
5-HTR1B主要通過調節5-羥色胺等神經遞質的釋放進而影響神經細胞的興奮性,其主要分布在紋狀體,其次在下丘腦、黑質、垂體等部位。5-HTR1B和TAAR1可作為體溫調節信號在下丘腦共表達,前者主要參與抑郁樣行為和厭食癥的發生[47]。由于5-HTR1B和TAAR1的表達譜重疊,而T1AM可激活TAAR1受體,因此Br?unig等[48]利用5-HTR1B過表達人胚胎腎細胞HEK293進行實驗探討T1AM是否可以激活5-HTR1B,結果提示,T1AM可通過激活5-HTR1B,偶聯抑制性G蛋白,從而使細胞內cAMP積累減少。然而,該學者利用5-HTR1B和TAAR1同時過表達的人胚胎腎細胞HEK293進行研究發現,T1AM僅通過激活TAAR1而偶聯興奮性G蛋白,但不激活5-HTR1B,這可能是因為T1AM與TAAR1有更高的親和力。因此,Br?unig等[48]推測,在給予TAAR1基因敲除小鼠T1AM后,小鼠的體溫仍會下降,這可能是T1AM作用于5-HTR1B所產生的體溫調節作用。
2.4 T1AM與毒蕈堿受體結合減少膀胱收縮
毒蕈堿受體廣泛存在于副交感神經節后纖維支配的效應器細胞上,分為5個亞型。毒蕈堿受體在中樞神經系統中表達,在記憶和疼痛回路中起主要作用,在外周參與平滑肌收縮、外分泌腺和內分泌腺分泌等生物學過程。有學者利用毒蕈堿受體過表達的中國倉鼠卵巢細胞CHO進行研究發現,T1AM可以抑制毒蕈堿受體激動劑碳酰膽堿誘導的大鼠膀胱收縮,提示T1AM是毒蕈堿受體弱的、非選擇性的拮抗劑[49]。
2.5 T1AM通過FoxO1信號通路減少心肌缺血再灌注損傷并誘導肌細胞萎縮
2.5.1 T1AM通過Akt/FoxO1信號通路減少心肌缺血再灌注損傷 心肌缺血再灌注損傷是缺血性心臟病溶栓或者介入治療后,影響臨床治療效果的重要因素[50]。在心肌缺血再灌注損傷過程中,T1AM可通過Akt/FoxO1信號通路來調控心肌細胞代謝,從而減少其凋亡,最終起到保護心肌的作用。本課題組前期研究首先建立了缺氧/復氧誘導的人心肌細胞AC-16損傷模型,發現低濃度的T1AM可提高損傷心肌細胞的活力,顯著降低損傷心肌細胞的耗氧率和凋亡率;其次,通過轉錄組學測序技術檢測T1AM對缺氧/復氧損傷心肌細胞轉錄組的影響,發現差異基因可富集到FoxO1信號通路上[7];最后,通過實時定量聚合酶鏈反應技術和免疫印跡法檢測FoxO1、Akt、Glut1、Bcl-2、Bax基因和Akt/FoxO1信號通路相關蛋白的表達水平,證實T1AM可以通過上述信號通路使AC-16細胞代謝降低,從而減少其凋亡[51],為心肌缺血再灌注損傷的治療提供了新的思路。
2.5.2 T1AM通過FoxO1信號通路誘導肌細胞萎縮 當細胞的分解代謝多于合成代謝時,會誘發肌肉萎縮[52]。Ju等[53]以小鼠肌細胞C2C12為研究對象進行實驗發現,經T1AM處理后,C2C12細胞直徑減小,去除T1AM 9 h后,C2C12細胞直徑基本恢復正常;免疫印跡實驗結果提示,經T1AM處理后,C2C12細胞合成代謝減少[磷酸化Akt1/Akt1、磷酸化雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)/mTOR、磷酸化核糖體蛋白S6激酶(ribosomal protein S6 kinase,S6K)/S6K降低了44%~56%,熱休克蛋白27和αB-晶體蛋白的表達水平分別降低了26%和47%],分解代謝增強(FoxO1蛋白表達水平增加了2.0倍,磷酸化FoxO1/FoxO1降低了65%;磷酸化FoxO3蛋白表達水平降低了42%,磷酸化FoxO3/FoxO3降低了39%)。綜合上述實驗結果分析,T1AM可通過激活FoxO1信號來增加分解代謝,抑制Akt/S6K信號通路介導的合成代謝,從而引起肌細胞萎縮,該機制為T1AM在肌肉肥大患者的治療應用奠定了理論基礎。
2.6 T1AM通過PKC/K+-ATP通道調節線粒體滲透性從而減輕心肌缺血再灌注損傷
Sabina等[16]以雄性Wistar大鼠為研究對象,建立心肌缺血再灌注模型進行實驗,發現低濃度T1AM可縮小缺血再灌注損傷模型大鼠的心臟梗死面積,且不影響其血流動力學參數,但高濃度T1AM無此效果;此外,PKC抑制劑白屈菜紅堿和K+-ATP通道阻滯劑格列本脲可消除T1AM介導的心臟保護作用。由此該研究團隊推測,T1AM可通過PKC/K+-ATP通道來調節線粒體的滲透性,從而減輕心肌缺血再灌注損傷,上述結果與本課題組前期研究結果一致[7]。
2.7 T1AM通過AMPK信號通路促進脂肪(細胞)分解
2.7.1 T1AM通過AMPK/ACC信號通路促進脂肪分解 Rogowski等[54]以小鼠胚胎成纖維細胞3T3-L1和人肝癌細胞HepG2為研究對象進行實驗,發現3T3-L1細胞經T1AM處理后脂質沉積減少,HepG2細胞經T1AM處理后脂肪分解增加,同時AMPK和ACC蛋白的磷酸化水平有所升高,推測細胞脂肪分解作用可能與該化合物激活AMPK/ACC信號通路而引起脂肪代謝變化有關。此外,另一項研究利用小鼠肌細胞C2C12進行實驗,結果提示,T1AM可明顯減低C2C12細胞耗氧量,通過增加腺苷一磷酸/腺苷三磷酸比例,激活AMPK磷酸化,使肉堿棕櫚酰轉移酶和丙酮酸脫氫酶激酶表達上調,ACC和丙酮酸脫氫酶磷酸酶表達下調,從而引起脂肪動員[55]。由此可見,T1AM可通過激活AMPK/ACC信號通路來促進脂肪分解,并減少細胞脂質沉積。
2.7.2 T1AM通過AMPK/FoxO1/脂肪甘油三酯脂肪酶/單酰基甘油脂肪酶信號通路分解脂肪細胞 肥胖是脂肪細胞在白色脂肪中的聚集。Kim等[56]通過誘導小鼠胚胎成纖維細胞3T3-L1脂滴積累,研究T1AM分解脂肪的機制,結果發現,T1AM可通過激活AMPK/FoxO1/脂肪甘油三酯脂肪酶/單酰基甘油脂肪酶信號通路將甘油三酯分解為游離脂肪酸和甘油,這種作用可以被脂肪甘油三酯脂肪酶抑制劑ATGListatin顯著抑制;此外,T1AM還可通過AMPK/ACC/肉毒堿棕櫚酰轉移酶1信號通路來促進游離脂肪酸進入線粒體并發生β氧化,從而提供能量。
2.8 T1AM作用于SIRT影響體質量、神經細胞
2.8.1 T1AM通過SIRT減輕體質量 SIRT是一類具有多種代謝調節酶活性的蛋白家族,共有7個家族成員[57-58]。其中,SIRT6在維持糖脂代謝穩態中起著重要作用,可減少糖酵解和甘油三酯合成[1,35];SIRT4是一種線粒體沉默調節蛋白,也是線粒體代謝的負調節因子,抑制SIRT4可增強肝臟和肌肉細胞的線粒體功能并加速脂肪酸氧化[37]。Assadi-porter等[59]研究發現,按10 mg/(kg·d)的劑量給予小鼠T1AM,7 d后其體質量較對照組下降10%;按25 mg/(kg·d)的劑量給予小鼠T1AM,7 d后其體質量較對照組下降18%;此外,與對照組比較,T1AM組小鼠體內的代謝物(乳酸、丙氨酸、琥珀酸等)含量、相關蛋白(SIRT6、SIRT4、葡萄糖激酶)表達及血清膽固醇水平等均有較大差異,且T1AM對初級代謝(尤其是氨基酸、脂質、碳水化合物及糖核苷酸代謝等)的影響尤為明顯;與此同時,相關基因轉錄和蛋白表達的檢測結果表明,T1AM可通過上調SIRT6表達、下調SIRT4表達來重新編碼脂肪酸和葡萄糖的代謝,從而使小鼠體質量下降。由此可見,T1AM可通過調控SIRT的表達來減輕實驗動物的體質量。
2.8.2 T1AM通過調控SIRT保護神經細胞 T1AM對神經退行性病變具有保護作用,可改善學習和記憶能力,除了作用于TAAR1這一靶點外,還可以通過上調SIRT6的表達來激活自噬,從而發揮對神經細胞的保護作用[3]。神經退行性病變的共同病理改變是錯誤折疊蛋白的聚集,有研究表明,T1AM可通過上調SIRT6表達,抑制mTOR磷酸化,誘導人膠質母細胞瘤細胞的自噬,降解異常蛋白,減少錯誤折疊蛋白的聚集,從而達到保護神經細胞的目的。
2.9 T1AM通過磷脂酰肌醇3激酶/Akt/mTOR信號通路誘導自噬,保護神經細胞
自噬是一種由細胞溶酶體介導的復雜生物學行為,其通過溶酶體降解來消除錯誤折疊蛋白、蛋白復合物或細胞器,是維持細胞穩態所必需的生理過程。自噬與阿爾茨海默病、帕金森病以及創傷和缺血性腦損傷后遺癥等神經退行性疾病的發生發展密切相關[60]。由此可見,誘導自噬可成為治療神經系統疾病的一種方法。為了探究T1AM在自噬過程中的作用,Bellusci等[3]以人膠質母細胞瘤細胞U-87MG為研究對象,以1 μmol/L的T1AM分別干預0.5、4、8、24 h,以觀察細胞自噬通量的改變。透射電鏡結果顯示,T1AM誘導U-87MG細胞產生自噬,且有時間依賴性;免疫熒光結果顯示,T1AM干預8 h后,細胞內自噬標志物微管相關蛋白1輕鏈3斑點形成明顯;免疫印跡實驗結果顯示,T1AM能夠顯著誘導U-87MG細胞中微管相關蛋白1輕鏈3-Ⅱ表達上調,自噬蛋白p62和磷酸化Akt表達下調[3]。磷脂酰肌醇3激酶/Akt/mTOR通路是調節自噬的重要通路,降低磷酸化Akt的表達,可抑制mTOR的活性,故上述研究團隊推測,T1AM可通過抑制Akt的激活來降低mTOR的活性,從而促進細胞自噬。綜上所述,T1AM可通過抑制磷脂酰肌醇3激酶/Akt/mTOR信號通路來誘導U-87MG細胞產生自噬,從而發揮神經保護作用,該化合物有可能成為神經退行性疾病的有效治療藥物。
3 結語
外源性T1AM作用于不同受體、通路發揮不同藥理學效應:在心血管系統,其可降低心輸出量、主動脈壓、冠脈流量、心率;在內分泌系統,其可促進脂肪分解、降低基礎代謝[11,13];在神經系統,其可改善學習及記憶能力。因其在極短時間內可發揮藥理學效應[1],故該物質可為今后心血管、神經、內分泌系統疾病等的治療提供新方向。盡管如此,目前關于T1AM的認識還是不足,主要表現為以下幾個方面:(1)T1AM在機體中的合成位點、合成途徑、失活形式尚未完全清楚;(2)T1AM可作用于多個受體,不僅可與TAAR1或TAAR其他亞型相互作用,還可與非G蛋白偶聯受體相互作用,但其作用模式仍存在爭議;(3)外源性T1AM的作用效果與濃度相關,其有效濃度的選擇也將是其臨床應用的巨大挑戰之一。
參考文獻
[ 1 ] SCANLAN T S,SUCHLAND K L,HART M E,et al. 3-iodothyronamine is an endogenous and rapid-acting derivative of thyroid hormone[J]. Nat Med,2004,10(6):638-642.
[ 2 ] ACCORRONI A,RUTIGLIANO G,SABATINI M,et al. Exogenous 3-iodothyronamine rescues the entorhinal cortex from β-amyloid toxicity[J]. Thyroid,2020,30(1):147-160.
[ 3 ] BELLUSCI L,RUNFOLA M,CARNICELLI V,et al. Endogenous 3-iodothyronamine(T1AM)and synthetic thyronamine-like analog SG-2 act as novel pleiotropic neuroprotective agents through the modulation of SIRT6[J]. Molecules,2020,25(5):E1054.
[ 4 ] FLIERS E,KLIEVERIK L P,KALSBEEK A. Novel neural pathways for metabolic effects of thyroid hormone[J]. Trends Endocrinol Metab,2010,21(4):230-236.
[ 5 ] BIEBERMANN H,KLEINAU G. 3-iodothyronamine induces diverse signaling effects at different aminergic and non-aminergic G-protein coupled receptors[J]. Exp Clin Endocrinol Diabetes,2020,128(6/7):395-400.
[ 6 ] HA K,SHIN H,JU H,et al. Behavioral hypothermia of a domesticated lizard under treatment of the hypometabolic agent 3-iodothyronamine[J]. Exp Anim,2017,66(2):99-105.
[ 7 ] ZHOU H Y,HU B L,ZHANG B,et al. Comparative tran- scriptome analysis reveals the potential cardiovascular protective targets of the thyroid hormone metabolite 3-iodothyronamine(3-T1AM)[J]. Biomed Res Int,2020,2020:1302453.
[ 8 ] GENCARELLI M,LAURINO A,LANDUCCI E,et al. 3-iodothyronamine affects thermogenic substrates’mobilization in brown adipocytes[J]. Biology(Basel),2020,9(5):E95.
[ 9 ] MITTAG J. More than fever-novel concepts in the regulation of body temperature by thyroid hormones[J]. Exp Clin Endocrinol Diabetes,2020,128(6/7):428-431.
[10] ZUCCHI R,RUTIGLIANO G,SAPONARO F. Novel thyroid hormones[J]. Endocrine,2019,66(1):95-104.
[11] K?HRLE J. The colorful diversity of thyroid hormone metabolites[J]. Eur Thyroid J,2019,8(3):115-129.
[12] LANDUCCI E,GENCARELLI M,MAZZANTINI C,et al. N-(3-Ethoxy-phenyl)-4-pyrrolidin-1-yl-3-trifluoromethyl-benzamide(EPPTB)prevents 3-iodothyronamine(T1AM)-induced neuroprotection against kainic acid ?toxicity[J]. Neurochem Int,2019,129:104460.
[13] LOUZADA R A,CARVALHO D P. Similarities and diffe- rences in the peripheral actions of thyroid hormones and their metabolites[J]. Front Endocrinol(Lausanne),2018,9:394.
[14] PIEHL S,HOEFIG C S,SCANLAN T S,et al. Thyrona- mines:past,present,and future[J]. Endocr Rev,2011,32(1):64-80.
[15] CUMERO S,FOGOLARI F,DOMENIS R,et al. Mitochondrial F(0)F(1)-ATP synthase is a molecular target of 3-iodothyronamine,an endogenous metabolite of thyroid hormone[J]. Br J Pharmacol,2012,166(8):2331-2347.
[16] FRASCARELLI S,GHELARDONI S,CHIELLINI G,et al. Cardioprotective effect of 3-iodothyronamine in perfused rat heart subjected to ischemia and reperfusion[J]. Cardiovasc Drugs Ther,2011,25(4):307-313.
[17] ZUCCHI R,ACCORRONI A,CHIELLINI G. Update on 3-iodothyronamine and its neurological and metabolic actions[J]. Front Physiol,2014,5:402.
[18] SACRIPANTI G,LORENZINI L,BANDINI L,et al. 3-iodothyronamine and 3,5,3′-triiodo-L-thyronine reduce SIRT1 protein expression in the HepG2 cell line[J/OL]. Horm Mol Biol Clin Investig,2020,41(1):20190045[2021-06-28]. https://doi.org/10.1515/hmbci-2019-0045.
[19] K?HRLE J,BIEBERMANN H. 3-iodothyronamine:a thyroid hormone metabolite with distinct target profiles and mode of action[J]. Endocr Rev,2019,40(2):602-630.
[20] LAURINO A,LANDUCCI E,RAIMONDI L. Central effects of 3-iodothyronamine reveal a novel role for mitochondrial monoamine oxidases[J]. Front Endocrinol(Lau- sanne),2018,9:290.
[21] PIEHL S,HEBERER T,BALIZS G,et al. Thyronamines are isozyme-specific substrates of deiodinases[J]. Endocrinology,2008,149(6):3037-3045.
[22] ACCORRONI A,SAPONARO F,ZUCCHI R. Tissue thyroid hormones and thyronamines[J]. Heart Fail Rev,2016,21(4):373-390.
[23] HACKENMUELLER S A,MARCHINI M,SABA A,et al. Biosynthesis of 3-iodothyronamine(T1AM)is dependent on the sodium-iodide symporter and thyroperoxidase but does not involve extrathyroidal metabolism of T4[J]. Endocrinology,2012,153(11):5659-5667.
[24] AGRETTI P,DE MARCO G,RUSSO L,et al. 3-iodothyronamine metabolism and functional effects in FRTL5 thyroid cells[J]. J Mol Endocrinol,2011,47(1):23-32.
[25] SABA A,CHIELLINI G,FRASCARELLI S,et al. Tissue distribution and cardiac metabolism of 3-iodothyronamine[J]. Endocrinology,2010,151(10):5063-5073.
[26] HOEFIG C S,K?HRLE J,BRABANT G,et al. Evidence for extrathyroidal formation of 3-iodothyronamine in humans as provided by a novel monoclonal antibody-based chemiluminescent serum immunoassay[J]. J Clin Endocrinol Metab,2011,96(6):1864-1872.
[27] HOEFIG C S,WUENSCH T,RIJNTJES E,et al. Biosynthesis of 3-iodothyronamine from T4 in murine intestinal tissue[J]. Endocrinology,2015,156(11):4356-4364.
[28] 趙強,吳鐳,李佳,等.重大疾病導向的G蛋白偶聯受體研究[J].中國基礎科學,2015,17(3):3-8,25.
[29] 李聰慧,崔詩遙,顧燕燕,等. G蛋白偶聯受體的研究進展[J].蠶桑通報,2019,50(2):4-7,15.
[30] LI X Y,XIE L,QU X L,et al. GPR91,a critical signaling mechanism in modulating pathophysiologic processes in chronic illnesses[J]. FASEB J,2020,34(10):13091- 13105.
[31] LINDEMANN L,EBELING M,KRATOCHWIL N A,et al. Trace amine-associated receptors form structurally and functionally distinct subfamilies of novel G protein-coupled receptors[J]. Genomics,2005,85(3):372- 385.
[32] LINDEMANN L,HOENER M C. A renaissance in trace amines inspired by a novel GPCR family[J]. Trends Pharmacol Sci,2005,26(5):274-281.
[33] RUTIGLIANO G,BR?UNIG J,DEL GRANDE C,et al. Non-functional trace amine-associated receptor 1 variants in patients with mental disorders[J]. Front Pharmacol,2019,10:1027.
[34] DHAKAL S,MACREADIE I. Tyramine and amyloid beta 42:a toxic synergy[J]. Biomedicines,2020,8(6):145.
[35] KOKKINOU M,IRVINE E E,BONSALL D R,et al. Reproducing the dopamine pathophysiology of schizophrenia and approaches to ameliorate it:a translational ima- ging study with ketamine[J]. Mol Psychiatry,2021,26(6):2562-2576.
[36] HOEFIG C S,ZUCCHI R,K?HRLE J. Thyronamines and derivatives:physiological relevance,pharmacological actions,and future research directions[J]. Thyroid,2016,26(12):1656-1673.
[37] CHIELLINI G,FRASCARELLI S,GHELARDONI S,et al. Cardiac effects of 3-iodothyronamine:a new aminergic system modulating cardiac function[J]. FASEB J,2007,21(7):1597-1608.
[38] BENJAMIN E J,BLAHA M J,CHIUVE S E,et al. Heart disease and stroke statistics-2017 update:a report from the American Heart Association[J]. Circulation,2017,135(10):e146-e603.
[39] LA COUR J L,CHRISTENSEN H M,K?HRLE J,et al. Association between 3-iodothyronamine(T1AM)concentrations and left ventricular function in chronic heart fai- lure[J]. J Clin Endocrinol Metab,2019,104(4):1232- 1238.
[40] LV J N,LIAO J,TAN W,et al. 3-iodothyronamine acting through an anti-apoptotic mechanism is neuroprotective against spinal cord injury in rats[J]. Ann Clin Lab Sci,2018,48(6):736-742.
[41] BANGERT C,RINDLER K,KRAUSGRUBER T,et al. Persistence of mature dendritic cells,TH2A,and Tc2 cells characterize clinically resolved atopic dermatitis under IL-4Rα blockade[J]. Sci Immunol,2021,6(55):eabe2749.
[42] DINTER J,KHAJAVI N,MüHLHAUS J,et al. The multitarget ligand 3-iodothyronamine modulates β-adrenergic receptor 2 signaling[J]. Eur Thyroid J,2015,4(Suppl 1):21-29.
[43] TOMINAGA M,CATERINA M J. Thermosensation and pain[J]. J Neurobiol,2004,61(1):3-12.
[44] TOMINAGA M,TOMINAGA T. Structure and function of TRPV1[J]. Pflügers Arch,2005,451(1):143-150.
[45] NILIUS B,OWSIANIK G,VOETS T,et al. Transient receptor potential cation channels in disease[J]. Physiol Rev,2007,87(1):165-217.
[46] KHAJAVI N,REINACH P S,SLAVI N,et al. Thyro- namine induces TRPM8 channel activation in human conjunctival epithelial cells[J]. Cell Signal,2015,27(2):315- 325.
[47] KENNETT G A,DOURISH C T,CURZON G. 5-HT1B agonists induce anorexia at a postsynaptic site[J]. Eur J Pharmacol,1987,141(3):429-435.
[48] BR?UNIG J,DINTER J,H?FIG C S,et al. The trace amine-associated receptor 1 agonist 3-iodothyronamine induces biased signaling at the serotonin 1b receptor[J]. Front Pharmacol,2018,9:222.
[49] LAURINO A,MATUCCI R,VISTOLI G,et al. 3-iodothyronamine(T1AM),a novel antagonist of muscarinic receptors[J]. Eur J Pharmacol,2016,793:35-42.
[50] Correction to:heart disease and stroke statistics-2017 update:a report from the American Heart Association[J]. Circulation,2017,135(10):e646
[51] ZHOU H Y,HU B L,LIU X D. Thyroid hormone metabolite 3-iodothyronamine(T1AM)alleviates hypoxia/reoxygenation-induced cardiac myocyte apoptosis via Akt/FoxO1 pathway[J]. Med Sci Monit,2020,26:e923195. DOI:10.12659/MSM.923195.
[52] LOMONOSOVA Y N,SHENKMAN B S,NEMIROVSKAYA T L. Attenuation of unloading-induced rat soleus atrophy with the heat-shock protein inducer 17-(allylamino)-17- demethoxygeldanamycin[J]. FASEB J,2012,26(10):4295-4301.
[53] JU H,KIM T,CHUNG C M,et al. Metabolic suppression by 3-iodothyronamine induced muscle cell atrophy via activation of FoxO-proteasome signaling and downregulation of Akt1-S6K signaling[J]. Biol Pharm Bull,2017,40(5):576-582.
[54] ROGOWSKI M,BELLUSCI L,SABATINI M,et al. Lipolytic effects of 3-iodothyronamine(T1AM)and a novel thyronamine-like analog SG-2 through the AMPK pathway[J]. Int J Mol Sci,2019,20(16):E4054.
[55] JU H,SHIN H,SON C,et al. 3-Iodothyronamine-media- ted metabolic suppression increases the phosphorylation of AMPK and induces fuel choice toward lipid mobilization[J]. Horm Metab Res,2014,47(8):605-610.
[56] KIM M,PARK K,CHOI I. The metabolic suppressor 3-iodothyronamine enhances lipolysis in 3T3-L1 adipocytes via activation of the adenosine monophosphate-activated protein kinase/forkhead box O1 signaling pathway[J]. J Physiol pharmacol,2020,71(3):409-416.
[57] RINE J,STRATHERN J N,HICKS J B,et al. A suppressor of mating-type locus mutations in Saccharomyces cerevisiae:evidence for and identification of cryptic ma- ting-type loci[J]. Genetics,1979,93(4):877-901.
[58] HSU Y C,WU Y T,TSAI C L,et al. Current understan- ding and future perspectives of the roles of sirtuins in the reprogramming and differentiation of pluripotent stem cells[J]. Exp Biol Med(Maywood),2018,243(6):563- 575.
[59] ASSADI-PORTER F M,REILAND H,SABATINI M,et al. Metabolic reprogramming by 3-iodothyronamine(T1AM):a new perspective to reverse obesity through co-regulation of sirtuin 4 and 6 expression[J]. Int J Mol Sci,2018,19(5):E1535.
[60] BELLUSCI L,LAURINO A,SABATINI M,et al. New insights into the potential roles of 3-iodothyronamine(T1AM)and newly developed thyronamine-like TAAR1 agonists in neuroprotection[J]. Front Pharmacol,2017,8:905.
(收稿日期:2021-07-19 修回日期:2021-12-15)
(編輯:鄒麗娟)

