Notch信號通路調控癌癥的研究進展
付治美 宋武琦 徐夢蔚 張鳳民
Notch基因得名于該基因的功能缺失突變導致黑腹果蠅翅緣缺刻的遺傳學研究。早在20世紀90年代,Notch突變與癌癥的密切關系就得到了證實[1]。
Notch信號是造血、免疫細胞分化的關鍵調節因子之一,與多種自身免疫性疾病、腫瘤的發生和腫瘤誘導的免疫抑制有關。Notch信號通路本身簡單,但它所調控的細胞進程卻相當復雜,通過基因組測序發現在多種腫瘤中都存在突變的Notch基因,事實上,異常活化的Notch信號涉及癌癥幾乎所有基本特征,如腫瘤血管生成、癌細胞的干性和上皮間充質轉化等[2]。本文綜述了Notch信號通路調控癌癥的相關機制,將為腫瘤的防治開辟新的思路。
一、經典Notch信號通路及其調控
經典Notch信號通路以細胞間接觸的方式傳遞信號,又稱為復合信號結合蛋白J(recombination signal binding protein J,RBP-J)依賴通路,需要Notch受體、配體、RBP-J和靶基因的參與[3]。哺乳動物中,Notch受體(Notch1、Notch2、Notch3和Notch4)和配體(Jagged1、Jagged2、DLL1、DLL3、DLL4)的結合啟動了Notch信號的傳遞。
Notch受體是由單一前體編碼的單程Ⅰ型跨膜蛋白,為多肽段構成的異二聚體,Furin樣蛋白酶在異二聚化結構域的非結構區的S1位點將其切割為N端胞外配體結合區(notch extracellular subunit,NEC)和C端跨膜亞單位(notch transmembrane subunit,NTM);而Notch受體與配體結合后,去整合素金屬蛋白酶(a disintegrin and metalloprotease,ADAM)在NTM外部的S2位點進行切割,切割產生的Notch片段,被早老素依賴的γ-分泌酶在其跨膜區內S3位點再次切割,釋放Notch胞內域(notch intracellular domain,NICD);NICD從膜上釋放并轉移到細胞核,形成一個由NICD、RBP-J和智者基因樣(mastermind-like,MAML)核轉錄激活蛋白家族組成的復合物,該復合物與Notch的一些調節元件結合之后,轉錄Notch下游基因[4]。
經典Notch信號激活上調的靶基因,已知有發狀分裂增強子1(hairy and enhancer of split 1,HES1)、與YRPW基序相關的發狀分裂增強子1(hairy and enhancer of split-related with YRPW motif 1,HEY1)、B細胞特異性MLV整合位點-1(B cell-specific MLV integration site-1,BMI1)、G1/S-特異性周期蛋白-D1(cyclin D1,CCND1)、細胞周期蛋白依賴性激酶抑制劑1A(cyclin dependent kinase inhibitor 1A,CDKN1A)等[5~8]。Notch本身作為轉錄共激活因子,轉錄反應非常復雜,可以和其他信號通路發生復雜的交叉作用,Notch通路可以調控以下這些癌癥相關通路繼而在不同癌癥中發揮不同功能(圖1)。

圖1 Notch信號通路與癌癥相關通路的關系
1.Notch與Wnt/β-catenin信號通路:Wnt /β-連環蛋白(Wnt/β-catenin)信號通路在多種腫瘤中被異常激活,主要是由轉錄因子β-catenin的錯義突變引起。Notch與Wnt信號通路的相互作用發生在許多水平上,Notch能抑制糖原合成酶激酶3β(glycogen synthase kinase3β,GSK-3β)激活β-catenin,最近的研究集中在Notch和Wnt信號在細胞和基質成分之間正常的交互作用上[9]。研究表明,Wnt信號通路在慢性淋巴細胞白血病中是核心調節通路之一,而失調的Notch2是腫瘤細胞中經典的Wnt信號激活的先決條件,抑制Notch信號會降低基質保護的CLL細胞在體內外的存活率[10]。在乳腺癌細胞中,Notch信號可以與Wnt及其他信號通路發生交叉作用被激活,目前已有文獻報道靶向Notch和Wnt通路來治療乳腺癌的聯合用藥方法[11]。肝細胞癌組織中也常發現Notch基因突變,已知Notch1調控Wnt通路上調乙肝病毒X蛋白的表達從而誘導肝癌發生[12]。Notch1在黑色素瘤中也能調控Wnt、絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)、蛋白激酶B(protein kinase B,PKB,又稱AKT)等信號通路,Notch1激活后,β-catenin上調,MAPK和AKT被激活,而抑制Wnt/β-catenin、MAPK和AKT通路能逆轉Notch1誘導的腫瘤生長和轉移[13]。結直腸癌(colorectal cancer,CRC)中,Notch與活化的β-catenin的結合干擾了CRC細胞中β-catenin的溶酶體的轉運和降解,從而干擾Wnt信號傳遞,結腸癌中Notch1表達的升高促進癌癥的進展,而Notch2升高卻可能起到抑制結腸癌生長的作用,因此,Notch通路在結腸癌中發揮作用尚不明確[14]。在子宮內膜癌(endometrial cancer,EC)中關于Wnt信號的報道較少,出人意料的是,通過對47例EC樣本的分析顯示,與相鄰的非腫瘤組織比較,EC組織中Notch 和Wnt信號分子的轉錄水平降低,NICD與Wnt通路重要效應分子體軸抑制因子(axis inhibitor,Axin)結合可減少β-catenin的累積,發揮腫瘤抑制功能[15]。
由此可見,Notch通過激活GSK-3β繼而激活Wnt通路。Notch結合Axin等使Wnt降解受阻,這樣的雙重作用使Notch與Wnt信號之間維持著一種動態平衡,一旦平衡被打破,組織和微環境中的信號轉導紊亂,就會導致腫瘤的發生、發展[4]。
2.Notch與PI3K/AKT信號通路:磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)/AKT信號通路的失調被認為是腫瘤發生的標志,在腦腫瘤、消化系統腫瘤、女性生殖系統腫瘤、血液免疫系統腫瘤、乳腺癌和皮膚癌中均存在。編碼受體的Notch基因可能通過典型的受體-配體相互作用激活AKT,還可通過與一些表面受體表達的增強子結合來激活PI3K/AKT信號,如白細胞介素7受體(interleukin 7 receptor,IL-7R)[16]。血液系統惡性腫瘤常表現出Notch信號的異常,最常見的是急性T淋巴細胞白血病(T-cell acute lymphoblastic leukemia,T-ALL)。2021年Padi等[17]證實了T-ALL早期對Notch抑制劑的耐藥就是PI3K激活的結果。在乳腺癌中Notch與PI3K/AKT的互相作用較為復雜。在低分化型乳腺癌中,Notch與PI3K/AKT通路共同活化可使乳腺癌惡性程度升高[18]。另一方面,Notch3可通過反式激活磷脂酶和張力蛋白同源物(phosphatase and tensin homolog,PTEN)的表達來抑制乳腺癌的增殖[19]。因此,關于Notch在乳腺癌中發揮作用的明確機制仍需進一步的研究。
3.Notch與NF-κB信號通路:核因子-κB(nuclear factor kappa B, NF-κB)通路能夠促進腫瘤的發生、發展,廣泛存在于乳腺癌、淋巴癌等腫瘤中,幾乎與所有癌癥的特征相關。膠質母細胞瘤(glioblastoma multiforme,GBM)中,Notch1可以直接激活NF-κB通路,還可通過誘導HES1的表達間接激活NF-κB通路[20]。Notch與NF-κB在白血病中的聯系更是緊密,如Notch3的異常激活可導致不同的NF-κB亞單位二聚化,調節參與白血病細胞分化或增殖的不同基因簇,在一定程度上還能增強NF-κB靶基因的表達介導白血病細胞抗凋亡作用[9]。
4.Notch與其他信號通路
(1)IL-6/STAT3信號通路:活化的轉錄激活因子3(signal transducer and activator of transcription 3,STAT3)擾亂了細胞的正常生存周期,在頭頸癌、多發性骨髓瘤等多種惡性腫瘤中發揮強烈的致癌作用。Notch通路的關鍵調節因子RBP-J通過增強白細胞介素6(interleukin 6,IL-6)表達激活STAT3通路,并介導膠質瘤的腫瘤進展及放化療耐藥[21]。
(2)p63信號通路:轉錄因子p63在鱗狀上皮組織中賦予基底細胞自我更新的活性,在鱗狀細胞癌(squamous-cell carcinoma,SCC)中過表達。Notch在SCC中與p63互相作用,鱗狀上皮細胞中p63的下調和Notch的激活啟動了細胞周期阻滯和終止鱗狀分化的程序,發揮腫瘤抑制功能,如近期就有研究提示Notch1的表達與口腔鱗癌的進展和預后有關,但Notch是如何發揮這些腫瘤抑制功能的,還有待于深入研究[22]。
(3)RAS/ERK信號通路:腫瘤中常出現大鼠肉瘤病毒(rat sarcoma virus,RAS)家族蛋白成員KRAS、NRAS、HRAS的突變。2019年,Huang等[23]研究發現Notch信號和RAS/細胞外信號調節激酶(extracellular signal-regulated kinase,ERK)信號可能通過交互作用共同參與了胃癌(gastric cancer,GC)細胞增殖的調控,Notch1在胃癌組織中高表達,與胃癌淋巴結轉移有關,抑制Notch1可以有效地抑制胃癌細胞的增殖。胰腺導管腺癌(pancreatic ductal adenocarcinoma,PDAC)是一種生存率極低的胰腺癌類型,小鼠遺傳學研究表明,Notch信號的激活與致癌的KRAS協同作用,使腺泡細胞的發育出現異常,也有研究發現Notch2基因的失活會抑制KRAS引起的PDAC的發展[24]。
(4)Hedgehog信號通路:激活Hedgehog信號通路會導致細胞過度增殖,與多種癌癥有關,包括髓母細胞瘤、膠質瘤、肺癌等。在膠質瘤和髓母細胞瘤中,Notch信號控制Hedgehog通路的關鍵因子G蛋白偶聯受體Smoothened蛋白的傳遞和膠質瘤相關癌基因同源物(glioma-associated oncogene homolog,GLI)基因的轉錄,Notch信號的激活導致Smoothened蛋白累積,繼而增高Hedgehog反應水平[25]。
(5)Hippo/YAP信號通路:Hippo/Yes相關蛋白(Yes-associated protein,YAP)信號通路可抑制細胞和組織生長,Notch3通過上調乳腺癌細胞腎臟腦蛋白(recombinant kidney and brain protein,KIBRA)激活Hippo/YAP通路來抑制乳腺上皮細胞間充質轉化,干擾腫瘤的侵襲和轉移[26]。
二、非經典Notch信號通路及其調控
除依賴于RBP-J的Notch通路以外,非經典的Notch信號通路在機體發育和成熟過程中同樣發揮著重要作用。在乳腺癌中,非經典Notch通路激活PI3K通路促進癌細胞的遷移,其中沒有明顯的RBP-J參與[27]。在部分肺癌、膠質瘤、卵巢漿液性癌等腫瘤中,表皮生長因子家族delta樣同源蛋白(delta-like 1 homolog,DLK1)缺乏Notch配體結構域,通過非經典通路拮抗Notch1信號轉導[28]。然而,非經典Notch信號通路主要以果蠅為模型進行研究,在人體生理學中的相關研究較少。
三、展 望
Notch信號失調是腫瘤發生、發展的重要因素,它和其他信號機制之間并不是彼此孤立的,而是形成復雜的相互作用網絡。現有研究已經證明,Notch信號通路不僅在腫瘤的發生、發展中至關重要,在預后中同樣不可或缺,作為腫瘤的治療靶點具有很大的前景(圖2)。因此,以Notch為靶點或許可以為癌癥預防和治療藥物開發提供新的策略。
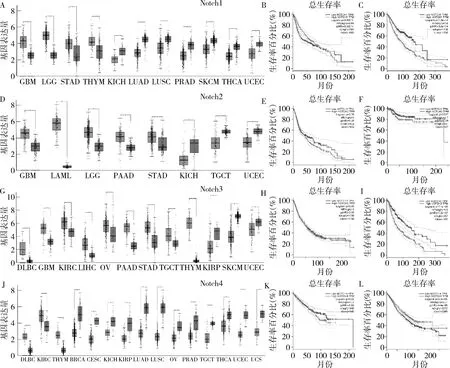
圖2 篩選Notch1~4基因在不同腫瘤及正常組織中表達的差異及預后分析GEPIA聯合TCGA和GTEx數據庫;A、D、G、J.篩選并分析Notch1~4表達差異有意義的腫瘤,紅色代表腫瘤組織,藍色代表正常組織;B、E、H、K.相比于正常組織Notch1-4高表達腫瘤的生存曲線;C、F、I、L.相比于正常組織Notch1~4低表達的生存曲線,紅色代表Notch1~4高表達的腫瘤,藍色代表Notch1~4低表達的腫瘤。*P<0.01
目前阻斷Notch信號通路的藥物和生物制劑已作為抗癌藥物正在進行研發,如單克隆抗體Demcizumab(OMP-21M18)、γ-分泌酶抑制劑Nirogacestat(PF-03084014)、抗體藥物偶聯物rovalpituzumab tesirine、雙特異性抗體Navicixizumab(OMP-305B83)等已進入臨床試驗階段[29]。這些藥物的抗腫瘤作用已經在一些難治性癌癥如彌漫型胃癌、胰腺癌中進行了測試,然而,Notch靶向療法尚未被批準用于癌癥患者的治療。首先,由于Notch通路與其他通路的互相作用的復雜性,簡單地靶向Notch受體的抗體可能不足以抑制腫瘤的生長或轉移;其次這些藥物的不良效應和毒性同樣是治療過程中不可忽視的阻礙。因此,Notch靶向療法的安全性和有效性仍需要進一步的研究。
Notch療法與其他療法的聯合應用會是一條癌癥防治的新思路。聯合療法的優點在于每種藥物的應用劑量都較低,毒性減少,產生耐藥性的風險也較小。關于聯合療法的開發和試驗雖有理論數據的支持,實際技術尚未成熟。2021年3月,Denny等[30]指出生物醫學方法、計算算法和高分辨率數據的可用性將在未來十年內急劇增加。這是一條新的思路,通過人工智能和基于自然語言處理和文本挖掘的認知計算構建Notch相關知識的數據庫,將優化在精準醫學時代的Notch靶向治療方法,為癌癥的預防和治療提供了新的策略。

