2013-2020年某醫院多重耐藥鮑曼不動桿菌的臨床分布、耐藥性及碳青霉烯酶基因檢測
糜曉梅,楊聞君
(重慶市紅十字會醫院/江北區人民醫院檢驗科,重慶 400020)
鮑曼不動桿菌(Acinetobacter baumannii,Ab)作為一種臨床常見的革蘭陰性桿菌,廣泛存在于自然界的水、土壤和醫院環境中,此外還存在于人體皮膚、呼吸道、消化道和泌尿生殖道等全身多部位,是一種常見的條件致病菌[1?3]。該菌在醫院環境中分布較為廣泛且存活時間較長,易導致危重患者院內感染的發生[4?5]。近年來隨著抗菌藥物的大量使用以及不合理使用,多重耐藥鮑曼不動桿菌(multi?drug resistantAcinetobacter baumannii,MDR?Ab)的檢出率逐年升高,其感染率及致死率也日趨嚴重[6?9]。鮑曼不動桿菌的耐藥機制極其復雜,其中產碳青霉烯酶是MDR?Ab最重要的耐藥機制。已有研究報道由于地域性差異和醫院治療方式不同,細菌面臨的選擇性壓力也存在一定的差異,容易引起細菌異質性耐藥[10?11]。為此,本研究針對重慶市紅十字會醫院2013-2020年臨床各科室分離的1 008株MDR?Ab的臨床分布、耐藥性和碳青霉烯酶基因進行分析,為MDR?Ab耐藥性的動態監測提供基線數據,以便制定合理有效的感染控制措施,最大限度地阻止MDR?Ab的播散。
1 材料與方法
1.1 菌株來源
收集2013-2020年重慶市紅十字會醫院臨床分離的MDR?Ab 1 008株,無效標本未納入此次研究。大腸埃希菌ATCC25922和銅綠假單胞菌ATCC27853作為本實驗的質控菌株。
1.2 儀器與試劑
儀器:DL96?Ⅱ型細菌測定系統(珠海迪爾生物工程有限公司);歐萊博恒溫培養箱(濟南千司生物技術有限公司)。試劑:血平板(重慶龐通公司生產);DL96?Ⅱ型細菌測定系統配套的細菌鑒定卡和藥敏卡(珠海迪爾生物工程有限公司)。
1.3 鮑曼不動桿菌分離鑒定及藥敏試驗
所有實驗菌株均由DL96?Ⅱ型細菌測定系統進行細菌鑒定和藥敏分析,并采用最小抑菌濃度(mini‐mal inhibit concentration,MⅠC)法對臨床常用抗菌藥物進行敏感性分析,具體參照2020版CLSⅠ?M100標準判讀結果,最后通過WHONET 5.6軟件對菌株的臨床分布和藥敏資料進行統計分析。本實驗室將對亞胺培南耐藥的鮑曼不動桿菌定義為MDR?Ab,并對各種抗菌藥物耐藥率進行統計分析。
1.4 碳青霉烯酶基因檢測
1.4.1 模板制備MDR?Ab菌株DNA采用金屬浴煮沸法進行提取,提取后放-80℃保存備用。
1.4.2 碳青霉烯酶基因的PCR檢測 以MDR?Ab菌株DNA為模板分別進行blaOXA‐51、blaOXA‐23、blaOXA‐24和blaOXA‐58基因的PCR擴增,各引物序列根據文獻設計[12],見表1。PCR體系:Taq PCR Master Mix體系12.5μL,ddH2O 9.5μL,上下游引物各1μL,模板DNA 1μL。PCR反應條件:94℃預變性5 min;94℃變性30 s;退火30 s,退火溫度見表1;72℃,延伸根據具體根據產物長度而定;變性、退火、延伸45個循環;72℃繼續延伸7 min。PCR擴增產物進行1%瓊脂糖凝膠電泳,并通過凝膠成像系統觀察電泳結果。

表1 PCR引物序列及產物長度Table 1 PCRprimer sequence and product length
1.4.3 碳青霉烯酶基因測序 將碳青霉烯酶基因陽性的擴增產物送重慶擎科新業生物技術有限公司測序,測序結果在GenBank進行Blast比對。
2 結果
2.1 菌株分布特征
1 008株MDR?Ab菌株的檢出率和分離率見表2。標本類型中痰液占84.2%,肺泡灌洗液占7.4%,分泌物占2.9%,中段尿占2.4%,血液占1.6%,其他占1.5%;年齡分布集中在71~90歲(占60.8%),其中81~90歲330人(占32.7%),71~80歲283人(占28.1%);科室分布主要為重癥醫學科、呼吸內科、腫瘤科和神經外科。見表3~表5。
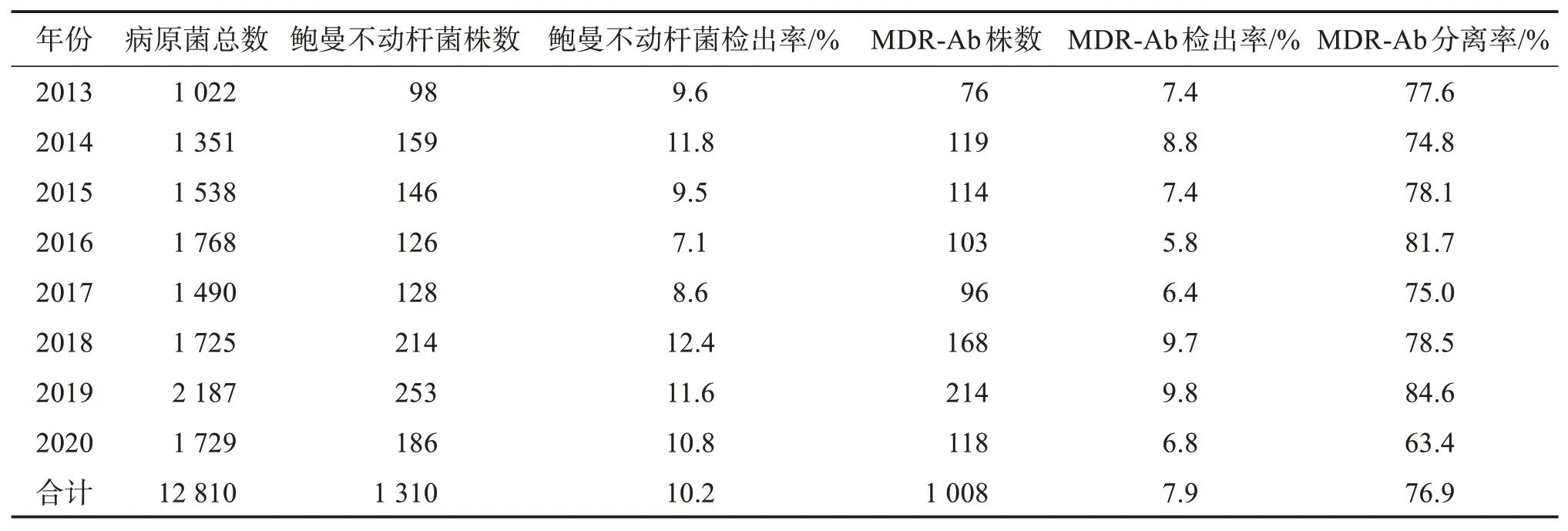
表2 2013-2020年MDR?Ab菌株的檢出情況Table 2 Detection of MDR?Ab strains from 2013 to 2020
2.2 抗菌藥物敏感性試驗結果
1 008株MDR?Ab對臨床常用抗菌藥物的耐藥率和敏感率均存在小幅度波動但基本維持穩定。見表6。

表6 2013-2020年MDR?Ab菌株耐藥率和敏感率Table 6 Resistance and sensitivity rates of MDR?Ab strains from 2013 to 2020 %
2.3 碳青霉烯酶基因PCR擴增結果
1 008株MDR?Ab的blaOXA‐51、blaOXA‐23基因型的檢出率分別為62.0%、71.9%,且以blaOXA‐51/blaOXA‐23基因型為主(59.5%),未檢出blaOXA‐24和blaOXA‐58基因型。部分菌株PCR產物電泳見圖1、圖2。
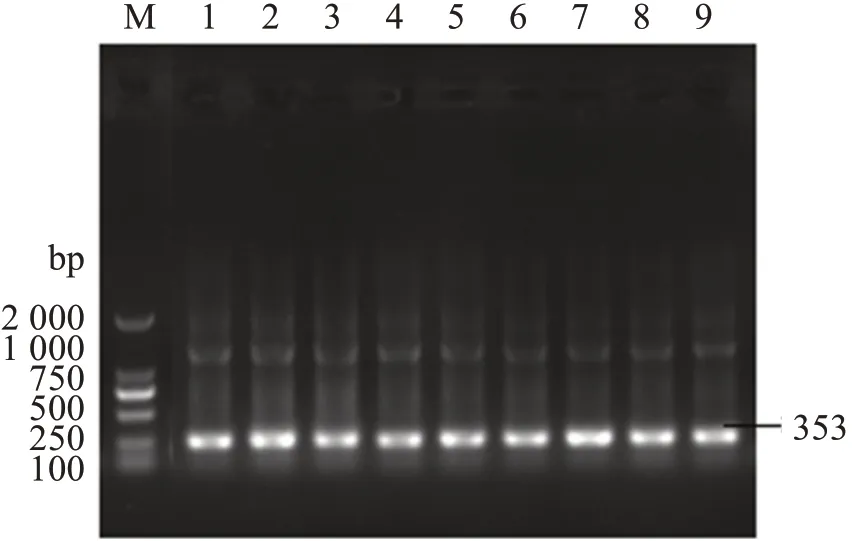
圖1 blaOXA‐51基因型陽性PCR產物電泳圖Figure 1 PCR products of blaOXA‐51 gene
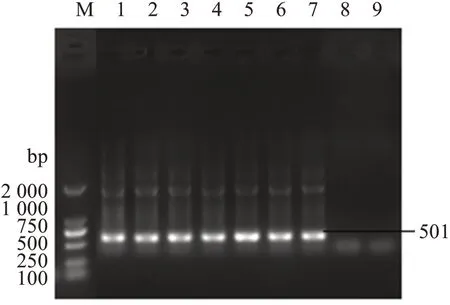
圖2 blaOXA‐23基因型陽性PCR產物電泳圖Figure 2 PCRproducts of blaOXA‐23 gene
2.4 PCR產物測序結果
碳青霉烯酶基因陽性菌株測序結果與GenBank進行序列比對,測序分析結果與電泳結果完全一致。
3 討論
本研究對2013-2020年重慶市紅十字會醫院臨床各科室分離的1 008株MDR?Ab菌株進行了回顧性分析,結果顯示,標本的質量控制較好,該菌株的檢出率和分離率未見明顯變化,陽性率穩定在5.8%~9.8%的檢出范圍內。MDR?Ab菌株的標本類型、年齡分布、科室分布等與國內多家醫院報道一致,這些病區患者多為危重癥患者、老年患者或者接受過氣管插管等有創治療,大多數患者的免疫力低下,同時還由于大量使用了碳青霉烯類抗生素,造成菌群失調,使得MDR?Ab菌株泛濫進而出現嚴重感染現象[13?16]。逐年比較發現:2019年MDR?Ab菌株出現較快增長,檢出率和分離率均為最高值,而2020年的檢出率和分離率卻呈現較大幅度降低,這可能與近年來加強醫院感染監測、注重醫院感染宣傳、加強手衛生和環境清潔、減少侵入性操作等各種措施有關[17?18]。此外,藥敏結果表明,1 008株MDR?Ab菌株對大部分臨床常見抗菌藥物的耐藥率都大于80%,僅對復方新諾明、左旋氧氟沙星和氨芐西林/舒巴坦的耐藥率低于80%。8年間MDR?Ab菌株對阿米卡星和慶大霉素的耐藥率呈上升趨勢,其耐藥率從2013年的23.7%、80.3%上升至2020年的88.1%、96.6%,對其他常用抗菌藥物的敏感率相對穩定。逐年比較發現:MDR?Ab菌株對美羅培南、替卡西林/克拉維酸、頭孢他啶、哌拉西林/他唑巴坦和環丙沙星的耐藥率均>90%,提示MDR?Ab菌株對這5種抗菌藥物高度耐藥。
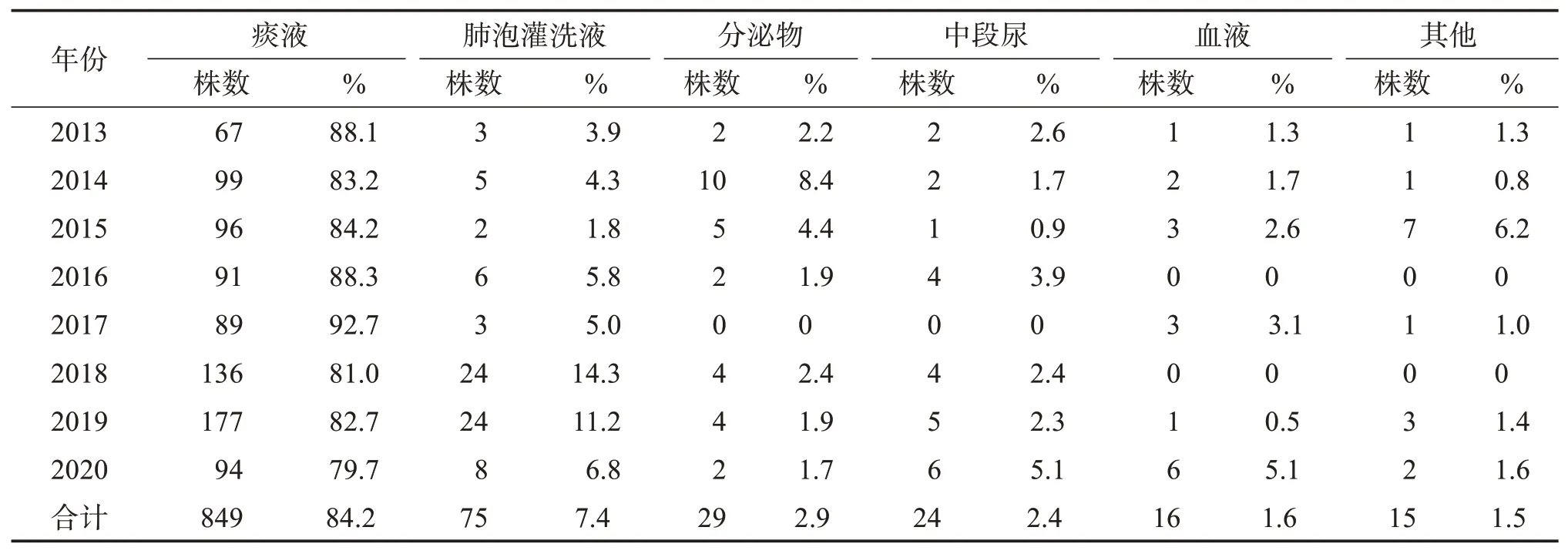
表32013 -2020年MDR?Ab菌株標本類型及構成Table3TypesandcompositionofMDR?Abstrainsamplesfrom2013to2020

表42013 -2020年MDR?Ab菌株感染患者的年齡分布Table4AgedistributionofpatientsinfectedwithMDR?Abstrainsfrom2013to2020

表52013 -2020年MDR?Ab菌株科室分布及構成比Table5 DistributionandcompositionofMDR?Abstrainsindifferentdepartmentsfrom2013to2020
以往研究報道,鮑曼不動桿菌存在較多的耐藥機制,包括產β?內酰胺酶、膜通透性下降、外排泵過度表達、生物膜的形成等[19]。復雜的耐藥機制已成為MDR?Ab迅速傳播的主要原因,而目前臨床針對MDR?Ab治療選擇的藥物非常有限,因此要求醫院各部門攜手并進,采取有力措施,包括:臨床醫護工作人員應加強醫療器械及物品的消毒管理,同時做好手衛生,并嚴格執行無菌操作及消毒隔離,避免院內感染的暴發流行和耐藥菌的進一步播散;檢驗科還需要提供準確的鑒定和藥敏結果,實時動態監測MDR?Ab菌株的耐藥性變化及同源性比較分析,為“精準”抗感染提供實驗室依據;臨床藥師和臨床醫生需要根據藥敏結果制定合理的用藥方案,精準用藥以延緩MDR?Ab菌株的產生[20?21]。
鮑曼不動桿菌是臨床最常見的病原菌之一,它容易引起呼吸道、泌尿道和胃腸道等全身多部位的感染[22?23]。碳青霉烯類抗菌藥物作為革蘭陰性菌感染最廣譜的抗菌藥物,對大多數產超廣譜β‐內酰胺酶具有較高的穩定性[24]。目前,隨著該類抗菌藥物的廣泛使用甚至過度治療,導致臨床耐碳青霉烯類鮑曼不動桿菌呈逐年增加趨勢,且耐藥范圍已分布于全球各地[25]。本研究結果顯示:1 008株MDR?Ab菌株blaOXA‐51基因型陽性率為62.0%,blaOXA‐23基因型陽 性 率 為71.9%,其 中blaOXA‐51/blaOXA‐23基 因 型 占59.5%,但未檢出blaOXA‐24和blaOXA‐58基因陽性攜帶情況,說明從攜帶碳青霉烯酶基因層面上來看,攜帶blaOXA‐51和blaOXA‐23基因產生耐藥是我院鮑曼不動桿菌對碳青霉烯類抗生素耐藥的一個重要機制,而blaOXA‐24和blaOXA‐58基因尚未在我院傳播流行。因此,預防和控制產OXA?513酶和OXA?23酶MDR?Ab是醫院感染是一項非常重要的工作。臨床上對疑似感染患者應盡早采集標本做出多重耐藥菌診斷,合理使用抗菌藥物,加強重點科室的感染控制工作,以減少多重耐藥菌的產生和傳播。
綜上所述,本研究通過對2013-2020年重慶市紅十字會醫院分離的MDR?Ab菌株臨床分布特征和耐藥特征結果進行回顧性分析,進一步了解了醫院MDR?Ab菌株的分布情況和耐藥性變遷規律,為今后MDR?Ab菌株的耐藥性動態監測提供基線數據,為更有效地控制MDR?Ab菌株引起的感染暴發和流行提供可靠的實驗室依據。

