葡萄糖改性尿素的反應特征及其對尿素轉化率的影響
張英強,袁 亮,張水勤,李燕婷,王立艷,趙秉強*
[1 中國農業科學院農業資源與農業區劃研究所/農業農村部植物營養與肥料重點實驗室,北京 100081;2 中國礦業大學(北京)化學與環境工程學院,北京 100083]
尿素是農田氮肥的主要品種,占我國氮肥總量的近65%[1]。尿素施入土壤后很快水解為氨和水,大量的銨極易通過氨揮發、硝化反硝化和淋溶等途徑損失,成為環境氮污染的主要來源[2]。
將增效材料與尿素科學配伍,對尿素進行改性以降低尿素的轉化速率,提高尿素肥料利用率是當前的一個研究熱點。常用的增效劑主要為腐殖酸、海藻酸等天然活性有機高分子。如袁亮等[3]將腐殖酸、海藻酸和氨基酸加入到熔融尿素中制得系列改性尿素,其氮肥表觀利用率較普通尿素提高了3.1~15.6個百分點,小麥籽粒產量增加了3.7%~13.6%。Zhang等[4]將腐殖酸與尿素熔融制得腐殖酸改性尿素,其在玉米上施用的增產效果較普通尿素增加了5.6%~8.7%,玉米氮素吸收量提高了11.5%~29.5%。小分子有機物葡萄糖的化學結構簡單,同樣含有較高反應活性的羥基和醛基官能團。已有研究表明葡萄糖改性尿素可降低尿素損失[5–6]。王彬[7]通過將葡萄糖與尿素在130℃熔融條件下制備出葡萄糖改性尿素,在室內培養試驗中,葡萄糖改性尿素短期(1天)內的水解速率低于尿素,在田間試驗中,較尿素提高了土壤礦質態氮含量、玉米產量和氮肥表觀利用率。陳栓虎等[8]、張蕾等[9]、Viswanathan 等[10–11]研究發現,葡萄糖在加熱條件下水解得到的5-羥甲基-2-糠醛 (HMF) 的醛基可能與尿素的胺基發生聚合反應。王彬等[6]通過傅里葉變換紅外光譜表征發現葡萄糖加入到熔融尿素中,會與尿素分子發生結合,減少尿素結構中伯酰胺氮含量。趙蕊[12]利用傅里葉紅外變換光譜表征發現,尿素胺基可能與糖類醛基發生交聯反應,將部分氨基保護起來,減少尿素損失。上述研究表明,葡萄糖中的活性官能團(羥基/醛基)可與尿素發生化學反應。但對葡萄糖與尿素熔融時的反應特征及其產物的具體化學結構研究相對較少,產物的化學結構與減緩尿素水解之間的關系尚不明晰。因此,我們通過傅里葉變換紅外光譜法(FTIR)、X射線光電子能譜法(XPS)和液相色譜-質譜聯用(LC-MS)等方法,研究了葡萄糖與尿素的反應位點及其產物化學結構,通過生物脲酶法探究葡萄糖對尿素轉化調控效應與反應產物結構之間的關系,旨在為高效氮肥研發提供理論和技術依據。
1 材料與方法
1.1 試驗儀器與試劑
Nicolet IS10紅外光譜儀(FTIR,美國Nicolet公司),ESCALab250型X射線光電子能譜儀(XPS,美國 Thermo Scientific 公司),安捷倫 Agilent 1100高效液相色譜儀(HPLC,日本島津公司)–Thermo Scientific TSQ Quantum Ultra 質譜聯用 (LC-MS,安捷倫Agilent公司和美國Thermo Scientific公司)。
葡萄糖(Glucose,Glu,分析純,國藥集團化學試劑有限公司),尿素(Urea,分析純,含量≥99.0%,國藥集團化學試劑有限公司),脲酶試劑(活力:~1 U/mg,Sigma公司)。
1.2 葡萄糖改性尿素的制備
將葡萄糖(Glu)按照10%的添加量加入到130℃熔融尿素中,攪拌30 s,冷卻后粉碎,過0.15 mm篩,制得葡萄糖改性尿素(GluU)[6]。同時制備僅熔融不添加葡萄糖的普通尿素(U)作為對照。將以上樣品利用FTIR、XPS和LC-MS等儀器表征其特征。預試驗表明,當葡萄糖添加量較小時,葡萄糖改性尿素中葡萄糖與尿素的反應產物含量過低,未達到儀器檢測閾值范圍,因此,選擇添加10%的葡萄糖與尿素熔融反應后所得產物進行結構表征,以明晰葡萄糖與尿素之間的反應特征,而添加量的變化對結構表征過程中反應產物的結構無影響。
同時參考上述肥料制備方式,分別制備葡萄糖添加比例分別為0.2%、0.5%和1.0%,反應時間30 s的葡萄糖改性尿素系列,分別記為GluU0.2、GluU0.5和GluU1.0,同時制備僅熔融不添加葡萄糖的普通尿素(U)作為對照。供試尿素性質見表1。
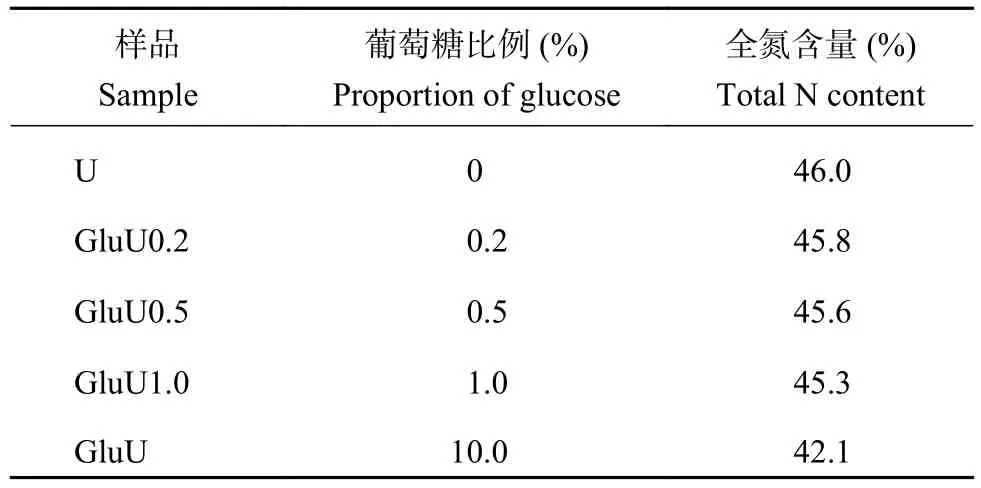
表1 供試尿素中葡萄糖添加比例及含氮量Table 1 Additive proportion of glucose and N content in prepared urea
1.3 材料結構表征
1.3.1 官能團結構測定試驗通過美國尼高力公司的IS10型紅外光譜儀對材料官能團結構分析。測試條件:將2 mg樣品和200 mg光譜純溴化鉀混合后,在紅外燈的烘烤下進行研磨、壓片,通過傅里葉紅外光譜儀記錄 4000 cm–1~400 cm–1波段內樣品的紅外光譜特征。每個樣品掃描32次,分辨率為4 cm–1。
1.3.2 供試肥料表面原子成鍵測定試驗通過美國賽默飛公司的ESCALab250型X射線光電子能譜儀對材料表面元素組分、化學價態和形式進行表征。測試條件:激發源為單色化Al Kα X射線,功率為150 W。分析時的基礎真空約為 6.5×10–10mbar。結合能用烷基碳 C 1s峰 (284.8 eV)校正。
1.4 供試尿素有機組分測定
試驗通過安捷倫公司的1100高效液相色譜儀和賽默飛TSQ Quantum Ultra質譜聯用分析樣品的物質組成。測試過程中流動相為乙腈∶水= 95∶5,流速為0.3 mL/min;質譜的離子源為電噴霧離子源,模式為ESI positive,電離電壓為8 kV,鞘氣壓力為45 psi,輔助氣壓力為15 psi,毛細管溫度為350℃,以液相色譜進樣方式進入,不流入色譜柱,進入質譜儀進行分析。
1.5 尿素轉化率測定
依據GB/T 35113—2017標準,將制得的GluU0.2、GluU0.5、GluU1.0和U分別加入脲酶溶液(活力 ~1 U/mg),置于(25±2)℃恒溫箱中培養30 min后,在分光光度計上比色,計算尿素分解率[13]。
尿素分解率 (%) = (初始尿素態氮含量–轉化后剩余尿素態氮含量)/初始尿素態氮含量×100
1.6 數據處理方法
傅里葉變換紅外光譜圖用OMNIC 9.0軟件進行基線校正和數據平滑校正,所有數據采用Origin 2021進行繪圖,采用SPSS 17.0和Duncan新復極差法進行方差分析和處理間差異顯著性分析(P<0.05),采用XPS PEAK41軟件對XPS數據進行分峰擬合。
2 結果與討論
2.1 葡萄糖改性尿素的官能團結構
由傅里葉變換紅外光譜(圖1)可知,與Glu和U相比,GluU保留了更多的普通尿素U特征,表現為在3441 cm–1左右出現了伯胺NH2反對稱伸縮振動,3348 cm–1左右出現了NH2對稱伸縮振動,1680 cm–1處出現了伯酰胺 C=O 伸縮振動,1625 cm–1左右出現了NH2變角振動,1466 cm–1左右出現了伯胺C―N伸縮振動,1154 cm–1左右出現了脂肪族伯銨C―N伸縮振動。不同的是,與U相比,GluU在1599 cm–1并沒有出現伯酰胺NH2變角振動,且GluU 在 3441 cm–1~3348 cm–1范圍伯胺 NH2雙峰伸縮強度減弱,推測葡萄糖與尿素胺基發生反應,影響了―NH2的振動強度,這與王彬等[6]發現10%的葡萄糖添加量熔融尿素在1600 cm–1處伯酰胺NH2變角振動消失的結果相吻合[6,14]。與Glu相比,GluU同樣在1078~1034 cm–1左右出現糖類C―OH伸縮振動,這與Mohsin等[15]表征葡萄糖結構結果一致,但不同的是 Glu 在 3441 cm–1~3348 cm–1的糖類 O―H 伸縮振動峰的振動強度和峰寬均低于GluU,這可能是GluU同時含有―OH和―NH2,二者在此處的特征峰發生堆疊,形成一個較寬的特征峰。紅外光譜對材料官能團結構進行了初步的分析但是由于特征峰的重疊,不能準確地判定葡萄糖與尿素發生反應的官能團結構,還需要通過XPS和LC-MS等手段對材料做進一步分析。
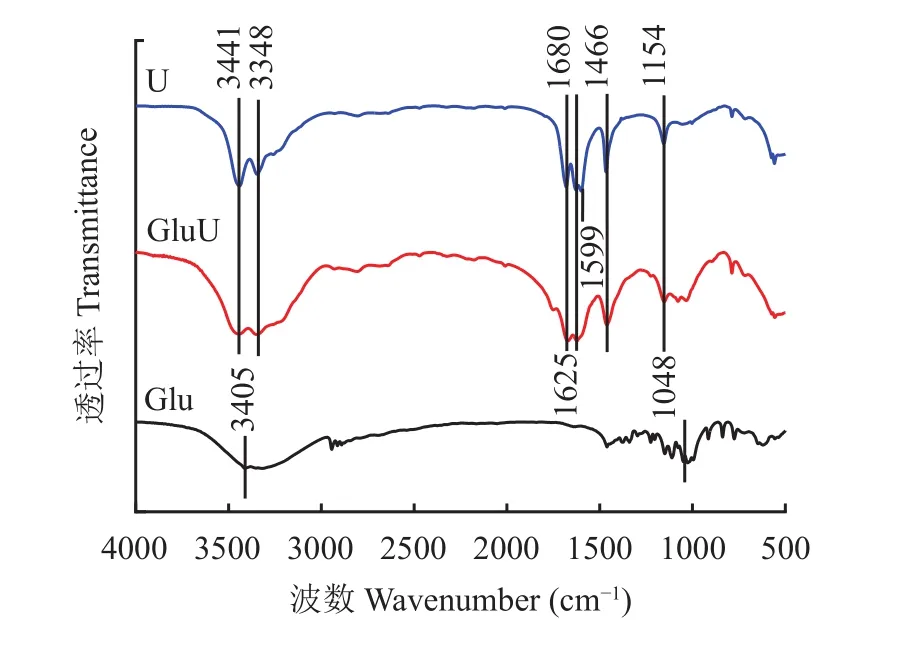
圖1 傅里葉變換紅外光譜Fig. 1 FTIR spectra of samples
2.2 葡萄糖改性尿素的表面原子成鍵
由U、GluU和Glu的XPS全譜圖(圖2)可知,GluU和U中主要含有C、N、O 3種元素,Glu中主要含有C、O兩種元素。XPS測得的各元素相對含量為測試材料表面10 nm以內的相對原子百分比含量。對GluU、U和Glu所含各元素所在區間進行窄掃,其分峰擬合圖見圖3、圖4和圖5,各材料表面元素及元素不同形態的相對含量見表2、表3和表4。由表面元素含量(表2、表3和表4)對比可知,與普通尿素相比,葡萄糖與尿素熔融后,葡萄糖改性尿素中碳元素和氮元素所占比例有所降低,而氧元素所占比例有所增加,這是由于葡萄糖不含氮元素,其碳元素含量為51.2%,低于普通尿素13個百分點;葡萄糖氧元素含量為48.8%,高于普通尿素30.9個百分點。
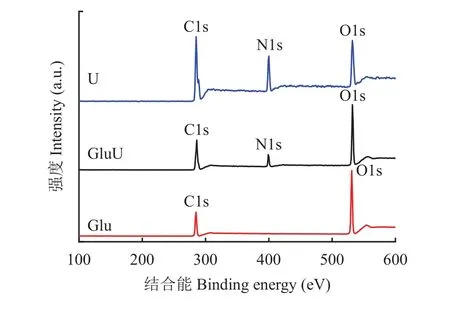
圖2 XPS全譜圖Fig. 2 The XPS full spectra of samples
由XPS C 1s分峰擬合結果(圖3和表2)可知,普通尿素U中有兩個不同碳類型的峰,結合能分別為289.0和284.8 eV,其中位于284.8 eV處的峰屬于空氣中污染碳,不參與尿素分子中碳類型的認定,因此普通尿素中的碳是以酰胺態碳(N―CO―N,289.0 eV)的形式存在[16]。Glu存在3個不同碳類型的峰,結合葡萄糖分子結構判斷,這3種碳類型分別是醛基碳(―CHO,286.6 eV)、羥基碳(C―OH,285.2 eV)和亞甲基碳/次亞甲基碳(C—C/C―H,284.8 eV),這3種形式的碳占所有含碳鍵比例分別為15.0%、35.1%和49.9%;葡萄糖與尿素熔融后的GluU除了含有上述的酰胺態碳(N―CO―N,289.1 eV)、羥基碳(C―OH,286.7 eV)和亞甲基碳/次亞甲基碳(C—C/C―H,284.7 eV)外,還檢測到了結合能為286.1 eV的碳,該碳可能是葡萄糖與尿素熔融反應結合的碳(―CX),這4種形式的碳占所有含碳鍵比例分別為9.0%、45.6%、20.1%和25.2%[17–19]。
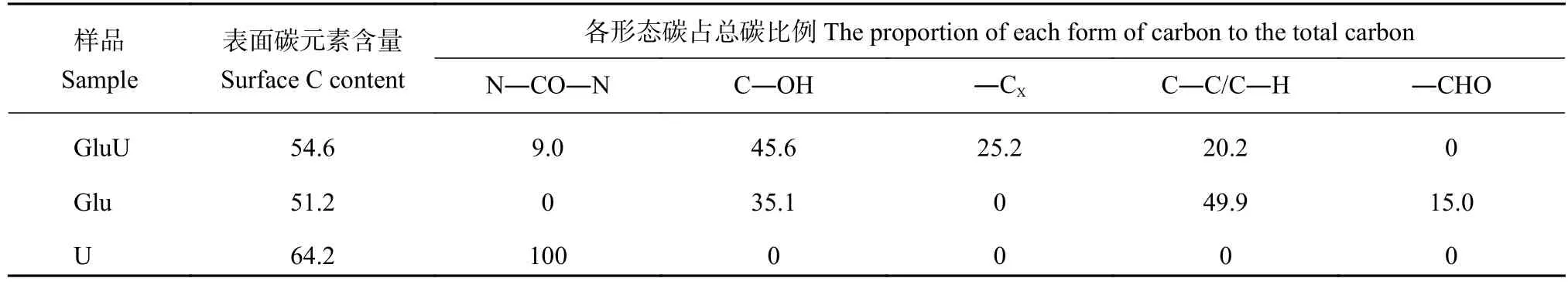
表2 肥料表面碳原子含量及C 1s峰中各形態碳的比例 (%)Table 2 Surface carbon atoms content in fertilizer and the contribution of each carbon form to C 1s peak

圖3 XPS C 1s分峰擬合圖Fig. 3 XPS C 1s peak fitting spectra of samples
進一步分析發現,與含有15.0%醛基碳(結合能286.6 eV)的Glu相比,GluU并未檢測到醛基碳(―CHO)的存在,該碳的結合能由286.6 eV偏移至286.1 eV,說明該碳的化學環境發生改變,與該碳相連的新原子電負性低于醛基碳中與碳相連的氧原子,該原子對碳原子吸電子能力變弱,導致該碳結合能降低[20],推測醛基碳與尿素發生化學反應,生成另一種類型的碳形態(―CX),同時發現羥基碳(C―OH)的結合能由 285.2 eV (Glu)偏移至 286.7 eV,說明GluU中羥基碳周圍的電子云密度增加[21–22],這表明葡萄糖與尿素發生反應的位置與羥基碳相鄰。綜合以上結果認為,葡萄糖的醛基與尿素發生反應過程中,葡萄糖中與羥基碳相鄰醛基上的碳氧雙鍵發生斷裂,形成電負性低于醛基碳的結構―CX,導致葡萄糖改性尿素中羥基碳周圍電子云密度高于葡萄糖[23]。
由XPS O 1s的分峰擬合結果(圖4和表3)可知,U中只含有羰基碳(C=O,531.8 eV),Glu含有兩個不同氧形態的峰,根據葡萄糖分子結構可知,這兩種氧類型分別是羥基氧(C―OH,531.4 eV)和醛基氧(―CHO,530.7 eV),其占所有含氧鍵總量分別為51.1%和48.9%。需要指出,對O 1s譜圖中531.4和530.7 eV進行峰歸屬時通過對比羥基氧與醛基氧的負電性,發現羥基氧的負電性較低,相應的結合能相對較高,對比二者的相對含量,發現峰歸屬結果一致[21,24],同時葡萄糖的羥基氧(C―OH)結合能(531.4 eV)與 Chen 等[25]發現羥基氧 (C―OH)的結合能位于531.4 eV結果吻合。此外,GluU中的氧以羥基氧 (C―OH,532.9 eV)和羰基氧 (C=O,532.3 eV)的形態存在,其占所有含氧鍵總量分別為50.65%和49.35%。
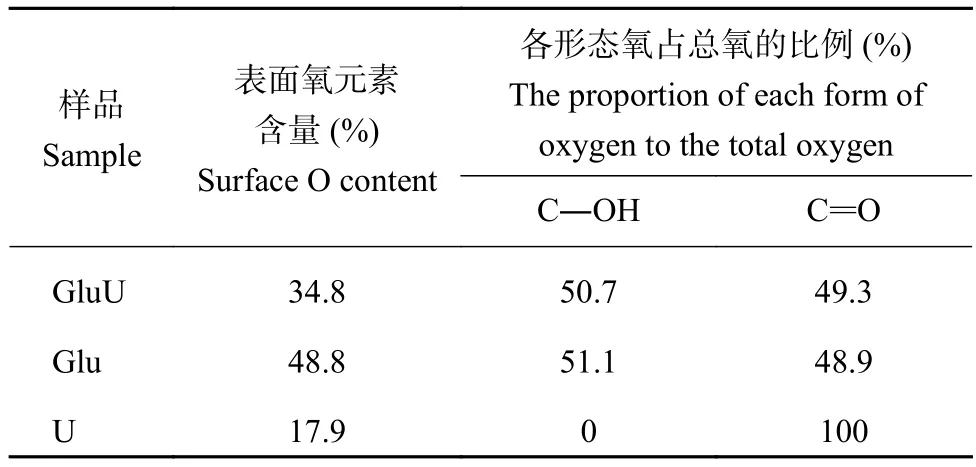
表3 肥料表面氧原子含量及O 1s峰中各形態氧的比例Table 3 Surface oxygen atoms content in fertilizer and the contribution of oxygen species to O 1s peak
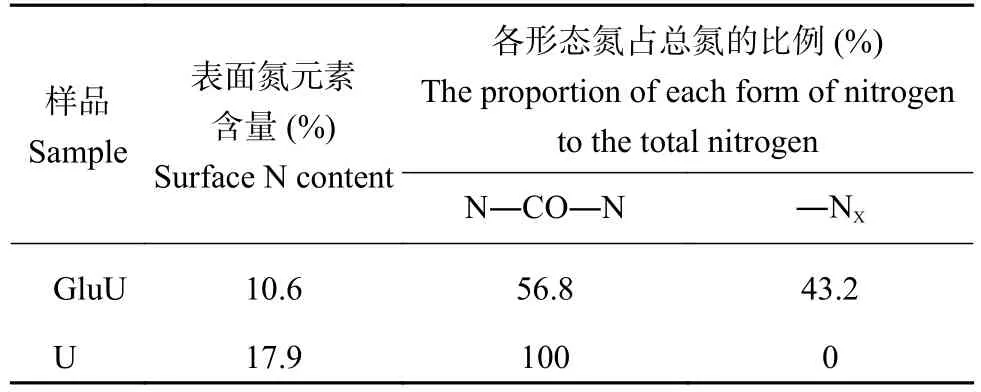
表4 肥料表面氮原子含量及N 1s峰中各形態氮的比例Table 4 Surface nitrogen atoms content in fertilizer and the contribution of each nitrogen form to N 1s peak
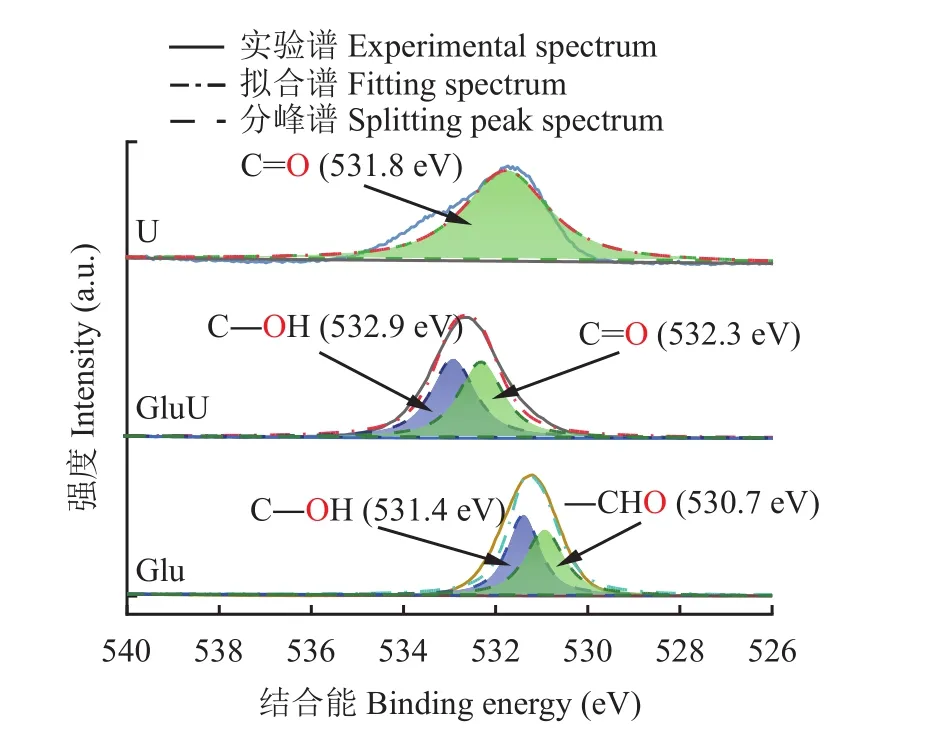
圖4 XPS O 1s分峰擬合圖Fig. 4 XPS O 1s peak fitting spectra of samples
對Glu和GluU中羥基氧(C―OH)和羰基氧(C=O)相對含量分析發現,葡萄糖與尿素熔融后并沒有大幅度提升羰基氧(C=O)相對含量,同時GluU羥基氧(C―OH)含量與Glu含量相當,這可能是由于尿素分子雖然含有羰基氧(C=O),但葡萄糖在與尿素熔融時,葡萄糖中的醛基氧(―CHO)參與反應,C=O化學鍵發生斷裂,與尿素反應生成新物質,導致羰基氧相對含量并未大幅提高[8–9]。該結果與 XPS C 1s中并未檢測到醛基碳 (―CHO),同時檢測出另一種未知碳形態(―CX)的結果吻合,推測是葡萄糖的醛基與尿素發生反應。
由XPS N 1s的分峰擬合結果(圖5和表4)可知,U中的氮形態是以酰胺態氮的形式(N―CO―N,399.7 eV)存在,在GluU中的氮主要是以酰胺態氮的形式(N―CO―N,400.1 eV)存在,同時還檢測到了結合能為399.4 eV的氮,該氮可能是葡萄糖的醛基與尿素的胺基反應結合的氮(―NX),其占所有含氮鍵總量的43.2%[19]。結合GluU C 1s圖譜中檢測到含有未知的碳結構(―CX),醛基碳(―CHO)結構消失,O 1s譜圖結果表明部分羰基C=O化學鍵發生斷裂,從這兩個依據進行推測,可能是葡萄糖的醛基與尿素的酰胺基發生了反應,導致未知氮結構(―NX)的結合能降低。該結果與FTIR圖譜(圖1)中GluU位于3441 cm–1處伯胺NH2反對稱伸縮振動強度減弱,在1599 cm–1并沒有出現伯酰胺NH2變角振動結果相一致。然而葡萄糖醛基與尿素胺基發生反應后產物的物質組成和產物結構尚不明晰,還需通過LC-MS進一步分析。
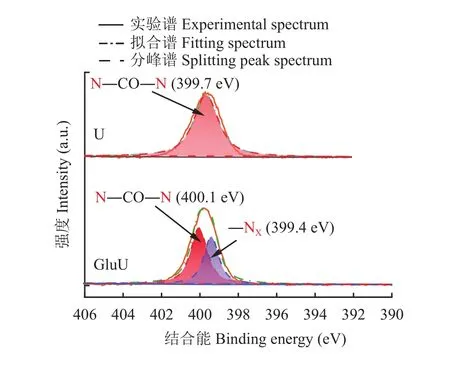
圖5 XPS N 1s分峰擬合圖Fig. 5 XPS N 1s peak fitting spectra of samples
2.3 葡萄糖改性尿素的物質組成
液相色譜–質譜聯用可以很好地根據物質的相對分子質量來推測物質的化學結構。采用LC-MS方法在正離子模式下對U和GluU進行分析,其質譜圖如圖6所示,根據相對分子質量的大小在質譜庫中尋到對應的產物。
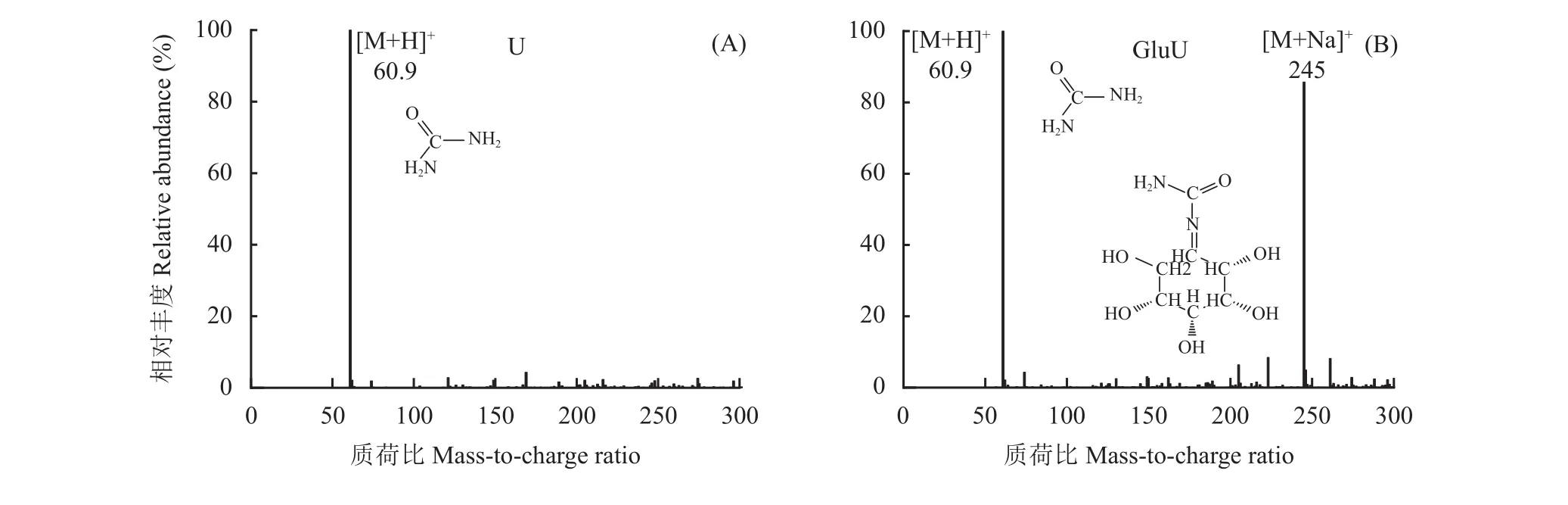
圖6 尿素(A)和葡萄糖改性尿素(B)特征峰質譜圖Fig. 6 MS spectra of urea (A) and glucose-modified urea (B) characteristic peaks
正離子條件下U出現準分子離子峰[M+H]+,離子碎片質荷比為60.9,結合表5中該離子碎片分子式為CH4N2O分析,這是U中尿素成分的體現,相對豐度為100%。正離子條件下GluU出現[M+H]+和[M+Na]+兩種準分子峰離子峰,離子碎片質荷比分別為60.9和245,相對豐度分別為100%和85%。結合表5離子碎片分子式分析,CH4N2O為GluU中尿素的成分,C7H14N2O6為尿素與葡萄糖反應的產物。該物質有較高的超離域度和完整的共軛體系,強配位的氧原子和合適的空間構型,易與Na+形成金屬絡合物[26]。推測葡萄糖在與尿素反應過程中,葡萄糖中的醛基和尿素的胺基發生了反應,生成C=N的同時脫去一分子水,其結構式如圖6 B所示。LC-MS測試結果表明葡萄糖的醛基(―CHO)與尿素的胺基(―NH2)發生反應,發生親核加成反應,生成含有C=N結構的新物質,這充分印證了FTIR和XPS的結果,即尿素的伯胺(―NH2)與葡萄糖的醛基發生反應,尿素伯胺發生變化,葡萄糖的醛基(―CHO)雙鍵發生斷裂,與尿素胺基結合生成含有新的碳形態(―CX,286.1 eV)的物質。3種測試結果相互佐證和支撐,證明葡萄糖的醛基與尿素的胺基發生了反應,生成了含有C=N結構的物質,該結果印證了XPS C 1s測試結果,即與碳相連的新原子電負性低于醛基碳中與碳相連的氧原子。同時XPS發現的未知碳形態 (―CX,286.1 eV)結合能與 Chiang 等[27]發現C=N的C 1s結合能位于286.1~286.3 eV結果相吻合,XPS發現未知氮結構(―NX,399.4 eV)的結合能小于尿素態氮(400.1 eV)與Dong等[28]和Steffan 等[29]發現 C=N―C (398.5 eV)結合能小于C―N―H (401.2 eV)結果相一致。
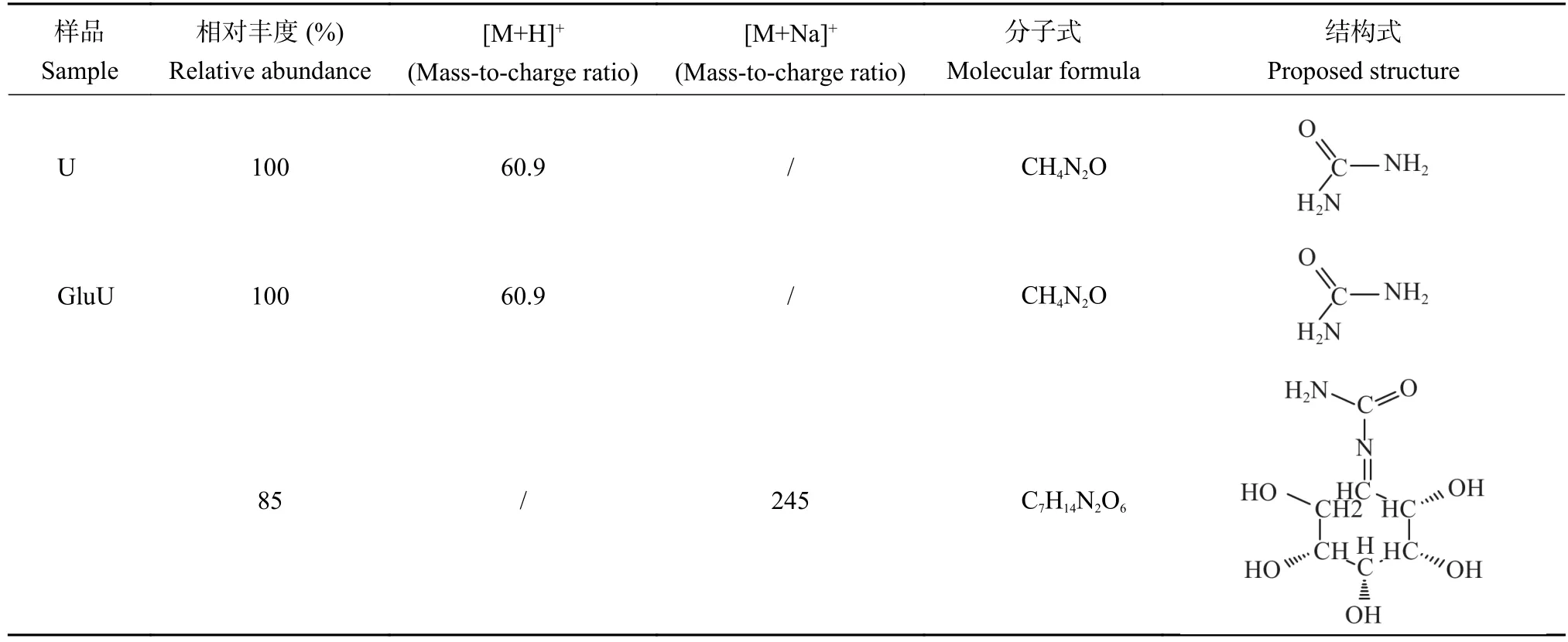
表5 U和GluU的質譜數據Table 5 Date for the MS spectra of U and GluU
2.4 不同葡萄糖添加量對尿素轉化的影響
一般來說,增效劑可能會影響脲酶活性,從而影響尿素在土壤中的轉化速率,改變土壤供氮強度[30]。將一定量的脲酶溶液分別加入系列尿素溶液中,模擬尿素在土壤中被脲酶分解的過程,通過檢測溶液中剩余的尿素態氮含量,進而計算此過程中的尿素轉化率。本研究中,葡萄糖以不同比例添加到熔融尿素中制備得到葡萄糖改性尿素(GluU0.2、GluU0.5和GluU1.0)和僅熔融不添加葡萄糖的普通尿素(U)的尿素轉化率結果(圖7)。
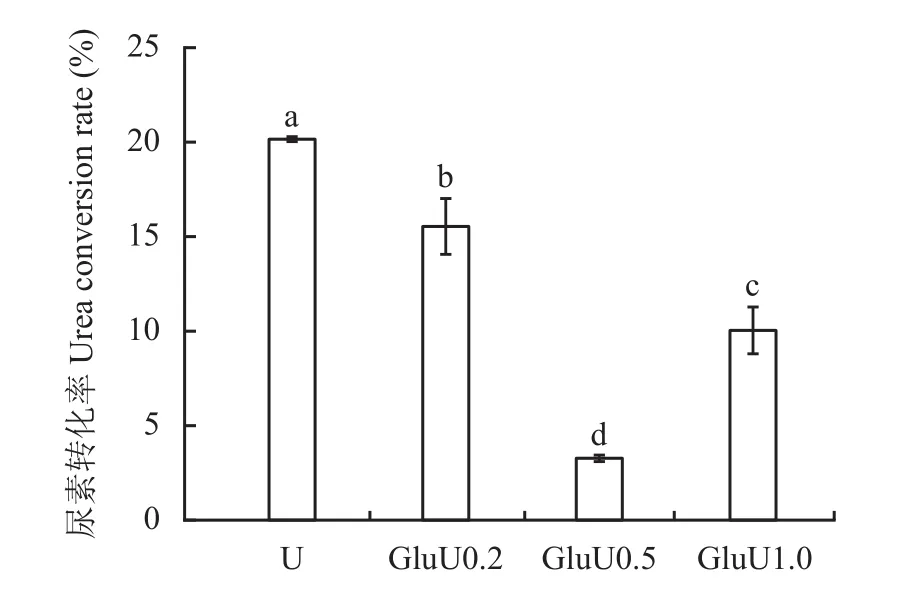
圖7 不同葡萄糖添加量下3類尿素的轉化率Fig. 7 Urea conversion rates of glucose-modified urea products as affected by inclusion rate of glucose
本試驗條件下,普通尿素轉化率為20.16%,GluU0.2、GluU0.5、GluU1.0 3個葡萄糖改性尿素的尿素分解率分別為15.5%、3.3%、11.0%,均顯著低于普通尿素,降低幅度為4.6~16.9個百分點。這可能是葡萄糖醛基與尿素發生反應,醛基能夠結合尿素的―NH2,降低尿素的轉化速度,同時葡萄糖改性尿素中存在C=N不飽和鍵,C=N不飽和鍵在一定程度上能夠抑制脲酶活性,進而影響尿素轉化[31–32]。3個葡萄糖添加量處理之間的尿素轉化率也差異顯著,以葡萄糖添加量為0.5%時最低,添加0.2%最高,這可能是葡萄糖在高添加量時會使GluU1.0溶液中pH下降,對脲酶產生一定的激活效應,對脲酶的抑制作用減弱,導致GluU1.0尿素轉化率高于GluU0.5[33],但不飽和鍵對脲酶抑制作用和pH對脲酶激活效應之間的關系有待進一步研究。不同葡萄糖添加量的葡萄糖改性尿素之間差異顯著,表明在中低添加量(0.2%和0.5%)已達到顯著降低尿素轉化率的效果,為高效氮肥研發提供理論和技術依據。
本研究,葡萄糖改性尿素制備過程中,葡萄糖的添加量較低,基本不改變尿素原有的理化性質[34],但是能夠顯著延緩尿素分解(圖7),抑制尿素轉化的效果以添加0.5%的葡萄糖最好[7]。田間試驗增加玉米產量的效果也以0.5%葡萄糖添加量最好。王彬等[6]對葡萄糖改性尿素的土培試驗結果發現,在培養至3~14 天時葡萄糖改性尿素較普通尿素提高土壤脲酶活性6.9%~8.5%,這可能因為葡萄糖改性尿素在土壤中分解后,葡萄糖為微生物提供了碳源,促進了微生物的活性[35]。張威等[36]研究表明葡萄糖與氮素配施加速了土壤有機氮的礦化速率,從側面證明了葡萄糖作為有機碳源可提高土壤微生物活性,在一定程度上促進氮肥轉化。因此,還需開展更加系統的土壤培養試驗,更全面深入地研究葡萄糖改性尿素在短期內抑制、在后期促進尿素轉化的機制。
3 結論
葡萄糖的醛基與尿素的胺基發生親核加成反應,具體表現在葡萄糖醛基的C=O化學鍵斷裂,碳原子與尿素的氮原子發生結合,生成含有C=N結構的物質。該結構解釋了葡萄糖改性后尿素分解在培養前期顯著降低的原因。不同葡萄糖添加量對葡萄糖改性尿素的轉化率影響顯著,以0.5%的葡萄糖添加量降低尿素轉化率的效果較為適宜。

