氟化鈉殼聚糖凝膠對乳牙釉質抗酸能力的影響
邱賽男,臧睿覺,梅予峰,張曉旻,曹 靈,周紅艷
Stomatology,2022,42(1):68-71,91
兒童因飲食習慣及有限的口腔衛生清潔能力,乳牙齲病高發,氟化物的使用可以有效地控制齲病的發展。pH值較低的酸會造成牙釉質的釉柱本身及釉柱間隙的脫礦溶解,酸持續作用會造成牙齒表面的溶解伴發釉質的軟化,并最終造成結構缺損。本實驗首先配制氟化鈉殼聚糖凝膠,觀察其基本性能;然后使用氟離子選擇電極檢測殼聚糖氟化鈉凝膠氟離子的釋放速率;最后比較氟化鈉殼聚糖凝膠及其他藥物預處理后的乳牙釉質試件在酸蝕后的脫出鈣離子濃度,探討氟化鈉殼聚糖凝膠的抗酸能力。
1 資料與方法
1.1 一般資料
選擇2017年9月—12月于南京醫科大學附屬口腔醫院兒童口腔科拔除的乳前牙28顆(已征得患兒及家長同意)。要求乳前牙沒有齲壞,磨耗量適中保證唇面釉質的面積大小,釉質表面沒有裂紋,拔除時注意不要用力過猛,造成不必要的裂紋。
1.2 儀器與試劑
配制氟化鈉殼聚糖凝膠及檢測所需:殼聚糖(Sigma 448877),氟化鈉(AR,無錫亞盛化工),鹽酸(AR,上海凌峰化學試劑有限公司),β-甘油磷酸鈉(AR,sigma),總離子強度緩沖液Ⅱ(TISAB Ⅱ,南京醫科大學公共衛生實驗室提供),去離子水。大型磁力攪拌儀(國華),制冰機(三洋),DD-2B電極電位儀(江蘇姜堰市光大儀器廠),pH儀(FiveEasy),燒杯。
試件釉質處理和抗酸實驗所需:乳酸(AR,滬試),抗酸指甲油(美寶蓮),原子吸收分光光度計(德國耶拿,AAS vario 6型)。
1.3 配制5%氟化鈉殼聚糖凝膠及性能測定
制備0.05 mol/L的鹽酸100 mL,放入殼聚糖,室溫攪拌24 h,制備出飽和的殼聚糖鹽酸溶液。使用離心機,去除多余的殼聚糖粉末,保留上清。將殼聚糖上清液置于廣口瓶中,高壓蒸汽滅菌30 min,靜置冷卻到常溫,放入4 ℃冰箱備用。pH儀測定殼聚糖鹽酸溶液的pH值,去離子水配制56%(質量濃度)的β-甘油磷酸鈉溶液。
取2 mL殼聚糖鹽酸溶液,加入0.189 4 g NaF(參考多樂氟5%NaF濃度配制),逐滴滴加β-甘油磷酸鈉溶液1.2 mL,在冰水浴下攪拌均勻,配制成5%(質量分數)的殼聚糖氟化鈉凝膠。
肉眼觀察其顏色、質地、性狀等,倒置實驗觀察其流動性,pH儀測定殼聚糖氟化鈉凝膠的pH值。
1.4 氟化鈉殼聚糖凝膠釋氟速率檢測
精確稱取4.2 g NaF,與100 mL去離子水混合,配制0.1 mol/L的標準氟化鈉溶液,使用TISAB Ⅱ緩沖,甘汞氟離子選擇電極測定,獲取氟離子濃度標準曲線。
制備三份殼聚糖氟化鈉凝膠樣本,甘汞氟離子選擇電極測定出氟離子的釋放濃度。
1.5 釉質抗酸實驗
1.5.1 釉質試件準備 拔出的乳前牙,用金剛砂平頸緣去除牙根,橡皮輪拋光釉質表面,三用槍沖洗表面30 s后,置于去離子水中,4 ℃冰箱保存。存放24 h后,取出乳前牙,使用低速切割機縱向切除部分舌側硬組織,留約3 mm厚唇側硬組織片。試件唇側釉質中央預留3 mm×3 mm的實驗區域,其余部分用抗酸指甲油涂3遍,待指甲油干燥后,置于去離子水中,4 ℃冰箱保存。
1.5.2 試件釉質處理 試件隨機分成4組,每組7片,用吸水紙吸干試件表面的水分。三組在實驗區分別均勻地涂上氟化鈉殼聚糖凝膠、殼聚糖空白凝膠、多樂氟,另一組不作處理作為空白對照。各組釉質片在經歷了5 min的酸蝕處理后,以Ekstrand增強肉眼光學檢查視診等級計分標準(表1)評定。
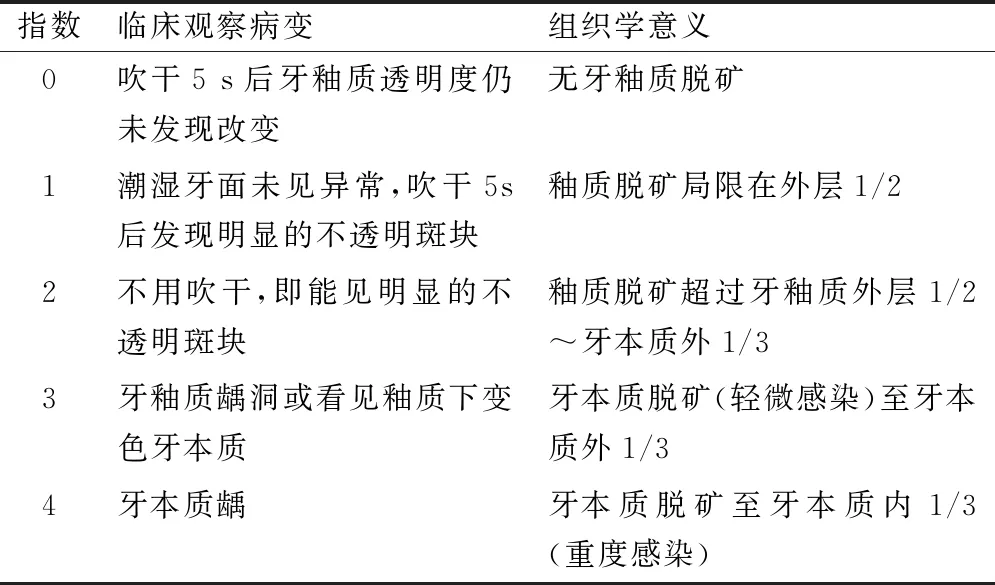
表1 Ekstrand增強肉眼光學檢查視診等級計分標準
上藥處理后,樣本置于燒杯中,加入去離子水,保持整體的濕潤環境,并放入37 ℃恒溫箱中4 h。取出各組試件,用尖刀片輕柔去除表面附著的藥物,用三用槍沖洗試件30 s,置于去離子水中備用。
1.5.3 釉質抗酸實驗 配制0.1 mol/L的乳酸溶液,常溫測定pH值為4.0。每一組的試件分別浸泡于5 mL 0.1 mol/L乳酸溶液,酸蝕5 min,取出試件,用3 mL去離子水沖洗,收集各樣本的酸蝕溶液和沖洗液8 mL。溶液進行火焰原子吸收分光光度法檢測溶液中鈣離子的濃度。
1.6 統計學處理
各組數值錄入SPSS19.0統計分析,不同組的鈣離子濃度進行方差分析。P<0.05為差異有統計學意義。
2 結 果
2.1 殼聚糖氟化鈉凝膠基本性能
殼聚糖氟化鈉凝膠常溫下呈淡黃色粘稠清亮液體,pH=6.98。放置在37 ℃恒溫箱內,3 min初步凝固,10 min后從恒溫箱內取出,呈軟白色果凍狀凝膠,質軟(圖1)。
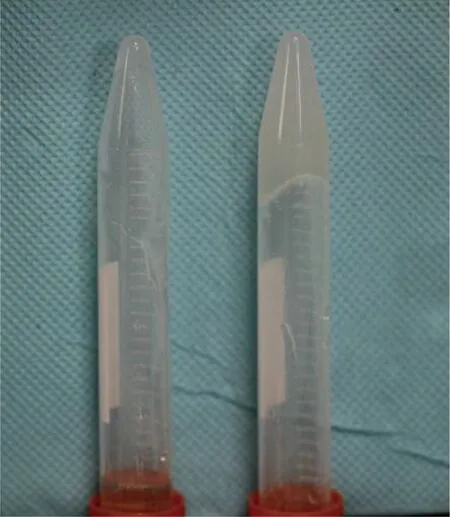
左側為殼聚糖氟化鈉凝膠常溫下保存;右側為殼聚糖氟化鈉凝膠經10 min 37 ℃恒溫箱保存
2.2 殼聚糖氟化鈉凝膠釋放率
氟化鈉標準液經氟離子選擇電極測定氟離子標準曲線函數為y=41.143x-66.667(x軸Ig濃度,y軸為氟離子選擇電極的測定值);線性相關指數R2=0.934 5(圖2)。
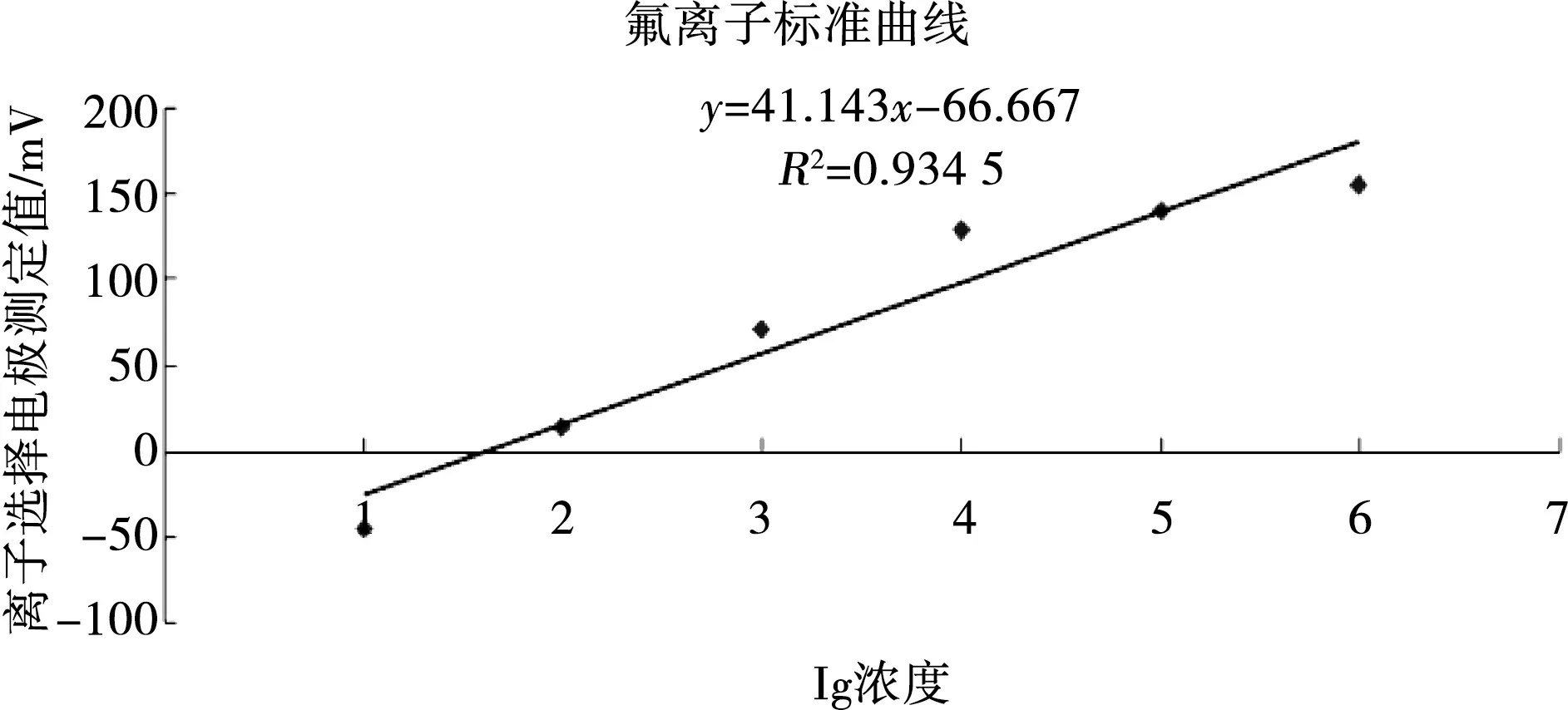
圖2 氟離子標準曲線圖
2.3 不同組釉質試件酸蝕后使用Ekstrand增強肉眼光學檢查視診等級計分
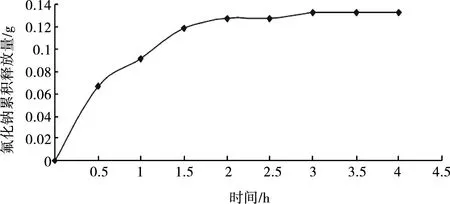
圖3 殼聚糖氟化鈉凝膠釋放曲線
各組吹干5 s后發現不透明的斑塊,均為1級計分,潮濕牙面無明顯異常,其中殼聚糖空白凝膠組和空白對照組表現的色澤較殼聚糖氟化鈉凝膠組及多樂氟組要更白,通透性更差。
2.4 不同組釉質試件乳酸溶液中鈣離子濃度比較
氟化鈉殼聚糖凝膠、殼聚糖空白凝膠、多樂氟、對照組鈣離子濃度分別為(4.29±0.65)、(7.20±0.88)、(4.22±0.34)、(7.34±1.41)mg/L。氟化鈉殼聚糖凝膠組與多樂氟組沒有統計學差異(P>0.05),與殼聚糖空白凝膠組及空白對照組有統計學差異(P<0.05),且鈣離子濃度低于殼聚糖空白凝膠組及空白對照組。
3 討 論
氟化物是公認的防齲藥物之一,從20世紀初就已經開始進行應用,具有降低釉質溶解度和促進釉質再礦化、影響致齲細菌代謝、改變牙齒萌出后的形態和結構的特點,從而具有防齲的功效[1]。含氟產品的使用可以是患者進行的自我保健方法,也可以是專業的口腔醫生給予的專業預防操作保健。對于兒童來說,使用含氟牙膏的量及含氟漱口水的用量控制尤為重要,因為兒童的含漱能力和吞咽的配合能力有限,過量氟化物的使用,會引起兒童的中毒反應。所以臨床上對兒童用氟的指導理念是小于4歲的不宜局部用氟,也不推薦使用含氟牙膏及含氟漱口水,而是由臨床醫生進行含氟涂料或凝膠的涂布操作。
Chau等[2]證實,氟化物可以抑制細菌生物膜的形成,且其活性與時間有一定的相關性。其在用量和次數上有更多的限制,這樣對于控制氟的過量攝入有很好的保證。涂料在操作方式和方法上和凝膠有相似之處,都需要保持釉質的干燥,在藥物涂布完后一定時間內不喝水不吃東西,從操作的簡便性上看,并不是很復雜的操作。不過操作的難度和兒童對命令以及行為控制的配合程度有關[3]。
歐洲兒科牙科學會(EAPD)發布的氟化物應用指南[4]指出兒童含氟凝膠較涂料的操作要更簡單,清潔完牙面只需患者佩戴牙合墊輕咬幾分鐘即可,操作的用量仍需要嚴格控制。多樂氟的出現,使得操作更為簡便,涂在釉質表面的多樂氟在遇到唾液后可以硬化,只要控制兒童4 h不進食飲水,唾液不下咽即可。
但多樂氟凝膠成本相對較貴,用殼聚糖水凝膠作為一種凝膠載體,它的原料殼聚糖是自然界中的第二大多糖甲殼素的脫乙酰基產物,來源豐富制取便宜,其價格便宜,同時Arnaud等[5]指出單純的殼聚糖溶液也有保護牙釉質、抵抗酸蝕的作用。
制作殼聚糖水凝膠的過程并不復雜,完成的凝膠為智能型凝膠,溫度升高凝膠由液相向膠體相轉變,這對于凝膠的保存以及使用時的方便程度都有很好的指導意義。臧圣奇等[6]的實驗通過對殼聚糖溫敏凝膠的凝膠時間、黏度、溶脹率、降解率、微觀結構等方面的研究,肯定了殼聚糖凝膠作為組織工程支架,復合細胞、藥物、蛋白的利用價值。
殼聚糖氟化鈉凝膠的pH值接近中性,對藥物和人體組織的損害較小,生物相容性較好。作為大分子多糖,殼聚糖氟化鈉凝膠提供的空間可以作為藥物的良好載體。近年來多樂氟作為口腔局部用藥的經典藥物,常作為評估其他藥物氟離子釋放率的參考標準,經我們研究發現氟化鈉殼聚糖凝膠組與多樂氟組4 h氟離子釋放率沒有統計學差異。Ruel-Gariépy等[7-9]的研究證明,殼聚糖溫敏凝膠作為藥物的載體,其釋放速率與藥物的分子量有關,藥物分子量越大,釋放速率越慢,本實驗中氟化鈉作為小分子親水藥物4 h釋放70%是可以接受的。同時Keegan等[10]制作的殼聚糖納米噴霧搭載氟化鈉,其最大搭載藥物量達到14%的氟化鈉含量,釋放率達到84.1%,證明了殼聚糖作為氟化鈉搭載載體的能力。因此本課題設計制作的殼聚糖氟化鈉凝膠是成功的,搭載了高濃度的氟化鈉,并且很好地控制了藥物的pH值,其藥物的釋放率也符合殼聚糖溫敏水凝膠的一般特性。
釉質的早期齲壞即為釉質表面在細菌代謝產物的酸蝕作用下出現的表面礦物質析出,呈現出白堊色的色澤變化,白堊色越不明顯說明其脫礦情況越低。經由Ekstrand增強肉眼光學檢查視診等級計分標準[11]評定,各組都表現為釉質脫礦集中在釉質外層1/2,類似于臨床上見到的釉質脫礦的早期齲壞。氟化鈉殼聚糖凝膠及多樂氟處理過的試件,在肉眼觀察其白堊色時,無單純殼聚糖水凝膠和未處理組明顯。Torlakovic等[12]的研究結果說明早期齲的白色病損,其病變程度和白堊色深度呈正相關的,本實驗的肉眼觀察結果說明氟化鈉殼聚糖凝膠及多樂氟抑制酸蝕的能力優于殼聚糖空白凝膠及空白對照組。
釉質表面的酸蝕液進行鈣離子濃度的檢測,是一種經典的定量檢測方法Grenby[13]早在1996年釉質檢測方法的綜述中就有詳細的描述,可以有效量化釉質表面脫礦的程度。而且這種方法在體內體外都可以進行。Young等[14]驗指出釉質的化學檢測在體內試驗中需要絕對的隔絕唾液,以防止影響檢測結果,而體外實驗的操作更加準確簡便。從我們的結果可知,實驗各組在酸蝕過程中脫出的鈣離子濃度是有區別的。組間的比較氟化鈉殼聚糖凝膠與多樂氟處理組析出的鈣離子濃度數值無差異,殼聚糖空白水凝膠與空白組無差異,同時氟化鈉殼聚糖凝膠、多樂氟析出的鈣離子濃度要遠低于殼聚糖空白水凝膠及空白組。這說明,氟化鈉殼聚糖凝膠及多樂氟抗酸的效果優于殼聚糖空白水凝膠,并且效果相似,這與肉眼觀察到的結果相同,說明了氟化鈉殼聚糖凝膠與多樂氟的抗酸蝕效果。
多樂氟作為防齲處理的金標準,一直被臨床廣泛應用,其pH值為4.5[15],Magalh?es等[16]進行的TiF4和NaF涂料的實驗,指出釉質表面在各種藥物處理后,最高可以持續抵抗酸蝕30 min。同時Arnaud的實驗[5]報道,殼聚糖溶液涂抹在釉質表面產生的抗酸效果是殼聚糖本身滲透入釉質層產生抗酸效果與本研究所提及的氟化鈉殼聚糖凝膠抗酸原理不同,本研究中的氟化鈉殼聚糖凝膠與殼聚糖空白凝膠的抗酸效果有統計學差異,且氟化鈉殼聚糖凝膠抗酸性能更好,這一效果提示其抗酸效果來自氟化物。
釉質的檢測方法有其多樣性,主要分為定量檢測和定性檢測[17]。SEM和EDS的聯合使用,使定性和定量的研究很好地結合在一起。在抗酸蝕的過程中,肉眼對于釉質表面的變化的觀察,在臨床應用中起到大致的指導性說明作用。乳牙牙釉質薄,平均約1 mm左右,打磨拋光制成標準試件則表面的釉質層可能已經剝脫,所以選用化學檢測這一經典方法,可以更明確地指出氟化鈉殼聚糖凝膠抗酸蝕的能力。
R?lla、Saunders等[18-19]的實驗證實,氟化物具有保護牙體硬組織免于酸蝕傷害的作用,雖然也有文獻指出氟化物的保護作用有限[20],但大多數的文獻支持的結論與我們研究的結果相似,殼聚糖凝膠作為載體很好地使氟化物與釉質接觸和反應,氟化鈉殼聚糖凝膠具有4 h的持續釋放能力,持續高濃度的氟化鈉提高了釉質的抗酸蝕能力。
氟化鈉殼聚糖凝膠處理后的乳前牙釉質,與金標準的多樂氟達到了一致的抗酸能力;所以氟化鈉殼聚糖凝膠有望作為防治乳牙早期齲的藥物,并應用于臨床。

