“即刻法”卡馬西平治療藥物監測的室內質量控制及藥學實踐
吳妍,李會婷,張哲弢,史天陸
[中國科學技術大學附屬第一醫院(安徽省立醫院)藥劑科,合肥 230001]
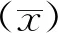
1 材料
1.1儀器 LC-2010A HT島津高效液相色譜儀(紫外檢測器,四元低壓泵,自動進樣器,LabSolutions Version 5.51色譜工作站);TGL-16B高速臺式離心機(上海安亭科學儀器廠);L2-6K臺式低速離心機(湖南可成儀器設備有限公司);FA2004B電子天平(上海精科天美科學儀器有限公司,感量:0.000 1 g);XH-C渦旋混合器(金壇區白塔新寶儀器廠);氮吹儀(上海皓莊儀器有限公司,型號:PBC-B2);移液器(規格:10,100及1000 μL,DRAGONLAB)。
1.2試劑 CBZ對照品(CAS#:100142-201105,批號:8RBB-6M7R,規格:100 mg,含量:99.7%)、奧硝唑對照品(ID:4QRY-WNB1,批號:100608-201102,規格:100 mg,含量:99.8%)以上均由中國食品藥品檢定研究院提供;三乙胺(批號:20130918,規格:500 mL,純度:分析純)、二氯甲烷(批號:20160822,規格:500 mL,純度:分析純),以上均由國藥集團化學試劑有限公司提供;磷酸二氫鉀(批號:180515,規格:500 g,純度:分析純,無錫市展望化工試劑有限公司);滅菌注射用水(批號:2004213201,規格:500 mL,石家莊四藥有限公司);色譜甲醇(批號:180702,規格:500 mL,純度:色譜純,西隴科學股份有限公司);醫用高純度氮氣(N2)。
2 方法與結果
2.1色譜條件 參考相關文獻[11],并結合實驗室工作實際,最終確定如下色譜條件,色譜柱:依利特Hypersil ODS(4.6 mm×250 mm,5 μm),流動相:甲醇:0.05 mol·L-1磷酸二氫鉀溶液=40:60,柱溫:30 ℃,檢測波長:210 nm,流速:1.0 mL·min-1,進樣量:20 μL。
2.2CBZ、奧硝唑工作液配制 精密稱取CBZ對照品5.0 mg至1.5 mL一次性離心管中,加1 mL色譜甲醇溶解得5 mg·mL-1CBZ儲備液。取適量色譜甲醇,依次將儲備液稀釋為5,10,20,40,80,100及160 μg·mL-1的系列濃度 CBZ工作液,儲存于-20 ℃冰箱備用。 另外精密稱取奧硝唑對照品5.0 mg至1.5 mL一次性離心管中,加1 mL色譜甲醇溶解得5 mg·mL-1奧硝唑儲備液。取適量色譜甲醇,將儲備液稀釋為1 mg·mL-1奧硝唑工作液,儲存于-20 ℃冰箱備用。
2.3自制CBZ血漿質控品 取健康人血漿90 μL,分別加入5,10,20,40,80,100及160 μg·mL-1的CBZ工作液10 μL,得新鮮配制的自制CBZ血漿質控品,濃度分別為0.5,1,2,4,8,10及16 μg·mL-1。
2.4即刻法室內質量控制
2.4.1標準曲線 取“2.3”項下系列濃度質控品分別加奧硝唑工作液5 μL,振蕩30 s后加二氯甲烷1 mL,渦旋操作3 min,劇烈振蕩約200次,5000 r·min-1離心5 min(r=6 cm),取下層澄清液于另一一次性離心管,50 ℃氮氣(N2)吹干,經甲醇100 μL溶解殘渣,渦旋1 min,10 000 r·min-1離心5 min(r=6 cm),取上清液60 μL,按“2.1”項色譜條件進樣分析,記錄峰面積。待測質控品標示濃度(X, μg·mL-1)作為橫坐標,CBZ與內標峰面積比值(Y)作為縱坐標,進行線性回歸分析,得回歸方程Y=0.077 7X-0.002 1(r=0.999 4)。該結果表明,CBZ血藥濃度檢測線性范圍為0.5~16 μg·mL-1。典型色譜圖見圖1。
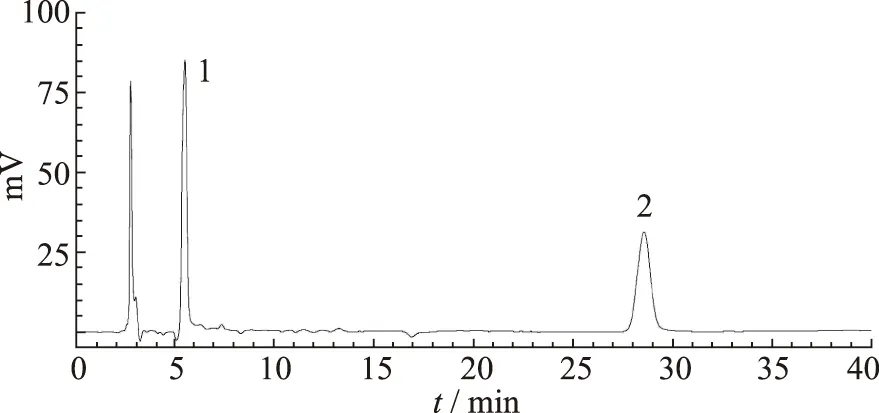
1.奧硝唑;2.卡馬西平。圖1 CBZ質控品HPLC色譜圖1.ornidazole;2.carbamazepine.Fig.1 HPLC chromatogram of carbamazepine quality control product
2.4.2精密度及提取回收率試驗 取新鮮配制高(10 μg·mL-1)、中(4 μg·mL-1)及低(1 μg·mL-1)濃度自制CBZ質控品,經“2.4.1”項方法進行血樣預處理后,吸取上清液60 μL,按“2.1”項色譜條件進樣分析。重復該步驟平行操作6次,計算得高、中及低濃度CBZ質控品日內精密度相對標準偏差(relative standard deviation,RSD)分別為2.47%,3.21%,6.34%。連續操作3 d,計算得日間精密度RSD分別為2.07%,5.35%,7.55%。與此同時,配制對應高、中及低濃度不含生物基質的CBZ對照品溶液(甲醇溶解),按“2.1”項色譜條件進樣。將質控品測得的信號強度與相同濃度標準溶液所測得的信號強度進行比較。每天平行操作6次,計算得CBZ高、中及低濃度質控品日內提取回收率分別為(72.18±3.01)%,(75.58±4.98)%及(65.15±2.18)%。連續操作3 d,計算得日間提取回收率分別為(73.73±7.24)%,(75.69±3.36)%及(69.76±5.17)%。具體見表1。試驗結果符合2015年版《中華人民共和國藥典》(四部)要求[12]。
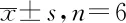
表1 CBZ質控品血藥濃度監測的精密度及提取回收率 Tab.1 Precision and extraction recovery rate of carbamazepine quality control produt's concentration
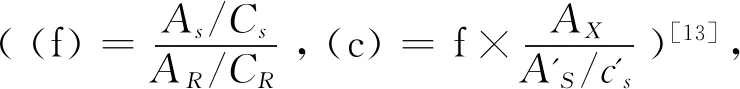
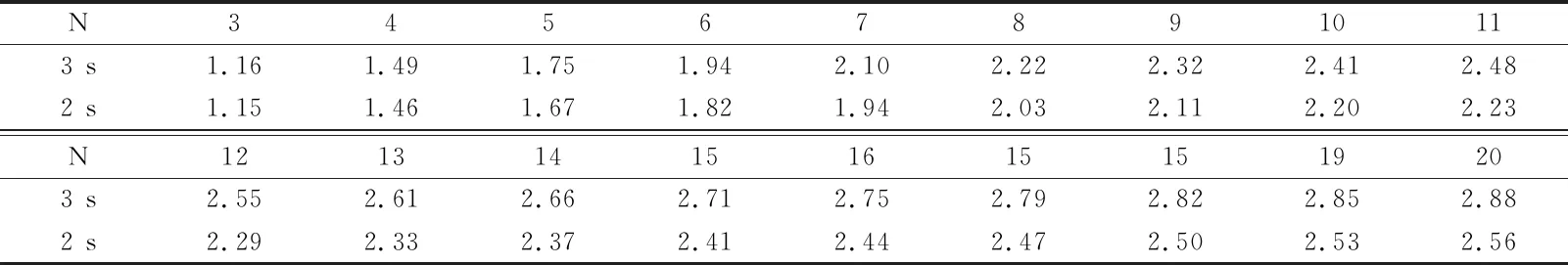
表2 即刻法SI界值Tab.2 Seperation index community of instant method
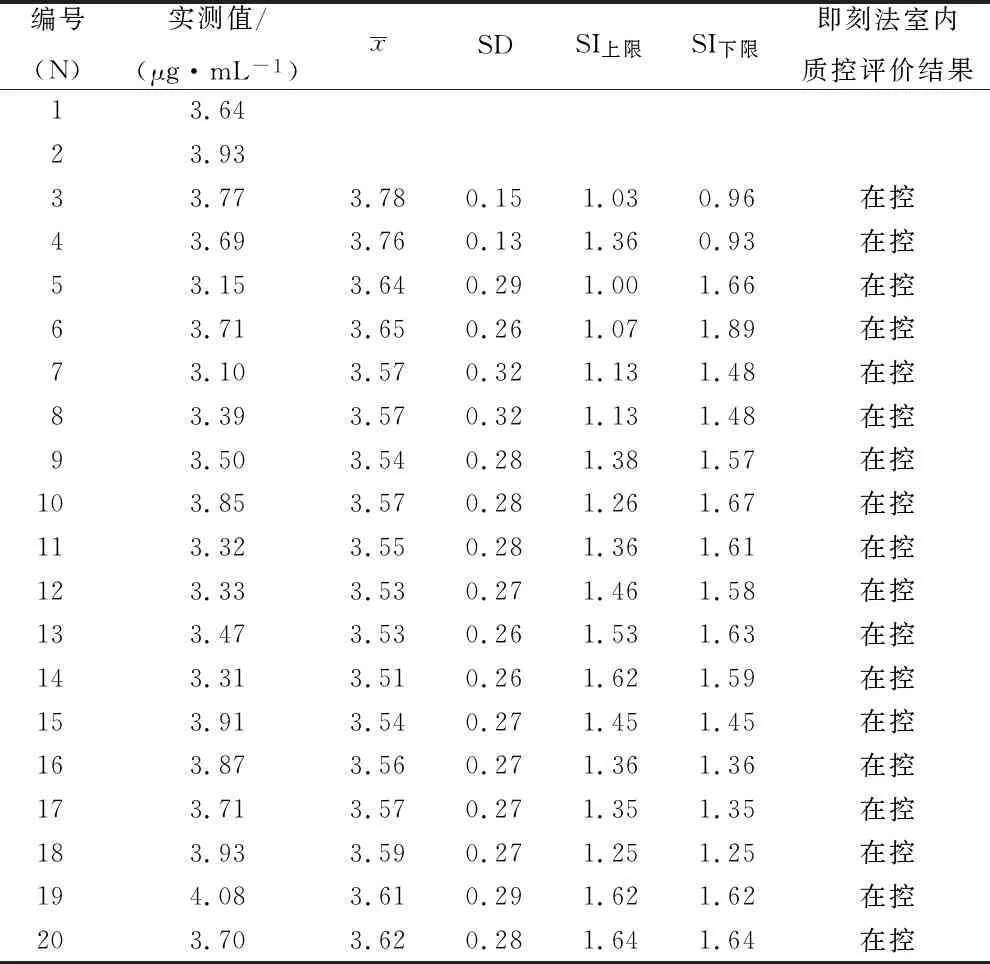
表3 CBZ治療藥物監測的即刻法室內質控數據 Tab.3 Internal quality control data of instant method for therapeutic drug monitoring of carbamazepine
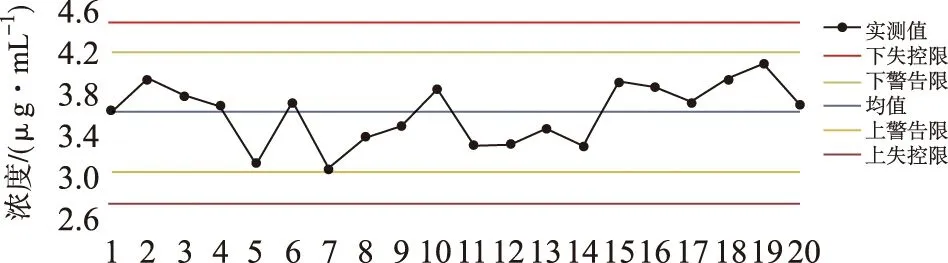
圖2 CBZ治療藥物監測的室內質控圖Fig.2 Internal quality control chart for therapeutic drug monitoring of carbamazepine
2.5CBZ治療藥物監測的藥學實踐
2.5.1患者基本信息 患者,男,70歲。2019年5月15日因“發作性四肢抽搐2 h”就診我院神經內科,入院診斷為“癥狀性癲癇、多發性腦梗死、高血壓病3期、2型糖尿病”。
2.5.2診療過程 2019年5月15日醫囑給予CBZ 0.2 g,bid,長期抗癲癇治療,住院期間癲癇未再發作;2019年5月21日監測CBZ穩態谷濃度5.05 μg·mL-1(隨行質控品實測值為3.64 μg·mL-1,該點為即刻法室內質控的第一個點,即N=1),癥狀好轉后出院。
2019年12月31患者因“發作性四肢抽搐4 h”再次入院,家屬代訴出院后遵醫囑長期規律服用CBZ 0.2 g,bid,次日早晨監測卡馬西平穩態谷濃度為6.22 μg·mL-1(隨行質控品實測值為3.39 μg·mL-1,N=8,N2s=2.03,計算即刻法SI上限=1.13,SI下限=1.48),臨床醫師考慮CBZ單藥抗癲癇效果不佳,2020年1月1日醫囑卡馬西平0.2 g,bid,聯合拉莫三嗪25 mg,bid,抗癲癇,癥狀好轉后出院。
2020年4月5日患者再次因“發作性四肢抽搐4 d”入院,家屬代訴出院后遵醫囑長期規律服用CBZ 0.2 g,bid,聯合拉莫三嗪25 mg,bid。病程中患者癲癇反復發作,尚有胡言亂語、精神障礙,高級皮層功能障礙,且有發熱。考慮病情較重,立即完善頭顱磁共振、腦脊液檢查,排除中樞神經系統感染可能,予以苯巴比妥 0.1g,im,q8h控制癲癇癥狀;2020年4月6日早晨監測CBZ 穩態谷濃度4.79 μg·mL-1(隨行質控品實測值為3.5 μg·mL-1,N=9,N2s=2.11,計算即刻法SI上限=1.38,SI下限=1.57);2020年4月7日予以調整口服抗癲癇藥物方案為CBZ 0.2 g,tid,聯合拉莫三嗪100 mg,qd;2020年4月14日早晨監測CBZ穩態谷濃度3.35 μg·mL-1(隨行質控品實測值為3.85 μg·mL-1,N=10,N2s=2.20,計算即刻法SI上限=1.26,SI下限=1.67);住院期間患者癲癇癥狀逐步控制,逐漸減量苯巴比妥至2020年4月18日停用。2020年4月20日臨床醫師考慮患者病情平穩,建議繼續維持CBZ 0.2 g,tid聯合拉莫三嗪100 mg,qd,口服抗癲癇藥物方案后出院。
2.5.3藥學實踐分析 基于TDM監測數據,2020年1月1日—2020年4年6日患者CBZ用量0.2 g,bid未調整,穩態谷濃度卻下降至4.79 μg·mL-1;2020年4月7日—2020年4月14日患者CBZ用量由0.2 g,bid增加至0.2 g,tid,穩態谷濃度仍持續下降,直至低于正常參考值下限,詳見圖3,但患者癲癇癥狀控制尚可,并未再次發作。臨床醫師希望藥師協助分析產生該現象的原因。
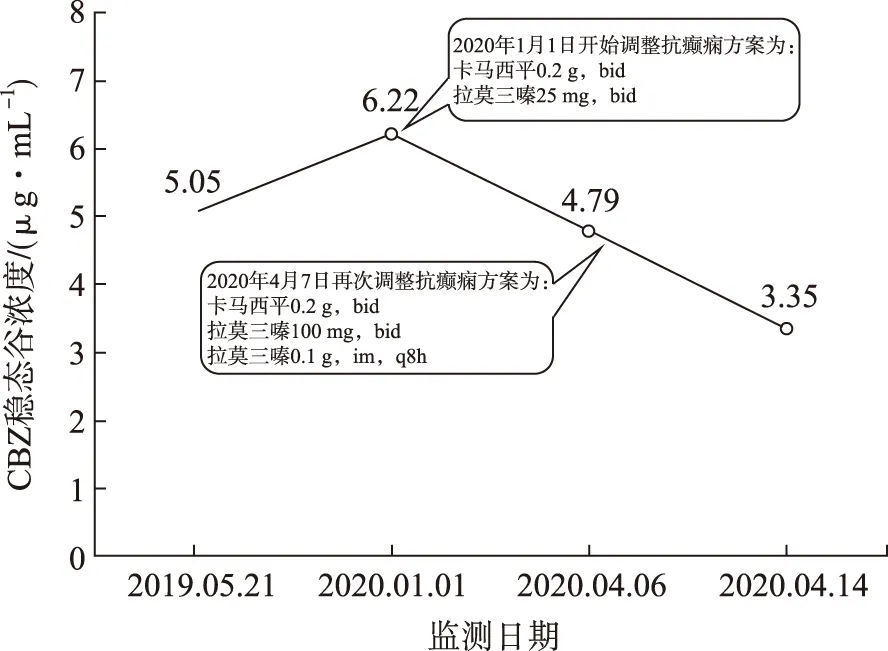
圖3 CBZ血藥濃度變化趨勢圖Fig.3 Trend chart of carbamazepine plasma concentration
依據“即刻法”室內質控評價理論,該患者4次CBZ血藥濃度監測的隨行質控品SI上限、SI下限均小于所對應SI界值表的N2s,表明實測值結果在控,提示血藥濃度監測數據準確。藥師通過與患者家屬進行溝通,排除了用藥依從性對血藥濃度造成的影響,分析導致患者CBZ穩態谷濃度持續降低的可能因素:CBZ口服吸收完全,80%經肝臟CYP3A4代謝為具有類似藥理作用的活性代謝產物10,11-環氧卡馬西平(carbamazepine epoxide,CBZ-E)[15-16]。CBZ與苯巴比妥均為CYP3A4誘導劑[15]。研究證實,卡馬西平可通過自身誘導作用,使其半衰期從35 h縮短為10~20 h[17]。有報道某患者長期服用卡馬西平,最初測得CBZ穩態血藥濃度為7.19 μg·mL-1,堅持原方案服藥,4個月后復測CBZ穩態血藥濃度僅2.53 μg·mL-1[18]。另外,苯巴比妥作為肝藥酶誘導劑,與CBZ聯用亦可加快其代謝,導致CBZ血藥濃度降低[19]。此外,拉莫三嗪作為一種新型廣譜抗癲癇藥物,其雖無明顯的肝藥酶誘導或抑制作用,但據報道難治性癲癇患者在接受原有抗癲癇方案治療至少3個月后,加用拉莫三嗪(平均日劑量200 mg)的所有患者CBZ-E穩態濃度均較前明顯增加,平均增加約16%。與此同時,部分患者CBZ穩態濃度較前降低約10%[20]。提示,拉莫三嗪與CBZ可能存在其他的潛在藥物相互作用,但確切機制尚未明確[20]。
患者出院后,藥師定期進行隨訪,家屬代訴癲癇癥狀控制較好,2021年1月21日門診復查,未訴特殊不適,監測CBZ穩態谷濃度為7.69 μg·mL-1。由此可見,抗癲癇藥物的藥動學特征非常復雜,多藥聯合使用時,開展抗癲癇藥物TDM,加強TDM的室內質控評價體系建設,可為臨床了解抗癲藥物以及合并用藥之間復雜的藥物相互作用提供大量有價值的信息。
3 討論
加強TDM的全面質量控制對于確保實驗數據的準確性意義重大[21]。通常,室間質評可用于反映實驗室測定數據的質量優劣,衡量該實驗室的質量控制效果[22]。室內質控則有助于及時發現實驗過程產生的誤差,確保了室間質評調查成績穩步提高[23]。2000年國際標準化組織專門針對醫學實驗室管理制定了ISO/FDIS15189《醫學實驗室的質量管理》標準,強調應建立實驗室內部質量體系。2001年我國也頒布了適合國情的《醫療機構臨床實驗室質量管理辦法》,逐步對臨床實驗室的室內質量控制實施全面管理。2019年《治療藥物監測工作規范專家共識(2019版)》正式將室內質控納為TDM 質量控制指標之一[24]。但TDM室內質量控制評價尚無統一標準[5]。
隨著分析檢測技術的不斷發展,TDM技術也在不斷推陳出新[5]。目前,國內外在用的CBZ血藥濃度檢測方法包括HPLC法[25]、CMIA法[26]、熒光偏振免疫分析法(fluorescence polarization immunoassay,FPIA)法[27]以及靈敏度更高的液相色譜-串聯質譜(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法[28]等。為確保不同TDM方法之間良好的相關性,促進監測結果的準確轉換,協助臨床醫師可參考不同TDM方法的監測數據制定最佳給藥方案。建立有效的TDM室內質量控制評價方法顯得尤為重要。課題組前期基于Westgard多規則理論,通過繪制Levey-Jennings質控圖建立了拉莫三嗪治療藥物監測的室內質量控制體系[10]。但是,筆者所在醫院用HPLC法監測CBZ血藥濃度的樣本量較少,同批次質控品短時間內連續監測20次難度較大。因此,不適宜采用Levey-Jennings質控圖開展室內質控,“即刻法”優點則在于同批號質控品只要連續測定3次,即可對第3次及以后的數據進行在控與失控狀態評價[4]。故本研究探索性使用“即刻法”進行CBZ治療藥物監測的室內質控并開展藥學實踐。查閱文獻發現,目前將室內質控評價理論應用于TDM的藥學服務實踐報道較少。諶介秀等[29]首次將質控圖聯合Westgard多規則法應用于1例腎移植術后長期接受他克莫司抗排斥治療特殊案例,分析了造成兩家醫療機構測定同一血漿樣品他克莫司血藥濃度測定結果不一致的原因,減少了他克莫司治療藥物監測的誤差,提高了醫師和患者對TDM結果的信任度。本研究結合實驗室CBZ隨行質控品監測數據,基于1例癥狀性癲癇患者HPLC法CBZ血藥濃度值波動的案例,應用“即刻法”進行室內質量控制評價,有效保證了監測結果準確性、可靠性。
當然,采用“即刻法”進行室內質控也存在一定的缺陷,即“遲后異常值”現象[3]。表現為在測定次數相對較少時,有些失控的離群值不會顯示為警告點,但隨著測定次數的增加,測定值逐漸趨于穩定后,以前未顯示的離群值將會暴露出來,顯示為警告甚至失控的狀態。因此,應結合“即刻法”室內質控圖及時觀察質控曲線的趨勢性變化,考慮諸多主、客觀因素可能造成的影響,做好日常工作中質量控制培訓,嚴格執行標準化操作流程。總之,課題組結合所在實驗室HPLC法CBZ治療藥物監測的送檢樣本量情況,量體裁衣,制定了“即刻法”室內質量控制評價體系,具有較強的臨床適用價值,建議針對臨床必需、但監測頻次相對較低的血藥濃度監測項目推廣應用。

