注射用培美曲塞二鈉包裝系統密封性檢查的方法學驗證報告
王進宇


摘要:注射劑包裝系統密封性檢查方法分來概率性方法和確定性方法兩大類,其中概率性方法包括:微生物挑戰法(浸入或氣溶膠法)、色水法、氣泡釋放法,選用何種方法均需進行適當的方法學驗證,本文就注射用培美曲塞二鈉選用概率性方法(色水法)的驗證報告展開綜述。
關鍵詞:培美曲塞二鈉;包裝系統密封性;驗證報告
【中圖分類號】 F763 【文獻標識碼】 A ? ? ? 【文章編號】2107-2306(2022)06--02
前言:注射劑包裝系統密封性檢查是產品無菌保障的關鍵檢查步驟,因此其測試方法必須經過方法驗證。注射用培美曲塞二鈉(規格500 mg)為凍干粉針劑,西林瓶加塞軋鋁蓋密封包裝,本文采用亞甲基藍色水浸入,結合紫外分光光度計方法對西林瓶密封性進行檢測,現對驗證結果進行匯總報告。
1 分析方法
1.1樣品制備
陽性對照:分別取注射用培美曲塞二鈉藥品5瓶,加水制成樣品濃度約為20 mg/mL,再將2 μm的微孔導管穿過膠塞垂直插入瓶內作為陽性對照(插孔位置為內圈)。
待測試樣品:用注射器向待測試樣品注射用培美曲塞二鈉的西林瓶中加入定量的水制成樣品濃度約為20 mg/mL。檢測數量根據具體的產品穩定性考察方案確定,確保待測試樣品的代表性。
1.2試液的配制
0.1%亞甲基藍溶液:稱取1g亞甲基藍置1000 mL水中,溶解混勻。可根據使用量,按比例適當增加配制量。
1.3測試條件
將待測試樣品和陽性對照固定好后倒置,放入含有0.1%亞甲基藍溶液的真空密封性測試儀中,溶液沒過全部試樣的底部。然后抽真空至真空度為90 kPa,維持30min,待真空裝置恢復至常壓保壓30 min,繼續倒置加壓120 kPa,維持30 min,恢復至常壓保持20 min。
1.4觀察方法
紫外可見分光光度法:取出所有樣品,用水沖洗瓶外壁,帶蓋上下振搖20次混勻,以水為空白,在664 nm波長下檢測紫外吸收。記錄吸光度值。(若為穩定性樣品,空白采用相同劑量的樣品加入等量在注射用水稀釋作為空白)。
1.5結果標準
紫外可見分光光度法檢測:陽性對照的吸光度值應大于空白,待測試樣品吸光度值應與空白一致。
2 方法驗證
2.1驗證范圍
該方法為定性的方法,根據USP<1225>,僅進行專屬性、檢測限以及耐用性的驗證。驗證范圍及可接受標準如下表。
表1驗證范圍及可接受標準
驗證范圍 可接受標準
專屬性 空白應無干擾,陰性應無干擾:即陰性對照吸光度值應與空白一致,陽性對照瓶中的吸光度應大于陰性對照。
紫外分光光度法檢測限 直接法:將亞甲基藍樣品溶液不斷稀釋后,在664 nm測量吸光度,吸光度大于0.001時的濃度。
方法檢測限 制備1 μm, 2 μm, 3.75μm , 5 μm的微孔導管陽性對照,確定最小檢測限(方法能檢測出的最小泄漏)。
耐用性 陽性對照瓶中的吸光度應大于陰性對照,陰性吸光度值應與空白一致。
2.2試劑試液、標準品與樣品
本次驗證過程中用到的試劑試液、標準品與樣品:0.1%亞甲基藍溶液,批號:20200615-03 ? 來源:自制,效期:2020.12.14;注射用培美曲塞二鈉,規格500mg,來源:自產;陽性對照:(1 μm, 2 μm, 3.75 μm, 5 μm) ,來源:上海眾林。
2.3檢驗設備
本次驗證過程中用到的檢驗設備:密封性測試儀,設備編號:I-181,校驗有效期:2020.08.26
氣密性測試儀,設備編號:I-185,校驗有效期:2020.10.01;紫外可見分光光度計,設備編號:I-118,校驗有效期:2020.10.23
2.4驗證內容
2.4.1專屬性
2.4.1.1樣品制備
分別取注射用培美曲塞二鈉(500mg)10瓶(瓶號1~10)。打開封口,加入25 mL水,制成樣品濃度約為20 mg/mL;)。
陰性對照:瓶號1~5,不做任何處理。
陽性對照:瓶號6~10采用3.75 μm的微孔導管通過膠塞垂直插入瓶內(插孔位置為內圈)。
空白溶液:取注射用培美曲塞二鈉(500mg)加25mL水溶解,亦可根據使用需要等比例配制。
2.4.1.2試液配置
0.1%亞甲基藍溶液:稱取1 g亞甲基藍置1000 mL水中,溶解混勻。可根據使用量,按比例適當增加配制量。
2.4.1.3測試條件
將所有陽性對照、陰性對照固定好后倒置放入含有0.1%的亞甲基藍的真空密封性測試儀中,溶液沒過所有試樣。然后抽真空至真空度為90 kPa,維持30 min,待真空裝置恢復至常壓保壓30 min,繼續倒置加壓120 kPa,維持30 min,恢復至常壓保持20 min。
2.4.1.4測試方法
紫外可見分光光度法:取出所有樣品,用水沖洗瓶外壁,帶蓋上下振搖20次混勻。以檢測空白(樣品濃度約為20 mg/mL),在664 nm出檢測紫外吸收,記錄吸光度值。
2.4.1.5可接受標準
空白應無干擾,陰性應無干擾:即3.75 μm的所有陽性對照瓶中的吸光度應大于空白。
陰性吸光度值應與空白一致。
2.4.1.6驗證結果與結論:
專屬性驗證結果見下表:
結論:通過上表可知陰性樣品吸光度與空白吸光度基本一致,陽性對照吸光度大于空白,說明空白無干擾,陰性亦無干擾,專屬性符合方案要求。
2.4.2紫外分光光度法的檢測限
2.4.2.1樣品制備:
空白溶液:取4瓶注射用培美曲塞二鈉加水容解并稀釋,制成樣品濃度約為20 mg/mL的空白溶液。
檢測限溶液:精密量取0.1%的亞甲基藍溶液1 mL到1000 mL的容量瓶中,用水稀釋至刻度制成1 ppm的儲備溶液A,精密量取0.5 mL儲備溶液A至10 mL的容量瓶中,用空白溶液稀釋至刻度制成0.05 ppm的儲備液B,精密量取儲備液B 0.8 mL至10 mL 容量瓶中,用空白溶液稀釋至刻度得0.004 ppm的檢測限溶液。
2.4.2.2測試方法:
紫外檢測限:在664 nm測試吸光度,以空白溶液為空白,測定檢測限溶液的吸光度。
2.4.2.3可接受標準
吸光度大于0.001時的最小亞甲基藍樣品溶液的濃度。
2.4.2.4驗證結果及結論
空白吸光度為0.0002, 檢測限濃度(0.004 ppm)的吸光度為0.0013大于0.001
結論:紫外分光光度法檢測限的濃度為0.004 ppm
2.4.3密封性方法檢測限
2.4.3.1樣品制備
分別取注射用培美曲塞二鈉20瓶(瓶號1~20)。打開封口,加水制成樣品的濃度約為20 mg/mL。
陽性對照:打開塑料封口,瓶號1~5采用1 μm的微孔導管通過膠塞垂直插入瓶內; 瓶號6~10采用2 μm的微孔導管通過膠塞垂直插入瓶內;瓶號11~15采用3.75 μm的微孔導管通過膠塞垂直插入瓶內;瓶號16~20采用5 μm的微孔導管通過膠塞垂直插入瓶內,所以插孔位置均為膠塞內圈。
檢測空白:同2.4.1.1空白溶液的制備
2.4.3.2試液配置
0.1%亞甲基藍溶液:稱取1 g亞甲基藍置1000 mL水中,溶解混勻。可根據使用量,按比例適當增加配制量。
2.4.3.3測試條件
將所有陽性對照固定好后倒置放入含有0.1%的亞甲基藍的真空密封性測試儀中,溶液沒過所有試樣。然后抽真空至真空度為90 kPa,維持30min,待真空裝置恢復至常壓保壓30 min,繼續倒置加壓120 kPa,維持30min,恢復至常壓保持20 min。
2.4.3.4測試方法
取出所有樣品,用水沖洗瓶外壁,帶蓋上下振搖20次混勻。以檢測空白為空白,在664 nm檢測紫外吸收,記錄吸光度值。
2.4.3.5可接受標準:
陽性對照溶液吸光度值大于等于檢測限吸光度的最小孔徑即為最小檢測泄漏孔徑。
2.4.3.6驗證結果及結論
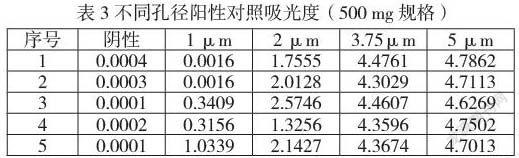
結論:根據紫外分光光度法的檢測限可知,檢測限的吸光度為0.0013。從表3可知,所有孔徑陽性的吸光度均大于檢測方法的檢測限,但由于1 μm的重現性較差,有接近于檢測限的情況(0.0016),而2 μm以上的孔徑重現性良好,且大于方法檢測限,故密封性測試方法的檢測限為2 μm。
2.4.4耐用性
2.4.4.1樣品配制
陽性對照:取注射用培美曲塞二鈉5瓶(瓶號1~5),打開塑料封口,按照2.4.1.1陽性樣品制備過程將3.75 μm的微孔導管通過膠塞垂直插入(插孔位置為內圈)。
陰性對照:取注射用培美曲塞二鈉5瓶(瓶號6~10),按照2.4.1.1陰性樣品制備過程制備。
2.4.4.2試液配置
0.1%亞甲基藍溶液:稱取1 g亞甲基藍置1000 mL水中,溶解混勻。可根據使用量,按比例增加配制量。
2.4.4.3測試條件
條件1:將陽性對照、陰性對照固定好后倒置放入含有0.1%的亞甲基藍的真空密封性測試儀中,溶液沒過所有試樣。然后抽真空至真空度為85 kPa,維持25 min,待真空裝置恢復至常壓保壓25 min,繼續倒置加壓115 kPa,維持25 min,恢復至常壓保持15 min。
條件2:將陽性對照、陰性對照固定好后倒置放入含有0.1%的亞甲基藍的真空密封性測試儀中,溶液沒過整個所有試樣。然后抽真空至真空度為95 kPa,維持35 min,待真空裝置恢復至常壓保壓35 min,繼續倒置加壓125 kPa,維持35 min,恢復至常壓保持25 min。
2.4.4.4測試方法
取出所有樣品,用水沖洗瓶外壁,帶蓋上下振搖20次混勻。以檢測空白為空白,在664 nm檢測紫外吸收,記錄吸光度值。
2.4.4.5可接受標準:
所有陽性對照瓶中的吸光度應大于陰性對照,陰性吸光度值應與空白一致。
2.4.4.6驗證結果及結論
結論:從以上表格可知,變動不同條件的情況下,所有陽性對照瓶中的吸光度均大于陰性對照,陰性吸光度值與空白基本一致,該方法的耐用性符合可接受標準
3 .偏差調查
驗證過程中未發生偏差。
4. 驗證總結論
通過上述各項目的驗證結果綜合評價,該注射用培美曲塞二鈉(500mg)包裝系統密封性測試方法(色水法)的專屬性、紫外分光光度法檢測限、方法檢測限、耐用性均符合驗證預期要求,可用于該產品的包裝系統密封性檢查。
參考文獻:
[1] 國家藥品監督管理局藥品審評中心. 《化學藥品注射劑包裝系統密封性研究技術指南(試行)》(2020年第30號)
[2] 藥品生產質量管理規范(2010年修訂)(衛生部令第79號)
[3]《藥品GMP指南 無菌藥品》中國醫藥科技出版社, 2011.
[4]《藥品生產驗證指南》化學工業出版社, 2003.
[5] USP <1207> Package integrity evaluation-sterile products.
[6] USP <1207.1> Package integrity testing in the product life cycle-test method selection and validation.
[7] USP <1207.2> Package Integrity Leak Test Technologies.
[8] USP<1207.3> Package Seal Quality Test Technologies.
[9] USP <1225> Package integrity evaluation-sterile products.

