基于網絡藥理學與分子對接探究寧心通郁滋腎方治療早發性卵巢功能不全的作用機制
馬佳文 李想 張翼宙
浙江中醫藥大學 杭州 310053
早發性卵巢功能不全(premature ovarian insufficiency,POI)是女性常見的內分泌疾病,是指40歲之前出現卵巢功能減退,臨床表現為月經稀發甚至閉經,嚴重者影響育齡期女性的生育能力[1]。POI在一般人群中的發病率為1%[2],由于女性工作與生活壓力的增大,近年來POI的發病率上升至3.7%[3],上升趨勢明顯。POI如不及時治療,將發展為卵巢早衰(premature ovarian failure,POF),此時卵巢功能衰竭,將出現絕經、生殖器官萎縮等絕經期表現[4],且無法逆轉。因此,POI的治療具有重要的臨床意義。
西醫臨床治療POI一般采用激素替代療法(hormone replacement therapy,HRT)[5],但世界衛生組織國際癌癥研究機構公布的致癌物清單提示,雌激素-孕激素更年期治療(合用),以及雌激素-孕激素口服避孕藥(合用)均屬于1類致癌物。由此可見,該療法存在不容忽視的致癌隱患。中醫學則從“天癸即元陽”和“腎主生殖”等整體思路出發,多靶點協同治療改善卵巢功能。中醫婦科經典著作《傅青主女科》記載了“年未老經水斷”的病證,采用“必須散心之郁,而大補其腎水”[6]的益經湯治療。本研究團隊以《傅青主女科》益經湯為基礎,化裁出寧心通郁滋腎方,研究發現該方對POI患者有較好的臨床療效,但其作用的藥效物質基礎尚不明確,活性成分及關聯性未知,這在一定程度上限制了該方的推廣使用。本研究基于四級桿-靜電軌道阱(Q exactive orbitrap,Q-Orbitrap)高分辨液質聯用系統分析結果,采用網絡藥理學方法對寧心通郁滋腎方治療POI的活性成分和作用靶點進行篩選,結合分子對接技術,為深入研究寧心通郁滋腎方的作用機制及藥效物質基礎提供理論依據。
1 材料和方法
1.1 儀器 Q Exactive高分辨質譜儀和UltiMate 3000 RS均購于賽默飛世爾科技有限公司;Direct-Q?5純水/超純水一體機系統購于德國默克密理博公司;D3024R型高速微量冷凍離心機為北京大龍興創實驗儀器有限公司產品;MTV-100多管渦旋混合儀購于杭州奧盛儀器有限公司。
1.2 試劑 中藥材包括熟地黃、龜板、黨參、山藥、酸棗仁、柴胡、菟絲子、當歸、白芍、丹皮等,均購于浙江中醫藥大學附屬第三醫院(批號:20210701、20210827、210601、210701、20210801、210201、20210501、20210702、20210801、20210801);色譜純甲醇購于賽默飛世爾科技有限公司;色譜純甲酸購于上海阿拉丁生化科技股份有限公司。
1.3 實驗方法
1.3.1 Q-Orbitrap高分辨液質聯用分析
1.3.1.1 質譜條件和色譜條件 (1)質譜條件:Q Exactive高分辨質譜儀以電噴霧電離源(electrospray ionization,ESI)為離子源,采用正負離子切換的掃描方式。檢測方式采用full mass/dd-MS2,設置分辨率為70 000(full mass)和17 500(dd-MS2),掃描范圍為150.0~2 000.0 m/z。電噴霧電壓為3.8 kV,毛細管溫度為300℃。碰撞氣采用高純氬氣;鞘氣采用氮氣,體積流量為40 Arb;輔助氣采用氮氣,溫度為350℃。數據采集時間為30 min。
(2)色譜條件:色譜柱為Welch XB-C18(50 mm×2.1 mm,1.8 μm);以0.1%甲酸水溶液(A)-甲醇(B)為流動相,色譜梯度為0~1 min,98%A;1~5 min,80%A;5~10 min,50%A;10~15 min,20%A;15~20 min,5%A;20~25 min,5%A;25~26 min,98%A;26~30 min,98%A;流速為0.30 mL/min;柱溫箱溫度為35℃;自動進樣器溫度為10℃;進樣體積為5 μL。
1.3.1.2 上樣溶液的制備 寧心通郁滋腎方由熟地黃30 g、龜板12 g、黨參12 g、山藥15 g、酸棗仁12 g、柴胡6 g、菟絲子12 g、當歸15 g、白芍12 g、牡丹皮9 g組成。加入8倍質量的單蒸水,覆蓋藥面浸泡30 min,大火煮沸后,小火煎煮40 min,濾出藥液,第2次煎煮法與第1次相同,最后將兩次藥液混合進行濃縮,獲得寧心通郁滋腎方水煎液。取水煎液200 μL,加入80%甲醇溶液1 mL,渦旋10 min。4℃下20 000r/min離心10 min,取上清液并過濾。
1.3.1.3 數據分析 Q-Orbitrap高分辨液質聯用采集的數據通過Compound DiscovererTM2.1軟件完成初步整理后,在mzCloud數據庫進行檢索比對,構建寧心益腎方水煎液成分數據庫。
1.3.2 網絡藥理學分析
1.3.2.1 寧心通郁滋腎方活性成分篩選及潛在靶點預測 通過Q-Orbitrap高分辨液質聯用分析,構建寧心益腎方水煎液成分數據庫,篩選出mzCloud數據庫匹配豐度(mzCloud best match)≥80的化合物。通過PubChem查找化合物的2D結構,并導入Swiss ADME數據庫(http://www.swissadme.ch/)[7]。 初步限定化合物的腸胃吸收度為“High”,以此篩選具有較好生物利用度的活性化合物。再者,篩選五種類藥性(Lipinski、Veber、Ghose、Egan、Muegge) 中有2個及以上為“Yes”的化合物,即為寧心通郁滋腎方中的活性成分。通過Swiss Target Prediction數據庫(http://www.swisstargetprediction.ch/)預測活性成分對應的藥物靶點。可能性(Probability)>0的靶點即為寧心通郁滋腎方的藥物靶點。
1.3.2.2 POI疾病靶點篩選 通過基因組注釋數據平臺(Genome Annotation Database Platform,GeneCard)(https://www.genecards.org/)和在線人類孟德爾遺傳(Online Mendelian Inheritance in Man,OMIM) 數據庫(https://www.omim.org/)得到與POI相關的疾病靶點,并與寧心通郁滋腎方的藥物靶點相匹配,獲取交集靶點。利用Cytoscape 3.8.2軟件構建寧心通郁滋腎方活性成分-交集靶點網絡圖。
1.3.2.3 蛋白互作(protein-protein interaction,PPI)網絡構建 將藥物與疾病的交集靶點導入String數據庫(http://string-db.org/cgi/input.pl),物種選擇為“Homo Sapiens”,置信度設定為0.7,從而構建PPI網絡。 將結果導入Cytoscape 3.8.2軟件,借助Cyto NCA中的度中心性(degree centrality,DC)、中介中心性(betweenness centrality,BC)、接近中心性(closeness centrality,CC)、特征向量中心性(eigenvector centrality,EC)、網絡中心性 (network centrality,NC)、 局部邊連通性(local average connectivity,LAC)等6個參數篩選節點,選取網絡連接度≥2倍中值的節點為關鍵靶點[8]。將關鍵靶點與活性成分對應的結果導入Cytoscape 3.8.2軟件,依據度值篩選出寧心通郁滋腎方治療POI的關鍵活性成分,構建“關鍵靶點-關鍵活性成分”網絡。
1.3.2.4 基因本體(gene ontology,GO)和京都基因與基因組百科全書 (Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析 通過生物學信息注釋數據庫(the Database for Annotation,Visualization and Integrated Discovery,DAVID)(https://david.ncifcrf.gov/)[9],對關鍵靶點進行GO分析和KEGG富集分析,獲取相關的生物學信息,從而分析寧心通郁滋腎方治療POI的可能作用機制。
1.3.3 分子對接 將1.3.2.3中篩選出關鍵靶點和關鍵活性成分依據度值降序排列。選取前8位的關鍵活性成分分別與該成分靶向的、且度值排序前10的關鍵靶點進行分子對接,以此驗證成分-靶點之間的相關性。 在UniPort(https://www.uniprot.org/)、RCSB蛋白數據庫(RCSB Protein Data Bank,RCSB PDB)(https://www.rcsb.org/)、ZINC數據庫(http://zinc.docking.org/)[10]中獲取成分和靶點的三維結構,利用SYBYL-X 2.1.1軟件中的Surflex-Dock進行分子結構對接,獲取對接分數(total score)。
2 結果
2.1 Q-Orbitrap高分辨液質聯用分析結果 本研究采用Q-Orbitrap高分辨液質聯用進行成分分析,中藥復方水煎液的總離子流圖見圖1。相關結果在mzCloud數據庫匹配到812個化合物,依據mzCloud數據庫匹配豐度降序排列。見表1。
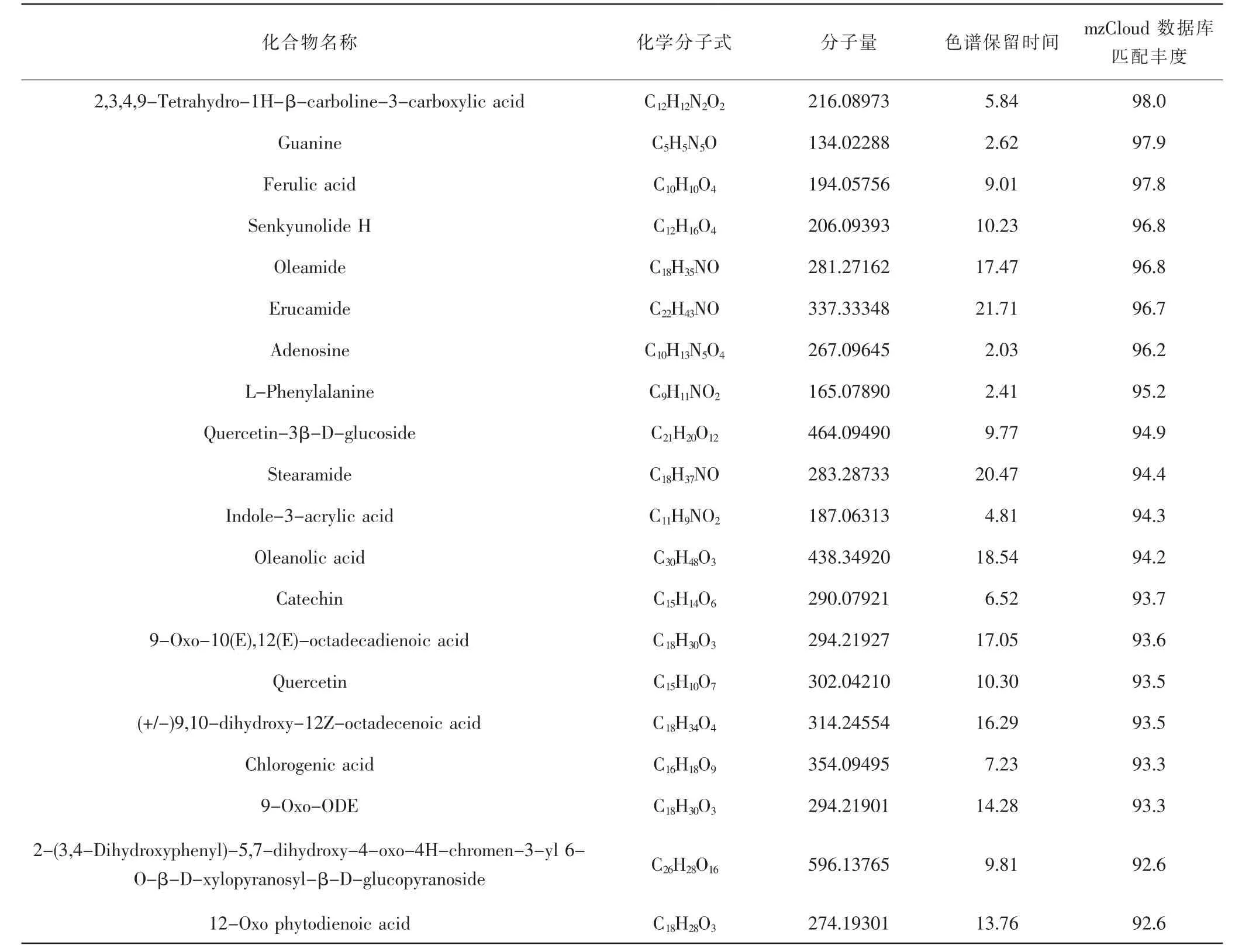
表1 寧心通郁滋腎方水煎液成分表Tab.1 Ingredients of the water extract of Ningxin Tongyu Zishen Formula
2.2 網絡藥理學分析結果
2.2.1 寧心通郁滋腎方活性成分及其靶點 選取寧心通郁滋腎方水煎液中mzCloud數據庫匹配豐度≥80的化合物共113個,根據生物利用度及五種類藥性的限定,最終確定符合標準的中藥活性成分71個。通過Swiss Target Prediction數據庫共查詢到相關靶點7 185個,滿足條件靶點共3 734個,篩選去重后獲得藥物靶點共807個。
2.2.2 寧心通郁滋腎方活性成分-交集靶點網絡圖通過Gene Card和OMIM數據庫共獲得1 143個疾病靶點,將這些疾病靶點與藥物靶點相匹配,共獲得交集靶點176個。利用Cytoscape 3.8.2軟件繪制寧心通郁滋腎方活性成分-交集靶點網絡圖。見圖2。
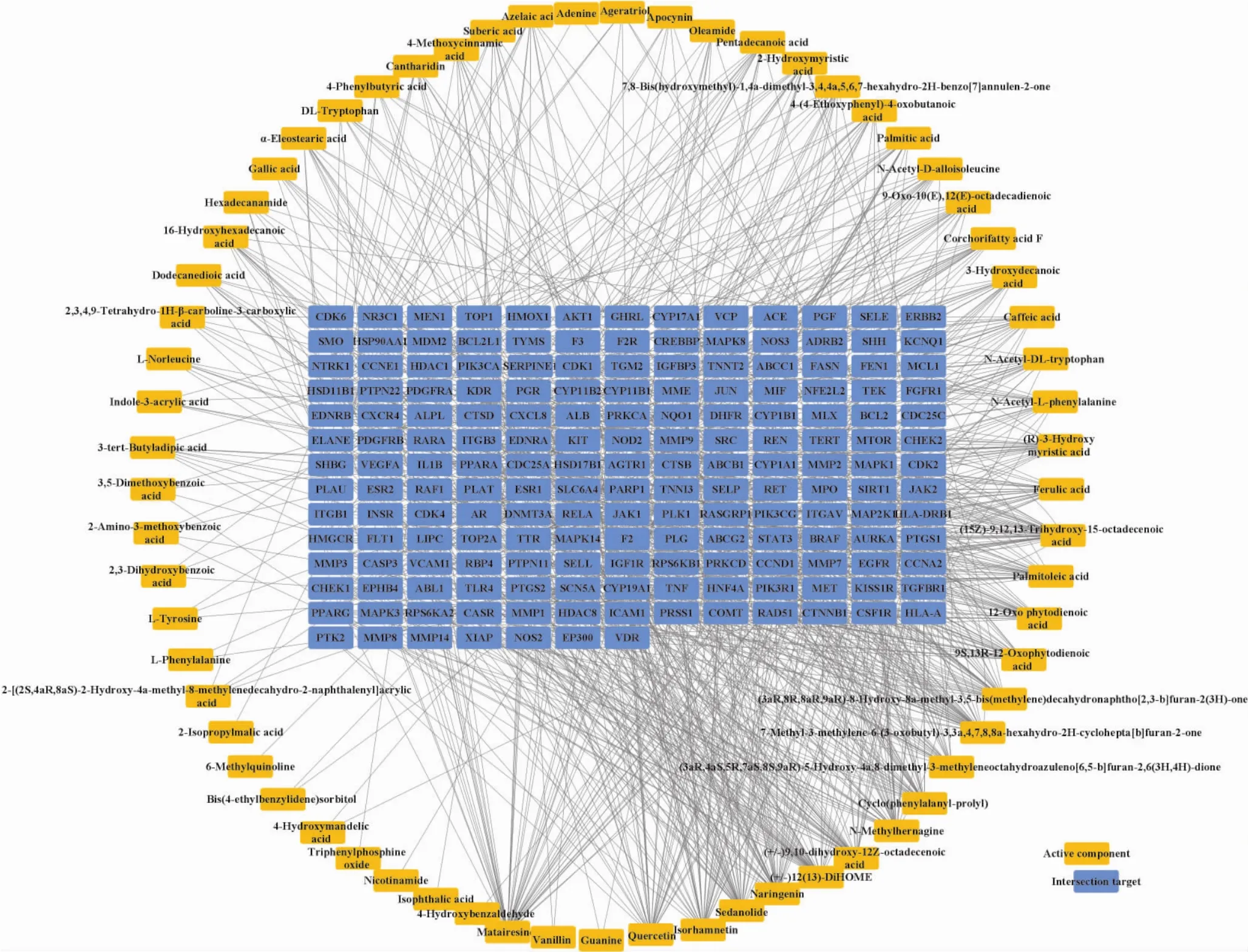
圖2 寧心通郁滋腎方活性成分-交集靶點網絡圖Fig.2 The active component-intersection target network of Ningxin Tongyu Zishen Formula
2.2.3 PPI網絡構建及分析 將176個交集靶點導入String數據庫,依據限定條件構建PPI網絡,共得到176個節點,2 904條邊。見圖3A。將結果導入Cytoscape 3.8.2軟件進行篩選后,共獲得關鍵靶點39個,并依據度值進行排序。見圖3B、C。這39個關鍵靶點即寧心通郁滋腎方治療POI的關鍵靶點。將關鍵靶點與對應化合物導入Cytoscape 3.8.2軟件進行網絡構建,共獲得55種關鍵活性成分。見圖4。依據度值降序,前8種關鍵活性成分認定為主要關鍵活性成分,分別為槲皮素(Quercetin)、 異鼠李素(Isorhamnetin)、 瑟丹內酯(Sedanolide)、咖啡酸(Caffeic acid)、柚皮素(Naringenin)、 羅漢松脂素(Matairesinol)、 阿魏酸(Ferulic acid)、棕櫚油酸(Palmitoleic acid)。
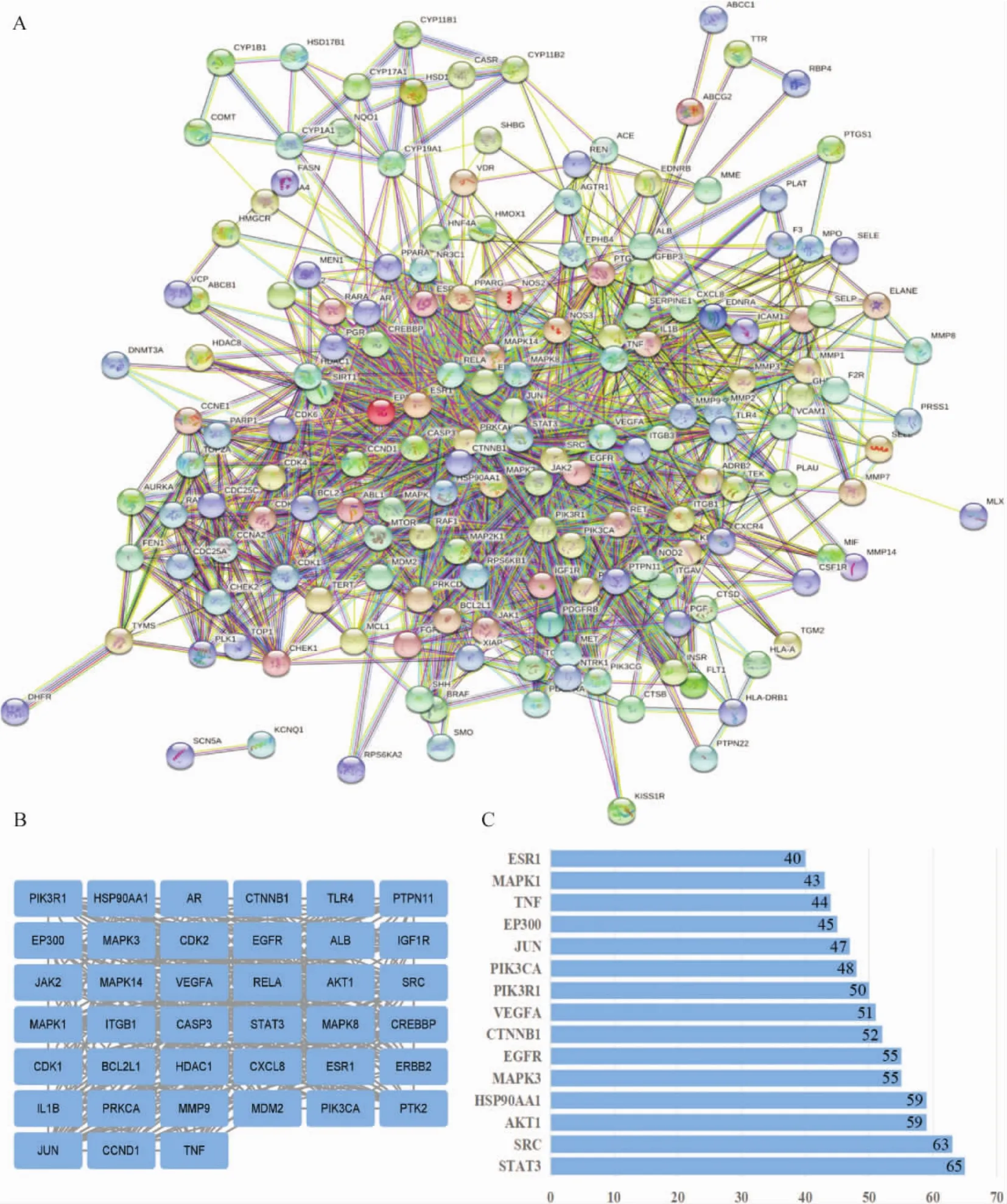
圖3 PPI網絡及關鍵靶點篩選圖Fig.3 PPI network and the key target screening map
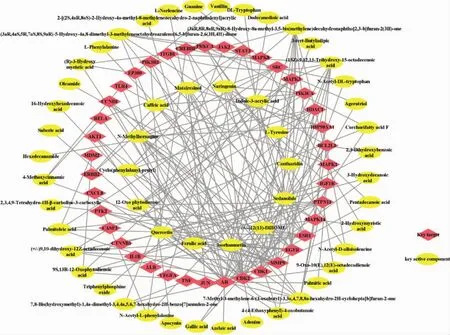
圖4 關鍵靶點-關鍵活性成分網絡圖Fig.4 key target-key active component network
2.2.4 GO分析 將寧心通郁滋腎方治療POI的39個關鍵靶點導入DAVID數據庫進行GO分析,以P<0.05為篩選標準,對GO分析獲取的生物學過程(biological process,BP)、細胞組 分 (cellular component,CC)、分子功能(molecular function,MF)的數據分別進行升序排列,并選取其中排名前15位者繪制富集氣泡圖。見圖5。結果顯示,寧心通郁滋腎方主要通過細胞液(cytosol)、細胞質(cytoplasm)、核質(nucleoplasm)、蛋白復合體(protein complex)、細胞核(nucleus)等細胞組分參與凋亡過程的負調控 (negative regulation of apoptotic process)、一氧化氮生物合成過程的正調控(positive regulation of nitric oxide biosynthetic process)、蛋白磷酸化正調控(positive regulation of protein phosphorylation)、RNA聚合酶Ⅱ啟動子的轉錄正調控(positive regulation of transcription from RNA polymerase Ⅱ promoter)、轉錄的正調控-DNA模板(positive regulation of transcription-DNA-templated)等生物過程,發揮酶結合(enzyme binding)、轉錄因子結合(transcription factor binding)、相同蛋白結合(identical protein binding)、激酶活性(kinase activity)、蛋白結合(protein binding)等分子功能,起到改善卵巢功能,治療POI的作用。
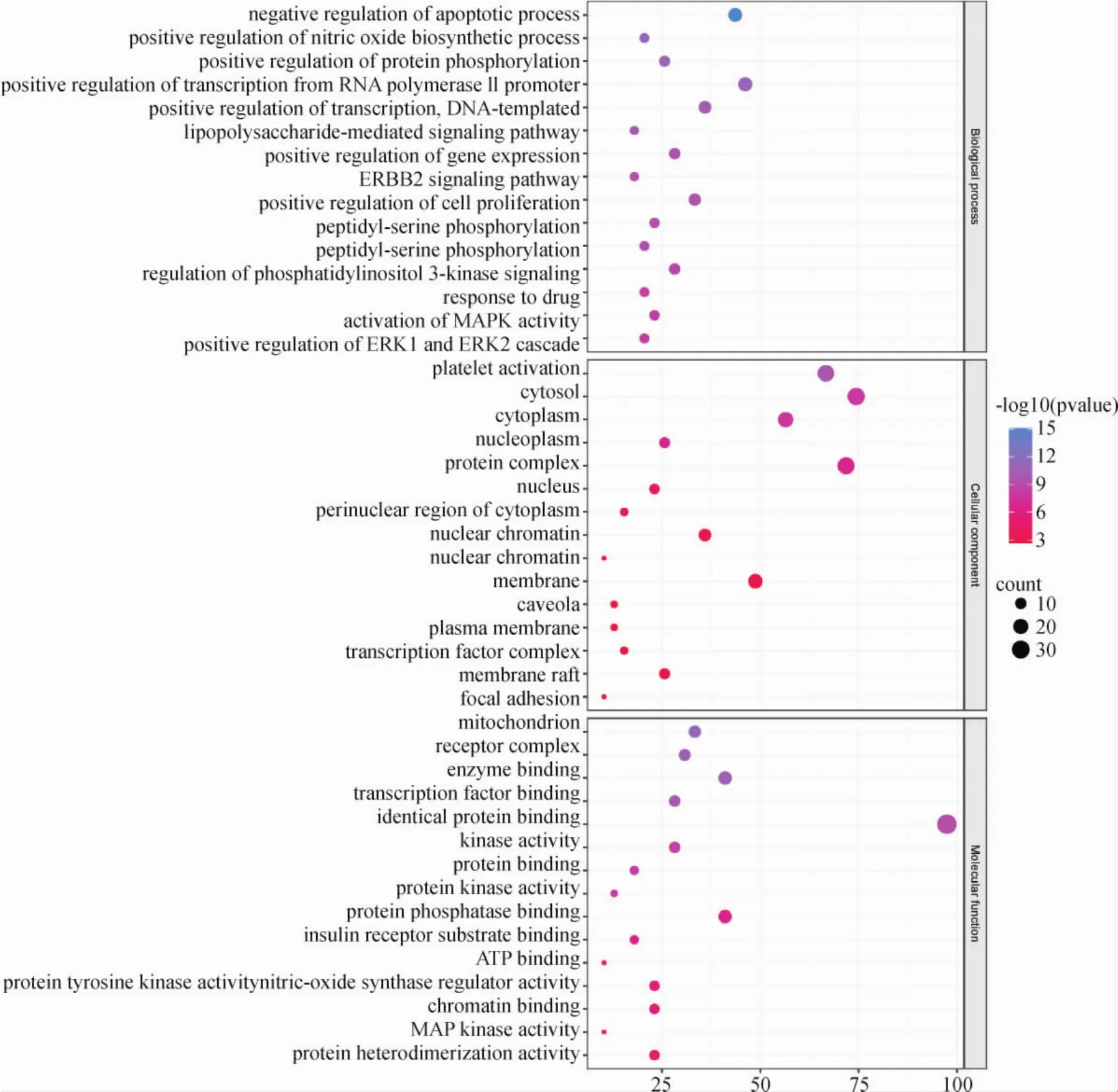
圖5 寧心通郁滋腎方治療POI靶點GO分析Fig.5 GO analysis of targets of Ningxin Tongyu Zishen Formula in the treatment of POI
2.2.5 KEGG富集分析 通過DAVID數據庫對39個關鍵靶點進行KEGG富集分析,得到具有統計學意義(P<0.05)的通路共111條,以P值為依據,選取前20條進行通路分類匯總。見圖6。由圖中可知,39個關鍵靶點主要富集在癌癥通路(pathways in cancer)、癌癥中的蛋白聚糖(proteoglycans in cancer)、乙型肝炎(hepatitis B)、前列腺癌(prostate cancer)、缺氧誘導因子-1(hypoxia inducible factor-1,HIF-1)、甲型流感(influenza A)、胰腺癌(pancreatic cancer)、催乳激素信號通路(prolactin signaling pathway)、黏附斑(focal adhesion)、叉頭蛋白O(forkhead box O,FoxO)、甲狀腺激素(thyroid hormone)、磷脂酰肌醇-3-激酶-蛋白激酶B(phosphatidylinositide 3-kinases-protein kinase B,PI3K-Akt)等信號通路。依據此20條信號通路的分子相互作用、反應和關系網絡,可分為人類疾病(human diseases)、生物系統(organismal systems)、環境信息處理 (environmental information processing)、細胞進程(cellular processes)共四大類。
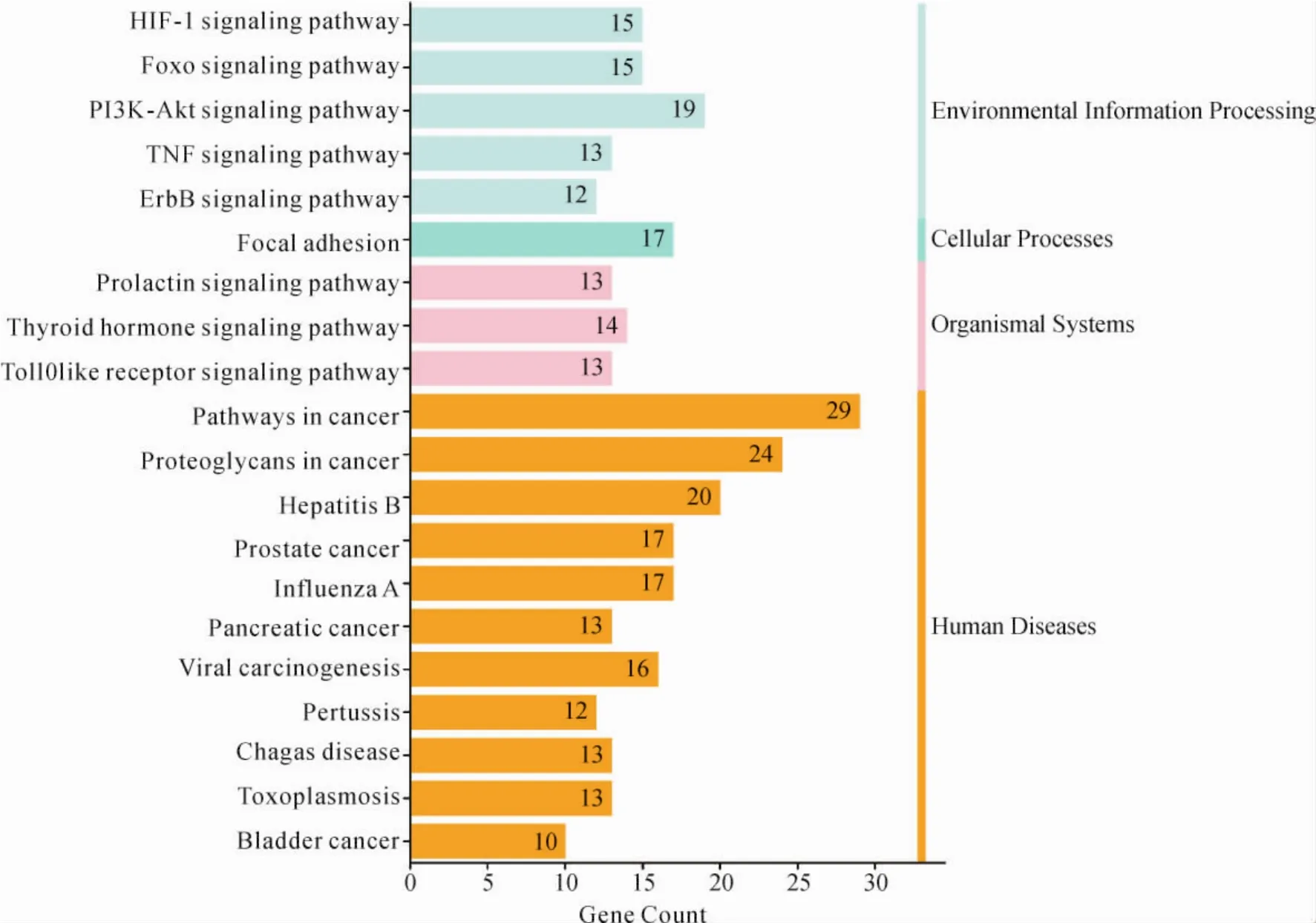
圖6 寧心通郁滋腎方治療POI靶點KEGG富集通路分析Fig.6 KEGG pathway analysis of targets of Ningxin Tongyu Zishen Formula in the treatment of POI
2.3 分子對接結果 采用Surflex-Dock分子對接程序,將2.2.3中所述主要關鍵活性成分分別與靶向相關且度值排序前10的關鍵靶點進行分子對接,從而獲得對接分數(total score)。見圖7。對接分數代表配體與靶蛋白受體結合的穩定性,分數越高則穩定性越好。當對接分數>5分時,提示分子與靶點蛋白的結合度較好。槲皮素是寧心通郁滋腎方的主要活性成分,其與對應關鍵靶點的對接分數均>5,說明均有較好的結合穩定性,分子對接圖見圖8。
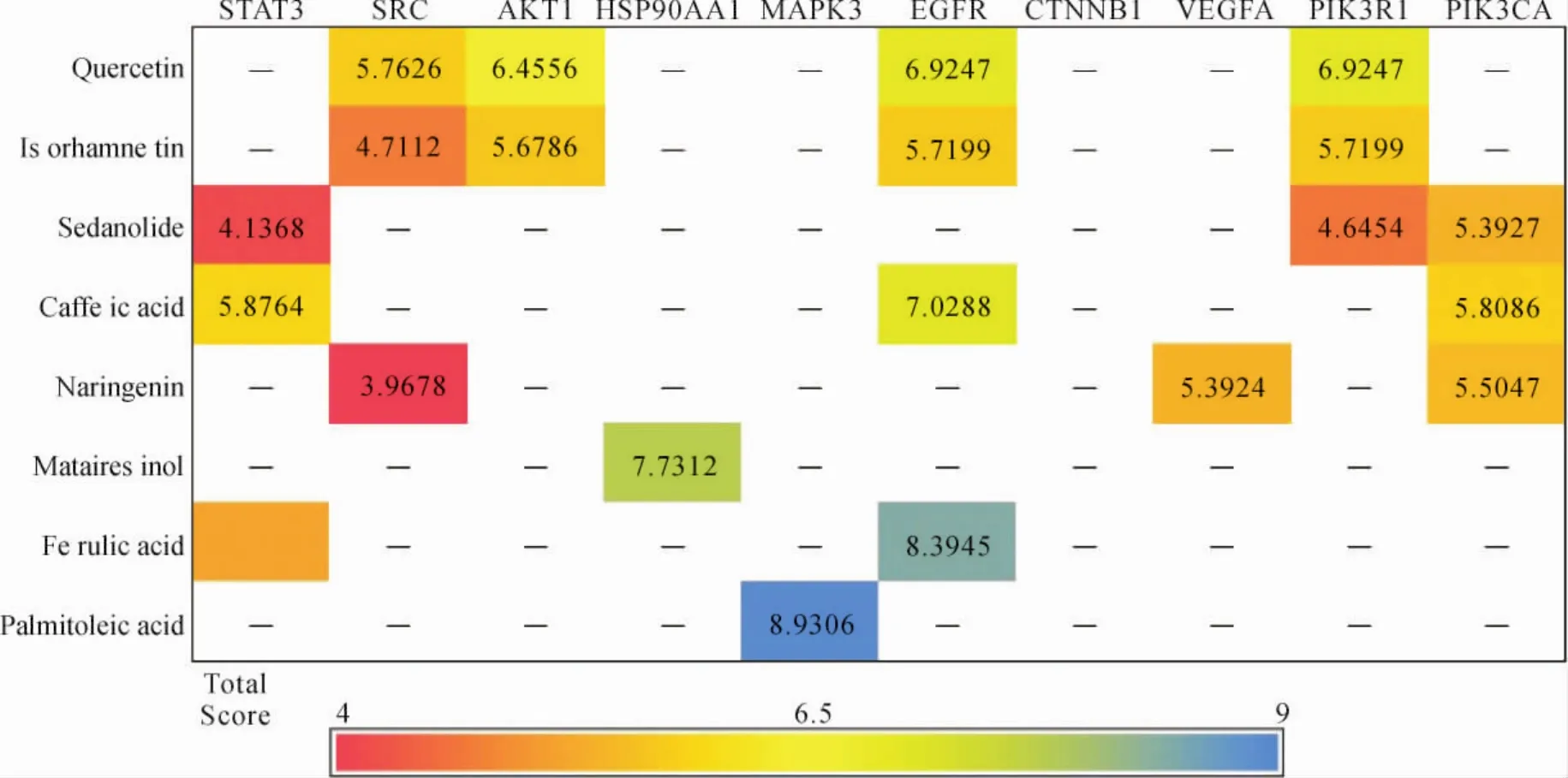
圖7 關鍵成分與關鍵靶點對接結果熱圖Fig.7 Heat map of docking results between key components and key targets
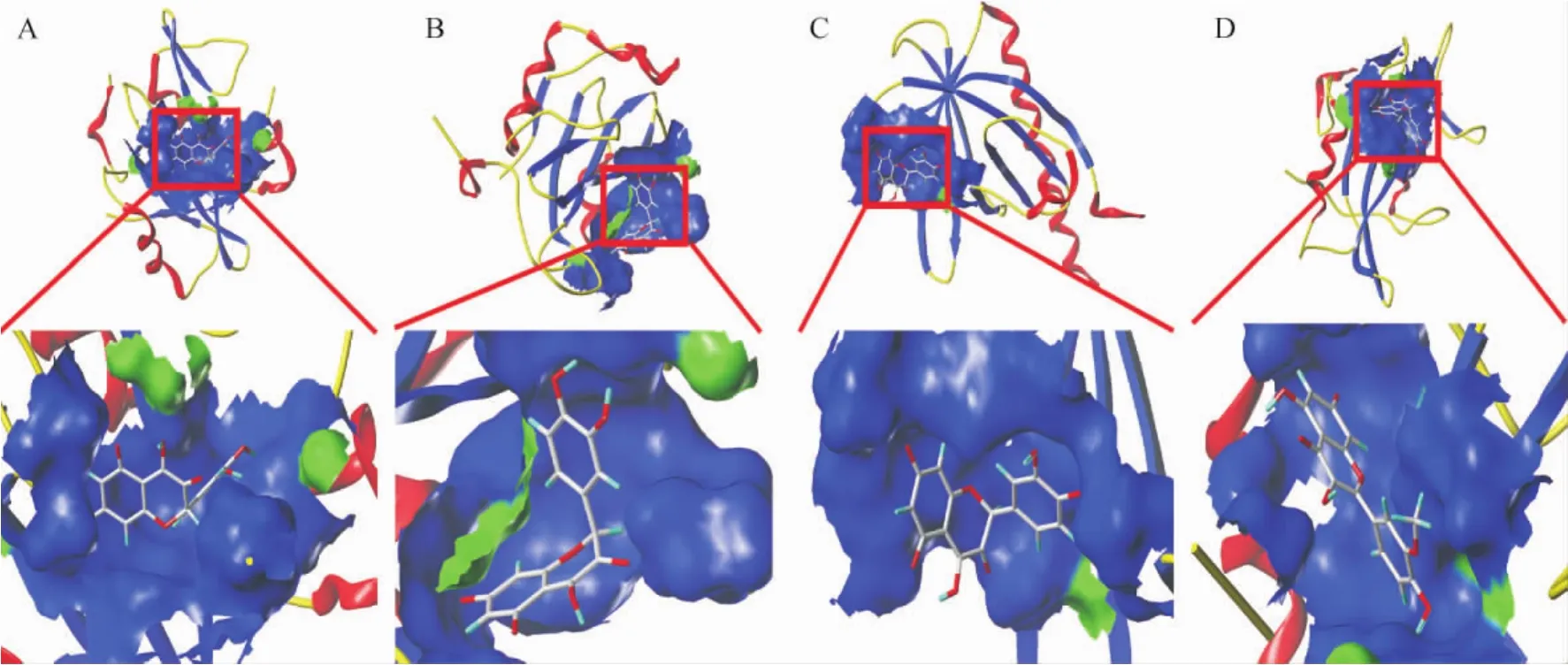
圖8 槲皮素與關鍵靶點分子對接圖Fig.8 Molecular docking of quercetin with key targets
3 討論
POI所表現出的卵巢功能衰退是一個漸進的過程,因此在疾病早期就應給予高度重視。2016年歐洲人類生殖與胚胎學會明確了POI的定義,并強調要采取必要的干預,以延緩病情發展至卵巢功能衰退的終末階段,即POF[2]。由于POI的病因復雜,發病機制尚不明確,故尚未研發出治療該病的特效藥物。本研究團隊自擬寧心通郁滋腎方,用于臨床治療POI,取得了良好的療效,但該方劑的作用機制尚不明確。由于中藥復方成分復雜,所以探明寧心通郁滋腎方治療POI的作用機制存在一定的困難。網絡藥理學具有整體性與系統性的特點,能夠從分子層面探究中醫藥治療疾病多成分、多靶點、多途徑的作用機制,近年來已被廣泛應用于中藥復方的研究[11]。本研究采用網絡藥理學分析結合分子對接的方式,為探究寧心通郁滋腎方治療POI的作用機制提供思路。
Q-Orbitrap高分辨液質聯用分析結合網絡藥理學研究結果表明,寧心通郁滋腎方治療POI的活性成分包括槲皮素、異鼠李素、瑟丹內酯、咖啡酸、柚皮素等。依據分子對接結果,其中主要活性成分槲皮素與磷酸肌醇3激酶調控亞基1(phosphoinositide-3-kinase regulatory subunit 1,PIK3R1)、 表皮生長因子受體(epidermal growth factor receptor,EGFR)、蛋白激酶B1(protein kinase B1,AKT1)、類固醇受體共激活因子(steroid receptor coactivator,SRC)等關鍵靶點的對接均較穩定,可能在POI的治療中起到關鍵作用。槲皮素是一種天然黃酮類化合物,具有抗氧化、抗炎、抗菌、抗癌等多種藥理活性[12]。研究表明,槲皮素能夠通過抑制PI3K-AKT途徑,下調AKT的表達,從而抑制原始卵泡的過度激活,防止卵泡池的提前耗竭[13]。雖然目前尚未證實槲皮素能夠通過PIK3R1、EGFR、SRC影響卵巢功能,但已有研究表明,槲皮素能夠對PIK3R1、EGFR、SRC的表達產生影響,例如槲皮素能夠與PIK3R1結合并抑制其活性,從而緩解慢性腎功能衰竭大鼠的腎纖維化[14];也能夠通過下調EGFR的表達,抑制人乳腺癌細胞株T47D的增殖,促進其凋亡[15];槲皮素作為毛茛甲醇提取物中的主要活性成分,還能夠靶向作用于SRC,發揮抗炎活性[16]。槲皮素是否通過PIK3R1、EGFR、SRC對卵巢組織發揮同樣作用,值得進一步驗證。
PPI網絡構建及分析提示,信號轉導和轉錄激活因子3(signal transducer and activator of transcription,STAT3)、SRC、AKT1、90kDa 熱休克蛋白αA19(heat shock protein 90kDa αA1,HSP90AA1)、促分裂原活化蛋白激酶3(mitogen-activated protein kinase 3,MAPK3)、EGFR等39個靶點可能是寧心通郁滋腎方治療POI的關鍵靶點。其中,STAT3的度值最高,可能在治療中起到非常關鍵的作用。STAT3是一種細胞內信號轉錄因子,能夠參與免疫反應、調節細胞周期和影響細胞存活。研究表明,在豬卵巢顆粒細胞中上調STAT3的表達能夠抑制細胞凋亡,而促進細胞增殖[17];STAT3還參與炎癥反應,當發生炎癥反應時,STAT3的磷酸化水平上升[17]。以上結果提示,上調STAT3表達或抑制STAT3的磷酸化水平也許有助于卵巢功能的改善。
對39個關鍵靶點進行GO和KEGG富集分析后發現,它們可能參與調控癌癥通路、癌癥中的蛋白聚糖、乙型肝炎、前列腺癌、HIF-1、甲型流感、胰腺癌、催乳激素信號、黏附斑、FoxO等信號通路,以及凋亡過程的負調控、一氧化氮生物合成過程的正調控、蛋白磷酸化正調控等生物過程,發揮酶結合、轉錄因子結合、相同蛋白結合等分子功能,從而治療POI。FoxO是重要的調節因子,參與細胞代謝、細胞增殖、DNA修復、自噬、氧化應激等多種細胞內過程[18]。該因子在細胞中廣泛表達,在哺乳動物細胞中FoxO家族共有4個成員:FoxO1、FoxO3、FoxO4和FoxO6。其中,FoxO1作為活性氧(reactive oxygen species,ROS)的感受器,參與不同水平的氧化應激調控[19]。FoxO1表達的上調會導致卵巢顆粒細胞的凋亡[20]。此外,它還能夠通過激活腫瘤蛋白53誘導的核蛋白1-腫瘤蛋白p53-細胞周期蛋白依賴性激酶抑制劑1A(tumor protein 53-induced nuclear protein 2-tumor protein p53-cyclin-dependent kinase inhibitor 1A,TP53INP1-p53-CDKN1A)通路,從而誘導卵巢顆粒細胞發生細胞周期阻滯[21]。而FoxO3a作為沉默信息調節因子1(sirtuin 1,SIRT1)的氧化還原靶分子,能夠參與卵巢的氧化應激調控[22]。
現代女性面對來自生活、工作、社會等各方面的壓力,身體處于慢性應激狀態,這也許是導致卵巢功能提前衰退的重要因素[23]。持續的慢性應激影響會誘使卵巢內ROS水平上升,氧化與抗氧化平衡失調,引起氧化應激反應[24]。氧化應激會促使卵巢顆粒細胞內炎性因子的釋放,促發炎癥反應[25];同時也通過破壞細胞成分,或激活凋亡相關信號通路,導致卵巢顆粒細胞凋亡[26]。由于卵巢功能的發揮依賴于卵巢顆粒細胞的正常生長分化[5],因此緩解氧化應激所致的一系列反應或許是治療POI的關鍵。
綜上所述,本研究基于Q-Orbitrap高分辨液質聯用分析,以及網絡藥理學與分子對接技術,發現寧心通郁滋腎方可能通過槲皮素、異鼠李素、瑟丹內酯、咖啡酸、柚皮素等關鍵活性成分,作用于對應的關鍵靶點,通過緩解氧化應激、修復氧化損傷、抑制卵巢顆粒細胞凋亡、促進卵巢顆粒細胞增殖等機制改善卵巢功能,延緩卵巢的衰退,從而治療POI。本研究結果為進一步研究寧心通郁滋腎方治療POI的作用機制提供了方向與思路。

