多套儀器組成的新型冠狀病毒核酸檢測系統的性能驗證方案設計*
軒乾坤,溫冬華,李廣波,郭文正,楊思敏,羽曉瑜
同濟大學附屬東方醫院南院檢驗科,上海 200123
新型冠狀病毒肺炎(COVID-19)正在全世界范圍內暴發,實驗室核酸檢測結果是COVID-19診斷的重要依據。《新型冠狀病毒肺炎防控方案(第八版)》及其附件10《新冠病毒樣本采集和檢測技術指南》[1]指出:新型冠狀病毒的病原學檢查應對其進行核酸檢測[2-7],現國內各醫學實驗室基本采用實時熒光定量PCR來進行檢測。黨中央、國務院高度非常重視新型冠狀病毒核酸檢測工作,中央應對新型冠狀病毒感染肺炎疫情工作領導小組會議作出部署,要求著力提升新型冠狀病毒核酸檢測能力,盡力擴大檢測范圍,要求加強各地實驗室建設,使其具備開展新型冠狀病毒核酸檢測的能力[8-10]。故全國各三級醫院、傳染病專科醫院、縣(區)級及以上疾控機構、海關等實驗室均安裝了多臺核酸提取儀和多臺實時熒光定量PCR儀,可以多臺儀器同時工作以完成新冠病毒核酸檢測工作。
《醫學實驗室質量和能力認可準則(ISO15189:2012)》和《新型冠狀病毒肺炎防控方案(第八版)》的附件10《新冠病毒樣本采集和檢測技術指南》均要求,實驗室應對檢測系統(包括核酸提取試劑、核酸提取儀、核酸擴增試劑和熒光定量PCR儀)進行性能驗證,以確定檢驗程序的性能特征是否符合廠商聲明[1,11-12]。現通用的新型冠狀病毒核酸檢測均包括核酸提取和PCR擴增兩個過程,其核酸提取試劑和核酸擴增試劑均是固定配套使用,為單一因素,而核酸提取儀和熒光定量PCR儀均有多臺,并且存在隨機組合的工作模式。現有文獻報道的性能驗證方案均是針對單套檢測系統或不同試劑檢測性能的比較[13-18],因而對于多套檢測系統進行性能驗證方案設計,選擇最好的方案,對保證檢測質量,提高臨床工作效率,降低消耗,具有重要意義。根據中國合格評定國家認可委員會(CNAS)2019年2月15日發布并實施的《分子診斷檢驗程序性能驗證指南》[19],針對臨床工作中新型冠狀病毒核酸在多臺核酸提取儀和熒光定量PCR儀上提取和檢測的情況,筆者制定出三套性能驗證方案,現報道如下。
1 儀器與試劑
此次性能驗證方案以4臺核酸提取儀和4臺熒光定量PCR儀為例來設計,4臺核酸提取儀分別命名為核酸提取儀A、核酸提取儀B、核酸提取儀C、核酸提取儀D;4臺熒光定量PCR儀分別命名為熒光定量PCR儀1、熒光定量PCR儀2、熒光定量PCR儀3、熒光定量PCR儀4;使用配套的核酸提取試劑和擴增試劑。
2 性能驗證參數
2.1方法符合率 選取陰性標本5例和陽性樣本(宜包含弱陽性的標本)10例,與參比方法進行比較,計算其符合率,應符合廠商試劑盒說明書中聲明的標準。
2.2精密度
2.2.1批內精密度 取2份標本,1份陰性,1份弱陽性,兩份標本各重復檢測20次,記錄陽性標本的CT值,并計算其變異系數(CV),應符合廠商試劑盒說明書中聲明的標準。
2.2.2批間精密度 取2份標本,1份陰性,1份弱陽性,兩份標本每天各重復檢測4次,連續檢測5 d,共計20次,記錄陽性標本的CT值,并計算其CV,應符合廠商試劑盒說明書中聲明的標準。
2.3檢出限 使用定值標準物質的標本,梯度稀釋至廠家聲明的檢出限濃度,重復測定5次,必須100%檢出靶核酸。
3 設計的三套性能驗證方案
3.1方案一 將1臺核酸提取儀和1臺熒光定量PCR儀綁定在一起作為一套系統,共驗證4套檢測系統的方法符合率、精密度和檢出限,見圖1。

圖1 性能驗證方案一流程圖
3.2方案二 按照排列組合的原理,將4臺核酸提取儀和4臺熒光定量PCR儀的16種組合形式均做一次性能驗證,共驗證16套檢測系統的方法符合率、精密度和檢出限,見圖2。
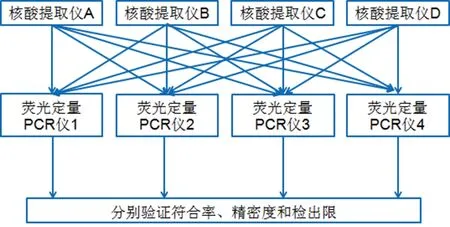
圖2 性能驗證方案二流程圖
3.3方案三 (1)在核酸提取儀A上提取核酸后,分別在熒光定量PCR儀1、熒光定量PCR儀2、熒光定量PCR儀3和熒光定量PCR儀4上擴增檢測,主要驗證4臺熒光定量PCR儀的方法符合率、精密度和檢出限;(2)在核酸提取儀A、核酸提取儀B、核酸提取儀C、核酸提取儀D上分別提取核酸后,均在熒光定量PCR儀1上擴增檢測,主要驗證4臺核酸提取儀的方法符合率、精密度和檢出限。見圖3。

圖3 性能驗證方案三流程圖
4 三套方案的比較
對三套性能驗證方案進行比較,見表1、2。

表1 三套性能驗證方案的比較

表2 三套性能驗證方案優缺點比較
5 小 結
目前通用的新型冠狀病毒核酸檢測流程均包括核酸提取和PCR擴增兩個步驟,檢測系統包括核酸提取試劑、核酸提取儀、核酸擴增試劑和熒光定量PCR儀四個部分,在進行性能驗證時,應確保覆蓋到所有部分;而在實際性能驗證工作中,對核酸提取儀的驗證往往被忽略。核酸提取儀有分液、加熱、磁吸、震蕩和排風等功能,在核酸提取過程中,這些功能對提高核酸提取效率有非常重要的作用,工作人員在做性能驗證時應引起重視。本課題組根據核酸提取儀和熒光定量PCR儀的不同組合,設計出了三套性能驗證方案。
以配置4臺核酸提取儀和4臺熒光定量PCR儀為例,通過對三套性能驗證方案的比較分析,筆者認為方案三最優。首先,在1臺核酸提取儀上提取核酸,分別在4臺熒光定量PCR儀上擴增檢測,驗證了4臺熒光定量PCR儀的性能;然后,分別在4臺核酸提取儀上提取核酸,在同一臺熒光定量PCR儀上擴增檢測,驗證了4臺核酸提取儀的性能;達到了16套組合檢測系統的驗證效果,保證了新型冠狀病毒核酸檢測的質量,試劑消耗和時間成本適中,可以有效、經濟、快速地評估各性能參數是否符合廠商的聲明。該性能驗證方案可以推廣,供其他實驗室參考。

