男性甲狀腺功能減退癥合并垂體病變的臨床特點及治療效果
劉妮娜 王佑民 杜益君 鐘 興 潘天榮
原發性甲狀腺功能減退癥(hypothymidism,簡稱甲減)是由于甲狀腺合成分泌甲狀腺激素減少導致的全身性代謝降低的一種綜合征。甲狀腺功能減退癥可合并垂體病變,常常存在誤診漏診,本研究主要總結男性患者原發性甲狀腺功能減退癥合并垂體病變的臨床特點和治療效果,為臨床診斷治療提供依據。
1 資料與方法
1.1 一般資料 2013年1月-2021年6月就診于安徽醫科大學第二附屬醫院門診的原發性甲狀腺功能減退癥的男性患者共30例。年齡18~50歲,平均年齡(42.47±10.89)歲。根據垂體磁共振(MRI)結果分為有垂體病變組(16例)和無垂體病變組(14例)。原發性甲狀腺功能減退癥診斷參照2017年成人甲狀腺功能減退癥臨床指南[1],我院甲狀腺功能正常參考值T3:1.3~3.1 nmol/L,T4:66~181 nmol/L,TSH:0.27~4.2 mIU/L。研究方案由我院倫理委員會批準(SL-YX2021-038)。
1.2 研究方法 收集患者臨床資料,治療前和治療6月后分別收集實驗室檢測結果、垂體MRI和國際勃起功能指數-5(IIEF-5)。血標本均在上午7:00-9:00從肘前靜脈采集,至少在最后一餐后12 h以上,分別進行生化及血清黃體生成素(LH)、卵泡刺激素(FSH)、催乳素(PRL)、總睪酮(TT)、三碘甲狀腺原氨酸(T3)、甲狀腺素(T4)、促甲狀腺素(TSH)、促腎上腺皮質激素(ACTH)和皮質醇(COR)水平檢測。采用化學發光免疫法及配套試劑盒(美國,BECKMAN公司)檢測LH、FSH、PRL、TT、ACTH、COR。采用電化學發光分析儀及配套試劑盒(瑞士,羅氏診斷公司)檢測T3、T4、TSH。采用日立7600全自動生化儀檢測甘油三脂(TG)、膽固醇(TC)、低密度膽固醇(LDL)。垂體MRI采用美國GE公司1.5T超導型MRI掃描儀,做頭顱冠狀位、矢狀位T1WI序列及軸位T2WI序列掃描。T1WI序列TR400 ms,TE20 ms,T2WI序 列TR3000 ms,TE120 ms,矩陣288×192,層厚2 mm,FOV18 cm×18 cm。增強掃描采用釓噴酸葡胺對比劑,劑量0.2 mL/kg。
1.3 治療方法 給予左甲狀腺素鈉片替代治療,起步劑量為25~50 ug/d,空腹口服,與早餐和其他進食間隔60 min以上。每4周復查甲狀腺功能,調整左甲狀腺素鈉片劑量,服藥3個月內調整TSH在0.27~4.2 mIU/L,左甲狀腺素鈉片藥物劑量不變繼續維持治療3個月。
1.4 統計學分析 采用SPSS19.0統計學軟件處理數據。符合正態分布的計量資料,以均數±標準差(±s)方式表示,兩組間比較用t檢驗或t'檢驗。不符合正態分布計量資料,以中位數M(Q1,Q3)表示,組間比較用非參數檢驗。采用MedCalc 18.2.1繪制受試者工作特征(ROC)曲線評價TSH、PRL、TT及三個指標聯合診斷原發性甲狀腺功能減退癥合并垂體病變的效果,并計算各指標的靈敏度、特異度、約登指數。其中聯合應用為回歸預測模型Log(P/1-P)模式。檢驗水準α=0.05。
2 結 果
2.1 病變情況和治療結果 有垂體病變16例(53.33%),其中10例表現為垂體增大,4例垂體飽滿,2例呈現垂體瘤樣改變,治療后垂體MRI病變均可恢復。
2.2 各種臨床指標結果比較 與無垂體病變組比較,有垂體病變組年齡輕、血清TSH水平較高、血清PRL水平升高、血清TT水平下降,血清LDL水平偏高,差異均有統計學意義(P<0.05);與無垂體病變組比較,垂體病變組IIEF-5評分下降、COR下降、ACTH升高,但差異均無統計學意義(P>0.05)。見表1。
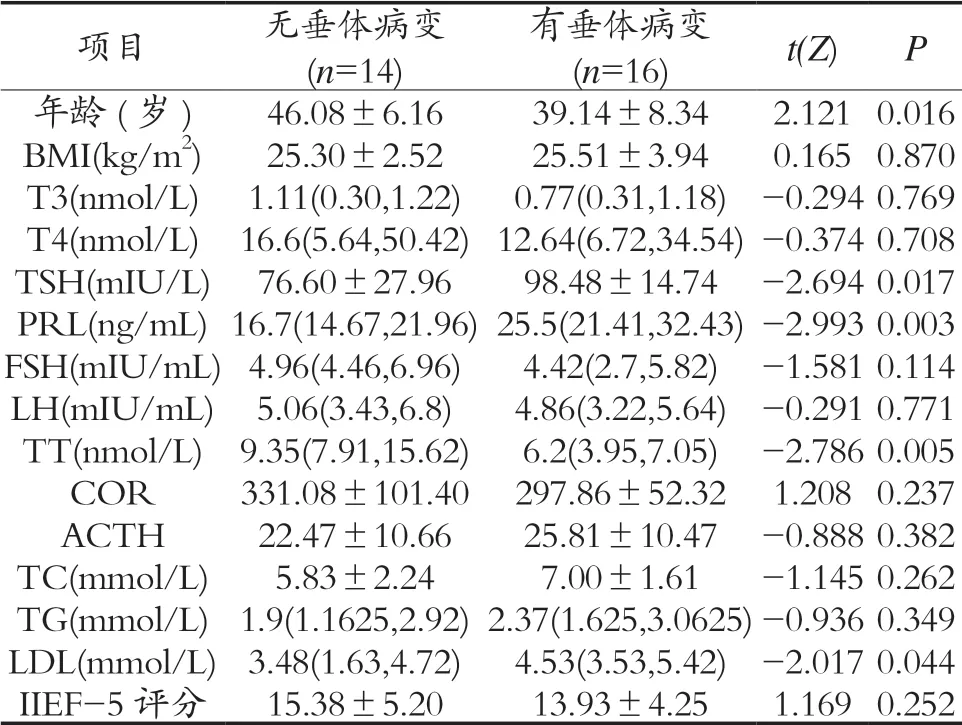
表1 臨床甲狀腺功能減退癥患者中有垂體病變組和無垂體病變組比較
2.3 血清TSH、PRL、TT水平對于原發性甲狀腺功能減退癥合并垂體病變的預測價值 進一步探討血清TSH、PRL、TT水平對于原發性甲狀腺功能減退癥合并垂體病變的預測價值:以有垂體病變組(n=16)為陽性樣本,以無垂體病變組(n=14)為陰性樣本,建立ROC(接收者工作特征曲線)診斷分析模型。以軟件擬合之ROC曲線讀取約登指數最大值點,對應計算理論閾值和各項參數如AUC、敏感度、特異度等。結果:TSH、PRL、TT三指標單獨應用時:ROC-AUC(0.95CI)分別為0.712(0.519-0.862)、0.828(0.647-0.940)、0.801(0.616-0.924),TSH和TT聯合診斷、TSH和PRL聯合診斷、TSH、PRL、TT三指標聯合診斷時:ROC-AUC(0.95CI)分 別 為0.853(0.676-0.955)、0.842(0.662-0.948)、0.906(0.743-0.982),可見聯合應用時預測效能更高。分析結果見表2,ROC分析曲線見圖1。
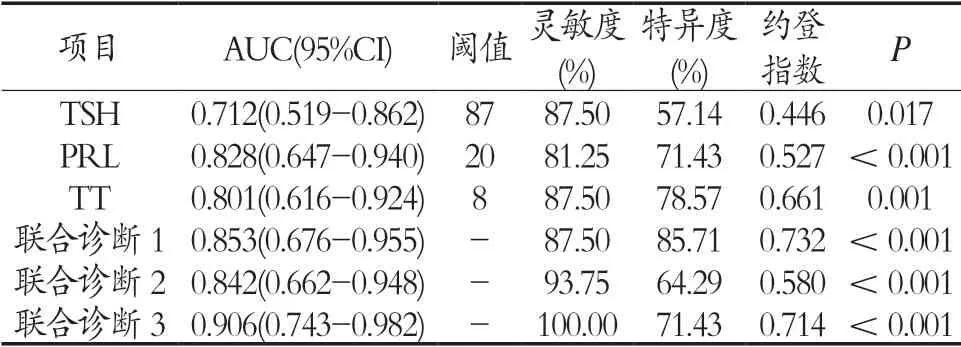
表2 血清TSH、PRL、TT水平對原發性甲狀腺功能減退癥伴垂體病變的預測價值
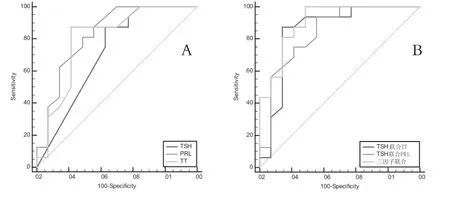
圖1 預測ROC曲線
3 討 論
甲狀腺功能減退癥因TSH水平明顯升高,可導致垂體TSH細胞明顯增生形成瘤體,常常出現誤診誤治,給患者造成不可逆損傷[2-4],需要前瞻性研究進一步明確原發性甲狀腺功能減退癥合并垂體病變特點,避免漏診和誤診。
原發性甲狀腺功能減退癥合并垂體病變發病率各家報道不一。Yamada T等[5]報道81%原發甲狀腺功能減退癥患者出現垂體體積增大,Han L等[6]研究提示原發性甲狀腺功能減退癥引起33.3%的繼發性垂體瘤樣增生。本研究對臨床甲狀腺功能減退癥患者進行垂體MRI篩查,發現合并垂體病變53.33%。不同研究報道差別較大,考慮可能與入組患者年齡、甲狀腺功能嚴重程度有關。既往研究中提示年齡與垂體病變相關,目前機制不清,可能與年輕患者垂體反應性更敏感,更容易出現TSH細胞增生有關[7-8],本研究納入18~50歲男性,較Han等研究入組患者年齡更輕,考慮為垂體病變比率較高原因。
垂體MRI為垂體病變檢測的有效方法。本研究中16例甲狀腺功能減退癥合并垂體病變組MRI表現:10例垂體增大,4例垂體飽滿,2例呈現垂體瘤樣改變。經過左甲狀腺素鈉片替代治療后復查垂體MRI均恢復正常,與其他研究結果一致[4]。MRI表現為垂體均勻增大,呈等T1、等T2信號,垂體后葉高信號存在,垂體柄居中或輕度偏移,增強掃描均勻一致強化[9],提示垂體病變可能為原發性甲狀腺功能減退導致,可待充分替代治療后復查垂體MRI,如垂體病變消失可進一步證明垂體病變為原發性甲狀腺功能減退癥導致,避免盲目手術導致患者垂體不可逆損傷。但垂體MRI需要治療后復查垂體病變消失才能明確垂體病變為原發性甲狀腺功能減退癥引起,有一定的滯后性,且臨床費用較高,不適合作為常規篩查。垂體病變組和非垂體病變組比較發現,垂體病變組PRL和TSH升高、TT下降,差異具有統計學意義。故本文進一步分析上述指標,希望尋找簡便篩查方法。
從本研究對與PRL、TSH和TT單獨的診斷價值中可以看出,PRL和TT AUCROC>0.8,可作為診斷指標,其中TT的靈敏度和特異性最佳。這可能因為垂體病變時通常性腺軸最先受累有關。TT水平受影響因素較少,結果相對比較穩定,可以作為是否存在垂體病變的篩查指標。需要注意的是TT與年齡有關,日后研究中可以擴大樣本量,根據年齡進行分層,探討不同年齡段TT的診斷切點。原發性甲減常常合并PRL升高[10],TSH可以作用于PRL細胞,促進泌乳素分泌;如形成垂體瘤,垂體瘤占位效應,導致PRL抑制劑多巴胺不足,進一步加重PRL水平升高。原發性甲狀腺功能減退癥患者如合并高泌乳素血癥需要與垂體泌乳素瘤相鑒別。有研究顯示,若PRL>250 ug/L,且排除其他原因,則支持泌乳素瘤的診斷;若PRL<100 μg/L,需結合具體情況謹慎診斷[11]。本研究發現垂體占位組PRL均值44.40 ug/L,最大值158.0 ug/L,最小值17.48 ug/L,除1人外,其余PRL均<100 μg/L,與其他個案報道相同[12],提示PRL水平為鑒別因素之一。對PRL進一步進行ROC曲線分析,發現PRL≥20 ng/mL需要警惕存在垂體病變可能。本研究對TSH、PRL、TT,TSH、PRL,TSH、TT分別進行多因素聯合診斷進行ROC曲線分析,發現TSH、PRL、TT三 指 標 聯 合AUCROC>0.9,診 斷 效 果最佳。結合對TSH單個因素ROC曲線分析,建議TSH≥87 mIU/L,可行血清PRL、TT檢測。
既往有研究提示原發性甲減與男性勃起功能障礙有關[13]。IIEF-5目前用于臨床評價患者勃起功能狀態,在多個高質量臨床研究中得到應用[14]。在本研究中有垂體病變組IIEF-5評分較無垂體病變組更低,但無統計學差異,與推測不符,可能需要擴大樣本量進一步研究。本研究發現臨床甲狀腺功能減退癥合并垂體占位并未影響下丘腦-垂體-腎上腺軸。提示如原發性甲狀腺功能減退癥合并有垂體占位如影響到下丘腦-垂體-腎上腺軸,需要隨訪明確是否垂體病變為甲狀腺功能減退癥引起。
總之,原發性甲狀腺功能減退癥常常合并高泌乳素血癥和垂體病變,特別是兒童和青年更容易出現垂體病變,常常與其他垂體病變混淆,造成誤診誤治。原發性甲狀腺功能減退癥導致垂體病變,充分治療后可恢復,治療前后垂體MRI變化可鑒別原發性甲狀腺功能減退癥導致垂體病變與其他垂體瘤,但均有一定滯后性。TSH、PRL、TT三項指標聯合檢測有助于在治療早期鑒別垂體病變是否源于原發性甲狀腺功能減退癥。

