重癥肌無力合并前縱隔腫物患者手術入路選擇研究
潘祖林 梁麗靜 陳何偉 馮書孌 乞國艷
重癥肌無力(MG)是臨床較少見的一種獲得性自身免疫性疾病,與乙酰膽堿受體抗體相關。胸腺是人體重要的免疫器官,調節乙酰膽堿受體抗體的免疫應答,參與MG的發生及發展的過程[1]。胸腺瘤是前縱隔腫物中最常見的交界性腫瘤,臨床常表現為以骨骼肌無力為主的重癥肌無力[2]。縱隔腫物及全胸腺的擴大切除術是公認的治療MG合并前縱隔腫物患者的治療方法,而目前全國胸外科臨床上常用的手術入路為正中開胸入路、肋間胸腔鏡入路及劍突下胸腔鏡入路三種。本研究通過重癥肌無力診療中心對三種手術入路的臨床各項資料比較,為重癥肌無力合并前縱隔腫物患者的手術方案選擇提供經驗。
1 資料與方法
1.1 一般資料 回顧性分析石家莊市人民醫院重癥肌無力診療中心胸腺外科于2013年10月至2019年12月行前縱隔腫物切除+胸腺擴大切除術的重癥肌無力合并前縱隔腫物患者186例。醫院倫理委員會批準本研究豁免知情同意的申請。
1.2 納入與排除標準
1.2.1 納入標準:①全身型重癥肌無力患者;眼肌型重癥肌無力患者經1年的內科藥物治療,效果不佳或者停藥后再次復發者;②胸部CT提示腫物位于前縱隔者;③心、肺、肝、腎等重要臟器無嚴重的器質性病變者;④排除遠處淋巴結、頭顱及腹腔等其他遠處部位轉移患者。
1.2.2 排除標準:①合并多種全身型疾病患者,心肺等臟器功能差,無法耐受手術者;②高齡(>75歲)患者,身體虛弱、惡病質患者;③處于重癥肌無力危象發作期患者;④合并妊娠、哺乳期者。
1.3 臨床操作指征
1.3.1 拔除經口氣管插管指征:①心率、血壓、呼吸等生命體征平穩;②試停呼吸機>1 h,接3~5 L/min吸氧(氧濃度),血氧飽和度維持>95%;③動脈血氣分析提示:pH值≥7.30、PO2≥12 kPa、PCO2≤6.7 kPa[3]。
1.3.2 拔除胸腔閉式引流管指征:患者咳嗽及深吸氣時胸腔引流瓶未見氣泡溢出,24 h胸腔引流量少于100 ml,胸腔引流液顏色為淡血性或淡黃色,胸部正側位CR片未見大量胸腔積液及明顯液氣平面。
1.3.3 術后轉肌無力內科組標準:患者的生命體征平穩,已拔除胸腔閉式引流管,手術切口愈合較良好。
1.3.4 重癥肌無力判定標準:典型的骨骼肌易疲勞,新斯的明試驗陽性,乙酰膽堿受體抗體檢測陽性,和(或)肌電圖提示低頻重復神經電刺激呈波幅遞減>10%[4]。
1.4 療效判定標準 (1)患者術后2周內進行術后近期緩解率的療效評價,應用許賢豪等[5]重癥肌無力的臨床絕對與相對評分方法,有效:明顯緩解(臨床相對評分為>50%),部分緩解(臨床相對評分為26%~50%);無效:不緩解(臨床相對評分為0~25%),加重(臨床相對評分為負值)。
1.5 手術入路及操作過程
1.5.1 手術入路:①正中開胸入路:患者呈仰臥位,后背墊枕,取胸骨正中切口10~20 cm,切開皮膚及皮下各層組織直達胸骨,從胸骨上切跡沿正中用胸骨鋸縱行開胸至劍突或第3肋間水平,根據腫物位置橫斷左側或右側胸骨。②肋間胸腔鏡入路:根據腫物位置選擇左側或右側肋間隙入路,患者平臥且手術側墊高呈前外體位,取術側腋前線的第5肋間行1.5 cm切口為觀察孔、腋中線的第3肋間作3~4 cm切口為輔助操作孔,鎖骨中線的第5肋間行1.5 cm切口為主操作孔。③劍突下胸腔鏡入路:患者呈仰臥分腿位,取胸骨正中線劍突下2~3 cm做切口為觀察孔、兩側肋緣下0.5~1 cm做切口為操作孔。依次切開胸骨劍突下正中處各層組織直達腹膜,用12 mm的長戳卡平行劍突向上穿過膈肌,連接二氧化碳(壓力為8~12 cm H2O),兩側肋緣下切口用5 mm長戳卡穿透膈肌進入前縱隔[6,7]。
1.5.2 操作過程:探查腫物與周邊臟器、血管及神經的關系,如腫物包膜完整界限清晰位于胸腺組織內,清掃左右心隔角處脂肪組織,沿兩側膈神經的上方和心包的前方進行鈍銳離斷。解剖上腔靜脈、胸廓內靜脈、無名靜脈及雙側隔神經,分別結扎供應胸腺的動靜脈,沿左無名靜脈前方向頸部分離達兩側的胸腺上極,離斷其與甲狀腺下極的纖維連接組織,將胸腺、腫物及縱隔脂肪組織等一并完整切除。如腫物侵犯心包、肺、血管、神經等,連同上述組織一并切除。徹底止血,放置引流管1~2根,逐層關胸,帶單腔經口氣管插管返回病房監護室。
1.6 觀察指標 (1)術前:年齡、性別、病程、MG危象既往史、術前激素沖擊、術前免疫球蛋白沖擊、臨床分型(Osserman)等基本臨床資料;(2)術中:手術時間、術中出血量、腫物最大直徑、腫物侵及部位;(3)術后:病理類型、Masaoka分期、呼吸機使用時間、監護室住院時間、第1天引流量、引流管留置時間、術后住院時間、肌無力近期緩解率、肌無力危象發生率。
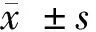
2 結果
2.1 3種手術入路患者各項臨床資料比較
2.1.1 3種手術入路術前各項指標比較:本研究入組患者186例,其中男83例,女103例;年齡19~74歲,平均年齡(47.63±11.93)歲;病程0.3~256個月,平均(34.99±51.83)月;有MG危象既往史者24例;術前激素沖擊者45例,丙種球蛋白沖擊者31例;臨床分型(Osserman):Ⅰ型32例,ⅡA型27例,ⅡB型87例,Ⅲ型32例,Ⅳ型8例。患者分為3組:正中開胸入路組62例,肋間胸腔鏡入路組55例,劍突下胸腔鏡入路組69例。3組患者年齡、性別比、病程、MG危象既往史、術前激素沖擊、術前免疫球蛋白沖擊、臨床分型(Osserman)差異無統計學意義(P>0.05)。見表1。

表1 3種手術入路患者各項臨床資料比較
2.1.2 3種手術入路患者腫物相關方面比較:病理類型方面,3組間差異無統計學意義(P>0.05)。腫物直徑方面,正中開胸入路組與其他2組比較切除腫物更大,存在統計學差異(P<0.05)。腫物侵犯部位方面,正中開胸入路組侵及血管明顯多于其他2組,差異有統計學意義(P<0.05),而侵及心包和肺者3組間差異無統計學意義(P>0.05)。Masaoka分期方面,Ⅰ期患者正中開胸入路組(13/62)少于肋間(23/55)及劍突下(27/69)胸腔鏡入路組(P=0.004),Ⅲb期患者正中開胸入路組(7/62)多于肋間胸腔鏡入路組(0/55)及劍突下胸腔鏡入路組(2/62)(P=0.011)。Ⅱa、Ⅱb、Ⅲa及Ⅳa期3組間差異無統計學意義(P>0.05)。劍突下入路能夠完成部分Ⅲb期及Ⅳa期的胸腺瘤切除,如2例Ⅲb期胸腺瘤侵犯左無名靜脈者,1例Ⅳa期胸腺瘤侵犯胸壁者;此外,肋間及劍突下組各有1例中轉為正中切口。見表2。

表2 3種手術入路患者腫物相關方面比較
2.2 3種手術入路在術中及術后相關指標比較
2.2.1 3種手術入路在術中相關指標比較:手術時間方面,劍突下胸腔鏡入路組明顯短于其他2組,差異有統計學意義(P<0.05);術中出血量方面,劍突下胸腔鏡入路組較其他2組更少,差異有統計學意義(P<0.05)。見表3。
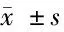
表3 3種手術入路術中相關指標比較
2.2.2 3種手術入路術后各項指標比較:術后第1天引流量及引流管留置時間方面,劍突下胸腔鏡入路組優于其他2組,差異有統計學意義(P<0.05)。呼吸機使用時間方面,劍突下胸腔鏡入路組明顯短于正中開胸入路組及肋間胸腔鏡入路組,差異有統計學意義(P<0.05);監護室住院時間及術后住院時間方面,劍突下胸腔鏡入路組天數較其他2組更少,差異有統計學意義(P<0.05)。見表4。
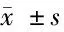
表4 3種手術入路術后指標比較
2.3 3種手術入路在MG近期緩解率及肌無力危象發生率比較 MG危象發生率方面,劍突下胸腔鏡入路組低于肋間胸腔鏡入路組及正中開胸入路組,差異有統計學意義(P<0.05);術后近期緩解率方面,3組差異無統計學意義(P>0.05)。見表5。

表5 3組術后MG危象發生率及肌無力近期緩解率比較 例(%)
3 討論
MG是一種世界公認的難治的慢性自身免疫性疾病,累及神經-肌肉接頭傳遞從而導致功能障礙,是由乙酰膽堿受體抗體介導、同時細胞免疫依賴及補體的參與[8]。可累及全身骨骼肌,且容易感到疲勞[9,10],臨床常表現為眼瞼下垂、眼內肌受累、肢體無力,嚴重者可累及延髓肌,甚至出現重癥肌無力危象。縱隔腫瘤中以前縱隔腫物的發病率最高,其中常見的病理類型有胸腺瘤、胸腺囊腫、畸胎瘤等,而胸腺瘤又是前縱隔腫物中最常見的原發性腫瘤[11],有報道顯示,10%~30%胸腺瘤的患者伴有MG,且10%~60%的MG的患者并發胸腺瘤[12]。目前外科手術切除腫物是治療前縱隔腫物的主要手段[13],美國神經病學會和歐洲指南與建議及我國重癥肌無力診斷和治療專家共識指出:無論MG合并胸腺腫物的分期及種類,縱隔腫物切除且同時行胸腺擴大切除手術均能使患者的肌無力癥狀得到明顯改善[14-16]。
2019版NCCN胸腺瘤/胸腺癌臨床實踐指南中指出,手術目標是通過完全切除病變,包括全胸腺切除術和完全切除連續性和非連續性的病變。胸腺瘤切除手術入路主要分為開胸及胸腔鏡兩大類,開胸包括有正中全劈胸骨入路、正中半劈胸骨入路、肋間側開胸入路、經頸部橫行切口入路、頸胸聯合切口入路,胸腔鏡包括有肋間胸腔鏡入路及劍突下胸腔鏡入路等,目前文獻中尚有一些胸腔鏡聯合縱隔鏡及機器人微創手術的報道。正中開胸入路是治療胸腺瘤伴MG的標準術式[17]。但是,隨著目前微創技術的不斷發展,胸腔鏡手術在治療MG合并胸腺瘤方面,因為具有出血少、創傷小、術后恢復快等優勢而廣泛的被應用于目前胸外科臨床[18-20]。劍突下胸腔鏡入路最早由Hsu等[21]報道,通過劍突下胸腔鏡手術入路行胸腺切除擴大切除術治療MG,安全性有效。目前,受各級臨床醫院基礎條件及患者經濟狀況的限制,正中開胸入路、肋間胸腔鏡入路及劍突下胸腔鏡入路為大多數胸外科醫生所采用。
本研究發現:(1)術中手術時間、手術出血量、術后第1天引流量、引流管留置、呼吸機使用時間、監護室住院時間及術后住院時間等方面,在劍突下胸腔鏡入路打開雙側縱隔胸膜減少術中鈍性分離操作,雙側胸腔的壁層胸膜重吸收,避免破壞胸骨造成滲血,保持了胸廓的完整性,避免肋間神經刺激及損傷從而減少了術后疼痛,術后恢復更快,從而使其優于正中開胸入路及肋間胸腔鏡入路。(2)腫物方面,B1/B2型及B2/B3型腫瘤的存在,說明一個腫瘤病理類型的多樣性。何健行等[22]報道:胸腺瘤體直徑>4 cm時,胸腔鏡受可視術野的限制,需于右側2肋間行輔助小切口協助暴露從而切除腫物,而李劍鋒等[23]則認為胸腔鏡使用限制的主要因素應該是胸腺瘤的侵襲性。我肌無力中心切除腫物最大直徑,正中開胸入路組為(6.02±2.95)cm、最大腫物17 cm,肋間胸腔鏡入路組為(3.91±1.91)cm、最大腫物11.8 cm,劍突下胸腔鏡入路組為(4.33±2.23)cm、最大腫物12.5 cm,3組比較差異明顯(P<0.05)。雖然在臨床中3種手術入路均切除過>10 cm腫瘤,但是存在術中操作困難、遮擋術野、取出時腫物完整性不能保證等。3種手術入路雖能完成Masaoka分期Ⅰ期、Ⅱ期及Ⅲa期的患者,與Zielinski等[24]報道相符,但肋間及劍突下胸腔鏡入路,因為手術視野及操作角度的關系,完成Ⅲb期及Ⅳa期的胸腺瘤切除相對困難;正中開胸入路能完成腫瘤分期更晚的手術,全面性更強;從而建議,腫物>5 cm和(或)腫瘤侵及血管等重要組織的應選擇正中開胸入路為佳。(3)術后MG危象發生率及MG近期緩解率方面,研究表明,胸腺擴大切除術后的患者MG危象的發生率為6.9%~19.2%[25],而MG危象又是導致患者死亡的重要原因。我中心劍突下胸腔鏡入路MG危象發生率為2.90%,明顯低于其他2組;3組MG患者近期緩解率無明顯差異,所以劍突下胸腔鏡入路更具有優越性。
正中開胸入路能完成所有分期及各種難度的胸腺瘤切除手術操作,而胸腺瘤切除的第一原則為完整切除腫物,以免復發及轉移;但是,我們應考慮胸腺瘤與MG既是兩個獨立的疾病,其關系又密不可分,如何在手術順利完成的條件下,兼顧術后肌無力癥狀的恢復及并發癥的減少,應該全盤考慮。劍突下胸腔鏡入路手術時間更短、出血量更少、創傷更小、術后恢復快、術后嚴重并發癥更少、術后住院時間更短,為MG患者的下一步內科治療及減少經濟負擔提供了較大的貢獻。
綜上所述,對于MG尤其是術前癥狀較重的患者,Ⅰ期、Ⅱa期、Ⅱb期、Ⅲa期及部分Ⅲb期的胸腺瘤可以選擇劍突下胸腔鏡入路解決,而較為困難的Ⅲb期及Ⅳa期胸腺瘤患者以正中開胸入路較佳。

